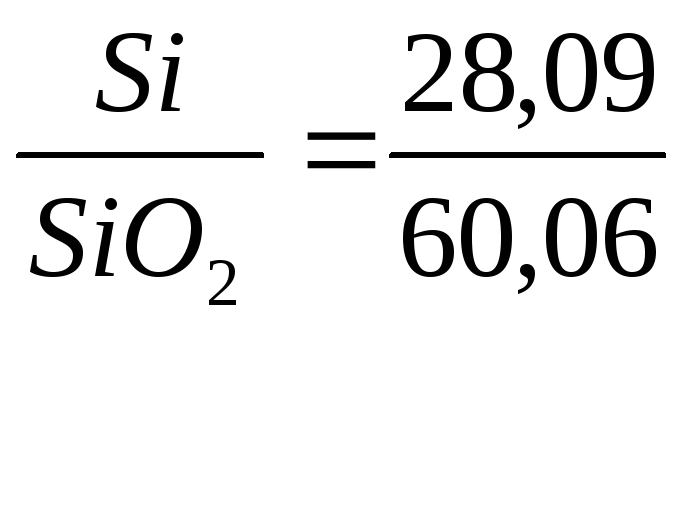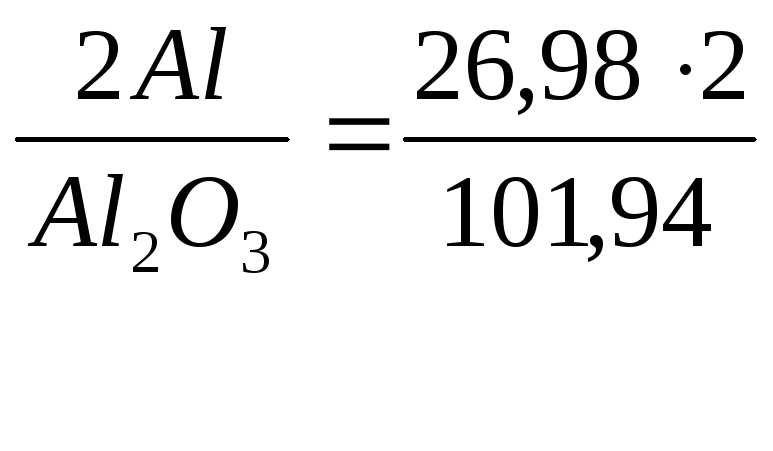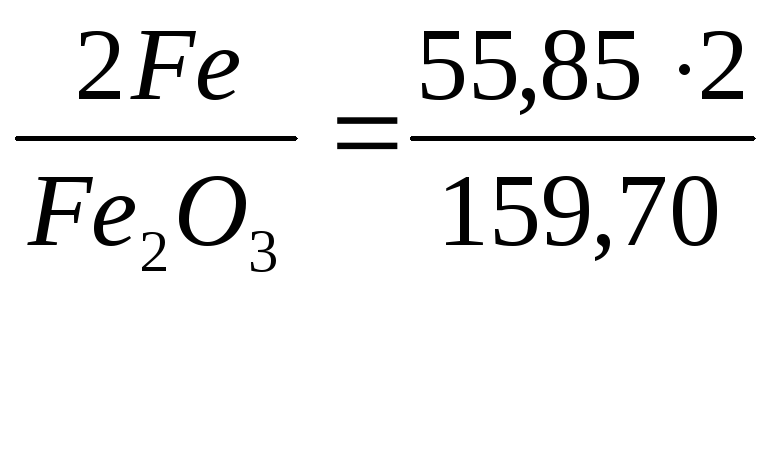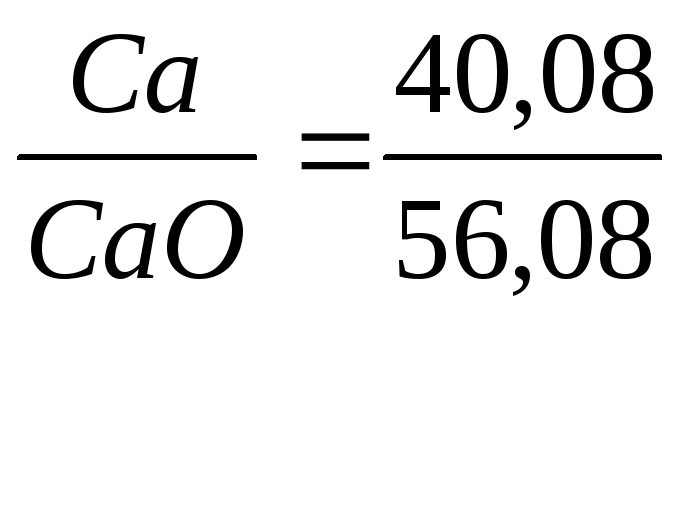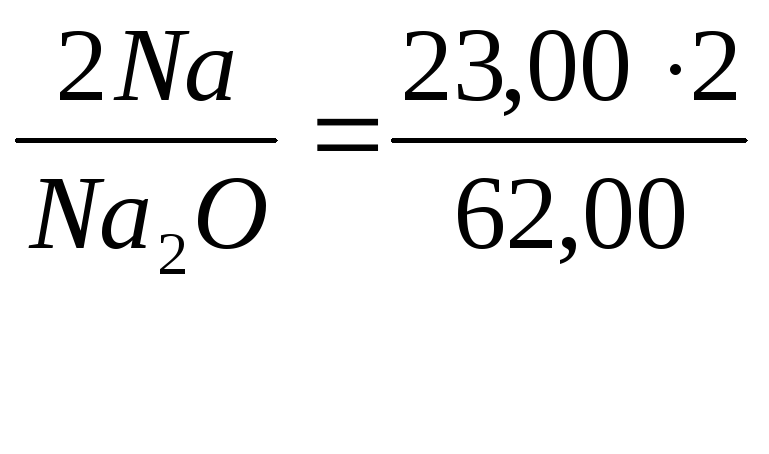- •Практическое руководство по химии почв
- •Введение
- •Раздел I. Валовой анализ
- •1.1. Способы разложения почв
- •1.1.1. Разложение почв кислотами.
- •1.1.2. Разложение почв сплавлением.
- •1.1.3. Разложение почвы спеканием.
- •1.2. Определение гигроскопической влажности
- •1.3. Определение потери при прокаливании
- •1.4. Спекание почвы с содой
- •1.5. Анализ элементного состава почв
- •1.5.1. Определение кремния желатиновым методом
- •Пример расчета. Для спекания взято 1,0224 г прокаленной почвы. Прокаленный осадок SiO2 весит 0,8014 г. Содержание SiO2 равно:
- •1.5.2. Определение полуторных оксидов гравиметрическим методом
- •1.5.3. Определение железа фотометрическим методом
- •1.5.4. Определение алюминия фотометрическим методом
- •1.5.5.Вычисленное содержание алюминия по разности
- •1.5.6. Определение кальция и магния комплексонометрическим методом
- •1.5.6.1. Определение кальция
- •1.5.6.2. Определение суммы кальция и магния
- •1.5.7. Пероксидный метод определения титана
- •1.5.8. Определение фосфора фотометрическим методом
- •1.6. Способы выражения результатов валового анализа
- •1.7. Пересчеты данных валового анализа
- •1.8. Использование данных валового анализа
- •1.8.1. Использование элементного состава для суждения о генезисе почв.
- •1.8.2. Использование элементного состава для оценки потенциального плодородия почвы.
- •1.8.3. Использование данных элементного состава для расчета молекулярных отношений
- •1.8.4. Использование данных элементного состава для расчета запасов химических элементов
- •Пример расчета. Найти запас SiO2 в т/га если его содержание равно 80,63 %, плотность сложения почвы 1,18 г/см3, мощность слоя 9 см.
- •1.8.5. Использование данных элементного состава при изучении биологического круговорота веществ
- •1.8.6. Использование данных элементного состава для
- •1.8.6.1. Метод прямого сравнения
- •1.8.6.2. Методы стабильного компонента
- •1.8.6.2.1. Метод молекулярных отношений
- •1.8.6.2.2. Метод элювиально-аккумулятивных (еа) коэффициентов
- •1.8.6.2.3. Метод баланса веществ
- •1.8.7. Использование данных элементного состава для диагностики минералов илистой фракции.
- •Контрольные вопросы
- •Литература
- •Раздел II. Ионно-солевой комплекс почв
- •2.1. Метод водной вытяжки
- •2.1.1. Влияние солей на сельскохозяйственные культуры
- •2.1.2. Достоинства и недостатки водной вытяжки как метода изучения засоленных почв
- •2.1.3 Анализ водной вытяжки
- •2.1.3.1. Определение величины рН водной вытяжки
- •2.1.3.2. Определение величины сухого остатка
- •2.1.3.3. Определение величины прокаленного остатка
- •2.1.3.4. Определение щелочности от растворимых карбонатов
- •2.1.3.5. Определение общей щелочности
- •2.1.3.6. Определение хлорид-ионов
- •2.1.3.7. Определение сульфат-ионов
- •2.1.3.8. Определение ионов кальция и магния комплексонометрическим методом
- •2.1.3.8.1. Определение кальция
- •2.1.3.8.2. Определение суммы кальция и магния
- •2.1.3.9. Определение натрия и калия
- •2.1.3.9.1. Определение натрия и калия методом фотометрии пламени
- •2.1.3.9.2. Определение содержания натрия и калия по разности
- •Форма 4. Данные анализа водной вытяжки
- •2.1.4. Интерпретация данных водной вытяжки
- •2.1.4.1. Характеристика солевого режима почв по величине сухого остатка
- •2.1.4.2. Оценка химизма (типа) засоления почв.
- •2.1.4.2.1. Общие принципы оценки химизма засоления почв
- •2.1.4.2.2. Оценка степени засоления почв по содержанию токсичных ионов
- •2.1.4.2.3. Оценка степени засоления почв по «суммарному эффекту» токсичных ионов
- •2.1.5. Расчет промывной нормы
- •2.2. Катионообменная способность почв
- •2.2.1. Общие представления о катионообменной
- •2.2.2. Методы определения катионообменной способности почв
- •2.2.2.1. Оценка эффективной емкости катионного обмена
- •2.2.2.2. Определение стандартной емкости катионного обмена по Бобко-Аскинази в модификации цинао
- •2.2.2.3. Определение суммы обменных оснований методом Каппена-Гильковица
- •2.2.2.4. Определение гидролитической кислотности
- •2.2.2.5. Определение обменных катионов по методу Пфеффера в модификации в.А. Молодцова и и.В. Игнатовой
- •2.2.2.5.1. Определение кальция комплексонометрическим методом
- •2.2.2.5.2. Определение суммы кальция и магния комплексонометрическим методом
- •2.2.2.5.3. Определение натрия и калия методом фотометрии пламени
- •2.2.3. Использование результатов определения катионообменной способности почв
- •2.2.3.1. Вычисление степени насыщенности почв основаниями
- •2.2.3.2. Расчет дозы извести
- •2.2.3.3. Вычисление степени солонцеватости почв
- •2.2.3.4. Расчет дозы гипса
- •Контрольные вопросы
- •Литература
- •Раздел III. Органическое вещество почвы
- •3.1. Подготовка почвы для определения содержания и состава гумуса
- •3.2. Методы определения содержания общего гумуса почвы
- •3.2.1. Прямые методы определения содержания углерода органических соединений (гумуса) почвы.
- •3.2.2. Косвенные методы определения содержания углерода органических соединений (гумуса) почвы
- •3.2.2.1. Определение гумуса методом и.В.Тюрина в модификации в.Н.Симакова
- •3.2.2.2. Другие модификации метода и.В. Тюрина.
- •3.2.2.2.1. Спектрофотометрический метод определения содержания гумуса (д.С. Орлов, н.М. Гриндель)
- •3.2.2.2.2. Определение содержания органического углерода почвы методом и.В.Тюрина в модификации б.А.Никитина.
- •3.3. Методы определения общего содержания азота почвы.
- •3.3.1. Определение общего содержания азота методом Кьельдаля.
- •3.3.2. Определение общего содержания азота микрохромовым методом и.В. Тюрина.
- •3.4. Использование данных по содержанию общего гумуса и азота
- •3.4.1. Расчет отношения c:n
- •3.4.2. Вычисление запасов гумуса, углерода и азота.
- •3.5. Методы определение группового и фракционного состава гумуса.
- •3.5.1. Определение группового и фракционного состава гумуса по методу и.В. Тюрина в модификации в.В.Пономаревой и т.А.Плотниковой
- •3.5.2. Определение группового и фракционного состава гумуса по модифицированной схеме в.В.Пономаревой и т.А. Плотниковой (т.А. Плотникова, н.Е. Орлова, 1984).
- •Ход анализа
- •3.5.3. Ускоренный пирофосфатный метод определения состава гумуса по м.М. Кононовой и н.П. Бельчиковой
- •3.6. Методы изучения некоторых свойств гумусовых кислот при анализе фракционно-группового состава гумуса
- •3.6.1. Определение порога коагуляции гуминовых кислот.
- •3.6.2. Оптические свойства гумусовых веществ.
- •3.6.2.1. Электронные спектры поглощения гумусовых веществ
- •3.6.2.2. Определение коэффициента цветности q4/6
- •3.6.3. Гель-хроматография гумусовых веществ
- •3.7. Показатели гумусового состояния почв
- •Продолжение таблицы 31
- •3.8. Методы определения содержания и состава органического вещества в болотных торфяных почвах.
- •3.8.1. Определение потери при прокаливании и зольности торфа.
- •3.8.2. Одновременное определение общего содержания углерода и азота в торфяных почвах методом Анстета в модификации в.В. Пономаревой и т. А. Николаевой
- •Вычисление результатов анализа
- •Для анализа используют следующие реактивы:
- •3.8.3. Определение общего содержания азота в растительных материалах (торфах, лесных подстилках и пр.) методом к.Е. Гинзбурга и г.М. Щегловой
- •3.8.4. Определение содержания органического азота в вытяжках из торфов микрохромовым методом и.В. Тюрина
- •3.8.5. Определение состава органического вещества торфяно-болотных почв по методу в.В. Пономаревой и т.А. Николаевой.
- •Контрольные вопросы
- •Литература
- •Раздел I. Валовой анализ ……………………………………
- •Раздел II. Ионно-солевой комплекс почв ……………………
- •Раздел III. Органическое вещество почв
1.6. Способы выражения результатов валового анализа
Результаты валового анализа обычно выражаются в виде процентного содержания высших оксидов элементов, входящих в состав почвы и определяемых в ходе анализа: SiO2, Al2O3, Fe2O3, CaO, MgO, Na2O, K2O, TiO2, MnO, SO3, P2O5 . Это традиционный и широко распространенный способ представления аналитических данных, дающий возможность быстрой проверки точности выполнения анализа.
Для проверки точности результатов анализа суммируют содержание всех оксидов, вычисленное в % от массы сухой почвы вместе с величиной потери при прокаливании (п.п.). Эта сумма должна быть равной 100% или отклоняться в пределах ±1,0-1,5%. В качестве примера аналитического баланса рассмотрим данные валового анализа приведенного в таблице 4.
Таблица 4. Валовой состав горизонта А1 (8-14 см) дерново-слабоподзолистой почвы в % от массы абсолютно сухой почвы
|
Оксид |
Содержание, % |
Оксид |
Содержание, % |
|
SiO2 |
77,29 |
K2O |
1,73 |
|
Al2O3 |
10,12 |
TiO2 |
0,53 |
|
Fe2O3 |
2,48 |
MnO |
0,20 |
|
CaO |
0,88 |
SO3 |
0,58 |
|
MgO |
0,66 |
P2O5 |
0,19 |
|
Na2O |
1,48 |
п.п |
4,13 |
|
Сумма = 100,27 | |||
Поскольку отклонение от 100% не превышает указанного предела, то точность анализа следует считать удовлетворительной.
Значительные отклонения суммы от 100%, как в меньшую, так и большую стороны, обусловлены ошибками, допущенными в ходе выполнения валового анализа. Сумма оксидов больше 100% – следствие плохого промывания и прокаливания осадков, сумма оксидов меньше 100% обусловлена потерей анализируемых веществ.
При интерпретации данных валового анализа необходимо иметь в виду, что выражение его результатов в форме процентного содержания высших оксидов являются условными и не совсем точными. Во-первых, элементы с переменной валентностью (Fe, Mn, S) могут находиться в почве в разных степенях окисления, во-вторых – только Si, Ti, Fe и Al частично присутствуют в почвах в форме высших оксидов в различной степени окристаллизованности. Остальные оксиды не могут существовать в почве в свободном состоянии. Кроме того, выражение результатов в форме оксидов исключает представление о соотношении количеств различных элементов. Это обусловлено тем, что у оксидов разных элементов неодинакова массовая и мольная доля кислорода.
Например, доля Р в составе P2O5 составляет 44% от массы оксида, а доля К в составе K2O равна 83%. Если судить по приведенным выше данным, то в горизонте А1 дерново-слабоподзолистой почвы содержится в 9 раз больше калия (1,73%) нежели фосфора (0,19%). При пересчете на элементы содержание калия оказывается равным 1,44%, фосфора – 0,08%. В этом случае количество К будет в 18 раз превосходить количество фосфора. Аналогичные примеры можно привести и в отношении других элементов. Следовательно, данные валового анализа, выраженные в форме оксидов не дают реального представления о содержании в почве химических элементов и их соотношениях. Данное обстоятельство имеет важное значение, поскольку количественные отношения между содержанием отдельных элементов широко используется для решения многих химических и агрономических вопросов.
Чтобы пересчитать оксиды на элементы необходимо содержание оксида в процентах умножить на соответствующий коэффициент. Коэффициент представляет собой частное от деления атомной массы определенного элемента на молекулярную массу соответствующего оксида (табл. 5)
Таблица 5. Пересчетные коэффициенты оксидов на элементы
|
Оксид |
Элемент |
Отношения |
Пересчетный коэффициент |
|
SiO2 |
Si |
|
0,468 |
|
Al2O3 |
Al |
|
0,529 |
|
Fe2O3 |
Fe |
|
0,699 |
|
CaO |
Ca |
|
0,715 |
|
MgO |
Mg |
|
0,603 |
|
TiO2 |
Ti |
|
0,599 |
|
MnO |
Mn |
|
0,774 |
|
SO3 |
S |
|
0,400 |
|
P2O5 |
P |
|
0,436 |
|
K2O |
K |
|
0,830 |
|
Na2O |
Na |
|
0,742 |
Правильная оценка химического состава почвы затруднена также вследствие того, что результаты валового анализа, даже если они представлены не в форме оксидов, а в элементах, выражаются в массовых процентах. Поскольку в химических реакциях и процессах участвуют ионы и молекулы, то и конечный результат будет зависеть от того, сколько их вступило во взаимодействие или было вовлечено в профильную дифференциацию веществ. Поэтому, итог процесса, его интенсивность должны быть выражены количеством частиц вещества, а не его массой.
В качестве примера обратимся к данным валового анализа горизонта А1 дерново-слабоподзолистой почвы. Здесь содержание Al2O3 = 10,12%, Fe2O3 – 2,48%, K2O – 1,73%. В пересчете на элементы это составляет 5,35% Al, 1,73% Fe и 1,44% К. По массе содержание алюминия в 3,1 раза превышает содержание Fe, однако атомные массы этих элементов существенно различаются и равны 26,98 и 55,85 для алюминия и железа соответственно. Вследствие этого в 100 г почвы будет содержаться 0,20 моля алюминия и 0,03 моля железа. Следовательно, по числу атомов алюминий будет превышать железо в 6,7 раза.
При сопоставлении железа и калия получается иная картина. Если по массе содержание железа в 1,2 раза превосходит содержание К, то по числу молей в 100 г почвы обнаруживается преобладание калия над железом – 0,05 моля калия и 0,03 моля железа соответственно.
Эти примеры показывают, что способ выражения данных валового анализа имеет важное значение для правильного суждения о состоянии химических элементов в почве. Поэтому, для получения объективной информации о химическом составе почвы, особенностях его трансформации, закономерностях миграции и аккумуляции элементов наиболее целесообразно выражать результаты валового анализа в молях на определенную массу или объем почвы.
В международной системе единиц измерения (СИ), моль – это количество вещества, содержащее столько же структурных элементов, сколько атомов содержится в 12 г изотопа углерода 12С, а именно 6,022∙1023 (число Авогадро). Структурными элементами наряду с атомами могут быть молекулы, ионы, электроны и другие частицы. Чтобы найти число молей элемента в 100 г почвы, нужно его процентное содержание в почве разделить на атомную массу. В таблице 6 приведен элементный состав темно-серой лесной легкосуглинистой почвы, выраженный различными способами.
Таблица 6. Элементный состав темно-серой лесной почвы в расчете на абсолютно сухую навеску
|
I. Содержание оксидов в % от массы почвы | ||||||||
|
Горизонт |
Глубина образца, см |
SiO2 |
Al2O3 |
Fe2O3 |
CaO |
MgO |
Na2O |
K2O |
|
А1 |
0-10 |
72,75 |
10,09 |
2,32 |
0,88 |
0,72 |
1,41 |
1,74 |
|
АВ |
29-39 |
75,70 |
11,48 |
3,52 |
0,70 |
0,65 |
1,52 |
1,96 |
|
В1 |
50-60 |
74,26 |
11,94 |
4,18 |
0,71 |
0,76 |
1,47 |
1,74 |
|
В2 |
70-80 |
72,18 |
14,42 |
4,49 |
0,71 |
0,69 |
1,58 |
1,66 |
|
ВС |
140-150 |
73,53 |
13,03 |
4,49 |
0,77 |
0,72 |
1,54 |
1,65 |
|
II. Содержание элементов в % от массы почвы | ||||||||
|
Горизонты |
Глубина образца, см |
Si |
Al |
Fe |
Ca |
Mg |
Na |
K |
|
А1 |
0-10 |
34,05 |
5,34 |
1,62 |
0,63 |
0,43 |
1,05 |
1,44 |
|
АВ |
29-39 |
35,43 |
6,07 |
2,46 |
0,50 |
0,39 |
1,13 |
1,63 |
|
В1 |
50-60 |
34,75 |
6,32 |
2,92 |
0,51 |
0,46 |
1,09 |
1,44 |
|
В2 |
70-80 |
33,78 |
7,63 |
3,14 |
0,51 |
0,42 |
1,17 |
1,38 |
|
ВС |
140-150 |
34,41 |
6,89 |
3,14 |
0,55 |
0,43 |
1,14 |
1,37 |
|
Ш. Содержание элементов в моль/100 г почвы | ||||||||
|
Горизонты |
Глубина образца, см |
Si |
Al |
Fe |
Ca |
Mg |
Na |
K |
|
А1 |
0-10 |
1,21 |
0,20 |
0,029 |
0,016 |
0,018 |
0,046 |
0,037 |
|
АВ |
29-39 |
1,26 |
0,23 |
0,044 |
0,013 |
0,016 |
0,049 |
0,042 |
|
В1 |
50-60 |
1,24 |
0,23 |
0,052 |
0,013 |
0,019 |
0,047 |
0,037 |
|
В2 |
70-80 |
1,20 |
0,28 |
0,056 |
0,013 |
0,017 |
0,051 |
0,035 |
|
ВС |
140-150 |
1,23 |
0,26 |
0,056 |
0,014 |
0,018 |
0,050 |
0,035 |
По весовому содержанию оксиды располагаются в следующий убывающий ряд:
SiO2 >>Al2O3> Fe2O3> K2O >Na2O >CaO, MgO.
При пересчете на элементы этот ряд сохраняется, но соотношения между элементами изменяются. Так если в пределах профиля в весовом отношении Al в 2,2-4,4 преобладает над Fe, то по числу атомов в 4,3-6,9 раза. По массе кальция содержится несколько больше чем магния, а калий преобладает над натрием, однако по числу атомов обнаруживается уже некоторое доминирование Mg над Ca и Na над К. Эти примеры показывают, что выбор способа выражения результатов валового анализа имеет принципиальное значение для правильного суждения об особенностях химического состава почвы.