
- •Триада Селье (стресса):
- •Стадия истощения.
- •3. Дыхательная недостаточность, её проявления. Изменения газового состава артериальной крови на различных стадиях дыхательной недостаточности.
- •2. Аллергические реакции III (иммунокомплексного) типа. Этиология, патогенез, клинические проявления. Патогенез сывороточной болезни. Аллергические реакции III типа (иммунокомплексные)
- •3. Хроническая почечная недостаточность; формы, причины, механизмы развития и клинические проявления. Уремическая кома.
- •2. Аллергия. Общая характеристика и значение в патологии. Связь аллергии и иммунитета. Аллергены и антитела, их виды и особенности. Стадии аллергической реакции.
- •3. Коронарная недостаточность; характеристика понятия, виды.
- •3. Острая артериальная гипотония; причины, виды и механизмы коллапса.
- •3. Нефрозы; формы, этиология, патогенез и основные клинические проявления.
- •Нефротический синдром
- •Этиология
- •Патогенез острого нефротического синдрома
- •Патогенез хронического нефротического синдрома
- •2. Изменения обмена веществ, структуры клеток и функции органов при лихорадке. Участие нервной, иммунной и эндокринной систем в развитии лихорадки. Отличие лихорадки от гипертермии.
- •3. Боль; причины и механизмы возникновения, значение для организма. Принципы обезболивания.
- •2. Местные и общие клинические проявления воспаления, их патогенез.
- •Местные (кардиальные) признаки воспаления
- •Общие признаки воспаления
- •3. Аллергические (инфекционно-аллергические) заболевания почек, Гломерулонефрит; формы, этиология, патогенез и клинические проявления, исходы.
- •Острый гломерулонефрит
- •Этиология
- •Патогенез иммунопатологического гломерулонефрита
- •2. Причины, механизмы развития, изменения газового состава артериальной и венозной крови при экзогенной, дыхательной, сердечно-сосудистой, кровяной и тканевой гипоксии. Смешанная гипоксия.
- •3. Печёночная кома; общая характеристика, виды, патогенез, клинические проявления и механизмы возникающих расстройств.
- •3. Этиология, патогенез и клинические проявления тромбофилического синдрома. Принципы лекарственной коррекции расстройств гемостаза.
- •2. Экссудация; изменения местного кровообращения и микроциркуляции, выход жидкой части крови в ткань и развитие отёка, их механизмы и значение. Виды и состав экссудатов.
- •3. Вторичные, симптоматические гипертонии (лекарственная, почечная, эндокринная, рефлексогенная и др.). Этиология, патогенез, клинические проявления, последствия, осложнения.
- •2. Общая характеристика гипоксии. Устойчивость разных органов и тканей к кислородному голоданию, факторы, определяющие устойчивость. Основные типы гипоксии.
- •3. Основные проявления расстройств деятельности почек, их происхождение. Изменения диуреза, состава мочи и крови; отёки, артериальная гипертония.
- •2. Лекарственная аллергия. Аутоаллергия.
- •1 Тип аллергии – реагеновый, атопический и анафилактический
- •Аллергические реакции I типа
- •(Реагиновые, атопические, анафилактические)
- •3. Ишемическая болезнь сердца; этиология, патогенез. Стенокардия, инфаркт миокарда; ведущие клинические проявления.
- •2. Аллергические реакции I (анафилактического, атопического) типа. Этиология, патогенез, клинические проявления. Патогенез бронхиальной астмы. Принципы лекарственной терапии.
- •1 Тип аллергии – реагеновый, атопический и анафилактический
- •Аллергические реакции I типа
- •(Реагиновые, атопические, анафилактические)
- •2. Пирогенные вещества; их химическая природа и места образования. Первичные и вторичные пирогены; лейкоцитарные пирогены (интерлейкин-I). Механизмы действия пирогенов.
- •2. Эмиграция клеток, ее молекулярные и другие механизмы. Фагоцитоз; виды, стадии, механизмы. Пролиферация; механизмы формирования и роль при воспалении.
- •2. Аллергические реакции замедленного типа (гзт) Этиология, патогенез, клинические проявления. Принципы лекарственной терапии.
- •Аллергическая реакция IV типа (туберкулиновая, клеточная, гзт)
- •Аллергические реакции IV типа
- •(Замедленного, клеточного, туберкулинового)
- •3. Патологическая гипертрофия миокарда, стадии, механизмы декомпенсации сердца.
- •Дыхательный (газовый) алкалоз
- •3. Артериальные гипотонии. Виды, причины и механизмы развития. Понятие о гипотонической болезни. Проявления и последствия гипотонических состояний.
- •Бронхо-легочная дыхательная недостаточность
- •3. Токсикомании; алкоголизм, наркомании и лекарственная зависимость. Этиология, механизмы формирования, клинические проявления на разных стадиях развития, исходы.
- •Билет 38
- •Триада Селье (стресса):
- •Стадия истощения.
- •Патогенез «шоковго легкого»
- •Синдром длительного раздавливания
- •(Краш-синдром)
- •Ожоговый шок
- •Шок в результате электротравмы
- •Кардиогенный шок
- •Гиповолемический шок
- •Постгемотрансфузионный шок
- •Токсико-септический шок
- •Травматический шок
- •Синдром длительного раздавливания
- •(Краш-синдром)
- •Ожоговый шок
- •Шок в результате электротравмы
- •Кардиогенный шок
- •Гиповолемический шок
- •Постгемотрансфузионный шок
- •Токсико-септический шок
- •Бронхо-легочная дыхательная недостаточность
- •2. Общие и специфические механизмы развития и клинические проявления коматозных состояний.
- •3. Коронарная недостаточность; характеристика понятия, виды.
- •3. Вторичные, симптоматические гипертонии (лекарственная, почечная, эндокринная, рефлексогенная и др.). Этиология, патогенез, клинические проявления, последствия, осложнения.
- •2. Проявление повреждения клетки в изменении обмена веществ, ее структуры и функции. Понятие о специфических и неспецифических проявлениях повреждения; обратимых и необратимых повреждениях.
- •3. Перегрузочная сердечная недостаточность. Понятие о перегрузке объёмом и давлением крови. Причины, механизмы развития и патоморфология перегрузочной недостаточности сердца.
- •2. Гипергидратация; виды, причины возникновения, механизмы развития, проявления и последствия. Принципы предупреждения и лечения гипергидратации.
- •3. Артериальные гипотонии. Виды, причины и механизмы развития. Понятие о гипотонической болезни. Проявления и последствия гипотонических состояний.
- •2. Патогенез сердечных, почечных, токсических, аллергических, голодных отёков. Местные и общие нарушения в тканях при отёках, их клинические проявления.
- •3. Боль; причины и механизмы возникновения, значение для организма. Принципы обезболивания.
- •3. Патологическая гипертрофия миокарда, стадии, механизмы декомпенсация сердца.
- •2. Гипероксия. Причины возникновения, формы. Механизмы повреждающего действия кислорода. Роль свободно-радикальных процессов. Понятие о системе антиокислительной защиты организма.
- •3. Виды, этиология, патогенез и клинические проявления геморрагических диатезов. Роль наследственных факторов, а также иммунопатологических механизмов в их патогенезе.
Прежде чем пациента вытащит из под завала на конечность выше повреждения наложить жгут, и начать реанимационные мероприятия. Далее оценить конечность, при показаниях – ампутации. При возможности сохранить конечность, жгут периодически снимают.
Ожоговый шок
Основные механизмы
Значительная болевая афферентация от обожженной кожи и мягких тканей.
Выраженная дегидратация в результате плазмопотери повышенная вязкость крови, сладжитромбообразование, расстройства микроциркуляции.
Выраженная интоксикация организма, ей способствуют:
Продукты термической денатурации белка и протеолиза.
Избытком образующихся при повреждении тканей (кинины, биогенные амины, олиго- и полипептиды и др.);
Токсинами микробов.
Развитие аутоиммунной реакции.
Особенности течения.
Длительная нейроэндокринная (эректильная) фаза, которая резко переходит в гемодинамическую (торпидную).
Частое поражение почек, обусловленное нарушением их кровоснабжения и гемолизом эритроцитов.
Шок в результате электротравмы
Основные механизмы
Нарушение электрических процессов в мозге и сердце (проводящей системе).
Электролиз воды образование свободных радикаловповреждение мембранных структуринтоксикация.
Особенности течения
Отсутствует нейроэндокринная (эректильная) фаза
Отсутствие сознания
Тяжелые нарушения гемодинамики
Кардиогенный шок
Основные механизмы
Выраженный болевой синдром
Снижение насосной функции сердца на фоне роста общего периферического сопротивления сосудов
Аритмии
Особенности течения
Отсутствует эректильная фаза
Развитие кардиогенного отека легких
Гиповолемический шок
Основные механизмы
Снижение объема циркулирующей крови
Рост ОПСС
Особенности течения
Выражены все 3 стадии шока.
Дефицит ОЦК усугубляется патологическим депонированием крови.
Выражена гемическая гипоксия.
Постгемотрансфузионный шок
Основные механизмы
Агглютинация эритроцитов перераздражение рефлексогенных зонрефлекторная гипотония сосудов.
Гемолиз эритроцитов и фагоцитоз агглютинатов выход тканевого и макрофагального тромбопластинаДВС-синдром.
Особенности течения
Нарушение кровоснабжения почек пре- и ренальная ОПН.
Закупорка клубочков агглютинатами
Гемолиз эритроцитов гемическая гипоксия
Гемолиз эритроцитов и гипербилирубинемия интоксикация
Анафилактичсекий шок
Основные механизмы
Действие БАВ:
Гистамин спазм сфинктеров печеночных венпатологическое депонирование крви в системе воротной веныгиповолемия.
Гистамин отрицательно инотропное и положительное хронотропное действие на средце.
Брадикини гипотония сосудов.
Гистамин, серотонин, брадикин, лейкотриены повышение проницамости сосудистой стенкиплазмопотеря.
Гистамин и лейкотриены С4, Е4, Д4 спазм гладкой мускулатуры бронховповышение функции слизеобразующих желез – обструктивная дыхательная недостаточность.
Серотонин активирует тромбоциты; брадикин активирует фактор Хагемана; гепарин обладает антитромбиновым эффектом тромбогеморрагический синдром.
Токсико-септический шок
Основные механизмы
Выраженная интоксикация.
Экзотоксин Гр+ микроорганизмов клеточный протеолизплазмокининыВазоплегия.
Эндотоксин Гр- микроорганизмов стимуляция мозгового слоя надпочечников и симпатической нервной системыгипердинамия сердцасменяется гиподинамией.
Токсемия – поражение печени, почек, миокарда.
Лихорадка.
Стимуляция выработки макрофагального тромбопластина раннее развитие ДВС-синдрома.
Шок
Типический патологический процесс.
Возникает под воздействием сверхсильных, нередко разрушительных чрезвычайных факторов.
Характеризуется стадийным прогрессирующим расстройством жизнедеятельности организма.
В результате нарастающего нарушения функций нервной, эндокринной, сердечнососудистой и других жизненно важных систем.
Коллапс
Остро развивающееся состояние
В результате значительного несоответствия ОЦК и емкости сосудистого русла.
Характеризуется резким снижение АД, недостаточности кровообращения, расстройством функции тканей, органов и систем.
3. Этиология, патогенез и клинические проявления тромбофилического синдрома. Принципы лекарственной коррекции расстройств гемостаза.
Тромбофилии:
Претромботические состояния – основа для тромбоза – склонность.
Тромбоз.
Основные механизмы тромбофилий:
Нарушение тромборезистентности сосудистой стенки: травма, васкулиты, ангиопатии, атеросклероз, вазоспазм.
Нарушение тока крови: турбулентный характер, замедление. Чаще в венозных сосудах, т.к медленный кровоток.
Варикозное расширение вен.
Аневризмы сердца и сосудов.
Атеросклероз, вазоспазм.
Патология форменных элементов крови:
Тромбоцитоз.
Активация тромбоцитов.
Эритремия – опухолевые заболевания – костный мозг производит большое количество эритроцитов.
Внутрисосудистый гемолиз эритроцитов.
Патология факторов системы гемостаза:
Активация прокоагулянтов.
Недостаток факторов фибринолиза.
Чрезмерная активация прокоагулянтов и проагрегантов:
Гиперлипопротеидемия.
Повышение уровня антифосфолипидных антител.
Массивные травмы мягких тканей, ожоги большой площади, шок, сепсис.
Увеличение в крови прокоагулянтов и проагрегантов:
Гиперкатехоламинемия.
Гиперкортицизм.
Атеросклероз артерий.
Септицемия.
Угнетение содержания и/или активности антикоагулянтов:
Наследственный дефицит антитромбина или снижение его сродства к гепарину.
Наследственный дефицит протеина С и S.
Вторичный дефицит при почечной, печеночной или панкреатической недостаточностях, сахарном диабете, лейкозах, респираторная дистерсс-синдроме, массивной травме.
Гиперлипопротеинемия.
Уменьшение уровня и/или подавление активности фибринолитиков:
Подавление синтеза активатора плазминогена (атеросклероз, ревматоидный артрит).
Гиперпродукция антплазмина.
Снижение продукции фактора XII (хагемана) при васкулите.
Претромботические состояния.
Диагностируются:
Снижение АВР
Снижение АЧТВ
Снижение тромбинового времени
Снижение времени агрегации тромбоцитов на стекле
Снижение времени спонтанного эуглобулинового лизиса
Повышение ПДФ
Толерантность плазмы к гепарину < 7 мин (в норме 7-11 минут)
Помощь: антиагреганты (аспирин).
Тромботические состояния
Диагностируются:
Снижение АВР
Снижение АЧТВ
Снижение тромбинового времени
Снижение времени агрегации тромбоцитов на стекле
Повышение времени спонтанного эуглобулинового лизиса
Повышение ПДФ
Толерантность плазмы к гепарину < 3 минут (в норме 7-11 минут)
Помощь: фибринолитик, перед его назначением обязательно нужно заблокировать свертывание крови – сначала назначают гепарин. И потом на фоне гепаринизации назначается фибринолитик.
Билет 43
2. Общая характеристика понятия, виды и основные патогенетические факторы развития коматозных состояний. Значение экзогенных и эндогенных интоксикаций, а также поражений центральной нервной системы в возникновении и развитии комы. Алкогольное и лекарственное отравление как причина комы.
Кома:
Общее, крайне тяжелое состояние организма.
Возникает в результате действия экзо- и эндогенных повреждающих факторов.
Характеризуется угнетением нервной деятельности, потерей сознания, гипо- и арефлексией, недостаточности функции органов и систем органов.
Комы:
Вследствие локального повреждения мозга
Вследствие энцефалопатий, распространенных в переделах всего головного мозга.
Локальные повреждения:
Трафматические – субдуральная гематома, эндуральная гематома, ушиб или сотрясение головного мозга.
Сосудистые паталогии – кровоизлияние в полость черепа или мозговую ткань, как осложнение гипертонической болезни, разрыв сосудистой аневризмы; инфаркт мозга вследствие тромбоэмболии мозговых сосудов.
Инфекционные – менингит, энцефалит, абсцесс.
Злокачественный клеточный рост: метастазы опухолей головного мозга, опухоли самого мозга, паранеопластические поражения мозговой ткани.
Локальный гипоэрго: в результате эпилептического статуса, после припадка
Факторы, способствующие нарушению всего ГМ:
Эндокринопатологии:
Гипофункция: инсулиновая недостаточность, микседема, гипокортицизм.
Гиперфункция: гиперинсулинизм, гипертиреоз
Нарушения газового состава крови:
Артериальная гипоксемия
Гиперкапния
Расстройства водно-электролитного обмена:
Гиперосмия
Гипоосмия
Гипонатриемия (<100 ммоль/л)
Гипокалиемия (<2 ммоль/л)
Гипомагниемия
Гиперкальциемия
Гипокальциемия
Гипохлоремия
Нарушения энергетического обмена:
Гипоксия
Голодание
Интоксикации:
Эндогенные:
Уремическая
Печеночная
Кетоацидотическая
Экзогенные:
Отравления угарным газом
Спиртами (метиловым, этиловым)
Тяжелыми металлами
Наркотиками и галлюциногенами
Побочные действия лекарств:
Наркотических анальгетиков
Барбитуратов
Трициклических антидепрессантов
Анестетиков-галлюциногенов
Нейролепткиов
Неблагоприятные действия факторов внешней среды:
Гипотермия
Гипертермия
Лучевая энергия
Значительные колебания барометрического давления
Патогенез ком
Первичная альтерация нервных клеток – к этому приводит воспаление, сотрясение, ушиб мозга, разможжение тканей мозга, расстройства мозгового кровообращения и ликворо-динамики.
На фоне гипоксии угнетаются аэробные процессы, стимулируется анаэробный гликолиз. Результатом гипоксии является уменьшение энергоемких соединений – АТФ и КФ, возрастают неорганические фосфаты – АДФ и АМФ. При этом нарушается биосинтез белков (липопротеидов, нуклеопротеидов), угнетается образование нейромедиаторов (необходимы для функции мозга), нарушается работа ионных каналов – формируется электроитный дисбаланс нейронов. Процессы белкового распада, катаболизм азотистых соединений преобладают над синтезом увеличивается содержание аммиака.
Дефицит энергии приводит к уменьшению образованию ДА, НА иАХ. С другой стороны уменьшается распд, инактивация ГОМК (гамма – оксимасляная) и ГАМК. Результат – снижение возбудимости и способности к проведению нервных импульсов.
Важный механизм – расстройство мозгового кровообращения. Нарушается тонус прекапиллярных сфинктеров. Повышению тонуса сфинктеров способствуют: артериальная гипертензия, гипокапния, гипероксия. Снижают тонус: артериальная гипотензия, гипоксемия, гиперкапния, лактоцидоз. Кроме того нарушению кровообращения способствуют БАВ.
Расстройство мозгового кровообращения является очень важным факторов в формировании отек-набухании. Изменение осмотического давления в крови (особенно низкое), гипоонкия и гипоосмия крови; повышение внутричерепного давления; снижение церебрального диффузионного давления гипоксия мозга; нарушение активности транспорта электролитовнакопление натрия в клетках --- все это ведет к отеку-набуханию.
Гипоксия сопровождается увеличением концентрации катехоламинов (в частности НА), активации и пероксидации липидов. Увеличение НА способствует активации аденилатциклазы -- увеличивается цАМФ—накопление кальция в саркоплазме клеток – активация фосфолипазы – способствует повреждению мембран митохондрий и лизосом. Повреждение мембран – вторичная альтерация.
Поверждение мембран клеток – подавление кальцийсвязывающей способности саркоплазмотический сети и саркоплазма – кальций накапливается в цитоплазме – разобщение окисления и фосфорилирования – снижение АТФ и КФ.
Нарушается пластическое обеспечение нервных клеток. Особенно снижается синтез РНК, белков, фосфолипидов. В результате нарушения повреждаются внутриклеточные ультраструктуры. При этом в клетке накапливаются незаменимые аминокислоты (гистидин, лейцин, фенилаламин), и снижаются заменимые (треонин, глютамин).
В продолговатом мозге – ДЦ, СДЦ. Как результат поражения СДЦ – снижение АД, нарушение функций сердца (аритмии). Результат повреждения ДЦ – центрогенная ДН.
Формируестя полиорганная недостаточность:
Поражение головного мозга сопровождается – нарушение дыхания, системного кровообращения, функций печени и ЖКТ, кислотно-щелочного, водно-электролитного баланса. Эндотоксикоз – нарушение свертывания крови – ишемия почек – кортикальный некроз – ОПН
Поражение головного мозга: нарушение системного кровообращения – шунтирование кровотока печени – циркулятроная гипоксия паренхимы печени – высвобождение ферритина – вазодилатация. От циркуляторной гипоксии печени – нарушение энергоообразования – нарушений функций печени: мочевинообразования, синтеза белка и факторов свертывания, гликогенеза, окисления кетокислот, дезаминирования аминокислот, экскреции.
Нарушение системного кровообращения – спазм сосудов брюшной стенки:
Угнетенеи секреторной и моторной функции ЖКТ – активация брожения и гниения – проникновение токсинов в кровь
Гипоксия – повышение проницаемости сосудов:
проникновение токсинов в кровь
отек кишечной стенки
Кровоизлияния и изъязвления слизистой желудка и кишечника
В кишечнике всегда присутствуют: токсины Гр- микроорганизмов. Они: снижают сократительную функцию миокарда, снижают чувствительность нейрорецепторов сосудов и повреждают эндотелий сосудов. Они способствуют прогрессивному нарушению гемодинамики.



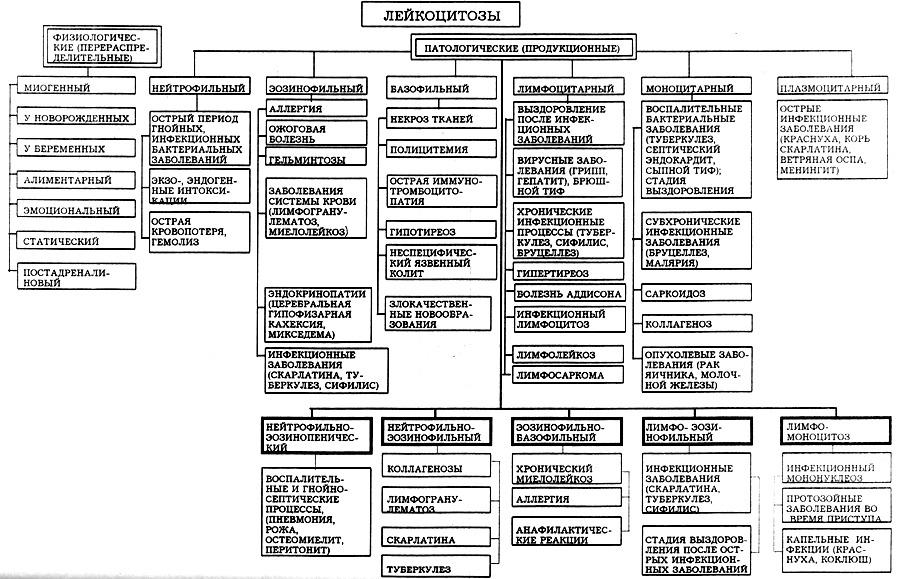
3. Виды лейкоцитозов, их причины, механизмы возникновения, функциональные и структурные изменения лейкоцитов и лейкоформулы.
Лейкоцитоз
Физиологические –
Алиментарный
Миогенный
Эмоциональный (ярко выражен у детей)
Их механизм перераспределительный.
При беременности – увеличивается продукция лейкоцитов костном мозге
У новорожденного
Патологические –
Концентрационные – связан с гемоконцентрацией (причина – потеря жидкости: рвота, диурез). Лейкоформула не изменяется, но возрастет гематокрит.
Продукционные – лейкоформула всегда изменяется. В зависимости от того какие клетки буду увеличиваться: базофильный, эозинофильный.
Базофилы
Накапливают БАВ (гепарин, гистамин, серотонин)
Аккумулируют продукты протеолиза
Имеют рецепторы к Ig E (от 10 до 40 тыс на одной клетке)
Продуцируют БАВ (в большей степени лейкотриены)
Базофилия – встречается: при некрозе тканей, злокачественных опухолях, аллергических реакциях немедленного типа.
Эозинофилы–
Содержат гистаминазу (клетки скорой помощи)
Фагоцитируют комплексы аг+ат
Имеют гистотоксины, которые могут действовать на гельминтов
Эозинофилия развивается при:
аллергических реакциях немедленного типа
коллагенозах (ревматизм, дерматомиозит)
при инфекционных заболеваниях с аллергизацией организма (скарлатина, сифилис, туберкулез)
при гельминтозах (описторхоз, трихинеллез, эхинококкоз и др.)
Нейтрофилы– различаются по оттенку цитоплазмы. Свойства: нейтрофил – это микрофаг, он способен фагоцитировать и переваривать бактерии (этот процесс сложный), в них активируются обменные процессы, потребляет много кислорода – кислородный взрыв, т.е образуется супероксид-анион (активный кислородный радикал). Этот радикал превращается в перекись водорода. Под действием миелопероксидазы образуются коллагеновые анионы – хлор, йод, бром. Повреждаются бактериальные стенки. После повреждения нейтрофил воздействует на микроб своими животными антибиотиками (дифинзин, лактоферрин), и микроб убивается. Под действием лизосомальных ферментов идет полное переваривание микроба.
Нейтрофилы вырабатывают большое количество цитокина. Цитокин-интерлейкин-1 – мощный пироген. Цитокины обладают антитоксическим эффектом. Исходя из свойств нейтрофилов.
Нейтрофилия
острый период гнойно-воспалительных заболеваний, бактериальных инфекций
при асептических воспалениях
при различных экзо- и эндогенных интоксикациях
после острой кровопотере, острого гемолиза
Сдвиги влево (регенеративный):
Сдвиг влево до палочкоядерных – при увеличении палочкоядерных. Характерно для гнойно-воспалительных инфекций легкой степени, при утяжелении состояния индекс нарастает, т.е в крови нарастают юные и..
Сдвиг влево до юных
До миелоцитов – появляются М, Ю,П,С
Сдвиг вправо (дегенеративный): молодые формы отсутствуют совсем или единично, и увеличивается количество сегментоядерных клеток, дегенеративные формы нейтрофила (полисигметация, гипосигментация, анизоцитоз, кариолиз, цитолиз, фрагментоз ядра, вакуолизация ядра и цитоплазмы, токсическая зернистость). Сдвиг вправо говорит о низком уровне индекса.
Лимфоциты–
Определяют специфическую защиту клеточную и гуморальную;
Синтезируют лимфокины (интреферон);
Имеют мембрано-ассоциированные ферменты (липазы, перфорин-протеолитический фермент);
Лимфоцитоз
Инфекции
Вирусные (грипп, краснуха)
Паразитарные (токсоплазмоз, хламидиоз)
Микозы
Бактериальные инфекции:
- Специфические (бруцеллез, сифилиз, туберкулез)
- иерсиниоз, туляремия, лептоспироз
Протозоонозы (малярия, лейшманиоз)
Аллергические реакции замедленного типа
Моноциты– макрофаг, самая большая клетка
осуществляет фагоцитоз (противомикробная, противовирусная, противопаразитная, противоопухолевая защита)
осуществляет процессинг антигена
синтезирует цитокины
Монокины – цитокины, вырабатывающиеся моноцитами.
Организует реакцию клеточной кооперации
Моноцитоз
Инфекции:
Хронические специфические
Вирусные
Септический эндокардит
Острые протозойные
Сыпной тиф
В стадию выздоровления при гнойно-воспалительных заболеваниях
Злокачественные опухоли: яичника, молочной железы
Аутоиммунные заболевания
Нейтрофильно-эозинофильный лейкоцитоз
При скарлатине, описторхозе, острой фазе туберкулеза
Нейтрофильно-эозинопенический лейкоцитоз
Тяжелые гнойно-септические заболевания
Эозинофильно-базофильный лейкоцитоз
При тяжелых аллергических реакциях немедленного типа, хронический миелолейкоз
Лимфоцитарно-моноцитарный лейкоцитоз
Развивается при инфекционном мононуклеозе; острые протозойные инфекции; капельные инфекции (краснуха, коклюш); хронические специфические инфекции (туьеркулез, бруцеллез, сифилис);
Билет 44
2. Иммунная толерантность. Общая характеристика, формы, механизмы и значение в патологии. Лекарственные методы получения иммунной толерантности.
Иммунологическая толерантность
Физиологическая
Патологическая
Индуцированная или медицинская – вследствие приема иммунодепрессантов или из-за реакции чужеродной ткани
R.Owen, 1945 – телята – близнецы – описана толерантность
P.Medowar, 1952 – мышам внутриутробно вводили Аг, после рождения могли быть пересажены любые органы, и перелита любая кровь все Аг, с которыми встречается наш организм внутриутробно, они воспринимаются как свои. Иммунная система начинает работать после рождения.
Механизмы физиологической толерантности
Клонально-селекционный – все клетки с возможность аутоагрессии, просто элиминируются, т.е. уничтожаются
Анергия Т-лимфоцитов не подвергшихся по стимуляции – клональная аллергия
Апоптоз лимфоцитов, активированных эндоаллергенами, т.е. мональная анергия
В тимусе аутоагрессивные Т-лимфоциты разрушаются – центральная селекция
Т-киллеры блокируются Т-супрессорами
Изоляционный механизм –
Механизмы патологической толерантности
Апоптоз цитотоксических лимфоцитов
Активация Т-супрессоров
Экранирование чужеродных антигенных детерминант иммуноглобулинами
Антигенная перегрузка иммунной системы (при значительных переливаниях)
Иммунодефицит
Иммунодефицитные состояния (ИДС)
Типовая форма патологии системы иммунобиологического надзора; характеризуется снижением эффективности или полной неспособностью ее осуществлять реакции обнаружения, деструкции и элиминации чужеродного антигена.
Иммунодефицитные состояния
Первичные – наследственные и врожденные – собственный иммунодефицит
Вторичные – приобретенные – иммунодеперссия
В зависимости от того какие компоненты повреждаются иммунобиологического надзора:
Т-зависимые (Т-клеточные)
В-зависимые (В-клеточные, гуморальные)
А-зависимые (А-клеточные, фагоцитарные)
Смешанные (комбинированные)
Первичные иммунодефициты
Наследственные, связанные с генетическим аппаратом, и передающиеся по наследству – составляют треть от первичных
Наиболее часто встречаются В-клеточные (больше половины), около 20% - Т+В (комбинированные), 15% - дефицит Т-системы, фагоцитарный дефект
Передаются обычно по рецессивному пути, могут быть аутосомные, сцепленные с Х – хромосомой
Врожденные заболевания – формируются внутриутробно – особенно 1 триместр беременности. Факторы: физические, ионизирующая радиация, флюорография, химические факторы (лекарственные препараты, например, 1 таблетки аспирина хватит для развития порока сердца), инфекционные, вирусные воздействия.
Синдромы:
В наличие тимуса:
Ди Джорджи
Незелофа
Вискотта-Олдрича
Дефицит Т-системы проявится: вирусная инфекция, генерализованные форма инфекции – герпес, вирусные пневмонии, хроническое течение вирусных инфекций, активируются грибковые инфекции (особенно кандидоз). Ослабленные живые вакцины (БЦЖ) смертельно опасны, они дают заболевания – туберкулез, полиомиелит.
Пересадка костного мозга, переливание крови. Реакция «трансплантат против хозяина» (РТПХ).
Патогенез – повреждение органов и тканей реципиента иммунными клетками донора.
Проявление: «рант» - болезнь карлика (у детей), гомологичная болезнь (у взрослых).
Клинические варианты течения: острая реакция «ТПХ», хроническая реакция «ТПХ» (страдают паренхиматозные органы, кожа).
Дефицит Т-киллеров – онкогенно опасная ситуация.
Дефицит Т-супрессоров – аллергия, аутоаллергия
Дефицит В-системы - селективный дефицит IgA (секреторный компонент, обеспечивает бактерицидность слизистых оболочек и кожи) – 1/600000 человек. Проявления: бактериальные инфекции кожи и слизистых, компенсаторно возрастает продукция IgE, Ig M и G – развитие аллергических заболеваний.
Дефицит В-системы
Агаммаглобулинемия, сцепленная с Х-хромосомой (болезнь Брутона) – выраженный полиартрит
Дефицит А-системы
Синдром Чедиага-Хигаси – альбинизм
Комбинированные иммунодефициты
Аутосомно-рецессивная форма («швейцарский» тип)
Рецессивная, сцепленная с Х-хромосомой
Синдром Луи-Бар (с атаксией, телеангиэктазией)
Ретикулярный дисгенез (отсутствие иммунитетов, фагоцитов)
Физиологические иммунодефициты
Сюда относятся все 9 месяцев беременности, т.е. развитие ребенка в организме – наличие Аг.
Также – это детский возраст.
+ возраст пожилой и старческий.
Вторичные, или приобретенные иммунодефициты
Активировался с появлением ВИЧ.
Возникают в результате действия иммунодепрессантов: глюкокортикоиды, цитостатики, антилимфоцитарная сыворотка, ионизирующая радиация, рентгеновское излучение, нарушение обменных процессов в организме (голодание, частичное и полное, дисмикролементозы, нарушение всасывания в ЖКТ, потеря бела, интоксикации, сахарный диабет), хронический стресс, на фоне опухолей.
Инфекционные факторы – нелимфотропные, не является прямым объектом поражения – икобактерия туберкулеза, сифилис, бруцеллез, грибы, вирусы, простейшие, гельминты.
СПИД
Патогенез: ВИЧ повреждает рецепторы CD4, расположенные на Т-хелперах, они просто погибают. Здоровые поврежденные Т-хелперы соединяются, и образуют мультиядерные клетки. снижение иммунного ответа.
Макрофаг – рассадник ВИЧа, их функциональная активность резко снижаетс, т.е. снижается антиген-прдставляющая функция, и макрофаг начинает продуцировать цитокины, в ответ на персистенцию вируса – ИЛ1 - длительная лифорадка, фактор некроза опухолей – кохиксин (худеет пациент). Активируется бактериальная микрофлора поражение ЖКТ. В-лимфоциты лишаются регулирующей функции Т-клеток и перераздражаются антигенами вируса и циркулирующими иммунными комплексами, и начинают вырабатывать аутоантитела. Гликопротеин 120 сходен по строению с антигенами собственных тканей. Сам вирус разрушает только часть клеток, полисистемность определяет аутоиммунный механизм. Идет самоповреждение.
Стадии:
Стадия инкубации – с момента заражения, до клинических проявлений
Проявления – может пациента ничего не беспокоить, уже серопозитивный период – выявляются аутоантитела
2 «Б» стадия – острая ВИЧ-инфекция без вторичных заболеваний (походи на симптомы других заболеваний)
2 «В» - с вторичными заболеваниями (ангина, герпес) – 2-3 недели, с периодическими обострениями
Латентная стадия – в крови прогрессивно снижаются Т-лимфоциты, лимфоднопатия – продолжительность 2-3 до 20 лет
Аппартунистические азболевнаия – инфекционные или опухолевые.
Развитие саркомы Капоши при СПИДе.
Терминальная стадия – необратимые поражения
3. Острая почечная недостаточность; формы, причины, механизмы развития и клинические проявления. Принципы лекарственной терапии.
Основные причины почечной недостаточности:
«Преренальные» - ведут к нарушению кровоснабжения почек:
Шок
Коллапс
Кровопотеря
Тромбоз почечных артерий
ОСН
«Ренальные»:
Острые нефриты, пиелонефриты, васкулиты;
Нефротоксические вещества;
Острый гемолиз, Краш-синдром, ДВС-синдром;
«Постренальные»:
Обтурация/сдавление мочевыводящих путей;
Перегиб мочеточников;
Патогенез ОПН:
Начальная (шоковая) стадия:
Снижение объема клубочковой фильтрации;
Прогрессирующее снижение диуреза;
Олиго-, анурическая стадия – обтурация канальцев, некроз клубочков и канальцев:
Гиперазотемия, уремия (интоксикация: слабость, головная боль, тошнота, запах мочевины изо рта, апатия, спутанность сознания, судороги, кома).
Нарушения водно-электролитного обмена (не выделяется вода): гиперволемия отек легких и мозга.
Гиперкалиемия нарушение атриовентрикулярной и внутрижелудочковой проводимости;
Гиперфосфатемия;
Гипокальциемия гиперрефлексия мышц;
Гипернатриемия артериальная гипертензия;
Гипермагниемия;
Метаболический ацидоз;
Полиурическая стадия – регенерация частично некротизированных нефронов, и склероз полностью некротизированных нефронов.
Восстановление и увеличение диуреза:
Гипоизостенурия
Гиповолемия
Дегидратация
Гипокалиемия
Стадия выздоровления – восстановление всех функций почек (6-12 месяцев).
