
- •Триада Селье (стресса):
- •Стадия истощения.
- •3. Дыхательная недостаточность, её проявления. Изменения газового состава артериальной крови на различных стадиях дыхательной недостаточности.
- •2. Аллергические реакции III (иммунокомплексного) типа. Этиология, патогенез, клинические проявления. Патогенез сывороточной болезни. Аллергические реакции III типа (иммунокомплексные)
- •3. Хроническая почечная недостаточность; формы, причины, механизмы развития и клинические проявления. Уремическая кома.
- •2. Аллергия. Общая характеристика и значение в патологии. Связь аллергии и иммунитета. Аллергены и антитела, их виды и особенности. Стадии аллергической реакции.
- •3. Коронарная недостаточность; характеристика понятия, виды.
- •3. Острая артериальная гипотония; причины, виды и механизмы коллапса.
- •3. Нефрозы; формы, этиология, патогенез и основные клинические проявления.
- •Нефротический синдром
- •Этиология
- •Патогенез острого нефротического синдрома
- •Патогенез хронического нефротического синдрома
- •2. Изменения обмена веществ, структуры клеток и функции органов при лихорадке. Участие нервной, иммунной и эндокринной систем в развитии лихорадки. Отличие лихорадки от гипертермии.
- •3. Боль; причины и механизмы возникновения, значение для организма. Принципы обезболивания.
- •2. Местные и общие клинические проявления воспаления, их патогенез.
- •Местные (кардиальные) признаки воспаления
- •Общие признаки воспаления
- •3. Аллергические (инфекционно-аллергические) заболевания почек, Гломерулонефрит; формы, этиология, патогенез и клинические проявления, исходы.
- •Острый гломерулонефрит
- •Этиология
- •Патогенез иммунопатологического гломерулонефрита
- •2. Причины, механизмы развития, изменения газового состава артериальной и венозной крови при экзогенной, дыхательной, сердечно-сосудистой, кровяной и тканевой гипоксии. Смешанная гипоксия.
- •3. Печёночная кома; общая характеристика, виды, патогенез, клинические проявления и механизмы возникающих расстройств.
- •3. Этиология, патогенез и клинические проявления тромбофилического синдрома. Принципы лекарственной коррекции расстройств гемостаза.
- •2. Экссудация; изменения местного кровообращения и микроциркуляции, выход жидкой части крови в ткань и развитие отёка, их механизмы и значение. Виды и состав экссудатов.
- •3. Вторичные, симптоматические гипертонии (лекарственная, почечная, эндокринная, рефлексогенная и др.). Этиология, патогенез, клинические проявления, последствия, осложнения.
- •2. Общая характеристика гипоксии. Устойчивость разных органов и тканей к кислородному голоданию, факторы, определяющие устойчивость. Основные типы гипоксии.
- •3. Основные проявления расстройств деятельности почек, их происхождение. Изменения диуреза, состава мочи и крови; отёки, артериальная гипертония.
- •2. Лекарственная аллергия. Аутоаллергия.
- •1 Тип аллергии – реагеновый, атопический и анафилактический
- •Аллергические реакции I типа
- •(Реагиновые, атопические, анафилактические)
- •3. Ишемическая болезнь сердца; этиология, патогенез. Стенокардия, инфаркт миокарда; ведущие клинические проявления.
- •2. Аллергические реакции I (анафилактического, атопического) типа. Этиология, патогенез, клинические проявления. Патогенез бронхиальной астмы. Принципы лекарственной терапии.
- •1 Тип аллергии – реагеновый, атопический и анафилактический
- •Аллергические реакции I типа
- •(Реагиновые, атопические, анафилактические)
- •2. Пирогенные вещества; их химическая природа и места образования. Первичные и вторичные пирогены; лейкоцитарные пирогены (интерлейкин-I). Механизмы действия пирогенов.
- •2. Эмиграция клеток, ее молекулярные и другие механизмы. Фагоцитоз; виды, стадии, механизмы. Пролиферация; механизмы формирования и роль при воспалении.
- •2. Аллергические реакции замедленного типа (гзт) Этиология, патогенез, клинические проявления. Принципы лекарственной терапии.
- •Аллергическая реакция IV типа (туберкулиновая, клеточная, гзт)
- •Аллергические реакции IV типа
- •(Замедленного, клеточного, туберкулинового)
- •3. Патологическая гипертрофия миокарда, стадии, механизмы декомпенсации сердца.
- •Дыхательный (газовый) алкалоз
- •3. Артериальные гипотонии. Виды, причины и механизмы развития. Понятие о гипотонической болезни. Проявления и последствия гипотонических состояний.
- •Бронхо-легочная дыхательная недостаточность
- •3. Токсикомании; алкоголизм, наркомании и лекарственная зависимость. Этиология, механизмы формирования, клинические проявления на разных стадиях развития, исходы.
- •Билет 38
- •Триада Селье (стресса):
- •Стадия истощения.
- •Патогенез «шоковго легкого»
- •Синдром длительного раздавливания
- •(Краш-синдром)
- •Ожоговый шок
- •Шок в результате электротравмы
- •Кардиогенный шок
- •Гиповолемический шок
- •Постгемотрансфузионный шок
- •Токсико-септический шок
- •Травматический шок
- •Синдром длительного раздавливания
- •(Краш-синдром)
- •Ожоговый шок
- •Шок в результате электротравмы
- •Кардиогенный шок
- •Гиповолемический шок
- •Постгемотрансфузионный шок
- •Токсико-септический шок
- •Бронхо-легочная дыхательная недостаточность
- •2. Общие и специфические механизмы развития и клинические проявления коматозных состояний.
- •3. Коронарная недостаточность; характеристика понятия, виды.
- •3. Вторичные, симптоматические гипертонии (лекарственная, почечная, эндокринная, рефлексогенная и др.). Этиология, патогенез, клинические проявления, последствия, осложнения.
- •2. Проявление повреждения клетки в изменении обмена веществ, ее структуры и функции. Понятие о специфических и неспецифических проявлениях повреждения; обратимых и необратимых повреждениях.
- •3. Перегрузочная сердечная недостаточность. Понятие о перегрузке объёмом и давлением крови. Причины, механизмы развития и патоморфология перегрузочной недостаточности сердца.
- •2. Гипергидратация; виды, причины возникновения, механизмы развития, проявления и последствия. Принципы предупреждения и лечения гипергидратации.
- •3. Артериальные гипотонии. Виды, причины и механизмы развития. Понятие о гипотонической болезни. Проявления и последствия гипотонических состояний.
- •2. Патогенез сердечных, почечных, токсических, аллергических, голодных отёков. Местные и общие нарушения в тканях при отёках, их клинические проявления.
- •3. Боль; причины и механизмы возникновения, значение для организма. Принципы обезболивания.
- •3. Патологическая гипертрофия миокарда, стадии, механизмы декомпенсация сердца.
- •2. Гипероксия. Причины возникновения, формы. Механизмы повреждающего действия кислорода. Роль свободно-радикальных процессов. Понятие о системе антиокислительной защиты организма.
- •3. Виды, этиология, патогенез и клинические проявления геморрагических диатезов. Роль наследственных факторов, а также иммунопатологических механизмов в их патогенезе.
В острую фазу не назначаются, только в этап пролиферации, или при коллагенозах.
Влияние реактивности на течение воспаления
Если у пациенты нормэргическоевоспаление. При таком воспалении мы увидим и местные и общие реакции, которые выражены адекватно по силе воздействия повреждающего фактора.
Смотрим какие механизмы защиты выражены, если есть, то выздоровление.
При гиперергическомвоспалении мы увидим очень выраженные общие признаки воспаления. Очень высокие цифры лихорадки, лейкемоидные реакции, активация иммунной защиты вплоть до развития аллергической реакции, выраженная интоксикация. Местно – чрезмерно активно выражена экссудация – вторичная альтерация.
При гипергическомвоспалении – общие признаки воспаление. Лихорадка не выражена, тяжелые повреждения ткани, содержание лейкоцитов либо в норме, либо чуть выше нормы. Нейтрофильный сдвиг вправо. Фагоцитарная активность может быть низкой. СОЭ – повышено, за счет и БОФ. В очаге воспаления – первичная альтерация.
3. Токсикомании; алкоголизм, наркомании и лекарственная зависимость. Этиология, механизмы формирования, клинические проявления на разных стадиях развития, исходы.
Психоактивные вещества:
Психотропные
Наркотики
Токсикоманические
Наркотические вещества –
химические вещества или лекарственные препараты, обладающие специфическим воздействием на ЦНС (эйфоризирующим, галлюциногенным и др.), которые способствуют развитию комплекса: привыкание – пристрастие – психическая и физическая зависимость.
Применение этого вещества имеет отрицательные социальные последствия.
Соответствующая государственная инстанция, обладающая необходимыми полномочиями, оценив вегетативные медицинские и социальные аспекты неконтролируемого применения этого вещества, может признать его наркотическим средством и внести в список веществ, запрещенных к немедицинскому применению.
Виды наркоманий:
Канабизм: марихуана, гашиш, масло гашиша
Опийная наркомания: морфин, кодеин, героин, омнопон
Кокаинизм: кокаин
Вызванная галлюциногенами: диэтиламид лезиргиновой кислоты, мескалин
Полинаркомания
Токсикоманические вещества – химические вещества, оказывающие специфические воздействия на ЦНС, но не являющиеся наркотиками.
Психотропные вещества: транквилизаторы, антидепрессанты, психостимуляторы, снотворные (барбитураты), противопаркинсонические средства, производыне лезиргиловой кислоты (ЛСД-25).
Токсикоманию вызывают: алкоголь, агонические растворители, веществ бытовой химии, инсектициды.
Формы патологии, вызываемые психоактивными веществами:
Наркомании. Причина: наркотические вещества.
Токсикомании. Причины – ненаркотические, психоактивные вещества, используемые с немедицинской целью.
Наркомания
Токсикомания
Это типовая форма психосоматических расстройств, проявляющихся стойким патологическим влечением, повторному приему соответствующего психоактивного вещества, как правило, в возрастающих дозах.
Характеризуется психической и физической зависимостью от психоактивного вещества, проявляющийся появлением абстинентного синдрома, при прекращении его приема.
Сопровождается патологическими изменениями личности, развитием комплекса психических, некротических, вегетативных и соматических расстройств.
Пьянство – потребление больших количеств спиртных напитков с последующим опьянением, или с целью опьянения в отличие от применения алкоголя, носящего церемониальный характер, связанного с получением удовольствия или являющегося своего рода средством общения, а также удовлетворения пищевых потребностей без намерения опьянеть (ВОЗ).
Алкоголизм:
Вид токсикомании, возникающий при повторном применении алкоголя
Характеризуется патологическим влечением к употреблению спиртных напитков
Формирование физической зависимости, с развитием абстинентного или похмельного синдрома («похмельного»), в случае прекращения приема этанола
При хроническом алкоголизме наблюдается деградация личности, стойкие соматические и психоневрологические расстройства.
Этиология
Причина – злоупотребление алкоголем
Условия:
Генетическая предрасположенность
Психологические особенности личности
Чем сильнее выражена болезнь, тем выше риск возникновения у родственников
С увеличением числа больных в семье возрастает риск заболевания у родственников
Риск заболевания выше, если человек относится к менее
Личностные особенности индивидуума:
Способность адаптироваться в окружающей обстановке, противостоять стрессорным воздействиям, разрешать конфликты и переносить эмоциональное напряжение – защищает.
Тип личности астеничный; тревожность, затруднение межличностных контактов – предрасполагает.
Социальные факторы:
Социальная политика государства
Социальное положение индивидуума:
Его экономическая обеспеченность;
Образование;
Семейное положение;
Этническая и религиозная принадлежность;
Обычаи ближайшего окружения;
Метаболизм алкоголя в организме
После приема алкоголя максимальная его концентрация в крови отмечается через 40-60 минут после употребления натощак и через 90-100 минут после приема пищи.
Элиминация в среднем 6.3 – 10 г/час. С выдыхаемым воздухом до 10%, с мочой (нет концентрации почками), с калом (минимальное количество).
В норме источник алкоголя – пируват, треонин, дезоксирибоза β-аланин этанол:
Путь с помощью АДГ
Путь – микросомальная этанол окисляющая система (МЭОС)
Путь – каталаза
Все они заканчиваются образованием ацетальдегида.
Ацетальдегид подвергается воздействию ацетальдегиддегидрогеназы, и образуется ацетат.
Окисление 1г этанола дает 7 ккал.
Этанол ацетальдегидуксусная кислотаацетилкоэнзим А:
ЦТК
синтез ЖК и холестерина
Последствия метаболизма алкоголя
избыточная «восстановленность» клетки: возрастает NADH/NAD нарушение окислительного потенциала клетки нарушение обмена углеводов, липидов, белков
нарушение обмена витамина А, некоторых ЖК
накопление ацетата образование NADФН усиление биосинтеза и накоплению ВЖК
токсическое действие ацетальдегида
Сам этанол уменьшает выделение адреналина, норадреналина и катехоламинов, а ацетальдегид наоборот.
Этанол способствует тому, что истощается симпато-адреналовая система. При этом образуется большое количество предшественников дофамина. И при взаимодействии этанола с дофамином образуются опиатоподобные вещества, β-компоненты.
Общие компоненты патогенеза нарко- и токсикоманий:
патологическое влечение к повторному употреблению психоактивного вещества
формирование психической зависимости от вещества
формирование толерантности к психоактивному вещества
формирование физической зависимости от вещества
стадии нарко- и токсикоманий:
начальная – психическое влечение, зависимость, адаптивная, невростеническая, психостеническая.
Средняя – визическая зависимость, наркоманическая, токсикоманическая, или стадия субкомпенсации.
Финальная – энцефалопатическая, соматическая, истощения, декомпенсации.
Основные симптомы стадий:
Стадия психической зависимости – психическая зависимость от психоактивного вещества, нерво- и психостенический синдром. При этом повышается толерантность к веществу. Если будет многократный повторный синдром, то количество рецепторов к этому веществу увеличивается. Нарушается подвижность рецепторов, увеличивается вязкость мембраны. Возникают провалы памяти.
Адаптация к негативному действию психоактивного вещества.
Стадия физической зависимости – формируется физическая зависимость. Проявляется абстиненцией. Прогрессирующее повышение толерантности к веществу, переход на токсические дозы. Психоактивное вещество входит в процесс обмена веществ. Деградация личности, расстройство функций органов.
Финальная стадия – физическая и психическая зависимость от вещества. Абстиненция. Снижается толерантность к веществу и потребляемой дозы. Полиорганная недостаточность. Деградация личности. Кохиксия.
Патогенез
Ацетальдегид, ацетат, NADH:
Нарушение углеводного, белкового, жирового обмена
Высвобождение катехоламинов, истощение их депо, повышение синтеза дофамина:
Снижается чувствительность дофаминергических систем мозга 1. Производыне опиатов; 2. Повышение синтеза энкефалинов
Дофамин + опиоидные пептиды абстинентный синдром
Опиаты + опиатно-дофаминовый комплекс психичесая и физическая зависимость
Билет 31
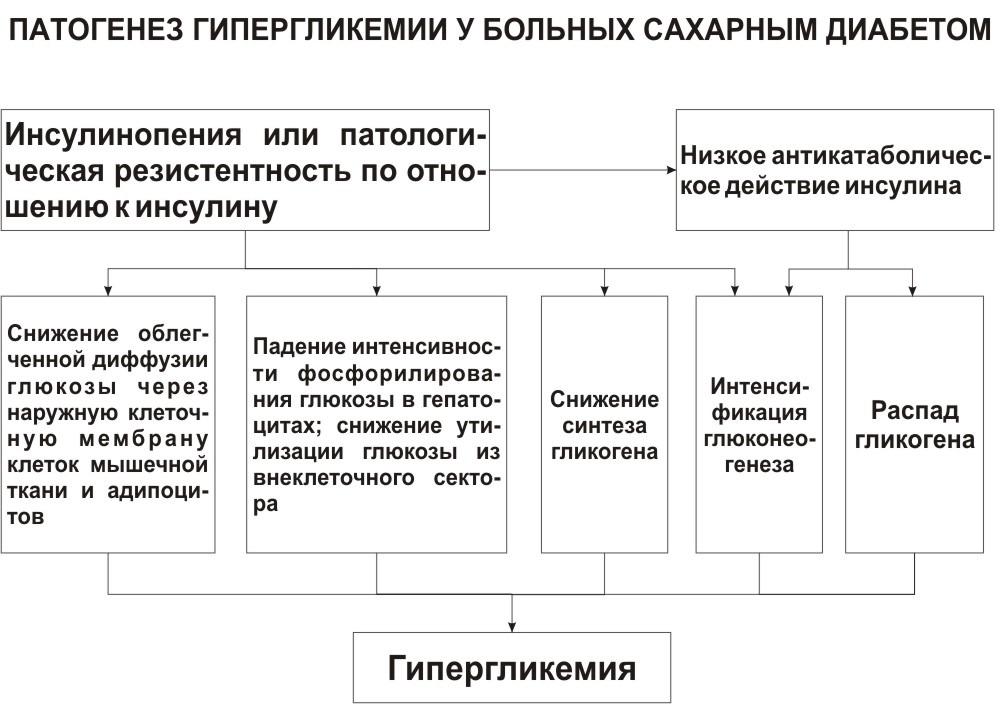
. Гипергликемические состояния; общая характеристика понятия, формы, причины и механизмы возникновения. Расстройства физиологических функций, обменных процессов и структуры тканей при гипергликемиях.
Основные причины гипергликемии:
Гипергликемия: алиментарного характера – после любого приема пищи, лекарственная , нейро- и психогенные расстройства (стресс, психическое возбуждение, боль), Эндокринопатии (избыток контр-инсулярных гормонов и дефицит инсулина).
Лекарственные вещества, способствующие гипергликемии: стероидные гормоны, пероральные контрацептивы, диуретики и гипотензивные средства (тиозиды, клофилин, урегит), психотропные средства (галоперидол, аминазин, хлорпротиксен), трициклические, адреналин, изадрин, анаприлин, дифенин, НПВС (аспирин, индометацин), цитостатики (циклофосфамид, Л-аспарогиназа), эфир – хлороформ.
Эндокринопатии:
Болезнь Иценко-Кушинга
Гипертиреоз
Феохромоцитома
Избыток СТГ
Очень частая причина – инсулиновая недостаточность.
В настоящее время больные сахарным диабетом составляют 5%, среди пожилых – каждый пятый, риск заболевания – удваивается на каждые 20% избытка массы.
Сахарный диабет– основа для развития других заболеваний. На фоне СД развивается ИМ (34.7%), 22% - инсульт.
СД – состояние хронической гипергликемии, которое может развиваться в результате воздействия многих экзогенных и генетических факторов, часто дополняющих друг друга.
СД – эндокринно-обменное заболевание, в основе которого лежат глубокие нарушения обмена веществ (углеводного, жирового, белкового и др). развивается вследствие дефицита инсулина в организме, обусловлено пониженной его секрецией или повышенной потребностью организма в этом гормоне.
Инсулиновая недостаточность:
Панкреатическая – нарушена продукция, синтез инсулина, при этом развивается инсулинзависимый СД – чаще у молодых людей, детей.
Внепанкреатическая – в основе лежит инсулинорезистентность (он вырабатывается) – СД 2 типа - инсулиннезависимый СД. Он развивается чаще у пожилых – СД тучных людей.
Панкреатическая (абсолютная) инсулиновая недостаточность:
Может передаваться по наследству – полигенно – необходимо несколько генов, комбинация их + экзогенное воздействие, способствующее магифестации
Недостаточность синтеза инсулина
Синтез аномального инсулина
Нарушение высвобождения инсулина из β-клеток
Физические факторы: травма поджелудочной железы, ионизирующая радиация.
Нарушение кровоснабжения поджелудочной железы (ишемия, часто – в основе атеросклероз сосудов)
Опухоли поджелудочной железы
Панкреонекроз
В-цитотропные факторы: вирусы эпидемического паратифа, коксаки, кори, краснухи, ветряной оспы, цитомегаловирусы.
Химические факторы: нитрозомочевина и другие амино-азосоединения, аллоксан, диазоксид, стрептозоцин, вакор – средство для дератизации.
Алкоголь
Бычий сывороточный альбумин – белок коровьего молока – у детей-искусственников. По структуре белок схож с инсулином, поэтому Ат вырабатываются.
Антидиабетогенные факторы:
Цинк
Серосодержащие аминокислоты
Антиоксиданты
Витамин РР
Полиненасыщенные ЖК
Внепанкреатическая (относительная) инсулиновая недостаточность:
Наследственность – аутосомно-доминантный тип наследования, полигенный.
Активация инсулиназы печени
Избыток КИГ – контринсулярный гормон (стероидный гормон)
Нейро- и психогенные факторы (стресс)
Гиперлипопротеинемия
Блокада инсулина альбумином (синальбумин-инсулин)
Аутоантитела к инсулину
Блокада и повреждение инсулиновых рецепторов
Уменьшение количества инсулиновых рецепторов
Метаболический синдром – инсулинорезистентность, смертельный квартет:
Гиперинсулинемия + инсулинорезистентность тканей: ИНСД – дислипидемия, атеросклероз – ожирение
Повышение толерантности клеток к инсулину и глюкозе
Гипергликемия (более 8.8 ммоль/л) – глюкозурия – полиурия – гиперосмия крови – осморецепторы – полидипсия.
Снижение активности ЦТК – гликолиза (компенсаторно) активация – увеличение уровня пирувата и лактата – метаболический ацидоз .
Активация глюконеогенеза – гиперазотемия – снижение синтеза белков.
Гиперлипидемия – жировая инфильтрация печени – нарушение обмена кетокислот.
Осложнения сахарного диабета:
Острые – комы
Хронические (поздние) – микроангиопатии: ретинопатии, нейропатии, нефорпатия, пангипопитуитаризм.
Патогенез микроангиопатий при СД:
Гипергликемия – гликозилирование белков плазмы и сосудистой стенки – стимуляция иммунных реакций – иммунный комплексы – инсулинотерапия ----- пролиферативный васкулит
Диабетическая ретинопатия
3. Кровопотеря; виды кровотечений. Расстройства обмена веществ, структуры и функции органов при кровопотере и в постгеморрагическом периоде. Приспособительные реакции при кровопотере; механизмы их формирования. Принципы терапии.
Кровопотеря:
Острая постгеморрагическая возникает вследствие одномоментной кровопотери – 20% и более от ОЦК или 5 мл и более на 1 кг массы тела. Имеет 3 стадии:
Нервно-рефлекторная. У пациента гиповолемия нормоцитемическая. В ответ на кровопотерю выбрасывается адреналин + стимуляция барорецепторов сосудов приводит к спазму периферических сосудов и централизации кровообращения;
Гидремическая стадия – в ответ на гиповолемию развивается ишемия почек – вырабатывают ренин (протеолитический фермент – альфа-2-глобулин) и образуется ангиотензин-1 под влиянием ангиотензин превращающего фермента превращаются в ангиотензин-2, который споосбствует синтезу альдостерона в коре надпочечников, который в свою очередь способствует задержке натрия, осмотическое давление в крови повышается и межклеточная и внутриклеточная жидкость идет в кровь – тем самым идет восполнение ОЦК.
Костно-мозговая. Начинается на 4-5 сутки с так называемого ретикуло-эритроцитарного криза – «потомки» нормального пути эритропоэза.
Хроническая постгеморрагическая анемия -
Анемия вследствие нарушенного кровообразования – железодефицитная анемия. Страдают почти 2 млрд. человек. В два раза больше людей страдают скрытым дефицитом железа.
Группы риска:
Дети и подростки: потребности в железе при быстром росте часто превышают его поступление;
Женщины: некомпенсированный потери железа во время менструаций, беременностей, родов;
Социально неблагополучные: плохое питание;
Доноры: если потери железа не компенсируются;
Пожилые люди: хронические гастроинтестинальные кровотечения, алиментарный фактор.

Первичной реакцией на потерю крови является спазм мелких артерий и артериол, возникающий рефлекторно в ответ на раздражение рецептивных полей сосудов (барорецепторов дуги аорты, синокаротидной зоны и вторично вовлекающихся в процесс хеморецепторов тканей) и повышение тонуса симпатического отдела вегетативной нервной системы. Благодаря этому при малой степени кровопотери и даже при большой, если она протекает медленно, возможно сохранение нормальной величины АД.
В порядке компенсации увеличивается сила сокращений сердца и уменьшается количество остаточной крови в его желудочках. В терминальной стадии сила сердечных сокращений уменьшается, остаточная кровь в желудочках не используется. Перенесённая кровопотеря изменяет функциональное состояние сердечной мышцы — снижается максимально достижимая скорость сокращения при сохранении силы сокращения. По мере падения АД уменьшается объём кровотока в коронарных артериях в меньшей степени, чем в других органах. Появляются изменения ЭКГ, характерные для прогрессирующей гипоксии миокарда, нарушается проводимость, что имеет значение для прогноза, поскольку от неё зависит степень координированности работы сердца.
Гипоксия тканей приводит к накоплению в организме недоокисленных продуктов обмена веществ и к ацидозу, который в начальных стадиях кровопотери носит компенсированный характер. При углублении кровопотери развивается некомпенсированный метаболический ацидоз со снижением pH в венозной крови до 7,0–7,05, в артериальной — до 7,17–7,20 и уменьшением щелочных резервов. В терминальной стадии кровопотери ацидоз венозной крови сочетается с алкалозом.
Билет 32
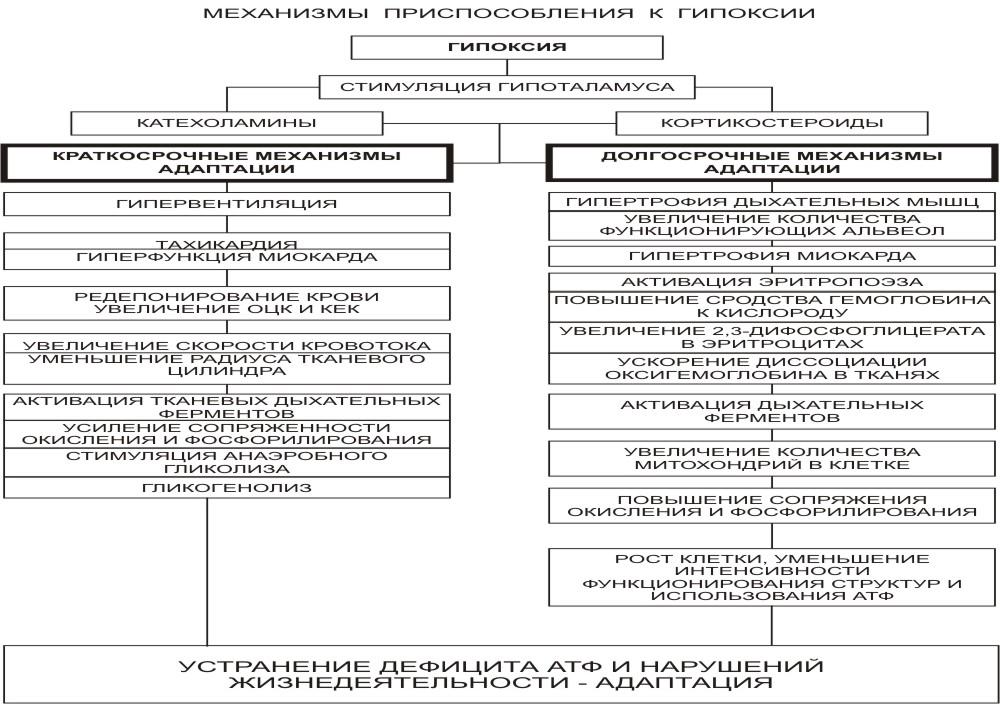
2. Механизмы и проявления экстренной и долговременной адаптации к гипоксии.
Механизм экстренной адаптации организма к гипоксии. Острая гипоксия:
Системы кислородного бюджета организма;
Эффекты
Система внешнего дыхания: увеличен объема альвеолярной аентиляции, увеличение частоты и глубины дыхания;
ССС: увеличение МОС (увеличение ударного выброса и числа сокращений), централизация кровообращения (увеличение кровотока в жизненноважных органах).
Система красной крови: увеличение кислородной емкости крови (КЕК) за счет редепонирования крови и усиления диссоциации оксигемоглобина в тканях.
Тканевое дыхание: повышение эффективности биологического окисления – активация ферментов тканевого дыхания, стимуляция гликолиза, повышение сопряжения окисления и фосфорилирования.
Хроническая гипоксия: системы кислородного бюджета организма, эффекты, механизмы эффектов:
Система внешнего дыхания: увеличение степени оксигенации крови в легких – гипертрофия дыхательных мышц, гипертрофия легких.
ССС: увеличение МОС за счет гипертрофии миокарда, увеличение числа митохондрий в кардиомиоцитах, возрастания скорости взаимодействия актина и миозина, увеличения количества капилляров, повышение активности систем регуляции сердца, артериальная гиперемия в функционирующих органах и тканях.
Система красной крови: увеличение кислородной емкости крови за счет активации эритропоэза, увеличения 2,3-ДФГ в эритроцитах, усиление диссоциации оксигемоглобина в тканях;
Тканевое дыхание: увеличение эффективности биологического окисления – митохондриогенез, повышение сопряжения окисления и фосфорилирования, переход на оптимальный уровень функционирования, повышение эффективности метаболизма.
Эффекты дозированной гипоксии:
Уменьшение чувствительности организма к ионизирующей радиации;
Уменьшение токсических эффектов цитостатиков;
Уменьшение побочных эффектов рентгено-контрастных веществ, глюкокортикоидов;
Ослабление действия галлюциногенов и судорожных веществ.
3. Виды, этиология, патогенез и клинические проявления геморрагических диатезов. Роль наследственных факторов, а также иммунопатологических механизмов в их патогенезе.
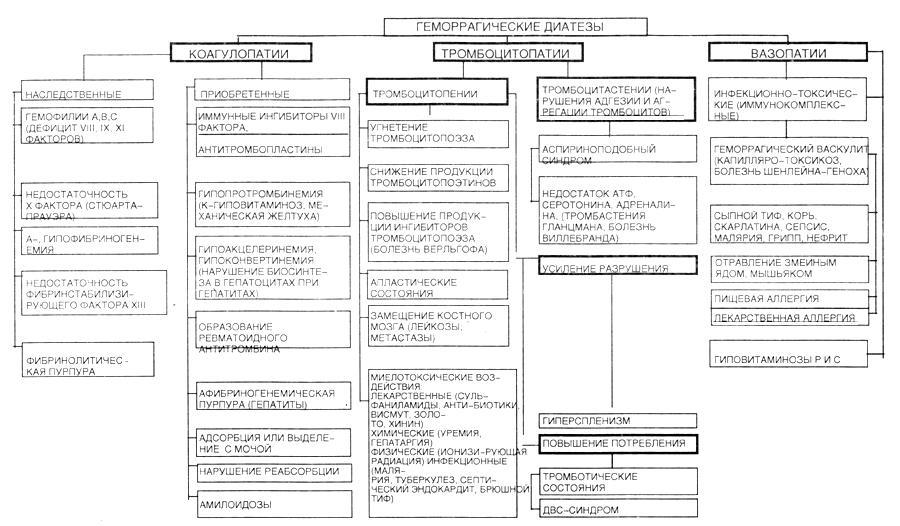
Геморрагические диатезы.
Разделяются в зависимости от повреждения компонента гемостаза:
Вазопатии:
Наследственные:
телеангиэктазия или болезнь Рандю-Ослера – наследуется аутосомно-доминантно, т.е дефект структуры сосудистой стенки, она истончается и образуются мешкообразные эктазы. Локализация: губы, верхняя часть туловища, лицо, волосистая часть головы, на слизистой оболочке, в полостях. Эти истонченные стенки хорошо травмируются. У пациента формируется хроническая анемия железодефицитная вследствие хронической кровопотери.
Приобретенные:
Гиповитаминозы С (цинга), РР – необходимы для полимеризации стенки сосудов – у пациента образуются петехии, васкулит. На симметричных участках кожи.
Геморрагичсекий васкулит (болезнь Шенлейна-Геноха):
Причина: бактерии, вирусы, паразиты, вакцины, лекарственные препараты, пищевые продукты. Заболевание имеет иммунокомплексный механизм, формируются циркулирующие иммунные комплексы – 3 тип аллергии. Имеет сезонный характер – весна. ЦИК – очень крупные, повреждают эндотелий сосудов, и способствуют образования воспалении. Результат – развитие иммунного воспаления. Формы: кожная, суставная. Если присутствуют на брюшине – абдоминальная форма, у пациента боли в животе. Эти ЦИК любят клубочки почек – почечная форма, формируется почечный синдром с симптомами гломерулонефрита.
Пробы на резистентность сосудистой стенки: Кончаловского (до определенного значения нагнетается давления в манжете, затем подсчитывается количество петехий), жгута (после наложения манжеты при измерении АД, смотрят на кожу – будут кровоизлияния), щипка (ущипнуть кожу).
Тромбоцитопатии:
Тромбоцитопении:
Болезнь Верльгофа (тромбоцитопеническая пурпура) – наследуется аутосомно-доминантно. Проявляется в виде синяков, причем цветут – кожа леопарда.
По наследству передается способность селезенки вырабатывать ингибитор тромбоцитопоэза (селезеночный фактор). Этот фактор ингибирует отшнуровку тромбоцитов от мегакариоцитов в костном мозге, количество мегакариоцито возрастает, а толку от них мало.
Лечат: удалением селезенки.
Приобретенные: НА ТЕЛЕФОНЕ ФОТО!
Миелотоксическое воздействие:
Экзогенные факторы: физические (ионизирующая радиация), химические (цитостатики, антибиотики, продукты нефтепереработки), биологические (вирусы, токсины микроорганизмов).
Эндогенные:
Угнетение нормальных ростков кроветворения.
Аутоиммунная тромбоцитопения.
Результат – носовые, десневые кровотечения, маточные, синяки.
Для дифференцировки существует биопроба, животному вводится сыворотка больного. Селезеночный фактор не обладает видоспецифичностью, поэтому он вызывает тромбоцитопению и у животного.
Тромбоцитастении – нарушение функциональных свойств тромбоцитов:
Наследственные: болезнь Гланцмана, болезнь Виллебранда (комплексный геморрагический диатез, потому что эндотелий в норме вырабатывает фактор Виллебранда, составную часть 8 фактора,. А по наследству передается извращенный синтез этого фактора. Фактор Виллебранада – фактор коагуляции).
Приобретенные:
Гиповитаминоз С, В12.
Уремия.
Переливание больших доз крови, плазмы, концентратов прокоагулянтов.
Миеломная болезнь, болезнь Вальденстрема (повышение в поазме нормальных и аномальных белков).
ДВСС (повышение ПДФ – продукты деградации фибрина)
Лекарственные - НПВС
Механизм тромбоцитоастений:
Нарушение синтеза и накопление в гранулоцитах тромбоцитов БАВ,
Нарушение дегрануляции и высвобождения тромбоцитарных факторов в плазм крови.
Диагностика тромбоцитопений и астений:
Количество тромбоцитов: 180-400*109/л.
Время агрегакции тромбоцитов: 14-18 сек
Процент клеток, вступивших в агрегацию – более 90.
Удлинение времени и уменьшение клеток вступивших – тромбоциастения.
Положительная проба Кончаловского – тромбоциты определяют трофику эндотелия сосудов, выделяют факторы роста необходимы для эндотелиоцитов. Если тромбоцитов мало – дефекты, ломкость сосудов повышается.
Коагулопатии – нарушение коагуляционного гемостаза:
Наследственные. По фазам свертывания:
Нарушение I фазы свертывания:
Гемофилия А (80% всех гемофилий) – дефицит VIII фактора.
Гемофилия В (10%) – дефицит IX фактора.
Гемофилия С (5%) – дефицит XI фактора.
Механизм наследования гемофилии: гемофилия А – это дефект X хромосомы. Здоровый отец, мама – носитель: здоровый сын, здоровая дочь, дочь-носитель, страдающий гемофилией сын. Заболевание проявляется сразу после рождения, у новорожденного возможны различные кровоизлияния (кефалогематома). Любая травма приводит к образованию гематом (тип кровоизлияния). Возможно формирование гемартрозов.
В и С гемофилии могут быть и у мужчин и у женщин.
Билет 33
2. Острые осложнения сахарного диабета. Диабетические комы; виды, механизмы и проявления.
Кома:
Общее, крайне тяжелое состояние организма.
Возникает в результате действия экзо- и эндогенных повреждающих факторов.
Характеризуется угнетением нервной деятельности, потерей сознания, гипо- и арефлексией, недостаточности функции органов и систем органов.
Диабетические комы
Гипергликемические
Кетоацидотичсекая
Гиперосмолярная
Гиперлактацидемическая
Гипогликемические
Наиболее часто встречается – кетоацидотическая. В основе – прогрессирующая нсулиновая недостаточность.
Способствующие факторы:
Отсутствие лечения при невыявленном СД;
Отказ от лечения;
Декомпенсация СД;
На фоне интеркурретных заболеваний;
Патогенез кетоацидотичсекой комы:
Прогрессирующая инсулиновая недостаточность – торможение гексокиназы – уменьшение постулпения глюкозы в клетки – дефицит энергии – стимулируется выработка контринсулярных кормонов (глюкагон, адреналин, глюкокортикоиды)
Контринсулярные гормоны стимулируют гликогенолиз и глюконеогенез – нарастает гипергликемия – глюкозурия – полиурия – обезвоживание.
Снижение тургора кожи, мягкие глазные яблоки.
Снижается ОЦК – МОС – АД.
Адреналин и глюкагон стимулируют липолиз гиперлипидемияжировая инфильтрация печенинарушение обмена кетокислотгиперкетонемиякетонурия.
Снижение активности ЦТК компенсаторно актвиируется гликолизповышение уровня пирувата и лактатаметаболический ацидоз. Кроме того и кетоз ведет к метаболическому ацидоз (у пациента дыхание Куссмауля, запах ацетона изо рта).
Кетонурия – потеря калия, натрия, фосфатов:
Гипокалиемия, гипонатриемия нарушения гемодинамики
Снижение 2,3-ДФГ и уменьшение глюкогемоглобина ухудшение диссоциации HbO2гемическая гипоксия
Гиперкетонемия, гиперазоемия, ацидоз интоксикация.
Гипергликемия повышение сорбитола и фруктозы в нейроцитахгиперосмиянабухание мозга
Циркуляторная + гемическая гипоксия.
Гиперосмолярная кома
Способствующие факторы: интеркуррентные заболевания, которые одновременно усугубляют относительную инсулиновую недостаточность и вызывают обезвоживание: диарея, рвота, ожоги и отморожения, форсированный энурез, перегревание, кровопотеря, злоупотребление сладостями, переливание больших доз глюкозы и солевых растворов, гемодиализ и реанимация.
Патогенез
Массивная гипергликемия, уровень глюкозы повышается в 5-10 раз, способствует ингибиции кетогенеза в печени. Глюкозурия, осмотический диурез – обезвоживание ингибиция липолиза в жировой ткани.
Обезвоживание гиповолемия полицитемическая – снижение АД, коллапс:
Олигоанурия
Активация РААС гипернатриемиягиперосмия
На фоне гемоконцентрации может формироваться ДВС-синдром.
Нарушение мозгового кровообращения, снижается и давление ликвора.
Гипергликемия образование сорбитола и фруктозы в нейроцитахгиперосмиянабухание мозга.
Гиперлактацидемическая кома
Способствующие факторы:
Гипоксия;
Почечная и печеночная недостаточность;
Инфекции;
Отравление салицилатами, метиловым спиртом;
Лечение сахароснижающими средствами (бигуаниды стимулируют гликолиз);
Патогенез
Инсулиновая недостаточность снижение активности ЦТКнарушение метаболизма пирувата и лактаталактацидоз (дыхание Куссмауля).
Лактацидоз гипокапнияартериальная гипотония.
Лактацидоз гиперкальциемия, гиперкальциемияблокада адренорецепторов сердцааритмии, снижение сократительной способности миокардафибрилляция.
Острая сердечнососудистая недостаточность нарушение мозговой гемодинамикигипоксия мозга.
3. Одышка и кашель, их значение. Периодическое и терминальное дыхание.
Типы одышки:
Одышка с углублением и учащением дыхания:
невротические состояния
эмоциональные потрясения
снижение рО2в воздухе
напряженная мышечная работа.
Чрезмерная импульсация от периферических рецепторов - возбуждение ДЦ - чрезмерное наполнение легочных альвеол - раздражение рецепторов легких - переключение на выдох.
Часто носит приспособительный характер.
Гипервентиляция легких возникает.
Включение резервных альвеол в легких (в норме 8 л/мин; до 20 л/мин при данном виде одышки).
При гипервентиляции возникает гипокапния (удаление СО2) - нарушение мозгового кровообращения (спазм мозговых сосудов) - обморок, судороги.
Глубокое, но медленное дыхание (брадипное).
В норме: у спортсменов в покое
после гипервентиляции
в состоянии сна
Патология: стенотическое дыхание при стенозу ВДП.
Воздух в легкие поступает с трудом
Заполнение альвеол идет медленно
Повышается порог легочного рефлекса и вдох долго не тормозится и не переключается на выдох.
Инспираторная одышка: затруднена фаза вдоха, вдох как бы в 2 фазы:

Частое поверхностное дыхание (тахипноэ).
Поражение нижних дыхательных путей (пневмония, эмфизема легких)
Перераздражение легочных рецепторов - порог легочного рефлекса понижается - не требуется полного расправления альвеол - переход на частое дыхание.
при переломах ребер - щадящее дыхание (боль в грудной клетке вызывает рефлекторное уменьшение глубины дыхания).
Экспираторная одышка (нарушена фаза выдоха):

Возникает при спазме легочных дыхательных путей: приступ бронхиальной астмы.
Эластической тяги легкого недостаточно для продвижения выходящего из альвеол воздуха и включается дополнительная дыхательная мускулатура.
Типы периодического дыхания: дыхание Чейна-Стокса, Биота. Все они характеризуются чередованием дыхательных движений и пауз – апноэ. В основе развития периодических типов дыхания лежат расстройства системы автоматического регулирования дыхания.
При дыхании Чейна-Стоксапаузы чередуются с дыхательными движениями, которые сначала нарастают по глубине, затем убывают.

При дыхании Биотапаузы чередуются с дыхательными движениями нормальной частоты и глубины.

К терминальным типам дыхания относятся дыхание Куссмауля (большое дыхание), апнейстическое дыхание, гаспинг дыхание. Они сопровождаются грубыми нарушениями ритмогенеза.
Для дыхания Куссмауля характерен глубокий вдох и форсированный удлиненный выдох. Это шумное, глубокое дыхание.

Оно характерно для пациентов с нарушением сознания при диабетической, уремической, печеночной комах. Дыхание Куссмауля возникает в результате нарушения возбудимости дыхательного центра на фоне гипоксии мозга, метаболического ацидоза, токсических явлений.
Гаспинг дыхание – это единичные, глубокие, редкие, убывающие по силе вздохи.






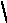


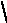





Гаспинг дыхание является другой, необычной формой дыхательных движений и проявляется при дальнейшем значительном углублении гипоксии. Дыхательные нейроны оказываются невосприимчивыми к внешним воздействиям. На характер гаспинга не влияют напряжение Расо2, перерезка блуждающих нервов, что позволяет предположить эндогенную природу гаспинга.
Билет 34
2. Хронические осложнения сахарного диабета. Виды, механизмы и проявления.
Хронические осложнения СД:
Диабетическая микроангиопатия (накопление гликопротеидов в базальной мембране артериол)
Диабетическая ретинопатия
Диабетическая нефропатия
Диабетическая макроангиопатия (артериосклероз крупных сосудов)
Коронарных артерий
Артерий мозга
Артерий нижних конечностей («диабетическая стопа»)
Диабетическая полинейропатия (демиелинизация периферических нервов вследствие хронической сосудистой недостаточности) – боли, парестезии
Патогенез микроангиопатий при СД:
Гипергликемия – гликозилирование белков плазмы и сосудистой стенки – стимуляция иммунных реакций – иммунный комплексы – инсулинотерапия ----- пролиферативный васкулит
3. Дыхательная недостаточность, её проявления. Изменения газового состава артериальной крови на различных стадиях дыхательной недостаточности.
Дыхательная недостаточность – состояние организма, при котором либо не обеспечивается поддержание нормального напряжения О2и СО2в артериальной крови, либо оно достигается за счет повышенной работы внешнего дыхания и других систем кислородного бюджета, что приводит к снижению функциональных возможностей организма.
По венозной системе кровь приходит к альвеолам
Атмосферный воздух: рО2= 159мм.рт.ст; рСО2=0.2мм.рт.ст
Альвеолярный воздух: рО2= 102мм.рт.ст; рСО2=40мм.рт.ст
Артериальная кровь: рО2= 100мм.рт.ст; рСО2=40мм.рт.ст
Венозная кровь: рО2= 40мм.рт.ст; рСО2=47мм.рт.ст
Стадии дыхательной недостаточности
Стадия – латентная:
В покое: нормальный газовый состав артериальной крови HbO2 (арт.) 94-98%; рСО2(арт.) 35-45мм.рт.ст
При нагрузке: артериальная гипоксемия HbO2(арт.) менее 94%
Стадия – парциальная:
В покое: артериальная гипоксемия HbO2(арт.) менее 94%; артериальная нормокапния
Глобальная :
Артериальная гипоксемия и артериальная гиперкапния
Билет 35
2. Нарушения конечных этапов белкового обмена. Причины, проявления и последствия нарушений образования и выделения мочевины. Гиперазотемия.
Конечным продуктом обмена белка и аминокислот является мочевина, выделяющаяся из организма с мочой. Синтез мочевины осуществляется гепатоцитами в орнитиновом цикле. Образование мочевины имеет большое физиологическое значение, так как благодаря этому процессу происходит обезвреживание высоко токсичного продукта - аммиака, отщепляющегося от аминокислот при их дезаминировании, а также поступающего в кровь из кишечника. Обезвреживание аммиака, образующегося в клетках различных органов, в том числе в мозге, достигается путем реакции амидирования, т.е. присоединение его к аспарагиновой и в особенности глутаминовой кислотам с образованием аминов аспарагина и глутамина. Процесс амидирования, так же как и образование мочевины, идет с потреблением энергии, источником которой является АТФ.
Синтез мочевины понижается при длительном белковом голодании (недостаток ферментов), при заболеваниях печени (циррозы, острые гепатиты с повреждением большого числа гепатоцитов, отравление печеночными ядами), а также при наследственных дефектах синтеза ферментов, участвующих в орнитиновом цикле образования мочевины (карбамилфосфатсинтетазы, аргининсукцинатсинтетазы и аргининсукцинатлиазы). При нарушении синтеза мочевины количество ее в крови и моче снижается и нарастает содержание аммиака и аминокислот, т.е. резидуального азота (продукционная гиперазотемия). Гипераммониемия играет важную роль в патогенезе печеночной энцефалопатии и комы.
Избыток аммиака может в некоторой степени устраняться за счет повышенного образования глутамина и присоединения к α-кетоглутаровой кислоте, которая при этом превращается в глутаминовую, и ее окисление в цикле трикарбоновых кислот резко снижается. Вследствие этого снижается образование АТФ.
Другой причиной накопления небелковых азотистых продуктов в крови (креатинин, мочевина) является нарушение выделительной функции почек при острой и хронической почечной недостаточности или при нарушении проходимости мочевыводящих путей. Возникающая в данном случае гиперазотемия называется ретенционной. При этом концентрация остаточного азота в крови возрастает до 140-215 ммоль/л, а содержание небелковых азотистых продуктов в моче снижается. Ретенционная гиперазотемия является одним из факторов, играющих роль в развитии уремической комы.
Возможно развитие смешанной (комбинированной) формы гиперазотемии, при которой повышенный распад белка в тканях сочетается с недостаточным выведением азотистых продуктов с мочой. Такое сочетание возможно при острой почечной недостаточности, развившейся на почве септического аборта, или обширном сдавлении тканей (синдром раздавливания). К комбинированной форме гиперазотемии относится гипохлоремическая гиперазотемия, возникающая при неукротимой рвоте, стенозе привратника и профузных поносах.
3. Ишемическая болезнь сердца; этиология, патогенез. Стенокардия, инфаркт миокарда; ведущие клинические проявления.
ИБС - патология сердца, обусловленная острой или хронической рецидивирующей ишемией миокарда вследствие сужения или закупорки атеросклеротическими бляшками просвета коронарных артерий сердца либо в результате сопутствующих атеросклерозу тромбоза или спазма коронарных артерий.
Этиология и патогенез. В основе И. б. с. всегда лежит коронарная недостаточность, обусловленная атеросклерозом коронарных артерий сердца, поэтому ее нельзя отождествлять с коронарной недостаточностью, к-рая может быть обусловлена и иными, чем атеросклероз, заболеваниями, напр, коронаритом. В то же время нельзя отождествлять И. б. с. и с атеросклерозом коронарных артерий, т. к. он не всегда сопровождается развитием коронарной недостаточности с ишемией миокарда.
Основой патогенеза ишемии миокарда при всех формах И. б. с. является несоответствие между потребностью сердечной мышцы в кислороде и питательных веществах и поступлением их по суженным коронарным артериям. Это несоответствие тем больше, чем уже просвет коронарных артерий и чем больше работа сердца; оно возрастает во время физической нагрузки, при психоэмоциональном напряжении, на фоне которых обычно появляются симптомы обострения И. б. с. Важным патогенетическим фактором развития ишемии миокарда при И. б. с. может быть спазм коронарных артерий сердца. Этот фактор является ведущим в возникновении коронарной недостаточности у больных с минимально выраженным атеросклерозом коронарных артерий. В тех случаях, когда склероз и обызвествление стенок артерий препятствуют изменению их просвета, обострению коронарной недостаточности может способствовать спазм окольных (коллатеральных) сосудов, принимающих участие в кровоснабжении участка миокарда, подверженного ишемии. Большое значение в патогенезе коронарной недостаточности при И. б. с. имеют нарушения функции тромбоцитов и повышение свертываемости крови, что может ухудшать микроциркуляцию в капиллярах миокарда и приводить к тромбозу артерий, которому способствуют атеросклеротические изменения их стенок и замедление кровотока в местах сужения просвета артерий. Повторяющиеся и затяжные приступы стенокардии при обострении И. б. с. нередко обусловлены развитием тромбоза. При этом постепенно прогрессирующее сужение просвета пораженной артерии тромбом ведет к увеличению продолжительности болевых приступов, усилению ишемии миокарда и развитию в нем дистрофии вплоть до некроза.
Ишемия миокарда отрицательно отражается на функциях сердца - его сократимости, автоматизме, возбудимости, проводимости. Кратковременная ишемия обычно проявляется приступом стенокардии или ее эквивалентами: преходящим нарушением ритма, одышкой, головокружением или др. При этом в миокарде не успевают возникнуть сколько-нибудь выраженные морфологические изменения. Если ишемия длится 20-30 мин, развивается очаговая дистрофия миокарда. Более длительная ишемия, особенно при закрытии коронарной артерии тромбом, завершается некрозом участка сердечной мышцы, подвергшегося ишемии, - инфарктом миокарда.
Билет 36
2. Негазовые ацидозы и алкалозы: ведущие причины и механизмы возникновения, компенсаторные процессы, расстройства в организме и их клинические проявления. Показатели этих форм нарушений кислотно-основного состояния. Принципы лекарственной терапии.
Метаболический (негазовый) ацидоз:
Причины:
Экзогенные – отравление кислотами
Эндогенные – гипоксические состояния (гипоксия, тяжелая физическая работа), нарушения метаболизма (голодания, сахарный диабет, печеночная недостаточность, опухоли, дисбактериозы).
Патогенез метаболического ацидоза:
Показатели: уменьшение суммы оснований (ВВ), дефицит оснований ( рост ВЕ «-»).
Механизмы компенсации:
Гипервентиляция - уменьшается напряжение углекислого газа и сумма бикарбоната .
Активация ацидо- и аммониогенеза – увеличение титрационной кислотности мочи.
Ионно-обменный механизм – протоны водорода поступают в клетку в обмен на ионы калия, поэтому у пациента гиперкалиемия, а в костной ткани 2 протона водорода обмениваются с кальцием гиперкальциемия.
Механизмы повреждения:
Перераздражение дыхательного центра кислотами дыхание Куссмауляпадает напряжение углекислотыснижение возбудимости ДЦ и СДЦ
Снижение рСО2 (гипокапния) уменьшение сосудистого тонусападает АД
На фоне сниженного АД ишемия почекснижение фильтрацииолигурия
При понижении рН мочи до 4.5 и ниже некроз клеток эпителия канальцев
Гиперкалиемия + гиперадреналинемия фибрилляция сердца
Повышается осмолярность внеклеточной жидкости обезвоживание клеток
Декальцинация костей
Выделительный ацидоз:
Почечный – развивается при накоплении кислот и потере оснований – при почечной недостаточности, интоксикации сульфаниламидами, обессоливании нефритов, гипоксия ткани почек.
Кишечный – потеря оснований – причины: диарея, фистула тонкого кишечника, открытая рана тонкого кишечника, рвота кишечным содержимым при непроходимости кишечника.
Гиперсаливационный – потеря оснований – при стоматитах, отравлении никотином, препаратами ртути, токсикоз беременных, гельминтоз.
Метаболический (негазовый) алкалоз
Этиология:
Экзогенные:
Отравление щелочами
Избыточный прием соды
Лечение глюкокортикостероидами
Эндогенные:
Гиперальдостеронизм
Болезнь Иценко-Кушинга
Потеря кислот
Выделительный алкалоз
Желудочный – при потере соляной кислоты. На фоне токсикоза беременных, при пилороспазмах и пилоростенозах, при кишечной непроходимости.
Почечный – увеличение реабсорбции оснований, повышении выделения хлоридов, калия, и усиление экскреции протонов водорода в почках. Это может быть результат: длительного применения диуретиков, антибиотиков, нитратов.
Кишечный – увеличение выделения калия из кишечника. Результат: злоупотребление слабительными, повторные применения клизм.
Дегидратационный – при потере хлоридов - при повышенном потоотделении.
Патогенез: при алкалозе в избытке в организме – основания, и в дефиците – протоны водорода. Показатели: рост общая сумма оснований, рост «+» ВЕ.
Механизмы компенсации:
Гиповентиляция – рост рСО2, и рост SB
Блокада ацидо- и аммониогенеза – титрационная кислотность = 0
Экскреция натрия с мочой – гипонатриемия –> вторичный альдостеронизм –гиперкалиурия – гипокалиемия
Калий в крови уменьшается, т.к выходят протоны водорода.
Механизмы повреждения:
Угнетение внешнего дыхания
Повышение нервно-мышечной возбудимости из-за гипокальциемии и гипокалиемии тетания
Повышение активности β-адренорецепторов, снижение тонуса вагуса тахикардия, снижение АД, запоры, уменьшение секреции пищеварительных соков
На фоне гипокалиемии нарушается деятельность сердца: удлинение Q-T, отрицательный зубец Т, желудочковая тахикардия.
3. Сердечная недостаточность; характеристика понятия, стадии и формы. Одышка, цианоз, сердцебиение и отёки; их происхождение.
Это типовая форма патологии, при которой сердце не обеспечивает потребности органов и тканей в адекватном (их функции и уровню пластических процессов) кровоснабжении.
Виды СН:
По происхождению:
Непосредственное повреждение – миокардиальная
Перегрузочная
Смешанная
По скорости развития:
Острая
Хроническая
По преимущественному повреждению отдела сердца:
Левожелудочковая
Правожелудочковая
Смешанная
Миокардиальная СН
Могут приводит:
Экзогенные факторы:
Физической природы – травмы, электрический ток (особенно если проходит, и затрагивает сердце), механическое сдавление сердца, например экссудатом, опухолью.
Химические факторы – сердечные гликозиды, адреномиметики, ингибиторы кальциевых каналов, разобщители окислительного фосфорилирования, алкоголь.
Биологические факторы – различные бактерии и их токсины, токсоплазма, грибы.
Эндогенные факторы: различные гипо- и авитаминозы, особенно группы В; голодание; гипоксия; поражение коронарных сосудов (ИБС); тиреотоксикоз; лихорадка (особенно длительная); стресс (особенно хронический); электролитно стероидное нарушение в организме; антимиокардиальные АТ; циркулирующие иммунокомплексыпри аутоиммунных заболеваниях, ревматизме и т.д.
Разделяется на:
Некоронарогенная
Коронарогенная
Перегрузочная СН
2 типа перегрузки:
Факторы, увеличивающие преднагрузку – увеличение объема крови.
Наблюдается при: гиповолемии, полицитемии, а также при пороках недостаточности клапанов сердца.
По закону Франка-Старлинга: чем больше растяжение мышечного волокна, тем больше сила его сокращения – гетерометрический тип сокращения, изотонический тип сокращения кардиомиоцитов повышение потребности в кислороде на 20%.
Увеличивающие постнагрзку – перегрузка сопротивлением. Формируется при наличии препятствия на пути выхода крови: артериальная гипертензия, коарктация аорты, стеноз ЛА, тромбоэмболия ЛА, стеноз клапанов сердца.
Преодоление повышенного сопротивления току крови рост напряжения мышечного волокнагетерометрический, изометрический тип сокращения кардиомиоцитовповышение потребности в кислороде на 200%.
Механизмы компенсации
Со стороны сердца: тахикардия и гипертрофия
Экстракардиальные: тахипноэ, эритроцитоз, активация ферментов тканевого дыхания.
Отек:
Уменьшение минутного объема сердца повышение давления в венозной части капилляровтранссудация жидкости в ткани
Ишемия почек активация ренин-ангиотензин-альдостероновой системы.
В ответ на уменьшение МОС рефлекторно увеличивается синтез альдостерона повышается реабсорбция Naповышается реабсорбция водыувеличивается ОЦК
Патогенез сердечных отеков
Уменьшение минутного объема сердца Снижение скорости кровотокациркуляторная гипоксия:
Гипоксия печени снижение синтеза альбуминовснижение онкотического давления крови
Активация анаэробного гликолиза ацидозповышение проницаемости сосудов
Транссудация жидкости в ткани
Билет 37
2. Недостаточность неспецифического и специфического иммунитета, гуморальных и клеточных его механизмов. Их клинические проявления.
Механизмы патологической толерантности
Апоптоз цитотоксических лимфоцитов
Активация Т-супрессоров
Экранирование чужеродных антигенных детерминант иммуноглобулинами
Антигенная перегрузка иммунной системы (при значительных переливаниях)
Иммунодефицит
Иммунодефицитные состояния (ИДС)
Типовая форма патологии системы иммунобиологического надзора; характеризуется снижением эффективности или полной неспособностью ее осуществлять реакции обнаружения, деструкции и элиминации чужеродного антигена.
Иммунодефицитные состояния
Первичные – наследственные и врожденные – собственный иммунодефицит
Вторичные – приобретенные – иммунодеперссия
В зависимости от того какие компоненты повреждаются иммунобиологического надзора:
Т-зависимые (Т-клеточные)
В-зависимые (В-клеточные, гуморальные)
А-зависимые (А-клеточные, фагоцитарные)
Смешанные (комбинированные)
Первичные иммунодефициты
Наследственные, связанные с генетическим аппаратом, и передающиеся по наследству – составляют треть от первичных
Наиболее часто встречаются В-клеточные (больше половины), около 20% - Т+В (комбинированные), 15% - дефицит Т-системы, фагоцитарный дефект
Передаются обычно по рецессивному пути, могут быть аутосомные, сцепленные с Х – хромосомой
Врожденные заболевания – формируются внутриутробно – особенно 1 триместр беременности. Факторы: физические, ионизирующая радиация, флюорография, химические факторы (лекарственные препараты, например, 1 таблетки аспирина хватит для развития порока сердца), инфекционные, вирусные воздействия.
Дефицит Т-системы проявится: вирусная инфекция, генерализованные форма инфекции – герпес, вирусные пневмонии, хроническое течение вирусных инфекций, активируются грибковые инфекции (особенно кандидоз). Ослабленные живые вакцины (БЦЖ) смертельно опасны, они дают заболевания – туберкулез, полиомиелит.
Дефицит В-системы
Агаммаглобулинемия, сцепленная с Х-хромосомой (болезнь Брутона) – выраженный полиартрит
Дефицит А-системы
Синдром Чедиага-Хигаси – альбинизм
Комбинированные иммунодефициты
Аутосомно-рецессивная форма («швейцарский» тип)
Рецессивная, сцепленная с Х-хромосомой
Синдром Луи-Бар (с атаксией, телеангиэктазией)
Ретикулярный дисгенез (отсутствие иммунитетов, фагоцитов)
Вторичные, или приобретенные иммунодефициты
Активировался с появлением ВИЧ.
Возникают в результате действия иммунодепрессантов: глюкокортикоиды, цитостатики, антилимфоцитарная сыворотка, ионизирующая радиация, рентгеновское излучение, нарушение обменных процессов в организме (голодание, частичное и полное, дисмикролементозы, нарушение всасывания в ЖКТ, потеря бела, интоксикации, сахарный диабет), хронический стресс, на фоне опухолей.
Инфекционные факторы – нелимфотропные, не является прямым объектом поражения – икобактерия туберкулеза, сифилис, бруцеллез, грибы, вирусы, простейшие, гельминты.
3. Желтухи; виды и проявления.
Желтуха
Это синдром, характеризующийся избыточным содержанием в крови интерстициальной жидкости и моче желчных пигментов, с желтушным окрашиванием кожи, слизистых и биологических жидкостей.
Билирубин образуется в результате гемолиза эритроцитов в РЭС. Образуется гемм билирубиннепрямой билирубин (он циркулирует в крови у всех, в норме до 20 мкмоль).
Непрямой билирубин захватывается гепатоцитами, и гепатоцит связывает его с 2 молекулами глюкуроновой кислоты прямой билирубин (связанный), т.е образуется в гепатоцитах.
Прямой билирубин по желчевыводящим путям поступает в кишечник. В кишечнике он превращается в уробилиноген по системе воротной вены поступает обратно в печень и в печни он расщепляется до пиррола. И второе вещество – стеркобилиноген, он не всасывается, идет в кал и обусловливает специфическую окраску кала.
Виды желтух:
Печеночная, или паренхиматозная.
В крови увеличивается содержание прямого билирубина моноглюкуронида. В кишечник поступает мало желчи там образуется мало стеркобилиногенакал гипохоличен, но реакция на стеркобилиноген будет положительной. Уробилиноген всасывается, поступает в печеньпечень отправляет его в общий кровоток, т.е в моче будет уробилиноген (реакция мочи положительная). Моча будет темная за счет прямого билирубина.
Еще характерный признак – холемия. У пациента будет кожный зуд, расчесы. Желчный кислоты обладают ваготропным эффектом у пациента брадикардия и артериальная гипотензия
Подпеченочная, или механическая.
Связана с обтурацией общего желчного протока. Частая причина – желчно-каменная болезнь. Кроме причинами могут быть: опухоль головки поджелудочной железы, гельминтозы (описторхи, аскариды).
Печень работает у пациента хорошо. Повышается давление внутри желчных ходов, и разрываются желчные капилляры. Признаком цитолиза является фермент щелочная фосфотаза.
В крови прямой билирубин диглюкуронил – гипербилирубинемия. Моча темная, и кожа цвета пива за счет прямого билирубина. Желчь в кишечник не поступает кал ахоличен, стеркобилиногена нет, в моче уробилиногена нет. Холемия, у пациента зуд, брадикардия, артериальная гипотензия.
В крови возрастает содержание холестерина (субстрат для синтеза желчных кислот) ксантомы – пропитывание холестерином кожи – пятна.
Формируется синдром ахолии: обесцвеченный кал, стеаторея, дисбиоз кишечника, диспепсия, кишечная аутоинтоксикация, дефицит жирорастворимых витаминов.
Дефицит жирорастворимого витамина К.
Проба Бондарь – пациенты вводят парентерально водорастворимый аналог витамина К.
Надпеченочная, или гемолитическая.
