- •Министерство образования и науки
- •1 Растворы
- •1.1 Основные понятия и определения
- •1.2 Способы выражения состава раствора
- •1.3 Закон Рауля. Идеальные растворы
- •1.4 Следствия из закона Рауля
- •1.4.1 Повышение температуры кипения идеального раствора
- •1.4.2 Понижение температуры замерзания раствора
- •1.5 Осмотическое давление
- •1.6 Реальные растворы
- •1.6.1 Отклонения от закона Рауля
- •1.6.2 Активность. Коэффициент активности
- •1.7 Растворимость
- •1.7.1 Растворимость твердых веществ в жидкости
- •1.7.2 Растворимость газов в жидкости
- •1.7.3 Взаимная растворимость жидкостей
- •1.8 Равновесие жидкий раствор – насыщенный пар в различных жидких смесях
- •1.8.1 Неограниченно смешивающиеся жидкости
- •1.8.1.1 Состав пара и жидкости. Законы Коновалова
- •1.8.1.2 Разделение бинарных смесей путем перегонки
- •1.8.2 Равновесие жидкость - пар для практически несмеши-вающихся жидкостей
- •1.8.3 Равновесие жидкость – пар для ограниченно смешивающихся жидкостей
- •1.9 Закон распределения Нернста. Экстракция
- •1.10 Примеры решения задач
- •1.11 Вопросы для самоконтроля
- •2 Электрохимия
- •2.1 Электрическая проводимость растворов электролитов
- •2.1.1 Сильные и слабые электролиты
- •2.1.2 Удельная электрическая проводимость
- •2.1.3 Молярная и эквивалентная электрические проводимости
- •2.1.4 Числа переноса
- •2.2 Кондуктометрия
- •2.2.1 Определение растворимости труднорастворимой соли
- •2.2.2 Определение предельной эквивалентной электрической проводимости растворов сильных электролитов
- •2.2.3 Кондуктометрическое титрование
- •2.3 Электродные процессы
- •2.3.1 Основные понятия и определения
- •2.3.2 Классификация электродов
- •2.3.3 Типы гальванических элементов
- •2.3.4 Диффузионный потенциал
- •2.3.5 Потенциометрическое титрование
- •2.4 Скорость электрохимической реакции
- •2.4.1 Поляризационные кривые
- •2.4.2 Перенапряжение
- •2.4.3 Электролиз
- •2.4.3.1 Электролиз водного раствора CuCl2
- •2.4.3.2 Электролиз водного раствора к2sо4 с использованием инертных анодов
- •2.4.3.3 Законы Фарадея
- •2.5 Примеры решения задач
- •2.6 Вопросы для самоконтроля
- •Кинетика
- •3.1 Скорость химической реакции
- •3.2 Кинетическая классификация химических реакций
- •3.2.1 Молекулярность реакции
- •3.2.2 Порядок реакции
- •3.3 Влияние температуры на скорость реакции. Энергия активации
- •3.4 Методы определения порядка реакции
- •3.5 Сложные реакции
- •3.5.1 Параллельные реакции
- •3.5.2 Обратимые реакции
- •3.5.3 Последовательные реакции
- •3.5.4 Сопряженные реакции
- •3.5.5 Метод стационарных концентраций
- •3.6 Примеры решения задач
- •3.7 Вопросы для самоконтроля
- •Литература
1.9 Закон распределения Нернста. Экстракция
Если взять две несмешивающиеся жидкости и добавить третий компонент, то он будет растворяться в разной степени в том и другом растворителе.
«При установлении равновесия отношение концентраций полученных растворов постоянно при данной температуре» - закон распределения Нернста (1.13).
![]() = К,
(1.13)
= К,
(1.13)
где
![]() - концентрации третьего компонента вI
и II
фазах; К - коэффициент
распределения.
- концентрации третьего компонента вI
и II
фазах; К - коэффициент
распределения.
Если растворенное вещество диссоциирует или ассоциирует в одном из растворителей, то уравнение Нернста имеет вид:
![]() = К,
(1.14)
= К,
(1.14)
Для нахождения Кип логарифмируем уравнение (1.14) и получаем уравнение прямой:
![]()
Построив
прямую в координатах
![]() ,
найдем «п»
как тангенс
угла наклона прямой (по любым двум
точкам, лежащим на прямой) tga
=
,
найдем «п»
как тангенс
угла наклона прямой (по любым двум
точкам, лежащим на прямой) tga
=
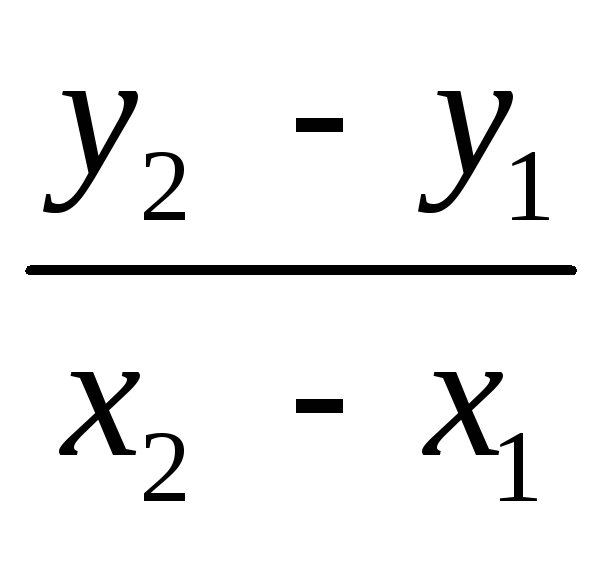 .
.
InK можно найти из уравнения, подставив в него значения любой точки, находящейся на прямой.
Закон распределения Нернста лежит в основе процесса экстракции. Экстракция это извлечение компонента из одной фазы в другую. Экстракция бывает твердофазная - извлечение веществ из твердой фазы в жидкую (например, заваривание чая, кофе, приготовление настоек, экстрактов трав и так далее) и жидкофазная - извлечение растворенного вещества из жидкого раствора экстрагентом. Раствор извлеченного вещества в экстрагенте называется экстрактом, а исходный раствор после извлечения из него вещества называется рафинатом.
Для расчета эффективности жидкофазной экстракции используют уравнение (1.15):
![]() ,
(1.15)
,
(1.15)
где х - доля неизвлеченного вещества в рафинате;
V - объем исходного раствора;
![]() - объем экстрагента;
- объем экстрагента;
К - коэффициент распределения
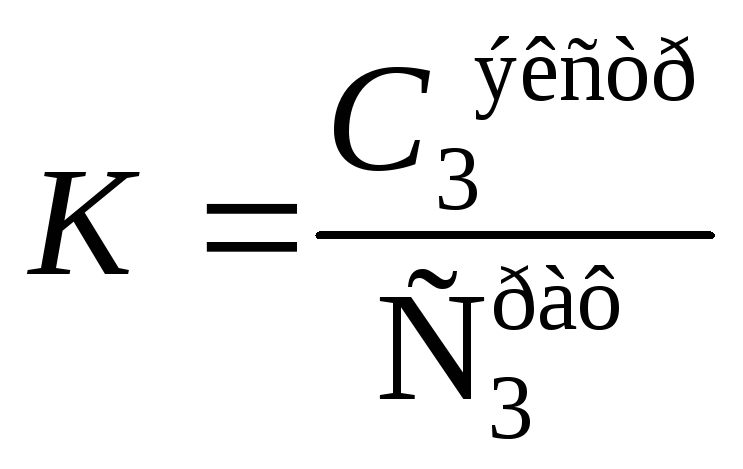 ;
;
п - число экстракций.
Как видно из уравнения (1.15), чем больше экстракций, тем меньше остается вещества в рафинате, то есть неизвлеченным, тем больше вещества извлекается экстрагентом. Эффективность экстракции в большой степени определяется величиной коэффициента распределения: чем больше коэффициент в пользу экстрагента, тем эффективнее экстракция.
Часто в справочнике дается коэффициент распределения как отношение концентраций в рафинате к экстракту, то есть величина, обратная той, что должна быть в уравнении (1.14). В этом случае следует взять величину обратную справочной и использовать в уравнении (1.15), или использовать другое уравнение, где
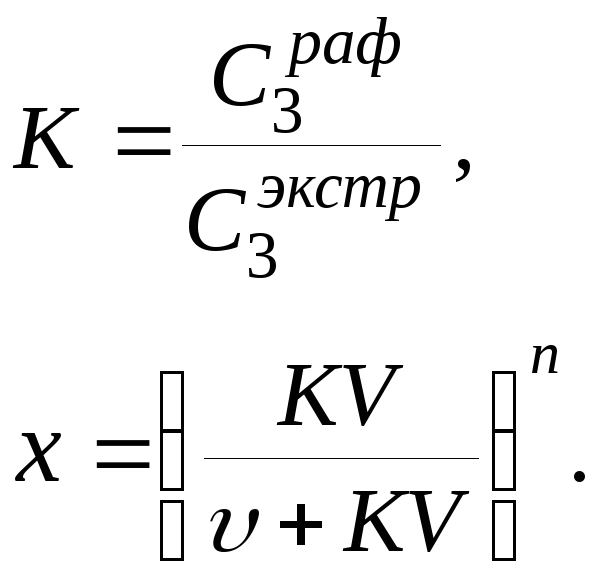
1.10 Примеры решения задач
Задача 1
50 г водного раствора FeCl2 с моляльностью 1,97 моль/кг с плотностью 1,332 г/см3 смешали со 150 мл 5 масс. % раствора FeCl2 с плотностью 1,038 г/см . Выразить состав полученного раствора всеми возможными способами.
Дано:
Раствор 1: Раствор 2:
![]() =50r
=50r ![]() =
150 мл
=
150 мл
b![]() =1,97моль/кг
=1,97моль/кг ![]()
![]() =
1,332 г/см3
=
1,332 г/см3 ![]() =
1,038 г/см3
=
1,038 г/см3
b3 = ? W3 = ? Х 3= ?
Решение:
Для каждого раствора найдем массу FeCl2 и Н20.
Раствор
1:
b![]() =
1,97 моль/кг, то есть на 1 кг воды приходится
1,97 моль FeCl2,
=
1,97 моль/кг, то есть на 1 кг воды приходится
1,97 моль FeCl2,
![]() =
l,97MFeCl2
=
1,97∙127,5 =251 г;
=
l,97MFeCl2
=
1,97∙127,5 =251 г;
![]()
![]() = 1000 г ; mp.pa=
1251 г
= 1000 г ; mp.pa=
1251 г
1251 г (р-ра) - 251г FeCl2 ;
50 г р-ра -
![]() х
FеCl2
х
FеCl2
![]() г.
г.
Итак, в растворе
1:
![]() = 10 г;
= 10 г;
![]() = 50 – 10 = 40 г.
= 50 – 10 = 40 г.
Раствор
2:
m
р.ра
=∙V
= 1,038 ∙ 50 =156 г;
![]()
![]() = 156-8=
148 г
= 156-8=
148 г
Раствор 3:
m
р-pa
= 50 + 156 = 206 г ;
![]() =10
+ 8=18г
=10
+ 8=18г
mH2O =40+ 148 = 188 г
![]()
b
![]()
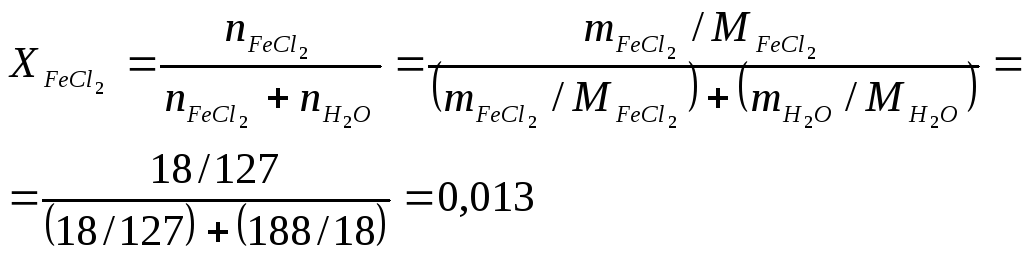
Рассчитать молярную концентрацию нет возможности, поскольку неизвестна плотность полученного раствора.
Задача 2
При 100 °С тетрахлорэтилен имеет давление насыщенного пара 400 мм.рт.ст., а бромбензол - 196 мм.рт.ст.. Найти состав раствора, кипящего при 100 °С под давлением 360 мм.рт.ст., и состав насыщенного пара над раствором. Считать раствор идеальным.
Дано:
![]() =400
мм.рт.ст.
=400
мм.рт.ст.
![]() =
196 мм.рт.ст.
=
196 мм.рт.ст.
t = 100 °С
Pобщ = 360 мм.рт.ст.
![]()
![]()
Решение:
Кипение наступает тогда, когда внешнее давление и давление насыщенного пара равны. Следовательно, 360 мм.рт.ст. - это и внешнее давление и общее давление насыщенного пара над раствором.
![]()
![]()
![]() ;
;
![]()
![]()
Задача 3
При 25 °С константа распределения иода между водой и амиловым спиртом равна 0,00435. Сколько граммов иода останется в трех литрах водного раствора (С = 1,3 г/л) после двухкратной экстракции амиловым спиртом, если всего израсходовано 400 мл спирта?
Дано:
К
= 0,00435 =
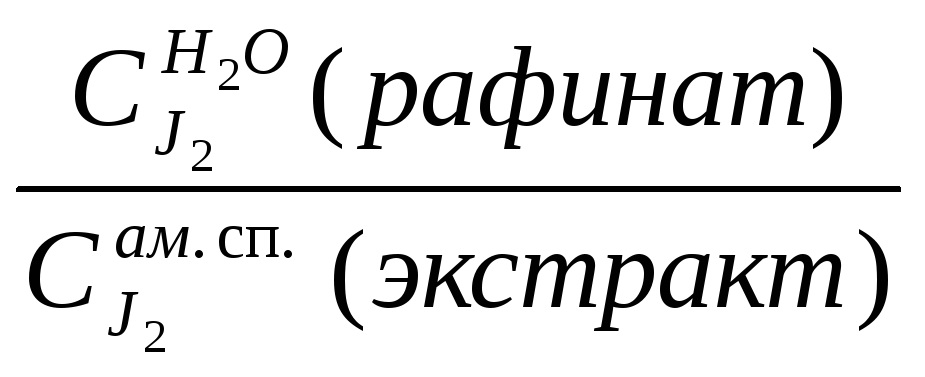
![]() =1,3г/л
=1,3г/л
п = 2
V= 3 л
![]() =
400/2 = 200 мл = 0,2 л
=
400/2 = 200 мл = 0,2 л
![]() =
?
=
?
Решение:
Экстрагентом является амиловый спирт. Следовательно, данная константа распределения является обратной, требуемой в уравнении для расчета эффективности экстракции:
![]()
Рассчитываем константу распределения:
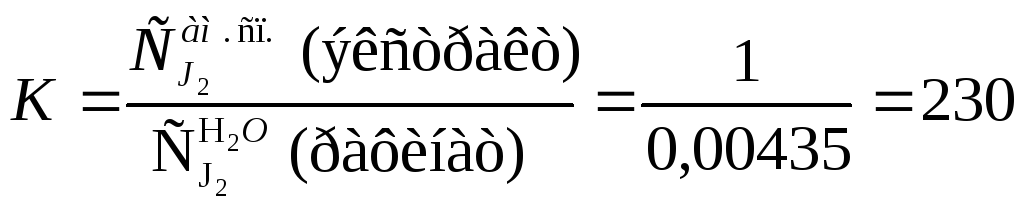
![]() - доля иода,
оставшегося в рафинате.
- доля иода,
оставшегося в рафинате.
Масса растворенного иода в исходном растворе:
![]()
m = m0x = 3,9.0,0037 = 0,014 г - масса иода, оставшегося в рафинате
Задача 4
Закрытый сосуд объемом 5,0 л содержит газ Н2S при температуре 20 0С и давлении равном 740 мм. рт. ст. Какой объем воды должен быть добавлен, чтобы парциальное давление Н2S понизилось до 500 мм. рт. ст.? Коэффициент абсорбции Н2S (α) равен 2,58.
Дано:
![]() =
5,0 л = 5,0∙10-3
м3
=
5,0 л = 5,0∙10-3
м3
t1 = 20 0C
T1 = T2 = 293 K
P = 740 мм.рт.ст.= 0,984∙105 Па
α = 2,58
![]() - ?
- ?
Решение:
Понижение давления происходит за счет растворения части Н2S в воде. Рассчитаем исходное количество Н2S и остаточное количество Н2S после растворения его в воде.
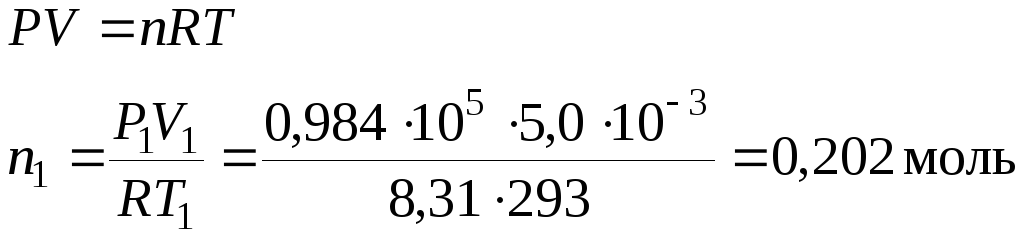
Пренебрежем изменением объема газа за счет добавления воды, то есть V2 = V1.
![]()
Рассчитаем количество Н2S, растворенное в воде:
![]()
Рассчитаем V0 – объем Н2S, приведенный к нормальным условиям (Р = 1,0133∙105 Па, Т = 273,15 К), который растворен в воде:
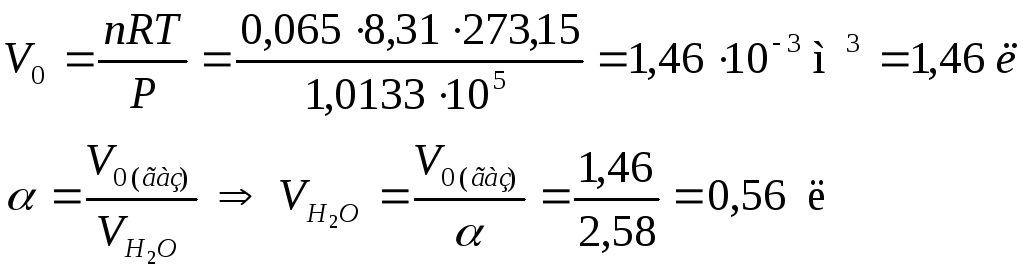
Задача 5
Метан плавится при температуре 90,5 К, его теплота плавления равна 70,7 Дж/моль. Определить растворимость метана в жидком азоте при температуре 50 К.
Дано:
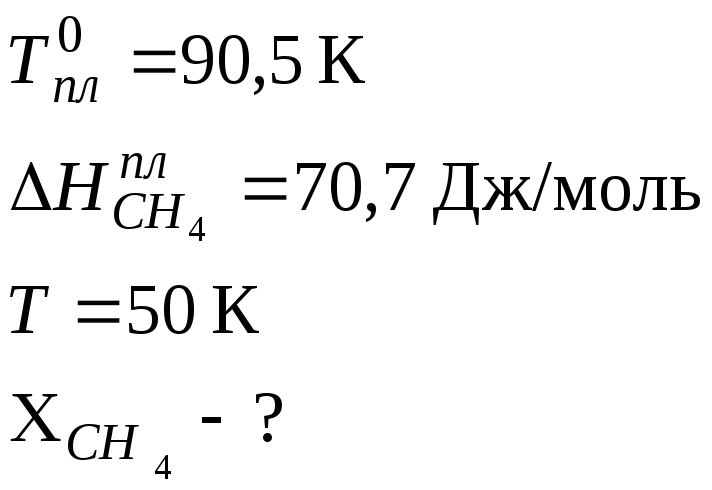
Решение:
Обычно мы знаем метан как газ, но в данном случае речь идет о твердом метане при температуре ниже его температуры плавления. Следовательно, надо найти растворимость твердого вещества в жидкости, что можно выполнить по уравнению Шредера: