
- •Министерство образования и науки
- •1 Растворы
- •1.1 Основные понятия и определения
- •1.2 Способы выражения состава раствора
- •1.3 Закон Рауля. Идеальные растворы
- •1.4 Следствия из закона Рауля
- •1.4.1 Повышение температуры кипения идеального раствора
- •1.4.2 Понижение температуры замерзания раствора
- •1.5 Осмотическое давление
- •1.6 Реальные растворы
- •1.6.1 Отклонения от закона Рауля
- •1.6.2 Активность. Коэффициент активности
- •1.7 Растворимость
- •1.7.1 Растворимость твердых веществ в жидкости
- •1.7.2 Растворимость газов в жидкости
- •1.7.3 Взаимная растворимость жидкостей
- •1.8 Равновесие жидкий раствор – насыщенный пар в различных жидких смесях
- •1.8.1 Неограниченно смешивающиеся жидкости
- •1.8.1.1 Состав пара и жидкости. Законы Коновалова
- •1.8.1.2 Разделение бинарных смесей путем перегонки
- •1.8.2 Равновесие жидкость - пар для практически несмеши-вающихся жидкостей
- •1.8.3 Равновесие жидкость – пар для ограниченно смешивающихся жидкостей
- •1.9 Закон распределения Нернста. Экстракция
- •1.10 Примеры решения задач
- •1.11 Вопросы для самоконтроля
- •2 Электрохимия
- •2.1 Электрическая проводимость растворов электролитов
- •2.1.1 Сильные и слабые электролиты
- •2.1.2 Удельная электрическая проводимость
- •2.1.3 Молярная и эквивалентная электрические проводимости
- •2.1.4 Числа переноса
- •2.2 Кондуктометрия
- •2.2.1 Определение растворимости труднорастворимой соли
- •2.2.2 Определение предельной эквивалентной электрической проводимости растворов сильных электролитов
- •2.2.3 Кондуктометрическое титрование
- •2.3 Электродные процессы
- •2.3.1 Основные понятия и определения
- •2.3.2 Классификация электродов
- •2.3.3 Типы гальванических элементов
- •2.3.4 Диффузионный потенциал
- •2.3.5 Потенциометрическое титрование
- •2.4 Скорость электрохимической реакции
- •2.4.1 Поляризационные кривые
- •2.4.2 Перенапряжение
- •2.4.3 Электролиз
- •2.4.3.1 Электролиз водного раствора CuCl2
- •2.4.3.2 Электролиз водного раствора к2sо4 с использованием инертных анодов
- •2.4.3.3 Законы Фарадея
- •2.5 Примеры решения задач
- •2.6 Вопросы для самоконтроля
- •Кинетика
- •3.1 Скорость химической реакции
- •3.2 Кинетическая классификация химических реакций
- •3.2.1 Молекулярность реакции
- •3.2.2 Порядок реакции
- •3.3 Влияние температуры на скорость реакции. Энергия активации
- •3.4 Методы определения порядка реакции
- •3.5 Сложные реакции
- •3.5.1 Параллельные реакции
- •3.5.2 Обратимые реакции
- •3.5.3 Последовательные реакции
- •3.5.4 Сопряженные реакции
- •3.5.5 Метод стационарных концентраций
- •3.6 Примеры решения задач
- •3.7 Вопросы для самоконтроля
- •Литература
1.8.2 Равновесие жидкость - пар для практически несмеши-вающихся жидкостей
В гетерогенных системах, состоящих из нерастворимых друг в друге жидкостей, компоненты испаряются независимо. Поэтому в образующемся насыщенном паре, который находится в равновесии с двухслойной жидкой системой, парциальные давления каждого из компонентов не зависят от соотношения этих компонентов, а будут равны давлению насыщенного пара этих компонентов в чистом виде.
![]()
![]() .
Общее давление
.
Общее давление
![]() .
(1.10)
.
(1.10)
(Сравните с формулой для парциальных и общего давления неограниченно смешивающихся жидкостей (уравнение 1.2).
Из уравнения (1.10) видно, что общее давление выше давления пара каждого из компонентов в отдельности.
Жидкость закипает при той температуре, при которой давление ее насыщенного пара равно внешнему. Следовательно, давление над такой смесью достигает внешнего при более низкой температуре, чем каждый компонент в отдельности, а значит, температура кипения смеси будет ниже температуры кипения каждой жидкости в отдельности при том же внешнем давлении (рисунок 1.17).
Состав насыщенного пара не зависит от соотношения слоев и может быть рассчитан:
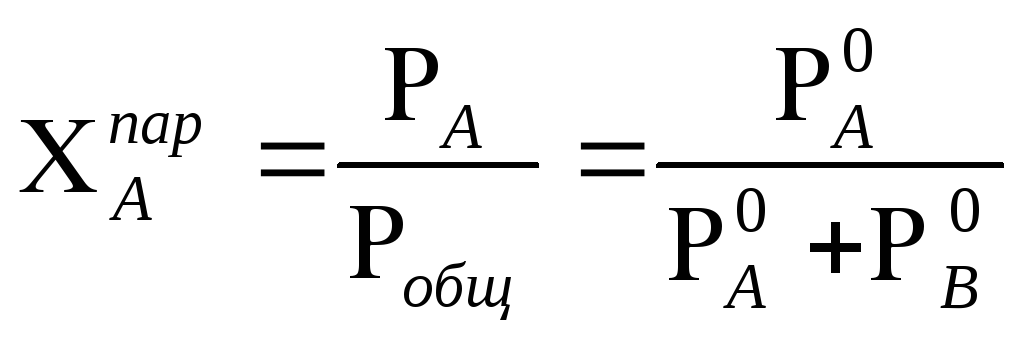 ,
,
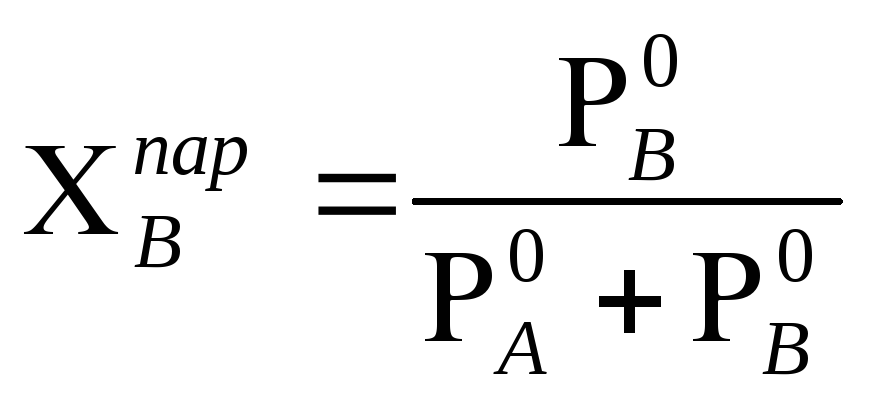 .
(1.11)
.
(1.11)
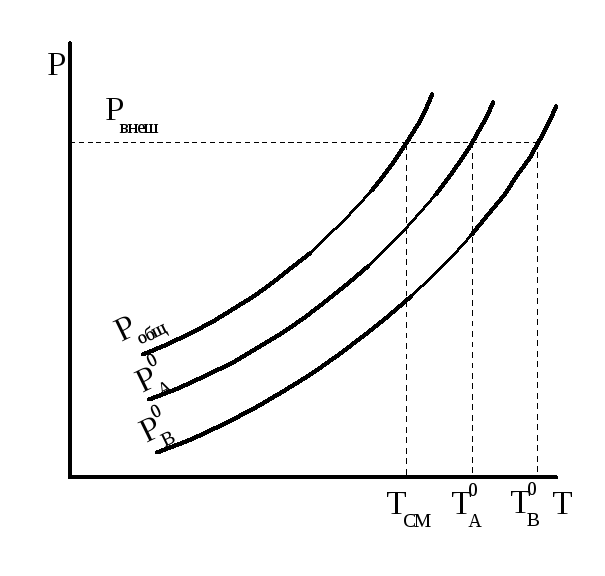
Рисунок 1.17 - Определение температуры кипения системы из несмешивающихся жидкостей
Рассмотренные особенности гетерогенных жидких систем широко используются на практике. Так, для очистки и выделения многих органических веществ, нерастворимых в воде, их перегоняют с водяным паром. Для этого сосуд с очищаемым веществом нагревают на водяной бане и пропускают водяной пар. Образующаяся гетерогенная смесь кипит при температуре < 100 °С. В дистилляте образуется два слоя: вода и органическое вещество. Перегонку с водяным паром используют для перегонки при более низкой температуре высококипящих веществ и веществ, разлагающихся при температуре их кипения.
Используя уравнения (1.11) можно рассчитать, так называемый, расходный коэффициент пара (g), то есть расход водяного пара на единицу массы отгоняемого вещества:
![]() ,
,
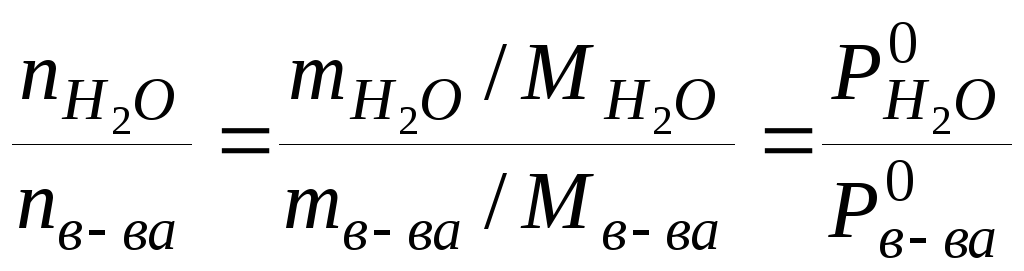 ,
откуда
,
откуда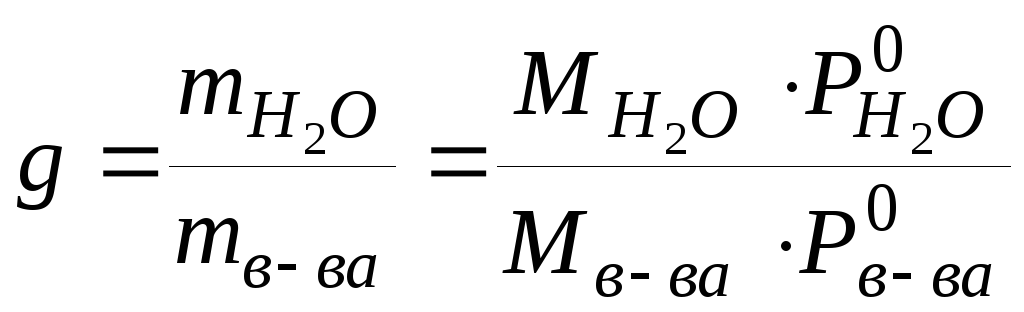 .
(1.12)
.
(1.12)
Из уравнения (1.12) следует, что расход водяного пара тем меньше, чем больше молярная масса и давление отгоняемого вещества.
1.8.3 Равновесие жидкость – пар для ограниченно смешивающихся жидкостей
Для жидкостей, образующих при смешении как области гомогенные, так и гетерогенные (двухслойные), диаграммы равновесия жидкость – пар могут быть построены в разных координатах.
Рассмотрим
построение диаграммы
![]() и
и![]() для случая, когда давления чистых
компонентов
для случая, когда давления чистых
компонентов![]() и
и![]() ,
не очень сильно отличаются друг от друга
(рисунок 1.18).
,
не очень сильно отличаются друг от друга
(рисунок 1.18).
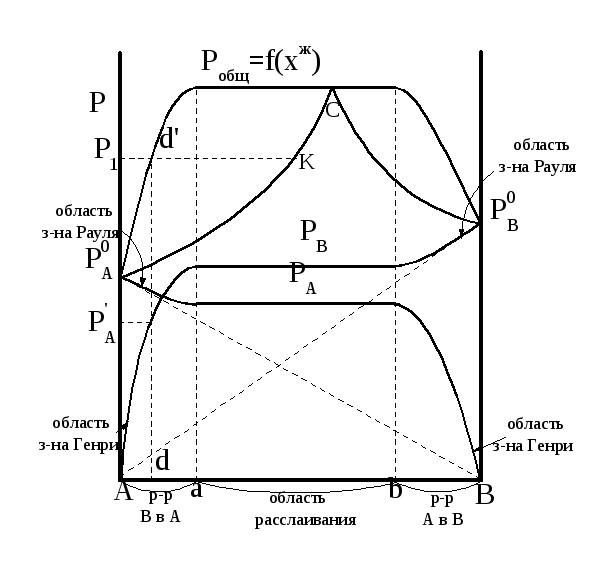
Рисунок 1.18 - Зависимость общего давления от состава жидкой фазы и пара для ограниченно смешивающихся жидкостей
Области А-а и В-b на оси состава – это области гомогенных растворов В в А и А в В, соответственно. Точки «а» и «b» - предел растворимости В в А и А в В, соответственно; а - b – область расслаивания, двухфазная область, равновесие двух жидких фаз состава «а» и «b».
Построение начинаем
с проведения пунктирных линий, отвечающих
идеальной зависимости парциальных
давлений от состава. Реальные кривые
будут отклоняться от этих кривых, имея
положительное
отклонение. Так, кривая
![]() в области действия закона Рауля (при ХА
→ 1) идет по пунктирной линии, затем
отклоняется до области расслаивания.
В области расслаивания
в области действия закона Рауля (при ХА
→ 1) идет по пунктирной линии, затем
отклоняется до области расслаивания.
В области расслаивания
![]() .
При ХА
→ 0 область действия закона Генри, линия
идет по прямой, но не по пунктирной.
Аналогично строим для РВ.
.
При ХА
→ 0 область действия закона Генри, линия
идет по прямой, но не по пунктирной.
Аналогично строим для РВ.
Далее строим линию
общего давления,
![]() ,
геометрически складывая значения
давлений при различных составах, начиная
с области расслаивания.
,
геометрически складывая значения
давлений при различных составах, начиная
с области расслаивания.
Построение линии
![]() начинаем с определения состава пара в
области расслаивания. Если два раствора
различного состава находятся в равновесии,
то химические потенциалы каждого из
компонентов в обоих растворах и в паре
должны быть одинаковы. Из этого следует,
что оба равновесных раствора дают пар
одинакового состава:
начинаем с определения состава пара в
области расслаивания. Если два раствора
различного состава находятся в равновесии,
то химические потенциалы каждого из
компонентов в обоих растворах и в паре
должны быть одинаковы. Из этого следует,
что оба равновесных раствора дают пар
одинакового состава:
![]()
В данной системе состав пара отвечает точке С – это равновесный пар для любой жидкой системы из области расслаивания а – b.
Аналогично находятся
составы пара над гомогенными системами
В
в А
и А
в В.
Так, для раствора d при общем давлении
над этим раствором Р1
парциальное давление компонента А
отвечает значению
![]() .
По уравнению (1.11) определяется состав
пара, равновесный с раствором d, и
отмечается на диаграмме точкой «К».
Таким образом, получается коннода,
соединяющая точки d´
и К, отвечающие равновесным фазам:
жидкости и насыщенному пару. Через
полученные точки проводим линии
.
По уравнению (1.11) определяется состав
пара, равновесный с раствором d, и
отмечается на диаграмме точкой «К».
Таким образом, получается коннода,
соединяющая точки d´
и К, отвечающие равновесным фазам:
жидкости и насыщенному пару. Через
полученные точки проводим линии
![]() и
и![]() .
.
