
- •Розділ 1. Організація вірусологічних лабораторій.
- •Обладнання вірусологічних лабораторій
- •Правила роботи в учбових вірусологічних лабораторіях
- •Практична частина
- •Контрольні питання та контрольні завдання
- •Література
- •Тема 1: Використання лабораторних тварин у вірусологічних дослідженнях
- •Природні інфекційні хвороби деяких лабораторних тварин, збудники яких є патогенними для людини
- •Індикаторні тварини
- •Гнотобіотичні тварини
- •Показники мікроклімату в приміщеннях для лабораторних тварин
- •Густота посадки в клітках лабораторних тварин та птахів
- •Причини канібалізму та заходи його профілактики
- •Основні показники нормальної життєдіяльності різних видів тварин
- •Зв’язок тропізму вірусу зі способом ураження чутливого організму та видом патологічного матеріалу
- •Допустимі дози досліджуваного матеріалу, що вводиться лабораторним тваринам, мл
- •Методи зараження через травний тракт
- •Перкутанне (нашкірне) зараження
- •Кутанне (шкірне) зараження
- •Субкутанне (підшкірне) зараження
- •Інтракутанне (внутрішньошкірне) зараження
- •Інтравенозне (внутрішньовенне) та інтракардіальне (внутрішньосерцеве) зараження
- •Інтрамускулярне (внутрішньом’язеве) зараження
- •Інтраперітонеальне (внутрішньочеревинне) зараження
- •Субокципітальне (каркове) зараження
- •Інтрацеребральне (внутрішньомозкове) зараження
- •Зараження в периферичний нерв
- •Інтратестикулярне (внутрішньосім’яникове) зараження
- •Інтраокулярне зараження
- •Корнеальне зараження
- •Інтракорнеальне зараження
- •Кон’юнктивальне зараження
- •Забір крові
- •Антикоагулянти
- •Лабораторне заняття
- •Тема 2. Курячі ембріони та їх використання у вірусології
- •Теоретична частина
- •Практична частина
- •Будова курячого ембріону
- •Практична частина Лабораторне заняття
- •Тема 3. Клітинні культури у вірусології
- •Теоретична частина
- •Класифікація тваринних культур клітин
- •Одношарові культури клітин
- •Чутливість первинних культур клітин до вірусів людини
- •Характеристика деяких із відомих клітинних ліній
- •Переваги та недоліки використання постійних культур клітин
- •Чутливість постійних клітинних культур до вірусів
- •Суспензійні культури клітин
- •Зберігання культур клітин
- •Умови культивування клітин in vitro
- •Поживні середовища
- •Середовище 199 (Морган, Мортон, Паркер; 1950 р.)
- •Контамінація культур клітин
- •Взаємодія вірусів із клітинами
- •Методи виявлення та ідентифікації вірусів у клітинних культурах
- •Цитопатична дія
- •Внутрішньоклітинні включення
- •Титрування вірусів у одношарових культурах клітин
- •Практична частина Лабораторне заняття
- •Хід роботи
- •Контрольні завдання
- •Контрольні запитання
- •Література
- •Розділ 3. Віруси бактерій
- •Теоретична частина Загальна характеристика вірусів бактерій
- •Практична частина Методи титрування бактеріофагів
- •Титрування фагу за методом Аппельмана (рідке середовище)
- •Хід роботи:
- •Практична робота: Виділення фагів із лізогенних культур
- •Розділ 4. Дослідження вірусів рослин
- •Теоретична частина
- •Практична частина
- •Тема. Способи передачі вірусів рослин. Рослини-індикатори.
- •Практична частина Лабораторне заняття
- •Тема. 2. Виділення, очистка та концентрування вірусів рослин
- •Практична частина
- •Теоретична частина
- •Розділ 5. Використання електронної мікроскопії у вірусологічних дослідженнях.
- •Практична частина Хід роботи
- •Розділ. 6. Методи діагностики вірусних інфекцій та ідентифікації вірусів
- •Тема 1. Серологічні методи досліджень
- •Теоретична частина Реакція гемаглютинації
- •Імунологічні методи дослідження
- •Імунодифузійні тести.
- •Радіоімунологічний аналіз (ріа)
- •Імунофлуоресцентний аналіз (іф)
- •Імуноферментний аналіз
- •Практична частина Практична робота №1
- •Хід роботи
- •Практична робота №2
- •Хід роботи
- •Список літератури
- •Тема 2. Застосування полімеразної ланцюгової реакції у вірусологчних дослідженнях
- •Обладнання для плр
- •Компоненти реакції.
- •Параметри температурних циклів
- •Аналіз плр-ампліфікованої днк
- •Real-time pcr (прл у реальному часі) та її застосування у вірусологічних дослідженнях.
- •Словник використаних термінів
- •Верхній агар
- •Нижній агар
- •Цитратний буфер, 0,1м, рН 3,0 –6,2
- •Ацетатний буфер,0,1м , рН 3.6-5,6 Розчин а
- •0,1М оцтова кислота
- •С) Солі та інші речовини, г/л
Радіоімунологічний аналіз (ріа)
В 1959 р. Р. Ялоу і С. Берсон розробили кількісний імунологічний метод виявлення інсуліну в плазмі людини з використанням інсуліну, міченого радіоактивним ізотопом йоду (151J). Використання радіоактивних ізотопів в поєднанні з імунохімічними методами досліджень дозволяє реалізувати виключну вибірковість останніх для мінімальних кількостей біополімерів. Особлива перевага радіоімунологічного аналізу – висока чутливість. З його допомогою вдається виявити нанограмові (10-9), а іноді і пікограмові (10-10) рівні антитіл та вірусів. В РІА поєднується специфічність, властива реакціям антиген-антитіло, з чутливістю, яку дає використання радіоактивної мітки.
Радіоімунологічний аналіз базується на законі дії мас, за яким речовина, що визначається, буде конкурувати зі своїм міченим аналогом (антигеном) за обмежену кількість зв’язуючих місць антитіла до досягнення хімічної рівноваги всіх компонентів реакційної суміші.
Принцип методу можна представити наступним чином:
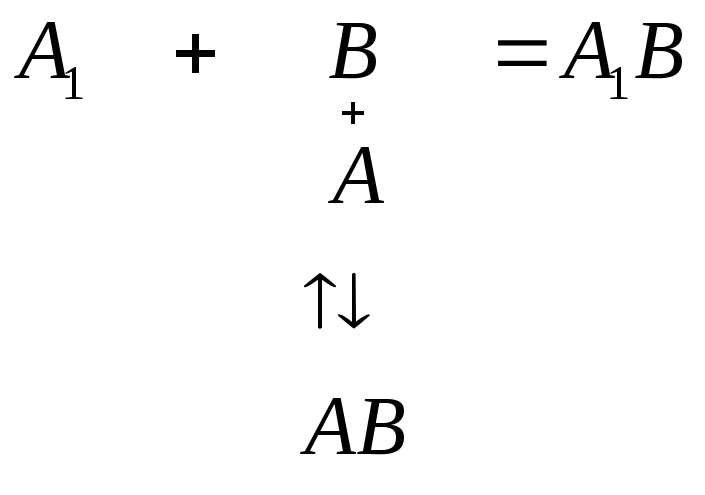
де А1 – вільний мічений антиген; В – специфічне антитіло; А – немічений антиген в дослідному матеріалі; А1В – зв’язаний мічений антиген; АВ – зв’язаний немічений антиген.
Мічений антиген зв’язується зі специфічним антитілом з утворенням міченого комплексу антиген-антитіло. При проведенні РІА проявляється здатність неміченого антигену дослідного матеріалу конкурувати за активні центри антитіл, пригнічуючи зв’язування міченого антигену. Як результат конкурентного пригнічення відношення зв’язаного з антитілом антигену до вільного міченого антигену зменшується при збільшенні концентрації неміченого антигену. Іншими словами, метод базується на здатності антитіл зв’язуватися з міченим радіоактивним ізотопом антигеном та на конкурентному пригніченні цієї реакції неміченим антигеном. Потім, коли цей антиген відділяється від незв’язаного, вимірюється радіоактивність однієї або обох фракцій.
Мітять препарати антигенів як правило радіоактивним 125І. Відомі різні засоби йодування білків: хлораміновий метод, лактопероксидазний, активованим ефіром та інші.
Існує декілька варіантів РІА, з яких в вірусології для практичної мети найчастіше використовують адсорбційний в різних модифікаціях: конкурентний метод (в рідкій фазі) та твердофазні прямий і непрямий методи. Останнім часом РІА використовується все рідше, оскільки пов’язаний з застосуванням радіоактивних ізотопів.
Імунофлуоресцентний аналіз (іф)
Імунофлуоресцентний аналіз, або метод флуоресціюючих антитіл, з’явився на початку 40-х років ХХ ст., коли А. Кунс з співробітниками використали здатність до флюоресценції одного з флюорохромів, кон’югували з ним антитіла і показали наявність збудника інфекції в тканинах. З того часу метод отримав значний розвиток і почав використовуватись в різних областях науки.
Особливість цього методу заключається в тому, що імунний комплекс стає видимим в люмінесцентному мікроскопі у випадку, якщо імуноглобулін кон’югується флюорохромом (флюоресцеіном, родаміном та ін.). В результаті ковалентного зв’язку антитіла з флюоресциюючим барвником утворюється нова сполука – флюоресциюючі антитіла. При цьому антитіла зберігають свою основну властивість – специфічність, а флюорохром – здатність до випромінювання світла.
Перевага імунофлуоресцентного аналізу в порівнянні з іншими методами полягає в дослідженні внутрішньоклітинної локалізації антигену (Рис. 20 (кольорова вклейка)).
Розроблені декілька варіантів реакції імунофлюоресценції: прямий, непрямий, сендвіч-метод, модифікація непрямого методу з використанням комплементу та інші (Рис.6.5).
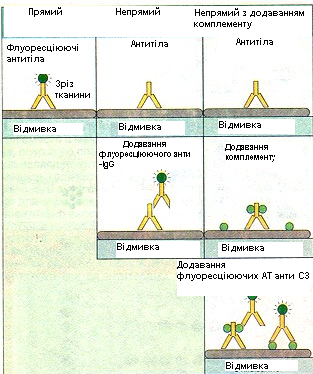
Рис. 6.5. Порівняння різних модифікацій імунофлюоресцентного аналізу.
