- •Розділ 1. Організація вірусологічних лабораторій.
- •Обладнання вірусологічних лабораторій
- •Правила роботи в учбових вірусологічних лабораторіях
- •Практична частина
- •Контрольні питання та контрольні завдання
- •Література
- •Тема 1: Використання лабораторних тварин у вірусологічних дослідженнях
- •Природні інфекційні хвороби деяких лабораторних тварин, збудники яких є патогенними для людини
- •Індикаторні тварини
- •Гнотобіотичні тварини
- •Показники мікроклімату в приміщеннях для лабораторних тварин
- •Густота посадки в клітках лабораторних тварин та птахів
- •Причини канібалізму та заходи його профілактики
- •Основні показники нормальної життєдіяльності різних видів тварин
- •Зв’язок тропізму вірусу зі способом ураження чутливого організму та видом патологічного матеріалу
- •Допустимі дози досліджуваного матеріалу, що вводиться лабораторним тваринам, мл
- •Методи зараження через травний тракт
- •Перкутанне (нашкірне) зараження
- •Кутанне (шкірне) зараження
- •Субкутанне (підшкірне) зараження
- •Інтракутанне (внутрішньошкірне) зараження
- •Інтравенозне (внутрішньовенне) та інтракардіальне (внутрішньосерцеве) зараження
- •Інтрамускулярне (внутрішньом’язеве) зараження
- •Інтраперітонеальне (внутрішньочеревинне) зараження
- •Субокципітальне (каркове) зараження
- •Інтрацеребральне (внутрішньомозкове) зараження
- •Зараження в периферичний нерв
- •Інтратестикулярне (внутрішньосім’яникове) зараження
- •Інтраокулярне зараження
- •Корнеальне зараження
- •Інтракорнеальне зараження
- •Кон’юнктивальне зараження
- •Забір крові
- •Антикоагулянти
- •Лабораторне заняття
- •Тема 2. Курячі ембріони та їх використання у вірусології
- •Теоретична частина
- •Практична частина
- •Будова курячого ембріону
- •Практична частина Лабораторне заняття
- •Тема 3. Клітинні культури у вірусології
- •Теоретична частина
- •Класифікація тваринних культур клітин
- •Одношарові культури клітин
- •Чутливість первинних культур клітин до вірусів людини
- •Характеристика деяких із відомих клітинних ліній
- •Переваги та недоліки використання постійних культур клітин
- •Чутливість постійних клітинних культур до вірусів
- •Суспензійні культури клітин
- •Зберігання культур клітин
- •Умови культивування клітин in vitro
- •Поживні середовища
- •Середовище 199 (Морган, Мортон, Паркер; 1950 р.)
- •Контамінація культур клітин
- •Взаємодія вірусів із клітинами
- •Методи виявлення та ідентифікації вірусів у клітинних культурах
- •Цитопатична дія
- •Внутрішньоклітинні включення
- •Титрування вірусів у одношарових культурах клітин
- •Практична частина Лабораторне заняття
- •Хід роботи
- •Контрольні завдання
- •Контрольні запитання
- •Література
- •Розділ 3. Віруси бактерій
- •Теоретична частина Загальна характеристика вірусів бактерій
- •Практична частина Методи титрування бактеріофагів
- •Титрування фагу за методом Аппельмана (рідке середовище)
- •Хід роботи:
- •Практична робота: Виділення фагів із лізогенних культур
- •Розділ 4. Дослідження вірусів рослин
- •Теоретична частина
- •Практична частина
- •Тема. Способи передачі вірусів рослин. Рослини-індикатори.
- •Практична частина Лабораторне заняття
- •Тема. 2. Виділення, очистка та концентрування вірусів рослин
- •Практична частина
- •Теоретична частина
- •Розділ 5. Використання електронної мікроскопії у вірусологічних дослідженнях.
- •Практична частина Хід роботи
- •Розділ. 6. Методи діагностики вірусних інфекцій та ідентифікації вірусів
- •Тема 1. Серологічні методи досліджень
- •Теоретична частина Реакція гемаглютинації
- •Імунологічні методи дослідження
- •Імунодифузійні тести.
- •Радіоімунологічний аналіз (ріа)
- •Імунофлуоресцентний аналіз (іф)
- •Імуноферментний аналіз
- •Практична частина Практична робота №1
- •Хід роботи
- •Практична робота №2
- •Хід роботи
- •Список літератури
- •Тема 2. Застосування полімеразної ланцюгової реакції у вірусологчних дослідженнях
- •Обладнання для плр
- •Компоненти реакції.
- •Параметри температурних циклів
- •Аналіз плр-ампліфікованої днк
- •Real-time pcr (прл у реальному часі) та її застосування у вірусологічних дослідженнях.
- •Словник використаних термінів
- •Верхній агар
- •Нижній агар
- •Цитратний буфер, 0,1м, рН 3,0 –6,2
- •Ацетатний буфер,0,1м , рН 3.6-5,6 Розчин а
- •0,1М оцтова кислота
- •С) Солі та інші речовини, г/л
Методи зараження через травний тракт
Зараження лабораторних тварин через травний тракт здійснюється трьома шляхами:
-
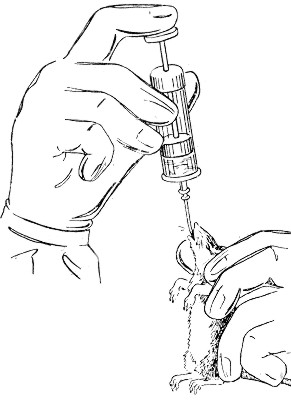
Оральний спосіб. Досліджуваний матеріал додають до сухого корму чи розчиняють у питній воді, або дають тварині у вигляді пігулок чи желатинових капсул, до складу яких вводять вірусовмісний матеріал і харчові продукти. При цьому методі тварин утримують в окремих клітках чи банках і за добу до введення не дають їжі (рис.2.8).
-
Матеріал у вигляді водних сумішей можна вводити безпосередньо в шлунок з допомогою різних засобів. Це може бути канюля – скляна трубка з відтягнутим кінцем або шприц з голкою, на якій напаяна на кінці голівка з олова, т.зв. “олива”. Так інфікують, в основному, мишей та пацюків. Для зараження мурчаків та кроликів використовують катетери, а для інфікування мишей, хом’яків, тхорів, пацюків, курей – тонкі гумові або металеві зонди діаметром 2-3 мм. Перед введенням гумовий зонд змочують гліцерином або рідким вазеліном. Металевий зонд виготовляють з трохи зігнутої голки для шприца з оливою на кінці. Зонд повинен проходити над язиком ближче до щік по задній стінці глотки по ходу стравоходу.
-
Ректальне зараження лабораторних тварин вірусовмісним матеріалом здійснюють через пряму кишку шляхом введення клізми, яка повинна мати температуру тіла тварини. Анальний отвір заклеюють лейкопластиром, завдяки чому прискорюється проникнення матеріалу в організм.
|
|
|
Рис.2.8. Оральний спосіб зараження лабораторних тварин через травний тракт. |
У вірусологічній практиці існує декілька методів зараження лабораторних тварин, при здійсненні яких об’єктом інфікування є шкіра тварин.
Перкутанне (нашкірне) зараження
Цей метод інфікування лабораторних тварин вірусовмісним матеріалом, так зване нашкірне зараження, проводять на неушкодженій шкірі тварин. Матеріал втирається в неушкоджену депільовану шкіру стерильним інструментом (кінець стерильної пробірки, фарфоровий товкачик). За даними багатьох дослідників цей метод майже не дає позитивних результатів.
Кутанне (шкірне) зараження
Це – так зване шкірне зараження лабораторних тварин на ушкоджену шкіру, яке здійснюється методом скарифікації. Для цього вибирають ділянку шкіри, яку тварина не може дістати лапами чи кігтями. Для різних тварин вона різна: спина (миші, мурчаки, пацюки, собаки), плантарна поверхня ступні (миші, хом’яки, мурчаки), бік (кролики), живіт (кролики), груди (кури) та сім’яники (кролики).
На вибраній ділянці шкіри роблять депіляцію та оброблюють її 3%-м розчином йоду. Потім роблять подряпини пером Дженнера чи хірургічною голкою до появи крапель лімфи, але щоб вони не кровоточили. На ушкоджену таким чином ділянку шкіри наносять матеріал краплями і втирають скляною паличкою, лопаткою, шпателем або обстриженою зубною щіткою.