- •«Национальный исследовательский
- •Томский политехнический Университет»
- •Е.В. Михеева, н.П. Пикула, а.П. Асташкина
- •Коллоидная химия
- •Оглавление
- •Глава 1 дисперсные системы
- •1.1. Общая характеристика дисперсных систем
- •1.1.1. Признаки объектов коллоидной химии
- •1.1.2. Специфические особенности высокодисперсных систем
- •1.2. Классификации дисперсных систем
- •1.2.1. Классификация по размерам частиц дисперсной фазы
- •1.2.2. Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •1.2.3. Классификация по силе межфазного взаимодействия дисперсной фазы и дисперсионной среды
- •1.2.4. Классификация по подвижности частиц дф (по структуре)
- •1.2.5. Классификация по фазовой различимости
- •1.2.6. Классификация по топографическому признаку (по форме частиц)
- •1.3. Методы получения дисперсных систем
- •1.3.1. Диспергационные методы
- •1.3.2. Конденсационные методы
- •1.3.2.1. Физические конденсационные методы
- •1.3.2.2. Химические конденсационные методы
- •2. Реакции обмена
- •3. Реакции окисления
- •1.3.3. Метод пептизации
- •1.4. Методы очистки дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 2 термодинамика поверхностных явлений
- •2.1. Классификация поверхностных явлений
- •2.2. Свободная поверхностная энергия и поверхностное натяжение
- •2.2.1. Физический смысл поверхностного натяжения
- •2.2.2. Термодинамическое определение поверхностного натяжения
- •2.2.3. Единицы измерения поверхностного натяжения
- •2.3. Влияние различных факторов на величину поверхностного натяжения
- •2.3.1. Влияние химической природы вещества
- •2.3.2. Влияние температуры
- •2.3.3. Влияние природы граничащих фаз
- •2.3.4. Влияние природы и концентрации растворенного вещества
- •2.4. Межмолекулярные и межфазные взаимодействия
- •2.4.1. Когезия
- •2.4.2. Адгезия
- •2.4.3. Растекание одной жидкости по поверхности другой
- •2.4.4. Смачивание
- •2.4.4.1. Анализ уравнения Юнга
- •2.4.4.2. Флотация
- •2.5. Особенности искривленной поверхности раздела фаз
- •2.5.1. Уравнение Лапласа
- •2.5.2. Капиллярное давление. Течение жидкости в капиллярах
- •2.6. Методы определения поверхностного натяжения
- •2.6.1. Метод наибольшего давления пузырька газа (метод Ребиндера)
- •2.6.2. Сталагмометрический метод (метод счета капель)
- •2.6.3. Метод капиллярного поднятия жидкости
- •2.7. Влияние кривизны поверхности на давление насыщенного пара
- •2.7.1. Уравнения Томсона (Кельвина)
- •2.7.2. Капиллярная конденсация
- •2.7.3. Изотермическая перегонка
- •Вопросыи задания для самоконтроля
- •Глава 3 адсорбция
- •3.1. Основные понятия и определения
- •3.1.1. Количественные способы выражения величины адсорбции
- •3.1.2. Классификации адсорбции
- •1. Классификация по природе границы раздела
- •2. Классификация по типу взаимодействия адсорбата и адсорбента
- •3.1.3. Основные экспериментальные зависимости адсорбции
- •3.2.Адсорбция на границе твердое тело – газ
- •3.2.1. Теория мономолекулярной адсорбции Лэнгмюра
- •3.2.2. Эмпирическое уравнение адсорбции Фрейндлиха
- •3.2.3. Теория полимолекулярной адсорбции Поляни
- •3.2.4. Дальнейшие представления о многослойной адсорбции. Теория бэт
- •3.2.5. Адсорбция на пористых адсорбентах
- •3.2.6.Адсорбенты и их характеристики
- •3.3.Адсорбция на границе жидкость – газ
- •3.3.1. Фундаментальное уравнение адсорбции Гиббса
- •3.3.2. Свойства поверхностно-активных (пав) и поверхностно-инактивных (пив) веществ
- •3.3.3. Строение адсорбционного слоя на границе раствор–газ
- •3.3.4. Уравнение Шишковского
- •3.3.5. Поверхностная активность. Правило Дюкло – Траубе
- •3.3.6. Расчет гиббсовской адсорбции из изотермы поверхностного натяжения методом графического дифференцирования
- •3.3.7.Применение уравнения изотермы Лэнгмюра к адсорбции на границе жидкость–газ. Расчет молекулярных характеристик исследуемого пав
- •3.3.8. Мицеллообразование в растворах коллоидных пав
- •3.3.9. Классификации пав
- •3.3.10. Солюбилизация
- •3.3.11. Практическое значение пав
- •3.3.12. Проблемы биоразлагаемости промышленных пав
- •3.4.Адсорбция на границе твердое тело – раствор
- •3.4.1. Молекулярная адсорбция
- •3.4.2. Ионная адсорбция
- •3.4.3. Ионообменная адсорбция. Ионный обмен
- •Вопросыи задания для самоконтроля
- •Глава 4 электрические свойства дисперсных систем
- •4.1. Электрокинетические явления
- •4.1.1. Механизм образования двойного электрического слоя
- •1. Неравенство электрохимических потенциалов ионов в кристаллической решетке твердого тела и ионов в растворе
- •Адсорбционный механизм образования дэс
- •Механизм поверхностной диссоциации
- •2. Специфическая адсорбции ионов на поверхности твердой фазы
- •3. Ориентированная адсорбция поверхностно-активных веществ
- •4.2. Теории строения двойного электрического слоя
- •4.2.1. Экспериментальные факты, послужившие основой для создания теорий строения дэс
- •4.2.2. Теория строения дэс Гельмгольца – Перрена
- •4.2.3. Теория строения дэс Гуи – Чэпмена
- •4.2.4. Современная теория строения дэс Штерна
- •4.3. Электрокинетический потенциал
- •4.3.1. Определение электрокинетического потенциала из электрокинетических явлений
- •4.3.2. Практическое значение электрокинетических явлений
- •4.4. Строение коллоидных мицелл
- •4.4.1. Примеры мицелл гидрофобных золей в природе
- •Вопросы и задания для самоконтроля
- •Глава 5 устойчивость и коагуляция лиофобных дисперсных систем
- •5.1. Основные понятия и определения
- •5.1.1. Факторы агрегативной устойчивости лиофобных систем
- •5.2. Коагуляция
- •Стадии коагуляции
- •5.2.1. Кинетика коагуляции. Теория кинетики быстрой коагуляции Смолуховского
- •5.2.2. Коагуляция золей электролитами
- •Эмпирические правила электролитной коагуляции
- •5.3. Теория устойчивости лиофобных дисперсных систем длфо
- •5.3.1. Расклинивающее давление
- •Составляющие расклинивающего давления
- •5.3.2. Энергия электростатического отталкивания
- •5.3.3. Энергия молекулярного притяжения
- •5.3.4. Потенциальные кривые взаимодействия частиц
- •5.4. Закономерности коагуляции гидрофобных золей электролитами
- •5.4.1. Особые явления при коагуляции
- •Коагуляция смесью электролитов
- •5.4.2. Примеры коагуляции. Образование почв
- •5.4.3. Физико-химические методы очистки сточных вод
- •Вопросыи задания для самоконтроля
- •Глава 6 структурно-механические свойства дисперсных систем
- •6.1. Типы структур
- •6.2. Реологические свойства дисперсных систем
- •6.2.1. Вязкость жидких дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 7 оптические свойства дисперсных систем
- •7.1. Рассеяние света в дисперсных системах
- •7.2. Поглощение света в дисперсных системах
- •7.3. Окраска дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 8 молекулярно-кинетические свойства дисперсных систем
- •8.1. Осмос
- •8.2. Диффузия
- •8.3. Броуновское движение
- •8.4. Седиментационное равновесие
- •8.5. Седиментационный анализ
- •Вопросы и задания для самоконтроля
- •Глава 9 краткая характеристика основных дисперсных систем
- •9.1. Системы с жидкой дисперсионной средой
- •9.1.1. Суспензии и золи
- •Классификация суспензий
- •Получение суспензий
- •Значение суспензий
- •9.1.2. Эмульсии
- •Классификация эмульсий
- •Агрегативная устойчивость эмульсии и природа эмульгатора
- •9.1.3. Пены
- •9.2. Системы с газообразной дисперсионной средой
- •9.2.1. Аэрозоли
- •Классификации аэрозолей
- •Агрегативная устойчивость аэрозолей. Коагуляция
- •Методы разрушения аэрозолей
- •9.3. Системы с твердой дисперсионной средой
- •Вопросыи задания для самоконтроля
- •Перечень используемой литературы
- •Коллоидная химия
- •В авторской редакции
- •Отпечатано в Издательстве тпу в полном соответствии с качеством предоставленного оригинал-макета
8.4. Седиментационное равновесие
Седиментация – осаждение частиц под действием силы тяжести. Частицы в дисперсных системах находятся под действием двух сил: силы тяжести и силы диффузии. Оценить седиментационную или кинетическую устойчивость дисперсной системы можно, сравнивая диффузионный поток JD и противодействующий ему поток седиментации JS.
|
Рис. 8.1. Соотношение между потоком диффузии JD и потоком седиментации JS в системе |
Поток седиментации (JS) – количество вещества, которое под действие силы тяжести проходит через площадку в 1 см2 в направлении перпендикулярном ей. От соотношения потоков диффузии и седиментации зависит устойчивость дисперсной системы (рис. 8.1). |
Если
![]() ,
то система будет являться седиментационно
или кинетически устойчивой. К таким
системам относятся системы молекулярного
уровня.
,
то система будет являться седиментационно
или кинетически устойчивой. К таким
системам относятся системы молекулярного
уровня.
Если
![]() ,
то система будет являться седиментационно
или кинетически неустойчивой. К таким
системам относятся грубодисперсные
системы.
,
то система будет являться седиментационно
или кинетически неустойчивой. К таким
системам относятся грубодисперсные
системы.
В высокодисперсных системах (коллоидных) частицы в равной степени подвержены диффузии и седиментации. В таких системах устанавливается седиментационно-диффузионное равновесие и наблюдается определенное распределение частиц по высоте.
Для любой дисперсной системы можно найти высоту h, на которой концентрация частиц уменьшилась в соответствующее число раз по гипсометрическому (от лат «hypsos» - высота) закону Лапласа:
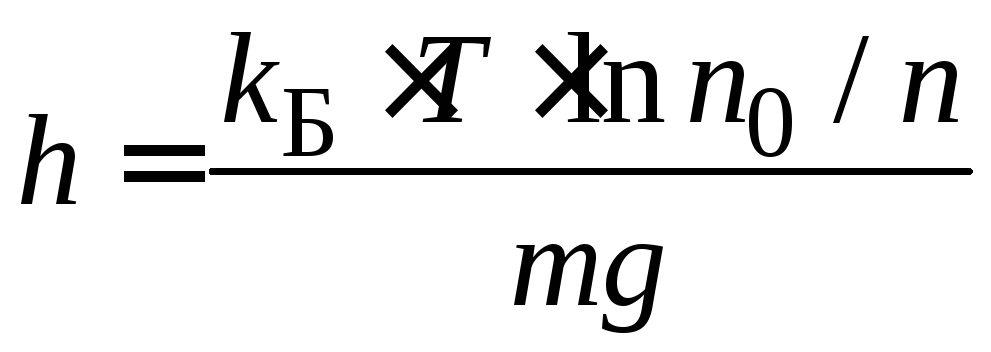 . (8.9)
. (8.9)
Уравнение Лапласа строго выполняется только для монодисперсных систем. В случае полидисперсных систем картина распределения частиц по высоте гораздо более сложная.
Несмотря на то, что для золей согласно гипсометрическому закону, концентрация должна уменьшаться очень быстро с высотой, часто дисперсные системы имеют одну и ту же концентрацию по всей высоте столба. Особенно это характерно для высокодисперсных золей. Такое явление объясняется тем, что с уменьшением размера частиц сила тяжести, обуславливающая оседание, уменьшается гораздо быстрее, чем сила трения.
8.5. Седиментационный анализ
В грубодисперсных системах частицы оседают под действием вилы тяжести намного быстрее, чем они смещаются в результате броуновского движения. Процесс седиментации используют для определения размеров частиц дисперсной фазы.
Расчеты в седиментационном анализе основаны на использовании уравнения Стокса: предполагается, что при оседании частицы сила вязкого сопротивления среды равна силе тяжести. Таким образом, для сферических частиц:
![]() , (8.10)
, (8.10)
где
![]() – объем дисперсной частицы;
– объем дисперсной частицы;![]() – разность между плотностью частицы
дисперсной фазы и плотностью дисперсионной
среды;g
– ускорение свободного падения;
– разность между плотностью частицы
дисперсной фазы и плотностью дисперсионной
среды;g
– ускорение свободного падения;
![]() – скорость оседания (седиментации)
частицы – скорость движения частицы;
η – вязкость дисперсионной среды;r
– радиус
частицы дисперсной фазы.
– скорость оседания (седиментации)
частицы – скорость движения частицы;
η – вязкость дисперсионной среды;r
– радиус
частицы дисперсной фазы.
Тогда скорость седиментации можно рассчитать:
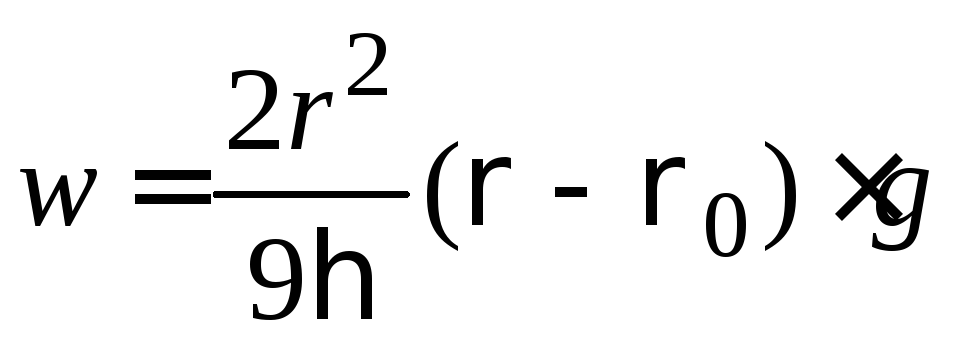 . (8.11)
. (8.11)
Согласно
уравнению (8.11) с увеличением радиуса
частицы дисперсной фазы и уменьшением
вязкости среды скорость седиментации
будет увеличиваться. Если
![]() ,
то происходит оседание, при
,
то происходит оседание, при![]() – всплывание частиц – обратная
седиментация (суспензия парафина в
воде, образование сливок в молоке).
– всплывание частиц – обратная
седиментация (суспензия парафина в
воде, образование сливок в молоке).
Уравнение (8.11) лежит в основе седиментационного анализа для определения размеров грубодисперсных частиц и имеет огромное практическое значение, т.к. дисперсность определяет производственные показатели многих промышленных и природных материалов:
 . (8.12)
. (8.12)
Уравнение (8.12) применимо для частиц с размерами от 10–7 до 10–4 м при условии сферической формы частиц и их независимого движения друг от друга.
В высокодисперсных (коллоидных) системах осаждению частиц противодействует броуновское движение, стремящееся равномерно распределить частицы по всему объему раствора. В результате действия сил тяжести и диффузии устанавливается седиментационно-диффузионное равновесие и наблюдается определенное распределение частиц по высоте и характеризующееся постепенным уменьшением концентрации дисперсной фазы в направлении от дна сосуда к верхним слоям раствора. Распределение монодисперсных частиц по высоте подчиняется гипсометрическому (от лат «hypsos» - высота) закону Лапласа – Перрена:
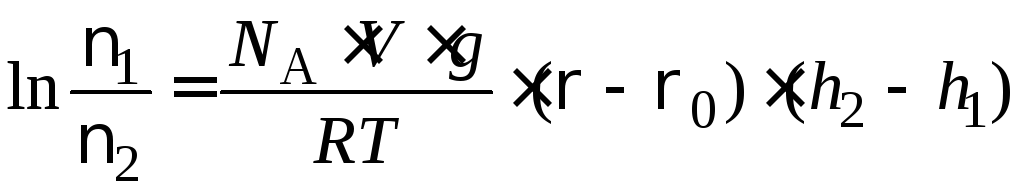 , (8.13)
, (8.13)
где
![]() и
и![]() –
число частиц в единице объема на
расстоянияхh1
и h2
от дна сосуда; V
– объем
частицы, м3;
NA
– число Авогадро;
–
число частиц в единице объема на
расстоянияхh1
и h2
от дна сосуда; V
– объем
частицы, м3;
NA
– число Авогадро;
![]() –
разность между плотностью частицы
дисперсной фазы и плотностью дисперсионной
среды, кг/м3;
g
– ускорение свободного падения, м/с2.
–
разность между плотностью частицы
дисперсной фазы и плотностью дисперсионной
среды, кг/м3;
g
– ускорение свободного падения, м/с2.
Пример 8.3. Гидрозоль золота состоит из частиц диаметром 2·10–9 м. На какой высоте при 27 °С число частиц в золе уменьшится в два раза? Плотность золота 19,6·103 кг/м3, плотность воды 1·103 кг/м3.
Решение:
1. Вычислим объем шарообразной частицы золя золота:
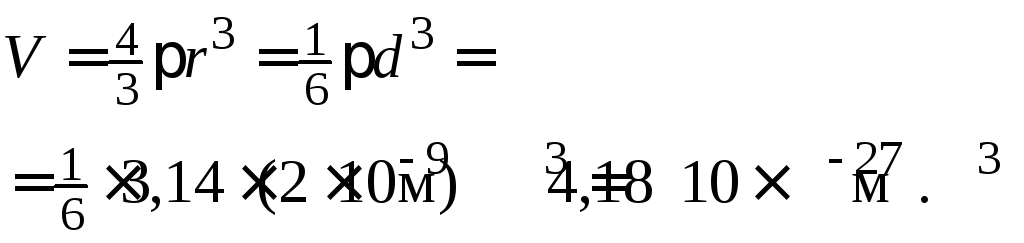 .
.
2. Найдем высоту, на которой число частиц уменьшится в два раза из уравнения (8.20):
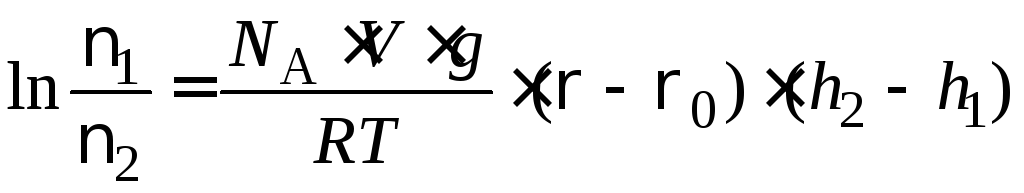 .
.
Тогда
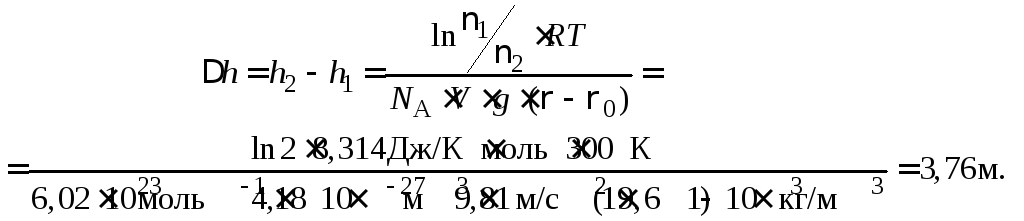
Следовательно, на высоте 3,76 м число частиц золя золота уменьшится в два раза.