
- •«Национальный исследовательский
- •Томский политехнический Университет»
- •Е.В. Михеева, н.П. Пикула, а.П. Асташкина
- •Коллоидная химия
- •Оглавление
- •Глава 1 дисперсные системы
- •1.1. Общая характеристика дисперсных систем
- •1.1.1. Признаки объектов коллоидной химии
- •1.1.2. Специфические особенности высокодисперсных систем
- •1.2. Классификации дисперсных систем
- •1.2.1. Классификация по размерам частиц дисперсной фазы
- •1.2.2. Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •1.2.3. Классификация по силе межфазного взаимодействия дисперсной фазы и дисперсионной среды
- •1.2.4. Классификация по подвижности частиц дф (по структуре)
- •1.2.5. Классификация по фазовой различимости
- •1.2.6. Классификация по топографическому признаку (по форме частиц)
- •1.3. Методы получения дисперсных систем
- •1.3.1. Диспергационные методы
- •1.3.2. Конденсационные методы
- •1.3.2.1. Физические конденсационные методы
- •1.3.2.2. Химические конденсационные методы
- •2. Реакции обмена
- •3. Реакции окисления
- •1.3.3. Метод пептизации
- •1.4. Методы очистки дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 2 термодинамика поверхностных явлений
- •2.1. Классификация поверхностных явлений
- •2.2. Свободная поверхностная энергия и поверхностное натяжение
- •2.2.1. Физический смысл поверхностного натяжения
- •2.2.2. Термодинамическое определение поверхностного натяжения
- •2.2.3. Единицы измерения поверхностного натяжения
- •2.3. Влияние различных факторов на величину поверхностного натяжения
- •2.3.1. Влияние химической природы вещества
- •2.3.2. Влияние температуры
- •2.3.3. Влияние природы граничащих фаз
- •2.3.4. Влияние природы и концентрации растворенного вещества
- •2.4. Межмолекулярные и межфазные взаимодействия
- •2.4.1. Когезия
- •2.4.2. Адгезия
- •2.4.3. Растекание одной жидкости по поверхности другой
- •2.4.4. Смачивание
- •2.4.4.1. Анализ уравнения Юнга
- •2.4.4.2. Флотация
- •2.5. Особенности искривленной поверхности раздела фаз
- •2.5.1. Уравнение Лапласа
- •2.5.2. Капиллярное давление. Течение жидкости в капиллярах
- •2.6. Методы определения поверхностного натяжения
- •2.6.1. Метод наибольшего давления пузырька газа (метод Ребиндера)
- •2.6.2. Сталагмометрический метод (метод счета капель)
- •2.6.3. Метод капиллярного поднятия жидкости
- •2.7. Влияние кривизны поверхности на давление насыщенного пара
- •2.7.1. Уравнения Томсона (Кельвина)
- •2.7.2. Капиллярная конденсация
- •2.7.3. Изотермическая перегонка
- •Вопросыи задания для самоконтроля
- •Глава 3 адсорбция
- •3.1. Основные понятия и определения
- •3.1.1. Количественные способы выражения величины адсорбции
- •3.1.2. Классификации адсорбции
- •1. Классификация по природе границы раздела
- •2. Классификация по типу взаимодействия адсорбата и адсорбента
- •3.1.3. Основные экспериментальные зависимости адсорбции
- •3.2.Адсорбция на границе твердое тело – газ
- •3.2.1. Теория мономолекулярной адсорбции Лэнгмюра
- •3.2.2. Эмпирическое уравнение адсорбции Фрейндлиха
- •3.2.3. Теория полимолекулярной адсорбции Поляни
- •3.2.4. Дальнейшие представления о многослойной адсорбции. Теория бэт
- •3.2.5. Адсорбция на пористых адсорбентах
- •3.2.6.Адсорбенты и их характеристики
- •3.3.Адсорбция на границе жидкость – газ
- •3.3.1. Фундаментальное уравнение адсорбции Гиббса
- •3.3.2. Свойства поверхностно-активных (пав) и поверхностно-инактивных (пив) веществ
- •3.3.3. Строение адсорбционного слоя на границе раствор–газ
- •3.3.4. Уравнение Шишковского
- •3.3.5. Поверхностная активность. Правило Дюкло – Траубе
- •3.3.6. Расчет гиббсовской адсорбции из изотермы поверхностного натяжения методом графического дифференцирования
- •3.3.7.Применение уравнения изотермы Лэнгмюра к адсорбции на границе жидкость–газ. Расчет молекулярных характеристик исследуемого пав
- •3.3.8. Мицеллообразование в растворах коллоидных пав
- •3.3.9. Классификации пав
- •3.3.10. Солюбилизация
- •3.3.11. Практическое значение пав
- •3.3.12. Проблемы биоразлагаемости промышленных пав
- •3.4.Адсорбция на границе твердое тело – раствор
- •3.4.1. Молекулярная адсорбция
- •3.4.2. Ионная адсорбция
- •3.4.3. Ионообменная адсорбция. Ионный обмен
- •Вопросыи задания для самоконтроля
- •Глава 4 электрические свойства дисперсных систем
- •4.1. Электрокинетические явления
- •4.1.1. Механизм образования двойного электрического слоя
- •1. Неравенство электрохимических потенциалов ионов в кристаллической решетке твердого тела и ионов в растворе
- •Адсорбционный механизм образования дэс
- •Механизм поверхностной диссоциации
- •2. Специфическая адсорбции ионов на поверхности твердой фазы
- •3. Ориентированная адсорбция поверхностно-активных веществ
- •4.2. Теории строения двойного электрического слоя
- •4.2.1. Экспериментальные факты, послужившие основой для создания теорий строения дэс
- •4.2.2. Теория строения дэс Гельмгольца – Перрена
- •4.2.3. Теория строения дэс Гуи – Чэпмена
- •4.2.4. Современная теория строения дэс Штерна
- •4.3. Электрокинетический потенциал
- •4.3.1. Определение электрокинетического потенциала из электрокинетических явлений
- •4.3.2. Практическое значение электрокинетических явлений
- •4.4. Строение коллоидных мицелл
- •4.4.1. Примеры мицелл гидрофобных золей в природе
- •Вопросы и задания для самоконтроля
- •Глава 5 устойчивость и коагуляция лиофобных дисперсных систем
- •5.1. Основные понятия и определения
- •5.1.1. Факторы агрегативной устойчивости лиофобных систем
- •5.2. Коагуляция
- •Стадии коагуляции
- •5.2.1. Кинетика коагуляции. Теория кинетики быстрой коагуляции Смолуховского
- •5.2.2. Коагуляция золей электролитами
- •Эмпирические правила электролитной коагуляции
- •5.3. Теория устойчивости лиофобных дисперсных систем длфо
- •5.3.1. Расклинивающее давление
- •Составляющие расклинивающего давления
- •5.3.2. Энергия электростатического отталкивания
- •5.3.3. Энергия молекулярного притяжения
- •5.3.4. Потенциальные кривые взаимодействия частиц
- •5.4. Закономерности коагуляции гидрофобных золей электролитами
- •5.4.1. Особые явления при коагуляции
- •Коагуляция смесью электролитов
- •5.4.2. Примеры коагуляции. Образование почв
- •5.4.3. Физико-химические методы очистки сточных вод
- •Вопросыи задания для самоконтроля
- •Глава 6 структурно-механические свойства дисперсных систем
- •6.1. Типы структур
- •6.2. Реологические свойства дисперсных систем
- •6.2.1. Вязкость жидких дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 7 оптические свойства дисперсных систем
- •7.1. Рассеяние света в дисперсных системах
- •7.2. Поглощение света в дисперсных системах
- •7.3. Окраска дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 8 молекулярно-кинетические свойства дисперсных систем
- •8.1. Осмос
- •8.2. Диффузия
- •8.3. Броуновское движение
- •8.4. Седиментационное равновесие
- •8.5. Седиментационный анализ
- •Вопросы и задания для самоконтроля
- •Глава 9 краткая характеристика основных дисперсных систем
- •9.1. Системы с жидкой дисперсионной средой
- •9.1.1. Суспензии и золи
- •Классификация суспензий
- •Получение суспензий
- •Значение суспензий
- •9.1.2. Эмульсии
- •Классификация эмульсий
- •Агрегативная устойчивость эмульсии и природа эмульгатора
- •9.1.3. Пены
- •9.2. Системы с газообразной дисперсионной средой
- •9.2.1. Аэрозоли
- •Классификации аэрозолей
- •Агрегативная устойчивость аэрозолей. Коагуляция
- •Методы разрушения аэрозолей
- •9.3. Системы с твердой дисперсионной средой
- •Вопросыи задания для самоконтроля
- •Перечень используемой литературы
- •Коллоидная химия
- •В авторской редакции
- •Отпечатано в Издательстве тпу в полном соответствии с качеством предоставленного оригинал-макета
Вопросыи задания для самоконтроля
Какие структурно-механические свойства дисперсных систем вы знаете?
Перечислите типы структур.
Что такое вязкость? Какие виды вязкости вы знаете? Каким образом количественно можно рассчитать величину вязкости?
Чем определяется вязкость дисперсной системы?
Глава 7 оптические свойства дисперсных систем
К оптическим свойствам дисперсных систем относятся: поглощение, отражение, преломление, пропускание, рассеяние света.
Специфика оптических свойств объектов коллоидной химии определяется их основными признаками: гетерогенностью и дисперсностью. Изучение оптических свойств дисперсных систем является самым оперативным и доступным средством определения размеров частиц, их формы, структуры, а также концентрации. Для коллоидных систем наиболее характерным является поглощение и рассеяние света.
7.1. Рассеяние света в дисперсных системах
Если рассматривать высокодисперсные системы (золи) в проходящем свете, то они кажутся прозрачными и ничем не отличаются от истинных растворов. Однако при наблюдении сбоку в этих же растворах наблюдается свечение, которое называют опалесценцией (боковым свечением). При наблюдении сбоку в растворе золе виден яркий светящийся конус (конус Тиндаля).
Причина эффекта Тиндаля: дисперсная система содержит мелкие взвешенные частицы дисперсной фазы, показатель преломления которых отличается от показателя преломления дисперсионной среды. При попадании на них пучка света эти частицы становятся центрами рассеяния света и образуемые ими вторичные волны усиливают друг друга и порождают рассеянный свет.
Светорассеяние (опалесценция) наблюдается только тогда, когда длина световой волны больше размера частицы дисперсной фазы. Светорассеяние является уникальным специфическим свойством высокодисперсных (коллоидных) систем (конус Тиндаля в истинных растворах не наблюдается).
Количественные закономерности рассеянного света для сферических частиц, не проводящих электрический, ток были выведены Релеем:
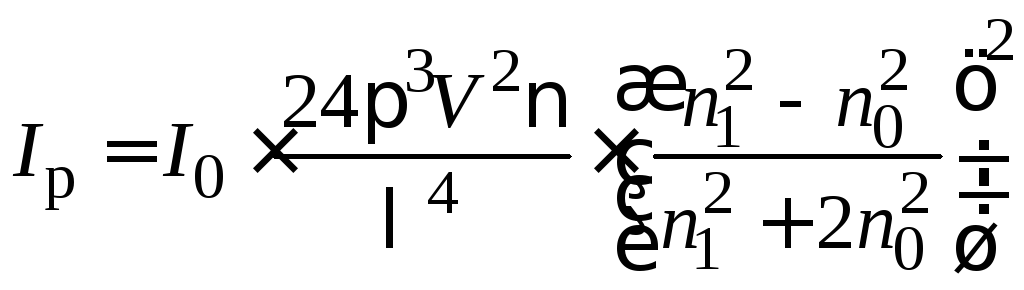 , (7.1)
, (7.1)
где
![]() и
и![]() – интенсивности падающего и рассеянного
света;V
– объем частицы; λ – длина волны падающего
света;
– интенсивности падающего и рассеянного
света;V
– объем частицы; λ – длина волны падающего
света;
![]() – частичная концентрация (число частиц
в 1 м3
золя); n1
и n0
– показатели преломления дисперсной
фазы и дисперсионной среды.
– частичная концентрация (число частиц
в 1 м3
золя); n1
и n0
– показатели преломления дисперсной
фазы и дисперсионной среды.
В
уравнение (7.1) входит частичная концентрация
дисперсной фазы
![]() ,
которая определяется числом частиц в
единице объема. Частичная концентрация
связана с массовой концентрацией
дисперсной фазы соотношением:
,
которая определяется числом частиц в
единице объема. Частичная концентрация
связана с массовой концентрацией
дисперсной фазы соотношением:
![]() , (7.2)
, (7.2)
где
С
– массовая концентрация (масса частиц
дисперсной фазы в 1 м3
золя); V
– объем частицы;
![]() –
частичная концентрация (число частиц
в 1 м3
золя);
–
частичная концентрация (число частиц
в 1 м3
золя);
![]() – плотность дисперсной фазы.
– плотность дисперсной фазы.
С учетом (7.2), уравнение Релея принимает вид:
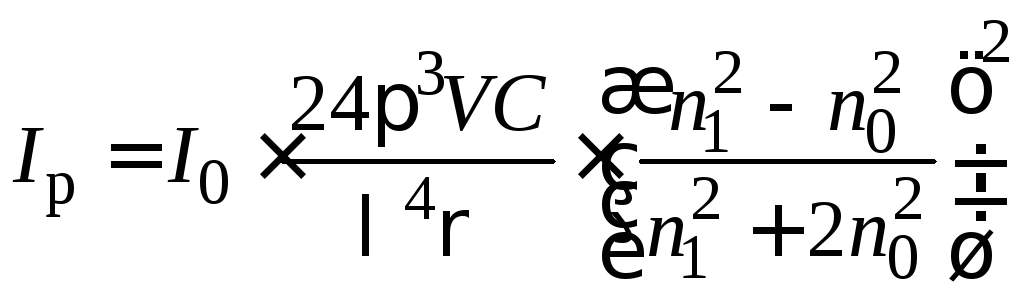 . (7.3)
. (7.3)
Уравнение Рэлея применимо для систем, частицы дисперсной фазы которых составляют не более 0,1 длины световой волны (т.е. для частиц не больше 40–70 нм) и находящихся друг от друга на достаточно больших расстояниях (разбавленные системы). Длины волн падающего света: 400 нм (синий) – 780 нм (красный).
Уравнение Релея показывает:
1.
Интенсивность рассеянного света прямо
пропорциональна числу частиц (концентрации
золя):
![]() .
Это позволяет определить концентрацию
дисперсной фазы по величине светорассеяния.
.
Это позволяет определить концентрацию
дисперсной фазы по величине светорассеяния.
2.
Интенсивность рассеянного света прямо
пропорциональна объему частиц (зависит
от размеров частиц):
![]() ;
;![]() .
Это позволяет определить размер частиц
дисперсной фазы.
.
Это позволяет определить размер частиц
дисперсной фазы.
3.
Интенсивность рассеянного света обратно
пропорциональна длине волны падающего
света:
![]() .
Следовательно, чем короче длина волны
падающего света, тем больше рассеяние.
.
Следовательно, чем короче длина волны
падающего света, тем больше рассеяние.
Таким образом, если на частицу будет падать белый свет, то наибольшее рассеяние будет испытывать синяя и фиолетовая части спектра, обладающие наименьшей длиной волны. Поэтому при боковом свечении дисперсные системы будут иметь голубоватую окраску, а в проходящем свете – красноватую, что связано с потерей в результате рассеяния синей и фиолетовой части спектра. Часть солнечных лучей, проходя через земную атмосферу, рассеивается, поэтому атмосфера Земли имеет голубоватую окраску. При восходе и закате Солнца поток лучей проходит насквозь, поэтому цвет неба становится красно-оранжевым.
Для светомаскировки применяют синие лампы (когда хотят чтобы они остались незамеченными с самолетов, т.к. синие лучи при прохождении через толстый слой воздуха, особенно если в нем содержаться частицы пыли или тумана, полностью рассеиваются), т.к. синий цвет больше всего рассеивается. Для сигнализации применяют красный свет (он плохо рассеивается в тумане).
4.
Интенсивность рассеянного света прямо
пропорциональна разности показателей
преломления дисперсной фазы и дисперсионной
среды
![]() .
Чем больше разность между показателями
преломления, тем больше рассеяние света.
Поэтому рассеяние металлическими золями
оказывается сильнее, чем неметаллическими
из-за их большой плотности и большой
величины показателя преломления
дисперсной фазы
.
Чем больше разность между показателями
преломления, тем больше рассеяние света.
Поэтому рассеяние металлическими золями
оказывается сильнее, чем неметаллическими
из-за их большой плотности и большой
величины показателя преломления
дисперсной фазы![]() ,
и дисперсионной среды
,
и дисперсионной среды![]() ,
следовательно, разности (
,
следовательно, разности (![]() ).
Если
).
Если![]() ,
то интенсивность рассеяния равна нулю
,
то интенсивность рассеяния равна нулю![]() = 0,
т.е. в однородных средах светорассеяние
не наблюдается.
= 0,
т.е. в однородных средах светорассеяние
не наблюдается.
Из уравнений (7.1) и (7.3) следует, что для одного и того же золя при прочих равных условиях будут выполняться соотношения:
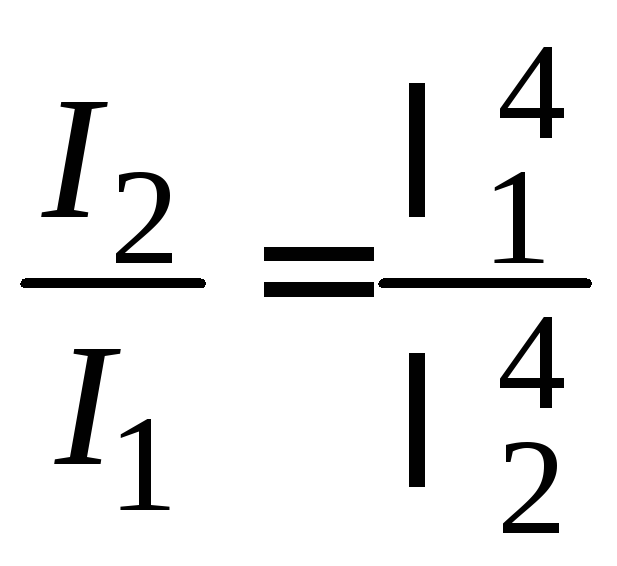 ;
;
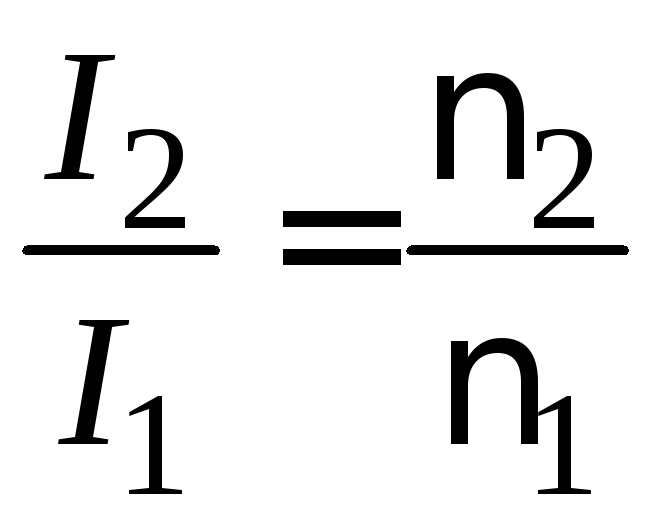 ;
;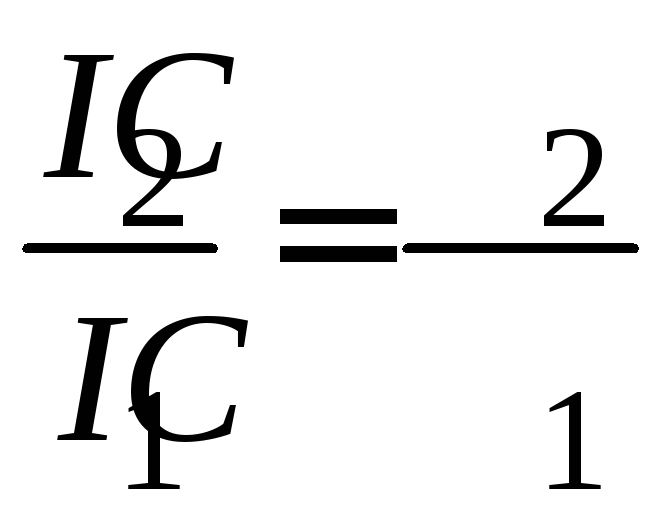 ;
;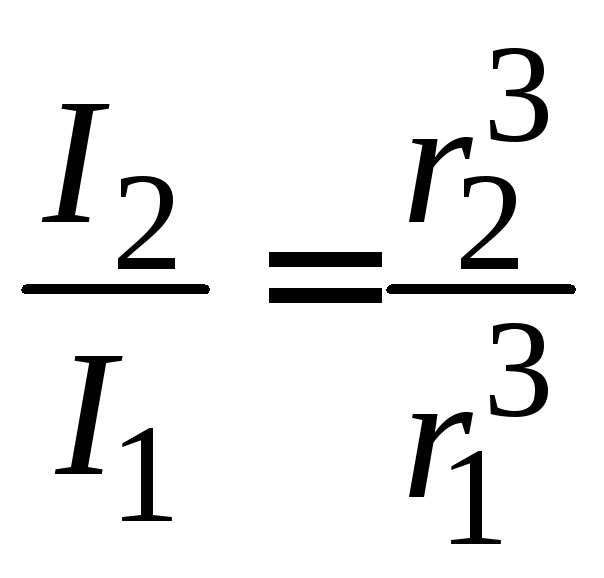 . (7.4)
. (7.4)
Рассеяние света используют для исследования дисперсных систем. К таким методам исследования относятся: ультрамикроскопия, турбидиметрия и нефелометрия.
Рассеяние
света происходит во всех направлениях,
но интенсивность его в разных направлениях
различна. Максимальная интенсивность
рассеянного света
![]() наблюдается в направлении, перпендикулярном
падающему свету
наблюдается в направлении, перпендикулярном
падающему свету![]() .
.
Рассеянный свет чаще всего поляризован и яркость светорассеяния будет зависеть от поляризации, которая максимальна в перпендикулярном направлении (под углом 90° к падающему свету).
Рассеяние света используют для исследования дисперсных систем. К таким метолам исследования относятся: ультрамикроскопия, турбидиметрия и нефелометрия.
Пример 7.1. Длина волны красного света равна 760 нм, а длина волны синего света равна 430 нм. В каком случае интенсивность рассеянного света будет больше и во сколько раз?
Решение:
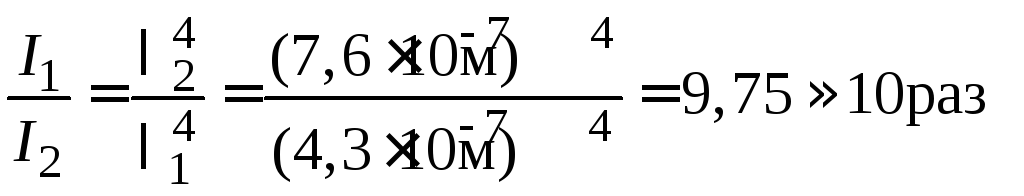 .
.
Интенсивность рассеяния в случае синего света будет больше в 10 раз.
Пример 7.2. Сравните интенсивности рассеяния света золями с радиусом частиц 15 и 75 нм. В каком случае и насколько интенсивность рассеяния света будет больше?
Решение:
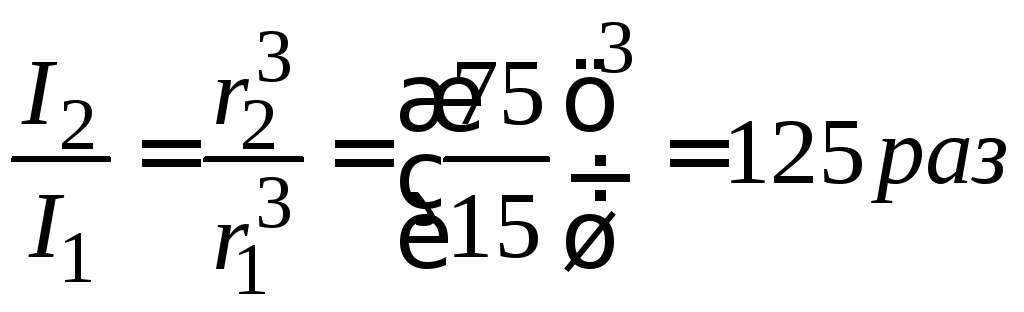 .
.
При увеличении размеров частиц с 15 до 75 нм интенсивность светорассеяния увеличилась в 125 раза.
Пример 7.3. Сравните интенсивности светорассеяния эмульсий гексана (n1 = 1,375) в воде (n0 = 1,33) и фенола (n1 = 1,54) в воде при 318 К. Размер частиц и концентрации эмульсий одинаковы.
Решение:
Согласно уравнению Релея (6.3):
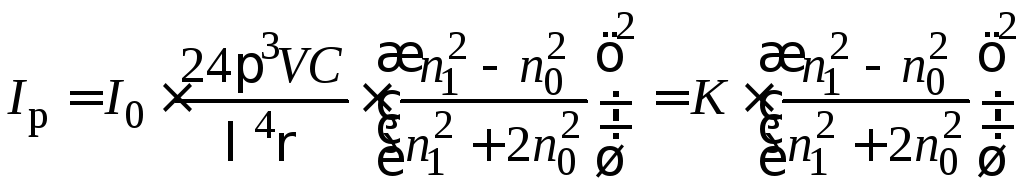 .
.
1. В случае эмульсии гексана:
 .
.
2. В случае эмульсии фенола:
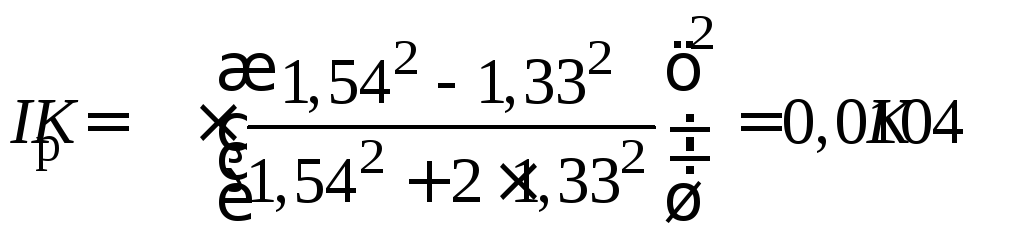 .
.
3. Отношение интенсивностей светорассеяния:
![]()
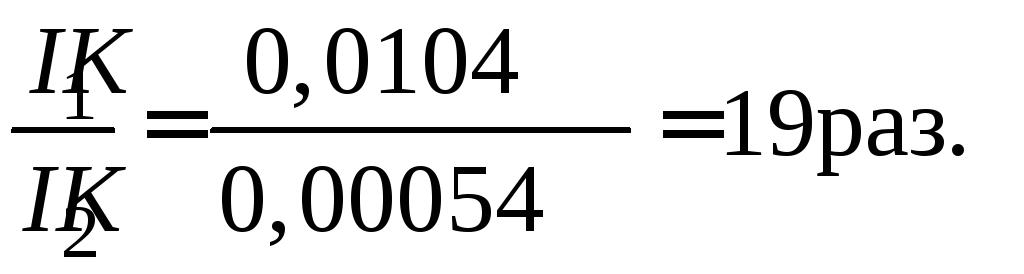
Таким образом, в случае эмульсии фенола с большим показателем преломления интенсивность светорассеяния будет больше в 19 раз, чем в случае эмульсии гексана.
