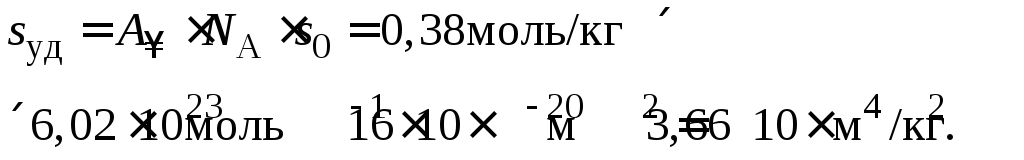- •«Национальный исследовательский
- •Томский политехнический Университет»
- •Е.В. Михеева, н.П. Пикула, а.П. Асташкина
- •Коллоидная химия
- •Оглавление
- •Глава 1 дисперсные системы
- •1.1. Общая характеристика дисперсных систем
- •1.1.1. Признаки объектов коллоидной химии
- •1.1.2. Специфические особенности высокодисперсных систем
- •1.2. Классификации дисперсных систем
- •1.2.1. Классификация по размерам частиц дисперсной фазы
- •1.2.2. Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •1.2.3. Классификация по силе межфазного взаимодействия дисперсной фазы и дисперсионной среды
- •1.2.4. Классификация по подвижности частиц дф (по структуре)
- •1.2.5. Классификация по фазовой различимости
- •1.2.6. Классификация по топографическому признаку (по форме частиц)
- •1.3. Методы получения дисперсных систем
- •1.3.1. Диспергационные методы
- •1.3.2. Конденсационные методы
- •1.3.2.1. Физические конденсационные методы
- •1.3.2.2. Химические конденсационные методы
- •2. Реакции обмена
- •3. Реакции окисления
- •1.3.3. Метод пептизации
- •1.4. Методы очистки дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 2 термодинамика поверхностных явлений
- •2.1. Классификация поверхностных явлений
- •2.2. Свободная поверхностная энергия и поверхностное натяжение
- •2.2.1. Физический смысл поверхностного натяжения
- •2.2.2. Термодинамическое определение поверхностного натяжения
- •2.2.3. Единицы измерения поверхностного натяжения
- •2.3. Влияние различных факторов на величину поверхностного натяжения
- •2.3.1. Влияние химической природы вещества
- •2.3.2. Влияние температуры
- •2.3.3. Влияние природы граничащих фаз
- •2.3.4. Влияние природы и концентрации растворенного вещества
- •2.4. Межмолекулярные и межфазные взаимодействия
- •2.4.1. Когезия
- •2.4.2. Адгезия
- •2.4.3. Растекание одной жидкости по поверхности другой
- •2.4.4. Смачивание
- •2.4.4.1. Анализ уравнения Юнга
- •2.4.4.2. Флотация
- •2.5. Особенности искривленной поверхности раздела фаз
- •2.5.1. Уравнение Лапласа
- •2.5.2. Капиллярное давление. Течение жидкости в капиллярах
- •2.6. Методы определения поверхностного натяжения
- •2.6.1. Метод наибольшего давления пузырька газа (метод Ребиндера)
- •2.6.2. Сталагмометрический метод (метод счета капель)
- •2.6.3. Метод капиллярного поднятия жидкости
- •2.7. Влияние кривизны поверхности на давление насыщенного пара
- •2.7.1. Уравнения Томсона (Кельвина)
- •2.7.2. Капиллярная конденсация
- •2.7.3. Изотермическая перегонка
- •Вопросыи задания для самоконтроля
- •Глава 3 адсорбция
- •3.1. Основные понятия и определения
- •3.1.1. Количественные способы выражения величины адсорбции
- •3.1.2. Классификации адсорбции
- •1. Классификация по природе границы раздела
- •2. Классификация по типу взаимодействия адсорбата и адсорбента
- •3.1.3. Основные экспериментальные зависимости адсорбции
- •3.2.Адсорбция на границе твердое тело – газ
- •3.2.1. Теория мономолекулярной адсорбции Лэнгмюра
- •3.2.2. Эмпирическое уравнение адсорбции Фрейндлиха
- •3.2.3. Теория полимолекулярной адсорбции Поляни
- •3.2.4. Дальнейшие представления о многослойной адсорбции. Теория бэт
- •3.2.5. Адсорбция на пористых адсорбентах
- •3.2.6.Адсорбенты и их характеристики
- •3.3.Адсорбция на границе жидкость – газ
- •3.3.1. Фундаментальное уравнение адсорбции Гиббса
- •3.3.2. Свойства поверхностно-активных (пав) и поверхностно-инактивных (пив) веществ
- •3.3.3. Строение адсорбционного слоя на границе раствор–газ
- •3.3.4. Уравнение Шишковского
- •3.3.5. Поверхностная активность. Правило Дюкло – Траубе
- •3.3.6. Расчет гиббсовской адсорбции из изотермы поверхностного натяжения методом графического дифференцирования
- •3.3.7.Применение уравнения изотермы Лэнгмюра к адсорбции на границе жидкость–газ. Расчет молекулярных характеристик исследуемого пав
- •3.3.8. Мицеллообразование в растворах коллоидных пав
- •3.3.9. Классификации пав
- •3.3.10. Солюбилизация
- •3.3.11. Практическое значение пав
- •3.3.12. Проблемы биоразлагаемости промышленных пав
- •3.4.Адсорбция на границе твердое тело – раствор
- •3.4.1. Молекулярная адсорбция
- •3.4.2. Ионная адсорбция
- •3.4.3. Ионообменная адсорбция. Ионный обмен
- •Вопросыи задания для самоконтроля
- •Глава 4 электрические свойства дисперсных систем
- •4.1. Электрокинетические явления
- •4.1.1. Механизм образования двойного электрического слоя
- •1. Неравенство электрохимических потенциалов ионов в кристаллической решетке твердого тела и ионов в растворе
- •Адсорбционный механизм образования дэс
- •Механизм поверхностной диссоциации
- •2. Специфическая адсорбции ионов на поверхности твердой фазы
- •3. Ориентированная адсорбция поверхностно-активных веществ
- •4.2. Теории строения двойного электрического слоя
- •4.2.1. Экспериментальные факты, послужившие основой для создания теорий строения дэс
- •4.2.2. Теория строения дэс Гельмгольца – Перрена
- •4.2.3. Теория строения дэс Гуи – Чэпмена
- •4.2.4. Современная теория строения дэс Штерна
- •4.3. Электрокинетический потенциал
- •4.3.1. Определение электрокинетического потенциала из электрокинетических явлений
- •4.3.2. Практическое значение электрокинетических явлений
- •4.4. Строение коллоидных мицелл
- •4.4.1. Примеры мицелл гидрофобных золей в природе
- •Вопросы и задания для самоконтроля
- •Глава 5 устойчивость и коагуляция лиофобных дисперсных систем
- •5.1. Основные понятия и определения
- •5.1.1. Факторы агрегативной устойчивости лиофобных систем
- •5.2. Коагуляция
- •Стадии коагуляции
- •5.2.1. Кинетика коагуляции. Теория кинетики быстрой коагуляции Смолуховского
- •5.2.2. Коагуляция золей электролитами
- •Эмпирические правила электролитной коагуляции
- •5.3. Теория устойчивости лиофобных дисперсных систем длфо
- •5.3.1. Расклинивающее давление
- •Составляющие расклинивающего давления
- •5.3.2. Энергия электростатического отталкивания
- •5.3.3. Энергия молекулярного притяжения
- •5.3.4. Потенциальные кривые взаимодействия частиц
- •5.4. Закономерности коагуляции гидрофобных золей электролитами
- •5.4.1. Особые явления при коагуляции
- •Коагуляция смесью электролитов
- •5.4.2. Примеры коагуляции. Образование почв
- •5.4.3. Физико-химические методы очистки сточных вод
- •Вопросыи задания для самоконтроля
- •Глава 6 структурно-механические свойства дисперсных систем
- •6.1. Типы структур
- •6.2. Реологические свойства дисперсных систем
- •6.2.1. Вязкость жидких дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 7 оптические свойства дисперсных систем
- •7.1. Рассеяние света в дисперсных системах
- •7.2. Поглощение света в дисперсных системах
- •7.3. Окраска дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 8 молекулярно-кинетические свойства дисперсных систем
- •8.1. Осмос
- •8.2. Диффузия
- •8.3. Броуновское движение
- •8.4. Седиментационное равновесие
- •8.5. Седиментационный анализ
- •Вопросы и задания для самоконтроля
- •Глава 9 краткая характеристика основных дисперсных систем
- •9.1. Системы с жидкой дисперсионной средой
- •9.1.1. Суспензии и золи
- •Классификация суспензий
- •Получение суспензий
- •Значение суспензий
- •9.1.2. Эмульсии
- •Классификация эмульсий
- •Агрегативная устойчивость эмульсии и природа эмульгатора
- •9.1.3. Пены
- •9.2. Системы с газообразной дисперсионной средой
- •9.2.1. Аэрозоли
- •Классификации аэрозолей
- •Агрегативная устойчивость аэрозолей. Коагуляция
- •Методы разрушения аэрозолей
- •9.3. Системы с твердой дисперсионной средой
- •Вопросыи задания для самоконтроля
- •Перечень используемой литературы
- •Коллоидная химия
- •В авторской редакции
- •Отпечатано в Издательстве тпу в полном соответствии с качеством предоставленного оригинал-макета
3.2.4. Дальнейшие представления о многослойной адсорбции. Теория бэт
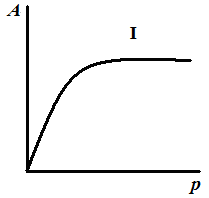
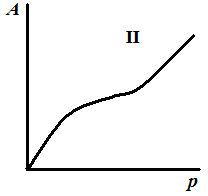
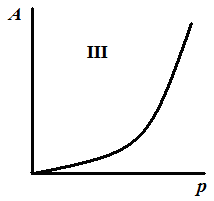
В 1915–1917 гг. было получено более 30 адсорбентов, на которых получено, пять основных типов изотерм адсорбции (рис. 3.15).
Современная обобщенная теория полимолекулярной адсорбции была развита в 1935–1940 гг. Брунауэром, Эмметом и Теллером. Эта теория получила название теории БЭТ по первым буквам имен авторов.
|
|
|
| |
|
|
| ||
Рис. 3.15. Пять основных типов изотерм адсорбции
Основные положения теории БЭТ
На поверхности адсорбента имеется определенное число равноценных в энергетическом отношении активных центров (поверхность однородна, все активные центры одинаковой силы).
Взаимодействие соседних адсорбированных молекул в первом и последующих слоях отсутствуют.
Каждая молекула предыдущего слоя представляет собой возможный активный центр для адсорбции молекулы следующего адсорбционного слоя (адсорбция многослойна).
Первый слой адсорбата образуется в результате действия сил Ван-дер-Ваальса между адсорбентом и адсорбатом, последующие в результате конденсации.
Все молекулы во втором и более далеких слоях ведут себя подобно молекулам жидкости.
Возможно построение последующих слоев при незаполненном первом.
Таким образом, адсорбированная фаза может быть представлена как совокупность адсорбционных комплексов – цепей молекул, первая из которых связана с поверхностью адсорбента. Все эти цепи энергетически не взаимодействуют друг с другом. Схема строения адсорбционного слоя по теории БЭТ показана на рис. 3.16.
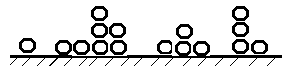
Рис. 3.16. Схема строения адсорбционного слоя по теории БЭТ
Для вывода уравнения в теории БЭТ приняты следующие допущения:
Уравнение Лэнгмюра применимо не только к первому слою, но и к последующим слоям.
Поверхность адсорбента однородна (все активные центры одинаковой силы).
Теория не учитывает взаимодействие между адсорбированными молекулами адсорбата.
Следовательно, теория БЭТ по методу – теория Лэнгмюра, а по природе – теория Поляни.
Процесс адсорбции можно представить в виде последовательных квазихимических реакций:
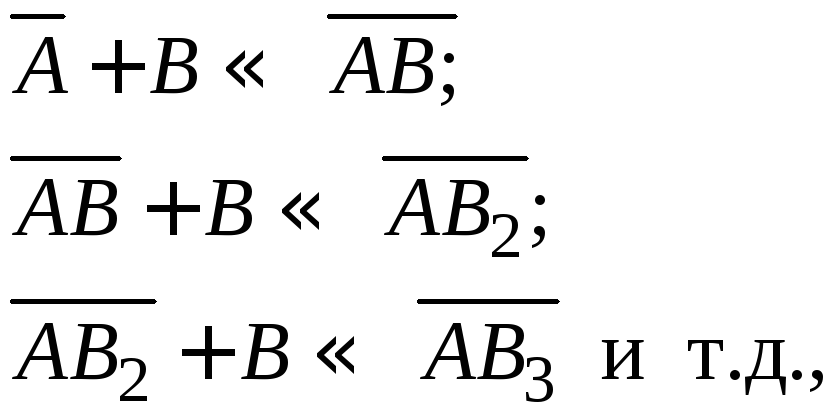
где
В
– адсорбат;
![]() – адсорбционный центр;
– адсорбционный центр;![]() – адсорбционный комплекс.
– адсорбционный комплекс.
С. Брунауэр, П. Эммет и Е. Теллер предложили уравнение полимолекулярной адсорбции БЭТ:
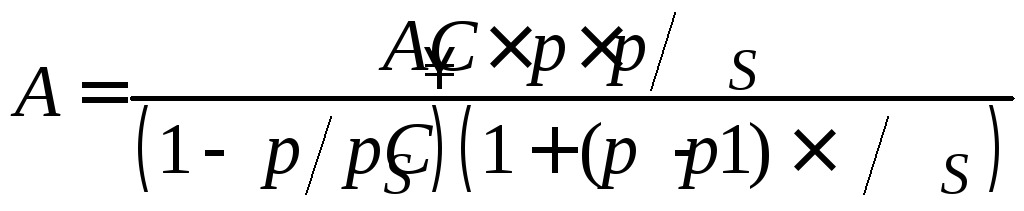 , (3.22)
, (3.22)
где
![]() – емкость одного адсорбционного
монослоя, зависящая от геометрии молекул
и определяемая площадью, которую занимает
одна молекула в насыщенном монослое;
– емкость одного адсорбционного
монослоя, зависящая от геометрии молекул
и определяемая площадью, которую занимает
одна молекула в насыщенном монослое;![]() – относительное давление пара (р
– равновесное давление пара, рS
– давление насыщенного пара); С
– константа, характеризующая энергию
взаимодействия в адсорбционном слое:
– относительное давление пара (р
– равновесное давление пара, рS
– давление насыщенного пара); С
– константа, характеризующая энергию
взаимодействия в адсорбционном слое:
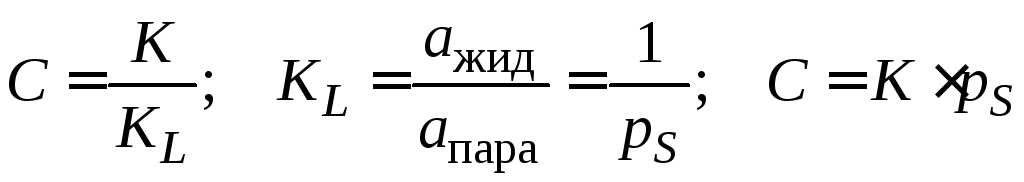 , (3.23)
, (3.23)
где К – константа адсорбционного равновесия в уравнении Лэнгмюра; КL – константа конденсации пара; рS – давление насыщенного пара (константа для каждого вещества).
Для расчета параметров адсорбции по теории БЭТ уравнение полимолекулярной адсорбции приводят к линейному виду. Для этого проводят следующие преобразования:
 ;
;
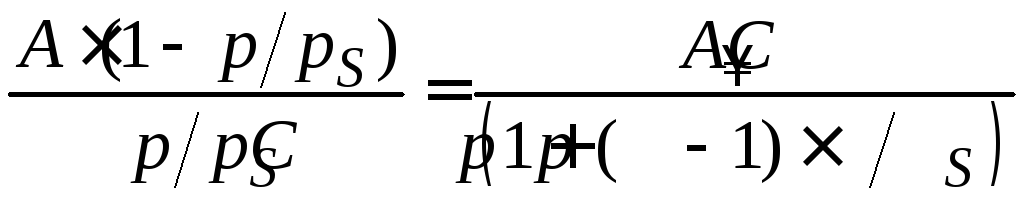 ;
;
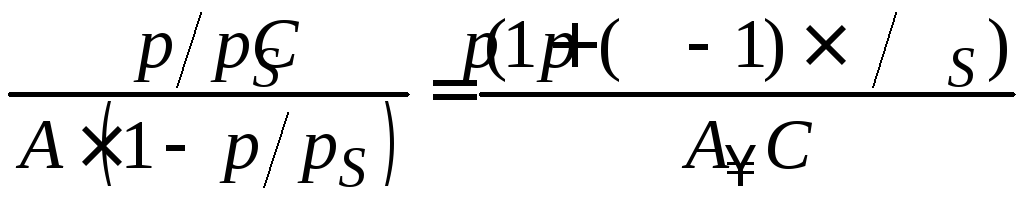 .
.
Получают уравнение полимолекулярной адсорбции БЭТ в линейной форме:
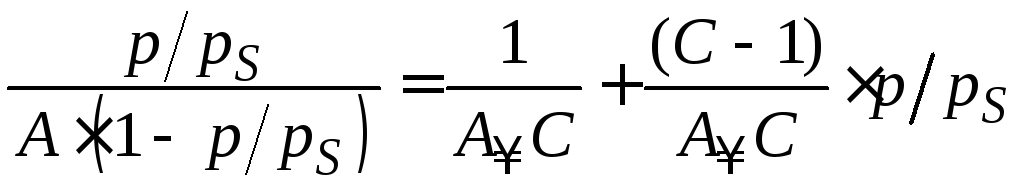 . (3.24)
. (3.24)
Строят изотерму адсорбции в координатах линейной формы уравнения БЭТ (рис. 3.17).
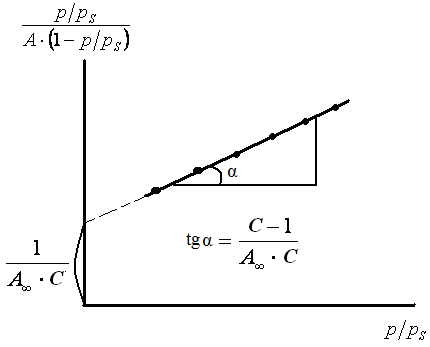
Рис. 3.17. Изотерма адсорбции БЭТ в линейных координатах
Экстраполяция зависимости до оси ординат дает отрезок, равный:
![]() ,
,
тангенс угла наклона прямой равен:
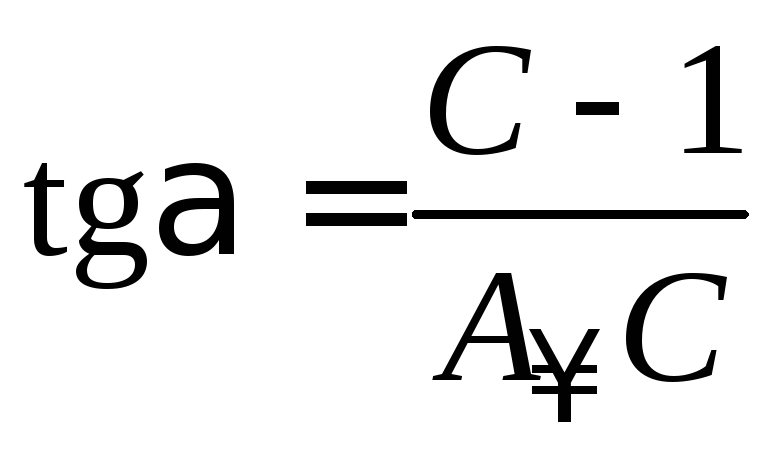 .
(3.25)
.
(3.25)
Для
многих газов и паров полимолекулярная
адсорбция имеет существенные отклонения
от теории БЭТ. Согласие с теорией тем
лучше, чем больше константа адсорбционного
равновесия (К).
Этому способствует увеличение сродства
адсорбата к адсорбенту и уменьшение
когезионных сил в конденсате на
поверхности. Уравнение изотермы БЭТ
хорошо выполняется при относительных
давлениях
![]() .
Прир/рS
< 0,05
в получаемые результаты вносит искажение
неоднородность поверхности, при р/рS
> 0,3
– начинает
сказываться взаимодействие между
адсорбированными молекулами.
.
Прир/рS
< 0,05
в получаемые результаты вносит искажение
неоднородность поверхности, при р/рS
> 0,3
– начинает
сказываться взаимодействие между
адсорбированными молекулами.
На
тории БЭТ основан стандартный метод
измерения удельной поверхности (![]() )
адсорбентов, катализаторов, порошков
и др. По экспериментальным данным находят
величину
)
адсорбентов, катализаторов, порошков
и др. По экспериментальным данным находят
величину![]() ,
а затем по уравнению (3.24) рассчитывают
удельную поверхность адсорбента:
,
а затем по уравнению (3.24) рассчитывают
удельную поверхность адсорбента:
![]() , (3.26)
, (3.26)
где
![]() – площадь, занимаемая одной молекулой
адсорбата;
– площадь, занимаемая одной молекулой
адсорбата;![]() – число Авогадро.
– число Авогадро.
В качестве адсорбатов используют инертные газы (азот, аргон, криптон и др.), которые характеризуются слабым межмолекулярным взаимодействием на поверхности адсорбента (физическая адсорбция), что обеспечивает достоверность результатов. Необходимо, чтобы форма молекулы адсорбата не слишком отличалась от сферической. Для увеличения адсорбции таких газов ее ведут при низких температурах, откуда и частое название метода БЭТ – метод низкотемпературной адсорбции.
В настоящее время предложено много модификаций уравнения теории БЭТ, но они, как правило, описывают только частные случаи изотерм адсорбции. Принципиальные основы теории БЭТ до настоящего времени сохраняют свое значение. В настоящее время теория находит применение в современных работах.
Пример 3.3. Ниже приведены экспериментальные данные адсорбции азота на TiO2 (рутиле) при 75 К.
|
|
0,078 |
0,149 |
0,217 |
0,279 |
0,348 |
|
А, моль/кг |
0,367 |
0,417 |
0,467 |
0,512 |
0,567 |
Вычислите
константы в уравнении БЭТ, используя
которые, рассчитайте удельную поверхность
адсорбента, если площадь, занимаемая
одной молекулой азота
![]() = 0,16 нм2.
= 0,16 нм2.
Решение:
1.
Для построения изотермы адсорбции азота
в координатах линейной формы уравнения
БЭТ (3.24) рассчитаем значения
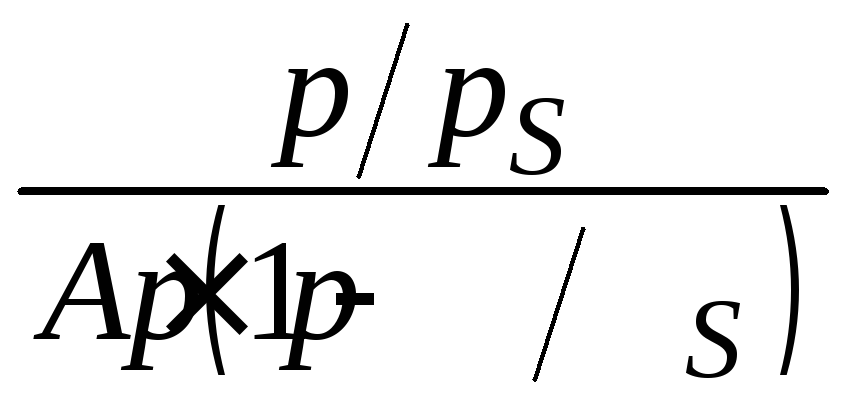 для
для![]() = 0,078:
= 0,078:
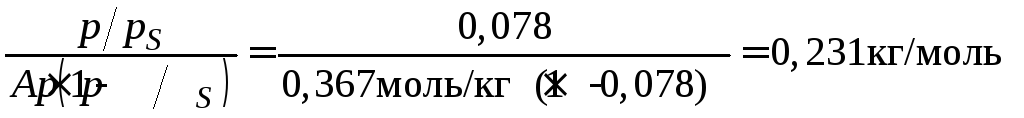 .
.
Аналогично
проведем расчет для других значений
![]() ,
полученные данные занесем в таблицу.
,
полученные данные занесем в таблицу.
|
|
0,078 |
0,149 |
0,217 |
0,279 |
0,348 |
|
|
0,231 |
0,420 |
0,593 |
0,756 |
0,941 |
2. По рассчитанным данным строим прямую в координатах линейной формы уравнения БЭТ.
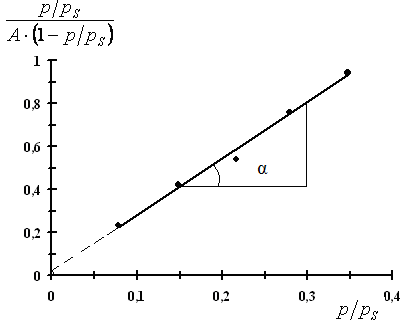
Рис. 3.18. Изотерма адсорбции БЭТ в линейных координатах
3. Из графика находим
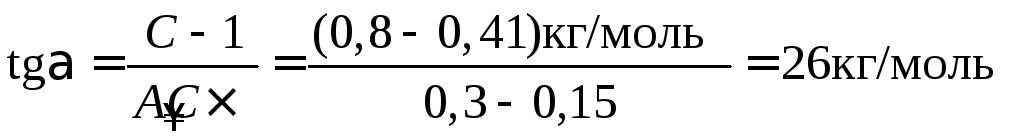 ;
;
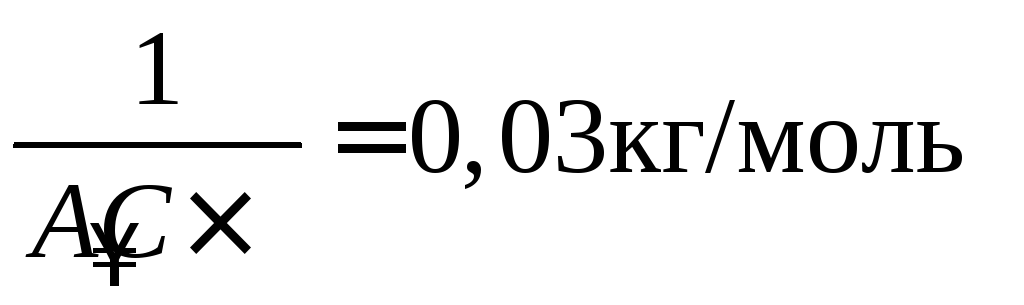 .
.
4. Для нахождения констант в уравнении БЭТ решаем совместно систему уравнений:
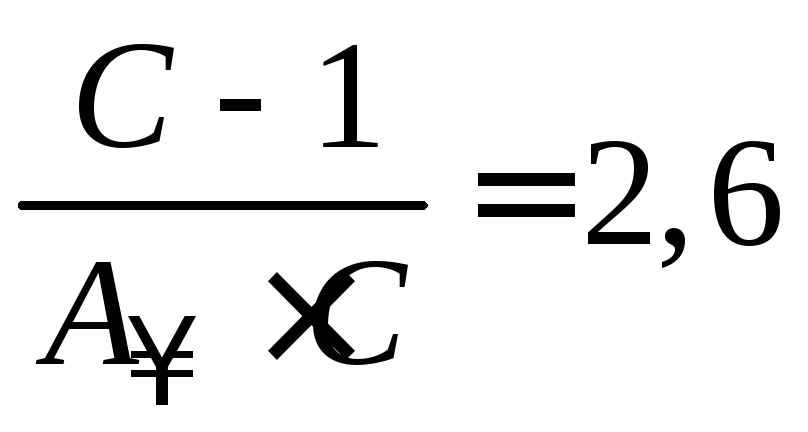 ; (а)
; (а)
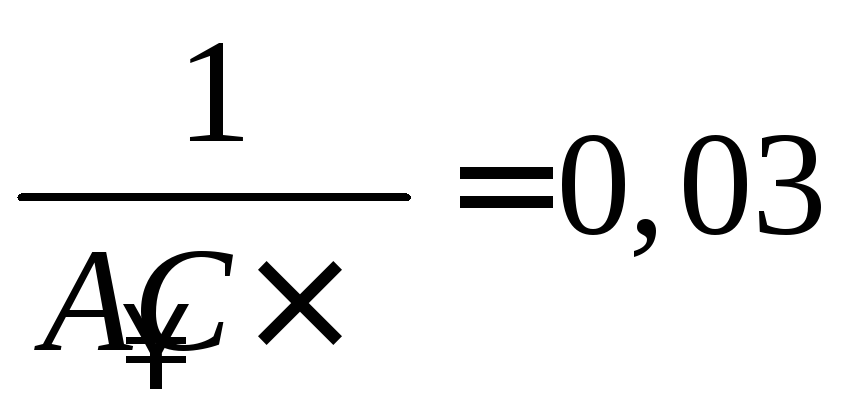 , (б)
, (б)
отсюда
![]() .
.
5. Удельную поверхность адсорбента рассчитываем по уравнению (3.26):