
- •«Национальный исследовательский
- •Томский политехнический Университет»
- •Е.В. Михеева, н.П. Пикула, а.П. Асташкина
- •Коллоидная химия
- •Оглавление
- •Глава 1 дисперсные системы
- •1.1. Общая характеристика дисперсных систем
- •1.1.1. Признаки объектов коллоидной химии
- •1.1.2. Специфические особенности высокодисперсных систем
- •1.2. Классификации дисперсных систем
- •1.2.1. Классификация по размерам частиц дисперсной фазы
- •1.2.2. Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •1.2.3. Классификация по силе межфазного взаимодействия дисперсной фазы и дисперсионной среды
- •1.2.4. Классификация по подвижности частиц дф (по структуре)
- •1.2.5. Классификация по фазовой различимости
- •1.2.6. Классификация по топографическому признаку (по форме частиц)
- •1.3. Методы получения дисперсных систем
- •1.3.1. Диспергационные методы
- •1.3.2. Конденсационные методы
- •1.3.2.1. Физические конденсационные методы
- •1.3.2.2. Химические конденсационные методы
- •2. Реакции обмена
- •3. Реакции окисления
- •1.3.3. Метод пептизации
- •1.4. Методы очистки дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 2 термодинамика поверхностных явлений
- •2.1. Классификация поверхностных явлений
- •2.2. Свободная поверхностная энергия и поверхностное натяжение
- •2.2.1. Физический смысл поверхностного натяжения
- •2.2.2. Термодинамическое определение поверхностного натяжения
- •2.2.3. Единицы измерения поверхностного натяжения
- •2.3. Влияние различных факторов на величину поверхностного натяжения
- •2.3.1. Влияние химической природы вещества
- •2.3.2. Влияние температуры
- •2.3.3. Влияние природы граничащих фаз
- •2.3.4. Влияние природы и концентрации растворенного вещества
- •2.4. Межмолекулярные и межфазные взаимодействия
- •2.4.1. Когезия
- •2.4.2. Адгезия
- •2.4.3. Растекание одной жидкости по поверхности другой
- •2.4.4. Смачивание
- •2.4.4.1. Анализ уравнения Юнга
- •2.4.4.2. Флотация
- •2.5. Особенности искривленной поверхности раздела фаз
- •2.5.1. Уравнение Лапласа
- •2.5.2. Капиллярное давление. Течение жидкости в капиллярах
- •2.6. Методы определения поверхностного натяжения
- •2.6.1. Метод наибольшего давления пузырька газа (метод Ребиндера)
- •2.6.2. Сталагмометрический метод (метод счета капель)
- •2.6.3. Метод капиллярного поднятия жидкости
- •2.7. Влияние кривизны поверхности на давление насыщенного пара
- •2.7.1. Уравнения Томсона (Кельвина)
- •2.7.2. Капиллярная конденсация
- •2.7.3. Изотермическая перегонка
- •Вопросыи задания для самоконтроля
- •Глава 3 адсорбция
- •3.1. Основные понятия и определения
- •3.1.1. Количественные способы выражения величины адсорбции
- •3.1.2. Классификации адсорбции
- •1. Классификация по природе границы раздела
- •2. Классификация по типу взаимодействия адсорбата и адсорбента
- •3.1.3. Основные экспериментальные зависимости адсорбции
- •3.2.Адсорбция на границе твердое тело – газ
- •3.2.1. Теория мономолекулярной адсорбции Лэнгмюра
- •3.2.2. Эмпирическое уравнение адсорбции Фрейндлиха
- •3.2.3. Теория полимолекулярной адсорбции Поляни
- •3.2.4. Дальнейшие представления о многослойной адсорбции. Теория бэт
- •3.2.5. Адсорбция на пористых адсорбентах
- •3.2.6.Адсорбенты и их характеристики
- •3.3.Адсорбция на границе жидкость – газ
- •3.3.1. Фундаментальное уравнение адсорбции Гиббса
- •3.3.2. Свойства поверхностно-активных (пав) и поверхностно-инактивных (пив) веществ
- •3.3.3. Строение адсорбционного слоя на границе раствор–газ
- •3.3.4. Уравнение Шишковского
- •3.3.5. Поверхностная активность. Правило Дюкло – Траубе
- •3.3.6. Расчет гиббсовской адсорбции из изотермы поверхностного натяжения методом графического дифференцирования
- •3.3.7.Применение уравнения изотермы Лэнгмюра к адсорбции на границе жидкость–газ. Расчет молекулярных характеристик исследуемого пав
- •3.3.8. Мицеллообразование в растворах коллоидных пав
- •3.3.9. Классификации пав
- •3.3.10. Солюбилизация
- •3.3.11. Практическое значение пав
- •3.3.12. Проблемы биоразлагаемости промышленных пав
- •3.4.Адсорбция на границе твердое тело – раствор
- •3.4.1. Молекулярная адсорбция
- •3.4.2. Ионная адсорбция
- •3.4.3. Ионообменная адсорбция. Ионный обмен
- •Вопросыи задания для самоконтроля
- •Глава 4 электрические свойства дисперсных систем
- •4.1. Электрокинетические явления
- •4.1.1. Механизм образования двойного электрического слоя
- •1. Неравенство электрохимических потенциалов ионов в кристаллической решетке твердого тела и ионов в растворе
- •Адсорбционный механизм образования дэс
- •Механизм поверхностной диссоциации
- •2. Специфическая адсорбции ионов на поверхности твердой фазы
- •3. Ориентированная адсорбция поверхностно-активных веществ
- •4.2. Теории строения двойного электрического слоя
- •4.2.1. Экспериментальные факты, послужившие основой для создания теорий строения дэс
- •4.2.2. Теория строения дэс Гельмгольца – Перрена
- •4.2.3. Теория строения дэс Гуи – Чэпмена
- •4.2.4. Современная теория строения дэс Штерна
- •4.3. Электрокинетический потенциал
- •4.3.1. Определение электрокинетического потенциала из электрокинетических явлений
- •4.3.2. Практическое значение электрокинетических явлений
- •4.4. Строение коллоидных мицелл
- •4.4.1. Примеры мицелл гидрофобных золей в природе
- •Вопросы и задания для самоконтроля
- •Глава 5 устойчивость и коагуляция лиофобных дисперсных систем
- •5.1. Основные понятия и определения
- •5.1.1. Факторы агрегативной устойчивости лиофобных систем
- •5.2. Коагуляция
- •Стадии коагуляции
- •5.2.1. Кинетика коагуляции. Теория кинетики быстрой коагуляции Смолуховского
- •5.2.2. Коагуляция золей электролитами
- •Эмпирические правила электролитной коагуляции
- •5.3. Теория устойчивости лиофобных дисперсных систем длфо
- •5.3.1. Расклинивающее давление
- •Составляющие расклинивающего давления
- •5.3.2. Энергия электростатического отталкивания
- •5.3.3. Энергия молекулярного притяжения
- •5.3.4. Потенциальные кривые взаимодействия частиц
- •5.4. Закономерности коагуляции гидрофобных золей электролитами
- •5.4.1. Особые явления при коагуляции
- •Коагуляция смесью электролитов
- •5.4.2. Примеры коагуляции. Образование почв
- •5.4.3. Физико-химические методы очистки сточных вод
- •Вопросыи задания для самоконтроля
- •Глава 6 структурно-механические свойства дисперсных систем
- •6.1. Типы структур
- •6.2. Реологические свойства дисперсных систем
- •6.2.1. Вязкость жидких дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 7 оптические свойства дисперсных систем
- •7.1. Рассеяние света в дисперсных системах
- •7.2. Поглощение света в дисперсных системах
- •7.3. Окраска дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 8 молекулярно-кинетические свойства дисперсных систем
- •8.1. Осмос
- •8.2. Диффузия
- •8.3. Броуновское движение
- •8.4. Седиментационное равновесие
- •8.5. Седиментационный анализ
- •Вопросы и задания для самоконтроля
- •Глава 9 краткая характеристика основных дисперсных систем
- •9.1. Системы с жидкой дисперсионной средой
- •9.1.1. Суспензии и золи
- •Классификация суспензий
- •Получение суспензий
- •Значение суспензий
- •9.1.2. Эмульсии
- •Классификация эмульсий
- •Агрегативная устойчивость эмульсии и природа эмульгатора
- •9.1.3. Пены
- •9.2. Системы с газообразной дисперсионной средой
- •9.2.1. Аэрозоли
- •Классификации аэрозолей
- •Агрегативная устойчивость аэрозолей. Коагуляция
- •Методы разрушения аэрозолей
- •9.3. Системы с твердой дисперсионной средой
- •Вопросыи задания для самоконтроля
- •Перечень используемой литературы
- •Коллоидная химия
- •В авторской редакции
- •Отпечатано в Издательстве тпу в полном соответствии с качеством предоставленного оригинал-макета
7.2. Поглощение света в дисперсных системах
Свет, проходя через дисперсную систему, частично поглощается ею. При этом интенсивность прошедшего через систему света зависит от интенсивности падающего света по закону Бугера – Ламберта – Бера:
![]() , (7.5)
, (7.5)
где I0 и I – интенсивности падающего и прошедшего света; l – толщина поглощающего слоя; k – коэффициент поглощения, характеризующий поглощающее вещество.
На практике уравнение (7.5) используют в следующем виде:
![]() , (7.6)
, (7.6)
где
А
– оптическая плотность или экстинкция;
![]() .
.
Таким образом, оптическая плотность прямо пропорциональна концентрации дисперсной системы:
![]() , (7.7)
, (7.7)
где ε – молярный коэффициент светопоглощения (экстинкции), зависящий от длины волны падающего света, температуры и природы дисперсионной среды; С – концентрация дисперсной фазы.
Закон Бугера – Ламберта – Бера, выведенный для гомогенных сред, оказался применимым и для дисперсных систем. В дисперсных системах поглощение света зависит от природы дисперсной фазы и размера частиц (степени дисперсности).
Для характеристики степени рассеяния световой волны часто используют мутность (τ):
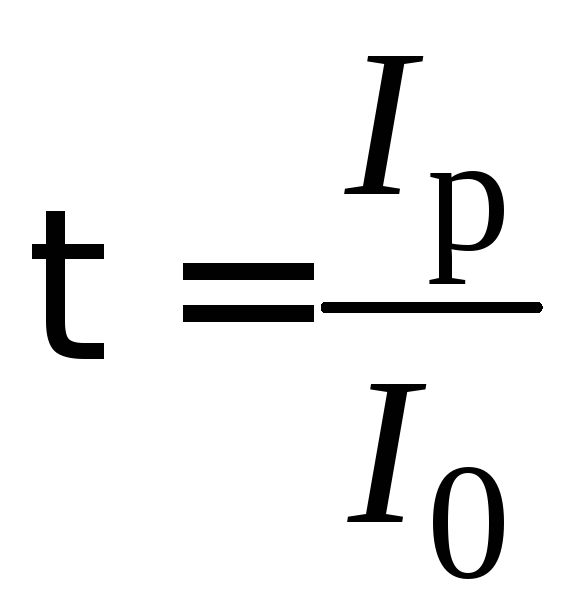 . (7.8)
. (7.8)
Мутность дисперсной системы связана с оптической плотностью (А) уравнением:
![]() , (7.9)
, (7.9)
где l – толщина кюветы.
7.3. Окраска дисперсных систем
Окраска дисперсных систем определяется явлениями рассеяния и поглощения света. Это относится особенно к системам, содержащим токопроводящие частицы (золям металлов). В зависимости от дисперсности золя его окраска может меняться. Например: высокодисперсный золь золота с радиусом частиц дисперсной фазы 20 нм (r = 20 нм) поглощает преимущественно зеленую часть спектра и имеет красную окраску; при увеличении размеров частиц до 50 нм золь золота приобретает синюю окраску. Зеленые растения поглощают красные лучи, т.к. они меньше рассеиваются атмосферой Земли, и приобретают окраску дополнительную к красной.
С явлениями избирательного поглощения и рассеяния света связана окраска драгоценных камней и самоцветов, содержащих высокодисперсные металлические включения: рубин – коллоидный раствор Cr или Au в Al2O3, синий цвет сапфиров обусловлен присутствием Ti в Al2O3, аметист – дисперсия Mn в SiO2.
Законы рассеяния и поглощения света дисперсными системами лежат в основе производства красителей, искусственных минералов.
Вопросыи задания для самоконтроля
1. Какие оптические свойства дисперсных систем вы знаете?
2. В каком случае происходит рассеяние света?
3. Каким уравнением количественно описывается рассеяние света?
4. От чего зависит интенсивность светорассеяния?
5. Какое уравнение количественно описывает поглощение света? Что такое оптическая плотность?
6. Чем определяется окраска дисперсных систем?
Глава 8 молекулярно-кинетические свойства дисперсных систем
К молекулярно-кинетическим дисперсных систем, связанным с тепловым движением частиц относятся: осмос, диффузия, броуновское движение, седиментационное равновесие. Эти свойства присущи для всех систем, содержащих достаточно малые частицы, способные принимать участие в тепловом движении. У дисперсных систем данные свойства характерны только для высокодисперсных систем.
8.1. Осмос
Осмос – процесс самопроизвольного перехода молекул растворителя через полупроницаемую мембрану (односторонняя диффузия дисперсионной среды). Давление, которое нужно приложить к системе, чтобы прекратился осмос – осмотическое давление (π).
Величина осмотического давления для разбавленных растворов неэлектролитов определяется уравнением Вант-Гоффа:
![]() , (8.1)
, (8.1)
где С – концентрация растворенного вещества, моль/л.
В
дисперсных системах вместо молярной
концентрации вводят понятие частичной
концентрации
![]() –
число кинетических единиц (коллоидных
частиц) в единице объема системы (1 л).
Частичная концентрация частиц связана
с молярной соотношением:
–
число кинетических единиц (коллоидных
частиц) в единице объема системы (1 л).
Частичная концентрация частиц связана
с молярной соотношением:![]() ,
тогда выражение для расчета осмотического
давления в коллоидных растворах примет
вид:
,
тогда выражение для расчета осмотического
давления в коллоидных растворах примет
вид:
![]() , (8.2)
, (8.2)
где
![]() – число Авогадро.
– число Авогадро.
Таким образом, осмотическое давление пропорционально числу частиц, принимающих участие в тепловом движении. Так как размер коллоидных частиц много больше размеров молекул или ионов в истинных растворах при равных массовых концентрациях, величина осмотического давления в коллоидном растворе будет много меньше величины осмотического давления в истинном растворе. Например, в 1% -м растворе сахара (М = 342 г/моль), представляющем из себя истинный раствор, осмотическое давление составляет 743 мм водяного столба. А в 1%-м растворе желатина (М = 2000 г/моль), образующем коллоидную систему, осмотическое давление всего 10 мм водяного столба.
