- •«Национальный исследовательский
- •Томский политехнический Университет»
- •Е.В. Михеева, н.П. Пикула, а.П. Асташкина
- •Коллоидная химия
- •Оглавление
- •Глава 1 дисперсные системы
- •1.1. Общая характеристика дисперсных систем
- •1.1.1. Признаки объектов коллоидной химии
- •1.1.2. Специфические особенности высокодисперсных систем
- •1.2. Классификации дисперсных систем
- •1.2.1. Классификация по размерам частиц дисперсной фазы
- •1.2.2. Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •1.2.3. Классификация по силе межфазного взаимодействия дисперсной фазы и дисперсионной среды
- •1.2.4. Классификация по подвижности частиц дф (по структуре)
- •1.2.5. Классификация по фазовой различимости
- •1.2.6. Классификация по топографическому признаку (по форме частиц)
- •1.3. Методы получения дисперсных систем
- •1.3.1. Диспергационные методы
- •1.3.2. Конденсационные методы
- •1.3.2.1. Физические конденсационные методы
- •1.3.2.2. Химические конденсационные методы
- •2. Реакции обмена
- •3. Реакции окисления
- •1.3.3. Метод пептизации
- •1.4. Методы очистки дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 2 термодинамика поверхностных явлений
- •2.1. Классификация поверхностных явлений
- •2.2. Свободная поверхностная энергия и поверхностное натяжение
- •2.2.1. Физический смысл поверхностного натяжения
- •2.2.2. Термодинамическое определение поверхностного натяжения
- •2.2.3. Единицы измерения поверхностного натяжения
- •2.3. Влияние различных факторов на величину поверхностного натяжения
- •2.3.1. Влияние химической природы вещества
- •2.3.2. Влияние температуры
- •2.3.3. Влияние природы граничащих фаз
- •2.3.4. Влияние природы и концентрации растворенного вещества
- •2.4. Межмолекулярные и межфазные взаимодействия
- •2.4.1. Когезия
- •2.4.2. Адгезия
- •2.4.3. Растекание одной жидкости по поверхности другой
- •2.4.4. Смачивание
- •2.4.4.1. Анализ уравнения Юнга
- •2.4.4.2. Флотация
- •2.5. Особенности искривленной поверхности раздела фаз
- •2.5.1. Уравнение Лапласа
- •2.5.2. Капиллярное давление. Течение жидкости в капиллярах
- •2.6. Методы определения поверхностного натяжения
- •2.6.1. Метод наибольшего давления пузырька газа (метод Ребиндера)
- •2.6.2. Сталагмометрический метод (метод счета капель)
- •2.6.3. Метод капиллярного поднятия жидкости
- •2.7. Влияние кривизны поверхности на давление насыщенного пара
- •2.7.1. Уравнения Томсона (Кельвина)
- •2.7.2. Капиллярная конденсация
- •2.7.3. Изотермическая перегонка
- •Вопросыи задания для самоконтроля
- •Глава 3 адсорбция
- •3.1. Основные понятия и определения
- •3.1.1. Количественные способы выражения величины адсорбции
- •3.1.2. Классификации адсорбции
- •1. Классификация по природе границы раздела
- •2. Классификация по типу взаимодействия адсорбата и адсорбента
- •3.1.3. Основные экспериментальные зависимости адсорбции
- •3.2.Адсорбция на границе твердое тело – газ
- •3.2.1. Теория мономолекулярной адсорбции Лэнгмюра
- •3.2.2. Эмпирическое уравнение адсорбции Фрейндлиха
- •3.2.3. Теория полимолекулярной адсорбции Поляни
- •3.2.4. Дальнейшие представления о многослойной адсорбции. Теория бэт
- •3.2.5. Адсорбция на пористых адсорбентах
- •3.2.6.Адсорбенты и их характеристики
- •3.3.Адсорбция на границе жидкость – газ
- •3.3.1. Фундаментальное уравнение адсорбции Гиббса
- •3.3.2. Свойства поверхностно-активных (пав) и поверхностно-инактивных (пив) веществ
- •3.3.3. Строение адсорбционного слоя на границе раствор–газ
- •3.3.4. Уравнение Шишковского
- •3.3.5. Поверхностная активность. Правило Дюкло – Траубе
- •3.3.6. Расчет гиббсовской адсорбции из изотермы поверхностного натяжения методом графического дифференцирования
- •3.3.7.Применение уравнения изотермы Лэнгмюра к адсорбции на границе жидкость–газ. Расчет молекулярных характеристик исследуемого пав
- •3.3.8. Мицеллообразование в растворах коллоидных пав
- •3.3.9. Классификации пав
- •3.3.10. Солюбилизация
- •3.3.11. Практическое значение пав
- •3.3.12. Проблемы биоразлагаемости промышленных пав
- •3.4.Адсорбция на границе твердое тело – раствор
- •3.4.1. Молекулярная адсорбция
- •3.4.2. Ионная адсорбция
- •3.4.3. Ионообменная адсорбция. Ионный обмен
- •Вопросыи задания для самоконтроля
- •Глава 4 электрические свойства дисперсных систем
- •4.1. Электрокинетические явления
- •4.1.1. Механизм образования двойного электрического слоя
- •1. Неравенство электрохимических потенциалов ионов в кристаллической решетке твердого тела и ионов в растворе
- •Адсорбционный механизм образования дэс
- •Механизм поверхностной диссоциации
- •2. Специфическая адсорбции ионов на поверхности твердой фазы
- •3. Ориентированная адсорбция поверхностно-активных веществ
- •4.2. Теории строения двойного электрического слоя
- •4.2.1. Экспериментальные факты, послужившие основой для создания теорий строения дэс
- •4.2.2. Теория строения дэс Гельмгольца – Перрена
- •4.2.3. Теория строения дэс Гуи – Чэпмена
- •4.2.4. Современная теория строения дэс Штерна
- •4.3. Электрокинетический потенциал
- •4.3.1. Определение электрокинетического потенциала из электрокинетических явлений
- •4.3.2. Практическое значение электрокинетических явлений
- •4.4. Строение коллоидных мицелл
- •4.4.1. Примеры мицелл гидрофобных золей в природе
- •Вопросы и задания для самоконтроля
- •Глава 5 устойчивость и коагуляция лиофобных дисперсных систем
- •5.1. Основные понятия и определения
- •5.1.1. Факторы агрегативной устойчивости лиофобных систем
- •5.2. Коагуляция
- •Стадии коагуляции
- •5.2.1. Кинетика коагуляции. Теория кинетики быстрой коагуляции Смолуховского
- •5.2.2. Коагуляция золей электролитами
- •Эмпирические правила электролитной коагуляции
- •5.3. Теория устойчивости лиофобных дисперсных систем длфо
- •5.3.1. Расклинивающее давление
- •Составляющие расклинивающего давления
- •5.3.2. Энергия электростатического отталкивания
- •5.3.3. Энергия молекулярного притяжения
- •5.3.4. Потенциальные кривые взаимодействия частиц
- •5.4. Закономерности коагуляции гидрофобных золей электролитами
- •5.4.1. Особые явления при коагуляции
- •Коагуляция смесью электролитов
- •5.4.2. Примеры коагуляции. Образование почв
- •5.4.3. Физико-химические методы очистки сточных вод
- •Вопросыи задания для самоконтроля
- •Глава 6 структурно-механические свойства дисперсных систем
- •6.1. Типы структур
- •6.2. Реологические свойства дисперсных систем
- •6.2.1. Вязкость жидких дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 7 оптические свойства дисперсных систем
- •7.1. Рассеяние света в дисперсных системах
- •7.2. Поглощение света в дисперсных системах
- •7.3. Окраска дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 8 молекулярно-кинетические свойства дисперсных систем
- •8.1. Осмос
- •8.2. Диффузия
- •8.3. Броуновское движение
- •8.4. Седиментационное равновесие
- •8.5. Седиментационный анализ
- •Вопросы и задания для самоконтроля
- •Глава 9 краткая характеристика основных дисперсных систем
- •9.1. Системы с жидкой дисперсионной средой
- •9.1.1. Суспензии и золи
- •Классификация суспензий
- •Получение суспензий
- •Значение суспензий
- •9.1.2. Эмульсии
- •Классификация эмульсий
- •Агрегативная устойчивость эмульсии и природа эмульгатора
- •9.1.3. Пены
- •9.2. Системы с газообразной дисперсионной средой
- •9.2.1. Аэрозоли
- •Классификации аэрозолей
- •Агрегативная устойчивость аэрозолей. Коагуляция
- •Методы разрушения аэрозолей
- •9.3. Системы с твердой дисперсионной средой
- •Вопросыи задания для самоконтроля
- •Перечень используемой литературы
- •Коллоидная химия
- •В авторской редакции
- •Отпечатано в Издательстве тпу в полном соответствии с качеством предоставленного оригинал-макета
1.2.5. Классификация по фазовой различимости
Эта классификация применима только для высокодисперсных систем. По фазовой различимости дисперсные системы могут быть разделены на два основных класса: суспензоиды и молекулярные коллоиды.
Суспензоиды – высокодисперсные гетерогенные системы (лиофильные или лиофобные), частицы которых представляют собой агрегаты атомов или молекул, отделенные четко различимой физической границей раздела фаз.
Молекулярные коллоиды – гомогенные однофазные системы, устойчивые и обратимые, образующиеся самопроизвольно, с отдельными сольватированными макромолекулами в качестве кинетических единиц (растворы высокомолекулярных соединений).
1.2.6. Классификация по топографическому признаку (по форме частиц)
Форма дисперсных частиц очень разнообразна. На многие свойства дисперсных частиц и образуемых ими дисперсных систем влияет соотношение между их размерами: длиной (l), шириной (h), и толщиной (d). По этому признаку частицы классифицируют на три группы:
Корпускулярные (объемные, трехмерные) – все три размера (l, h, d) примерно одинаковы.
Ламинарные (поверхностные, двумерные) – толщина (d) отвечает дисперсному интервалу, а длина и ширина имеют макроскопические значения – пленки.
Фибриллярные (линейные, одномерные) – интервалу дисперсных размеров отвечает поперечный размер – тонкие нити, волокна.
1.3. Методы получения дисперсных систем
Так как дисперсные системы широко используются в различных областях промышленности, следовательно, такие системы необходимо получать с необходимым набором физических и химических свойств (состав, агрегатное состояние, размер, форма, структура, поверхностные свойства).
При получении дисперсных систем решают две важные задачи:
Получение дисперсных частиц нужного размера и формы.
Стабилизация дисперсных систем, т.е. сохранение размеров дисперсных частиц в течение достаточно длительного времени (особенно актуальна для наночастиц).
Методы получения дисперсных систем делятся на три большие группы: диспергационные, конденсационные и методы пептизации.
1.3.1. Диспергационные методы
Методы заключаются в измельчении крупных (макроскопических) образцов данного вещества до частиц дисперсных размеров. При диспергировании химический состав и агрегатное состояние вещества обычно не меняются, меняется размер частиц и их форма. Диспергирование происходит, как правило, не самопроизвольно, а с затратой внешней работы, расходуемой на преодоление межмолекулярных сил при дроблении вещества.
Диспергационные методы используют в основном для получения грубодисперсных частиц – от 1 мкм и выше. Например, производство цемента (1 млрд тонн в год), измельчение руд полезных ископаемых, получение пищевых продуктов и лекарств и т.д.
Работа, необходимая для диспергирования твердого тела, затрачивается на работу деформирования тела (Wдеф) и работу образования новой поверхности (Wп):
![]() . (1.3)
. (1.3)
Работа деформирования пропорциональна объему тела: Wдеф = kV, где k – коэффициент пропорциональности, равный работе объемного деформирования единицы объема твердого тела; V – объем тела.
Работа
образования новой поверхности при
диспергировании пропорциональна
приращению поверхности:
![]() ,
где
,
где![]() – энергия образования единицы площади
поверхности или поверхностное натяжение;
– энергия образования единицы площади
поверхности или поверхностное натяжение;![]() – приращение поверхности или площадь
образовавшейся поверхности.
– приращение поверхности или площадь
образовавшейся поверхности.
Полная работа, затрачиваемая на диспергирование, выражается уравнением Ребиндера:
![]() . (1.4)
. (1.4)
При дроблении материалы разрушаются по местам прочностных дефектов (трещин). Поэтому, при измельчении прочность частиц возрастает, что используется для получения более прочных материалов. В связи с этим можно привести высказывание П.А. Ребиндера: «Путь к прочности материала лежит через его разрушение».
Для диспергирования твердых тел используют механические (дробление, истирание и т.п.), электрические (распыление в электрическом поле) методы, взрывы. В лабораторных условиях диспергирование проводят в шаровых и вибрационных мельницах.
|
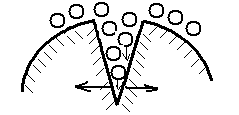
Рис. 1.3. Механизм уменьшения твердости
|
Для облегчения диспергирования твердых тел используют понизители твердости (растворы электролитов, поверхностно-активные вещества) – вещества, повышающие эффективность диспергирования за счет образования микротрещин (эффект П.А. Ребиндера). |
Понизители твердости обычно составляют 0,1 % от общей массы измельчаемых веществ и при этом снижают энергозатраты на получение дисперсных систем наполовину.
Механизм уменьшения твердости заключается в том, что добавляемое вещество (понизитель твердости) адсорбируется в местах дефектов кристаллической решетки (в микротрещинах) твердого тела, что приводит к экранированию сил сцепления, действующими между противоположными поверхностями щели (при адсорбции электролитов возникают силы электростатического отталкивания между одноименно заряженными ионами). С другой стороны поверхностно-активные вещества понижают поверхностное натяжение на границе раздела твердое тело – газ, что облегчает деформирование твердого тела.
Добавки помогают не только разрушить материал, но и стабилизируют систему в дисперсном состоянии, адсорбируются на поверхности частиц и мешают их обратному слипанию.
Для диспергирования жидкостей и получения мелких капель в аэрозолях и эмульсиях используют механические способы: встряхивание, быстрое перемешивание с кавитационными взрывами, воздействие ультразвука, распыление при течении жидкости через тонкие отверстия при быстром движении струи. Процессы диспергирования жидкостей имеют большое значение в энергетике – обеспечение эффективного сжигания жидкого топлива, в медицине и т.д.
При диспергировании газов используют: барботирование – прохождение газовой струи через жидкость с большой скоростью; одновременное смешивание потоков жидкости и газа в специальных устройствах.
Значение диспергационных методов. Диспергационные методы занимают ведущее место в мировом производстве различных веществ. Вещество в дисперсном состоянии обеспечивает удобство расфасовки, транспортировки, дозировки, способствуют увеличению скорости химических реакций и процессов растворения, сорбции, экстракции, дают возможность получать однородные материалы при составлении смесей и материалы с более высокими прочностными свойствами, материалы с большой удельной поверхностью (катализаторы, сорбенты). Методы используются при дроблении руды, угля, цемента, минеральных удобрений, получении пищевых продуктов и т.д.