- •«Национальный исследовательский
- •Томский политехнический Университет»
- •Е.В. Михеева, н.П. Пикула, а.П. Асташкина
- •Коллоидная химия
- •Оглавление
- •Глава 1 дисперсные системы
- •1.1. Общая характеристика дисперсных систем
- •1.1.1. Признаки объектов коллоидной химии
- •1.1.2. Специфические особенности высокодисперсных систем
- •1.2. Классификации дисперсных систем
- •1.2.1. Классификация по размерам частиц дисперсной фазы
- •1.2.2. Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •1.2.3. Классификация по силе межфазного взаимодействия дисперсной фазы и дисперсионной среды
- •1.2.4. Классификация по подвижности частиц дф (по структуре)
- •1.2.5. Классификация по фазовой различимости
- •1.2.6. Классификация по топографическому признаку (по форме частиц)
- •1.3. Методы получения дисперсных систем
- •1.3.1. Диспергационные методы
- •1.3.2. Конденсационные методы
- •1.3.2.1. Физические конденсационные методы
- •1.3.2.2. Химические конденсационные методы
- •2. Реакции обмена
- •3. Реакции окисления
- •1.3.3. Метод пептизации
- •1.4. Методы очистки дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 2 термодинамика поверхностных явлений
- •2.1. Классификация поверхностных явлений
- •2.2. Свободная поверхностная энергия и поверхностное натяжение
- •2.2.1. Физический смысл поверхностного натяжения
- •2.2.2. Термодинамическое определение поверхностного натяжения
- •2.2.3. Единицы измерения поверхностного натяжения
- •2.3. Влияние различных факторов на величину поверхностного натяжения
- •2.3.1. Влияние химической природы вещества
- •2.3.2. Влияние температуры
- •2.3.3. Влияние природы граничащих фаз
- •2.3.4. Влияние природы и концентрации растворенного вещества
- •2.4. Межмолекулярные и межфазные взаимодействия
- •2.4.1. Когезия
- •2.4.2. Адгезия
- •2.4.3. Растекание одной жидкости по поверхности другой
- •2.4.4. Смачивание
- •2.4.4.1. Анализ уравнения Юнга
- •2.4.4.2. Флотация
- •2.5. Особенности искривленной поверхности раздела фаз
- •2.5.1. Уравнение Лапласа
- •2.5.2. Капиллярное давление. Течение жидкости в капиллярах
- •2.6. Методы определения поверхностного натяжения
- •2.6.1. Метод наибольшего давления пузырька газа (метод Ребиндера)
- •2.6.2. Сталагмометрический метод (метод счета капель)
- •2.6.3. Метод капиллярного поднятия жидкости
- •2.7. Влияние кривизны поверхности на давление насыщенного пара
- •2.7.1. Уравнения Томсона (Кельвина)
- •2.7.2. Капиллярная конденсация
- •2.7.3. Изотермическая перегонка
- •Вопросыи задания для самоконтроля
- •Глава 3 адсорбция
- •3.1. Основные понятия и определения
- •3.1.1. Количественные способы выражения величины адсорбции
- •3.1.2. Классификации адсорбции
- •1. Классификация по природе границы раздела
- •2. Классификация по типу взаимодействия адсорбата и адсорбента
- •3.1.3. Основные экспериментальные зависимости адсорбции
- •3.2.Адсорбция на границе твердое тело – газ
- •3.2.1. Теория мономолекулярной адсорбции Лэнгмюра
- •3.2.2. Эмпирическое уравнение адсорбции Фрейндлиха
- •3.2.3. Теория полимолекулярной адсорбции Поляни
- •3.2.4. Дальнейшие представления о многослойной адсорбции. Теория бэт
- •3.2.5. Адсорбция на пористых адсорбентах
- •3.2.6.Адсорбенты и их характеристики
- •3.3.Адсорбция на границе жидкость – газ
- •3.3.1. Фундаментальное уравнение адсорбции Гиббса
- •3.3.2. Свойства поверхностно-активных (пав) и поверхностно-инактивных (пив) веществ
- •3.3.3. Строение адсорбционного слоя на границе раствор–газ
- •3.3.4. Уравнение Шишковского
- •3.3.5. Поверхностная активность. Правило Дюкло – Траубе
- •3.3.6. Расчет гиббсовской адсорбции из изотермы поверхностного натяжения методом графического дифференцирования
- •3.3.7.Применение уравнения изотермы Лэнгмюра к адсорбции на границе жидкость–газ. Расчет молекулярных характеристик исследуемого пав
- •3.3.8. Мицеллообразование в растворах коллоидных пав
- •3.3.9. Классификации пав
- •3.3.10. Солюбилизация
- •3.3.11. Практическое значение пав
- •3.3.12. Проблемы биоразлагаемости промышленных пав
- •3.4.Адсорбция на границе твердое тело – раствор
- •3.4.1. Молекулярная адсорбция
- •3.4.2. Ионная адсорбция
- •3.4.3. Ионообменная адсорбция. Ионный обмен
- •Вопросыи задания для самоконтроля
- •Глава 4 электрические свойства дисперсных систем
- •4.1. Электрокинетические явления
- •4.1.1. Механизм образования двойного электрического слоя
- •1. Неравенство электрохимических потенциалов ионов в кристаллической решетке твердого тела и ионов в растворе
- •Адсорбционный механизм образования дэс
- •Механизм поверхностной диссоциации
- •2. Специфическая адсорбции ионов на поверхности твердой фазы
- •3. Ориентированная адсорбция поверхностно-активных веществ
- •4.2. Теории строения двойного электрического слоя
- •4.2.1. Экспериментальные факты, послужившие основой для создания теорий строения дэс
- •4.2.2. Теория строения дэс Гельмгольца – Перрена
- •4.2.3. Теория строения дэс Гуи – Чэпмена
- •4.2.4. Современная теория строения дэс Штерна
- •4.3. Электрокинетический потенциал
- •4.3.1. Определение электрокинетического потенциала из электрокинетических явлений
- •4.3.2. Практическое значение электрокинетических явлений
- •4.4. Строение коллоидных мицелл
- •4.4.1. Примеры мицелл гидрофобных золей в природе
- •Вопросы и задания для самоконтроля
- •Глава 5 устойчивость и коагуляция лиофобных дисперсных систем
- •5.1. Основные понятия и определения
- •5.1.1. Факторы агрегативной устойчивости лиофобных систем
- •5.2. Коагуляция
- •Стадии коагуляции
- •5.2.1. Кинетика коагуляции. Теория кинетики быстрой коагуляции Смолуховского
- •5.2.2. Коагуляция золей электролитами
- •Эмпирические правила электролитной коагуляции
- •5.3. Теория устойчивости лиофобных дисперсных систем длфо
- •5.3.1. Расклинивающее давление
- •Составляющие расклинивающего давления
- •5.3.2. Энергия электростатического отталкивания
- •5.3.3. Энергия молекулярного притяжения
- •5.3.4. Потенциальные кривые взаимодействия частиц
- •5.4. Закономерности коагуляции гидрофобных золей электролитами
- •5.4.1. Особые явления при коагуляции
- •Коагуляция смесью электролитов
- •5.4.2. Примеры коагуляции. Образование почв
- •5.4.3. Физико-химические методы очистки сточных вод
- •Вопросыи задания для самоконтроля
- •Глава 6 структурно-механические свойства дисперсных систем
- •6.1. Типы структур
- •6.2. Реологические свойства дисперсных систем
- •6.2.1. Вязкость жидких дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 7 оптические свойства дисперсных систем
- •7.1. Рассеяние света в дисперсных системах
- •7.2. Поглощение света в дисперсных системах
- •7.3. Окраска дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 8 молекулярно-кинетические свойства дисперсных систем
- •8.1. Осмос
- •8.2. Диффузия
- •8.3. Броуновское движение
- •8.4. Седиментационное равновесие
- •8.5. Седиментационный анализ
- •Вопросы и задания для самоконтроля
- •Глава 9 краткая характеристика основных дисперсных систем
- •9.1. Системы с жидкой дисперсионной средой
- •9.1.1. Суспензии и золи
- •Классификация суспензий
- •Получение суспензий
- •Значение суспензий
- •9.1.2. Эмульсии
- •Классификация эмульсий
- •Агрегативная устойчивость эмульсии и природа эмульгатора
- •9.1.3. Пены
- •9.2. Системы с газообразной дисперсионной средой
- •9.2.1. Аэрозоли
- •Классификации аэрозолей
- •Агрегативная устойчивость аэрозолей. Коагуляция
- •Методы разрушения аэрозолей
- •9.3. Системы с твердой дисперсионной средой
- •Вопросыи задания для самоконтроля
- •Перечень используемой литературы
- •Коллоидная химия
- •В авторской редакции
- •Отпечатано в Издательстве тпу в полном соответствии с качеством предоставленного оригинал-макета
2.4.4.2. Флотация
Флотация относится к наиболее распространенным методам обогащения полезных ископаемых. Этим методом обогащается около 90 % руд цветных металлов, уголь, сера и др. природные материалы.
Флотационное обогащение (разделение) основано на различной смачиваемости водой ценных минералов и пустой породы. В случае пенной флотации через водную суспензию измельченной руды (пульпу) барботируют воздух, к пузырькам которого прилипают гидрофобные частицы ценного минерала (чистые металлы или их сульфиды), всплывающие затем на поверхность воды, и с образовавшейся пеной снимаются механически для дальнейшей переработки. Пустая порода (кварц, алюмосиликаты) хорошо смачивается водой и оседает во флотационных машинах.
Флотацию применяют для удаления из сточных вод нерастворимых диспергированных примесей, а также для удаления ПАВ в нефтеперерабатывающих, целлюлозно-бумажных машиностроительных и др. производств. Достоинствами флотации являются непрерывность процесса, широкий диапазон применения, малые эксплуатационные затраты, простая аппаратура и селективность выделения примесей.
Различают следующие способы флотационной обработки сточных вод: с выделением воздуха из растворов, с механическим диспергированием воздуха, с подачей воздуха через пористые материалы, электро- и химическую флотацию.
Очистка сточных вод от взвешенных частиц методом электрофлотации проходит при помощи пузырьков газа, образующихся при электролизе воды. Поднимаясь по сточной воде, эти пузырьки флотируют взвешенные частицы. При использовании растворимых электродов происходит образование хлопьев коагулянтов и пузырьков газа, что способствует более эффективной флотации.
Пример 2.3. Приготовлены водные суспензии из порошков кварца, малахита и талька. Какая из этих суспензий будет наиболее устойчива, если краевой угол смачивания водой для кварца 0°, а для малахита 17°, для талька 69°.
Решение. Так как для кварца θ = 0° – полное смачивание, то кварц будет полностью смачиваться водой и будет оседать на дно емкости. Для малахита и талька 90° > θ > 0° – неполное смачивание. Так как краевой угол смачивания у малахита более острый, чем у талька, то более устойчивой будет суспензия талька, а малахит постепенно осядет.
2.5. Особенности искривленной поверхности раздела фаз
2.5.1. Уравнение Лапласа
Рассмотрим еще одно важное качество дисперсных систем, связанное с раздробленностью – резкое увеличение кривизны поверхности частиц по сравнению с плоскостью.
За
счет кривизны поверхности жидкой
дисперсной фазы возникает избыточное
внутримолекулярное давление
![]() (рис. 2.6):
(рис. 2.6):
![]() , (2.18)
, (2.18)
где
![]() – разность давлений над искривленной
поверхностью (
– разность давлений над искривленной
поверхностью (![]() )
и давлением над плоской поверхностью
(
)
и давлением над плоской поверхностью
(![]() ).
).
Равнодействующая
сил поверхностного натяжения
![]() как векторная величина компенсируется
силой
как векторная величина компенсируется
силой![]() ,
которая направлена к центру частицы и
перпендикулярна ее поверхности.
,
которая направлена к центру частицы и
перпендикулярна ее поверхности.
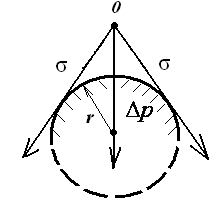
Рис.
2.6. Схема образования
избыточного
внутреннего давления
![]()
В
результате искривления поверхности
совершается работа
![]() ,
которая приводит к уменьшению объема
тела на величинуdV.
,
которая приводит к уменьшению объема
тела на величинуdV.
![]() . (2.19)
. (2.19)
Выразим
изменение поверхностной энергии через
энергию Гиббса при условии
![]() :
:
![]() , (2.20)
, (2.20)
где
Т
– температура; S
– энтропия; р
– давление; V
– объем; s
– площадь поверхности;
![]() – поверхностное натяжение;
– поверхностное натяжение;![]() – химический потенциалi-го
компонента; ni
– число моль
i-го
компонента;
– химический потенциалi-го
компонента; ni
– число моль
i-го
компонента;
![]() – электрический потенциал;q
– количество
электричества.
– электрический потенциал;q
– количество
электричества.
При
постоянных T,
p,
![]() ,q
и в условии равновесия (
,q
и в условии равновесия (![]() )
имеем
)
имеем
![]() , (2.21)
, (2.21)
тогда
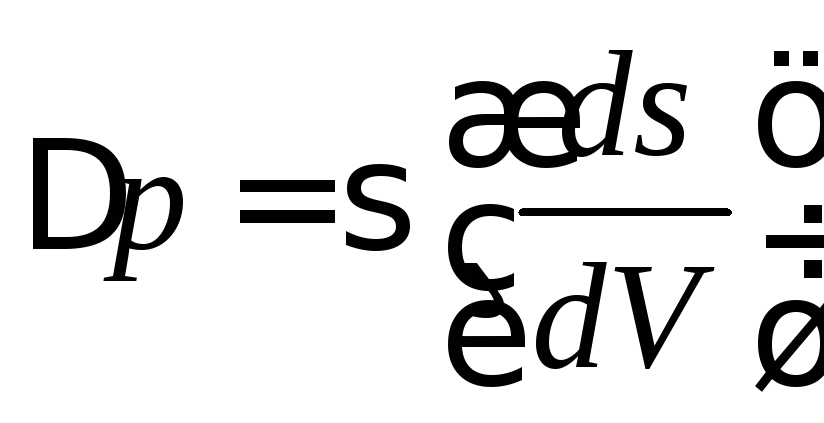 . (2.22)
. (2.22)
Величину
![]() называют кривизной поверхности.
называют кривизной поверхности.
для сферической поверхности:
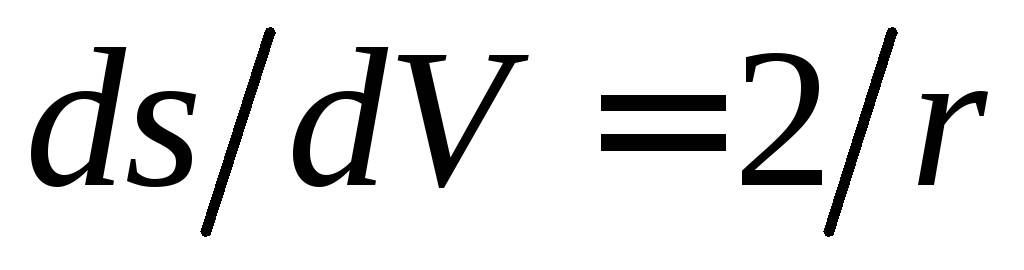 ;
;для цилиндрической поверхности:
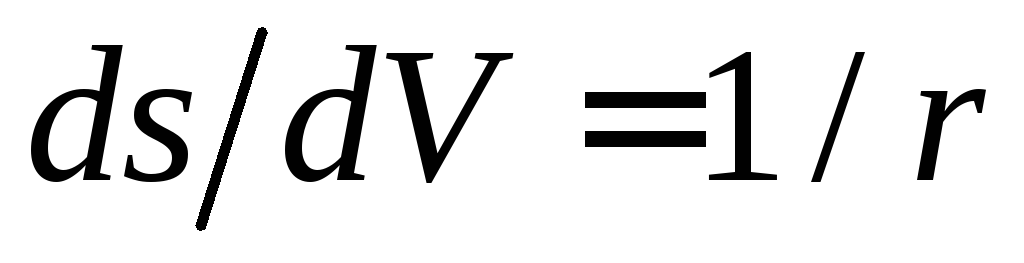 ;
;для частиц произвольной формы:
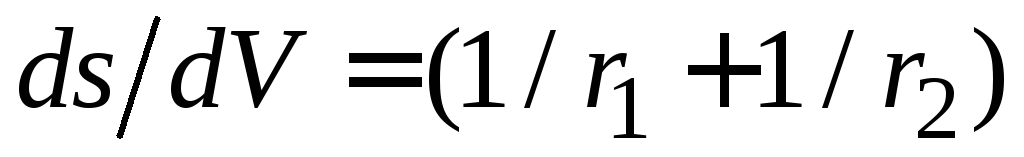 ,
,
где
![]() и
и![]() – главные радиусы кривизны поверхности.
– главные радиусы кривизны поверхности.
Получим
уравнение, связывающее избыточное
внутримолекулярное давление
![]() с радиусом кривизны поверхностиr:
с радиусом кривизны поверхностиr:
для сферической поверхности:
![]() ; (2.23)
; (2.23)
для цилиндрической поверхности:
![]() ; (2.24)
; (2.24)
для частиц произвольной формы:
![]() . (2.25)
. (2.25)
Уравнения (2.23)–(2.25) представляет собой закон капиллярного давления Лапласа для сферической, цилиндрической поверхностей и поверхности произвольной формы. Кривизна поверхности может быть положительной и отрицательной.
Если
центр окружности находится внутри тела
(рис. 2.7), то кривизна поверхности считается
положительной
![]() ,
тогда
,
тогда![]() > 0
– выпуклая поверхность, дополнительное
избыточное давление увеличивает
внутреннее давление жидкости (сжимает
ее).
> 0
– выпуклая поверхность, дополнительное
избыточное давление увеличивает
внутреннее давление жидкости (сжимает
ее).
Знак «+» в уравнении Лапласа для выпуклой поверхности:
![]() .
.
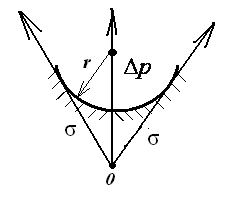
Если
центр окружности находится вне тела
(рис. 2.8), то кривизна поверхности считается
отрицательной
![]() ,
тогда
,
тогда![]() <
0 – вогнутая поверхность, дополнительное
избыточное давление уменьшает внутреннее
давление жидкости (растягивает ее).
<
0 – вогнутая поверхность, дополнительное
избыточное давление уменьшает внутреннее
давление жидкости (растягивает ее).
Знак «–» в уравнении Лапласа для вогнутой поверхности:
![]() .
.
|
|
|
|
Рис. 2.7. Схема образования избыточного давления для поверхности с положительной кривизной |
Рис. 2.8. Схема образования избыточного давления для поверхности с отрицательной кривизной |