- •«Национальный исследовательский
- •Томский политехнический Университет»
- •Е.В. Михеева, н.П. Пикула, а.П. Асташкина
- •Коллоидная химия
- •Оглавление
- •Глава 1 дисперсные системы
- •1.1. Общая характеристика дисперсных систем
- •1.1.1. Признаки объектов коллоидной химии
- •1.1.2. Специфические особенности высокодисперсных систем
- •1.2. Классификации дисперсных систем
- •1.2.1. Классификация по размерам частиц дисперсной фазы
- •1.2.2. Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •1.2.3. Классификация по силе межфазного взаимодействия дисперсной фазы и дисперсионной среды
- •1.2.4. Классификация по подвижности частиц дф (по структуре)
- •1.2.5. Классификация по фазовой различимости
- •1.2.6. Классификация по топографическому признаку (по форме частиц)
- •1.3. Методы получения дисперсных систем
- •1.3.1. Диспергационные методы
- •1.3.2. Конденсационные методы
- •1.3.2.1. Физические конденсационные методы
- •1.3.2.2. Химические конденсационные методы
- •2. Реакции обмена
- •3. Реакции окисления
- •1.3.3. Метод пептизации
- •1.4. Методы очистки дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 2 термодинамика поверхностных явлений
- •2.1. Классификация поверхностных явлений
- •2.2. Свободная поверхностная энергия и поверхностное натяжение
- •2.2.1. Физический смысл поверхностного натяжения
- •2.2.2. Термодинамическое определение поверхностного натяжения
- •2.2.3. Единицы измерения поверхностного натяжения
- •2.3. Влияние различных факторов на величину поверхностного натяжения
- •2.3.1. Влияние химической природы вещества
- •2.3.2. Влияние температуры
- •2.3.3. Влияние природы граничащих фаз
- •2.3.4. Влияние природы и концентрации растворенного вещества
- •2.4. Межмолекулярные и межфазные взаимодействия
- •2.4.1. Когезия
- •2.4.2. Адгезия
- •2.4.3. Растекание одной жидкости по поверхности другой
- •2.4.4. Смачивание
- •2.4.4.1. Анализ уравнения Юнга
- •2.4.4.2. Флотация
- •2.5. Особенности искривленной поверхности раздела фаз
- •2.5.1. Уравнение Лапласа
- •2.5.2. Капиллярное давление. Течение жидкости в капиллярах
- •2.6. Методы определения поверхностного натяжения
- •2.6.1. Метод наибольшего давления пузырька газа (метод Ребиндера)
- •2.6.2. Сталагмометрический метод (метод счета капель)
- •2.6.3. Метод капиллярного поднятия жидкости
- •2.7. Влияние кривизны поверхности на давление насыщенного пара
- •2.7.1. Уравнения Томсона (Кельвина)
- •2.7.2. Капиллярная конденсация
- •2.7.3. Изотермическая перегонка
- •Вопросыи задания для самоконтроля
- •Глава 3 адсорбция
- •3.1. Основные понятия и определения
- •3.1.1. Количественные способы выражения величины адсорбции
- •3.1.2. Классификации адсорбции
- •1. Классификация по природе границы раздела
- •2. Классификация по типу взаимодействия адсорбата и адсорбента
- •3.1.3. Основные экспериментальные зависимости адсорбции
- •3.2.Адсорбция на границе твердое тело – газ
- •3.2.1. Теория мономолекулярной адсорбции Лэнгмюра
- •3.2.2. Эмпирическое уравнение адсорбции Фрейндлиха
- •3.2.3. Теория полимолекулярной адсорбции Поляни
- •3.2.4. Дальнейшие представления о многослойной адсорбции. Теория бэт
- •3.2.5. Адсорбция на пористых адсорбентах
- •3.2.6.Адсорбенты и их характеристики
- •3.3.Адсорбция на границе жидкость – газ
- •3.3.1. Фундаментальное уравнение адсорбции Гиббса
- •3.3.2. Свойства поверхностно-активных (пав) и поверхностно-инактивных (пив) веществ
- •3.3.3. Строение адсорбционного слоя на границе раствор–газ
- •3.3.4. Уравнение Шишковского
- •3.3.5. Поверхностная активность. Правило Дюкло – Траубе
- •3.3.6. Расчет гиббсовской адсорбции из изотермы поверхностного натяжения методом графического дифференцирования
- •3.3.7.Применение уравнения изотермы Лэнгмюра к адсорбции на границе жидкость–газ. Расчет молекулярных характеристик исследуемого пав
- •3.3.8. Мицеллообразование в растворах коллоидных пав
- •3.3.9. Классификации пав
- •3.3.10. Солюбилизация
- •3.3.11. Практическое значение пав
- •3.3.12. Проблемы биоразлагаемости промышленных пав
- •3.4.Адсорбция на границе твердое тело – раствор
- •3.4.1. Молекулярная адсорбция
- •3.4.2. Ионная адсорбция
- •3.4.3. Ионообменная адсорбция. Ионный обмен
- •Вопросыи задания для самоконтроля
- •Глава 4 электрические свойства дисперсных систем
- •4.1. Электрокинетические явления
- •4.1.1. Механизм образования двойного электрического слоя
- •1. Неравенство электрохимических потенциалов ионов в кристаллической решетке твердого тела и ионов в растворе
- •Адсорбционный механизм образования дэс
- •Механизм поверхностной диссоциации
- •2. Специфическая адсорбции ионов на поверхности твердой фазы
- •3. Ориентированная адсорбция поверхностно-активных веществ
- •4.2. Теории строения двойного электрического слоя
- •4.2.1. Экспериментальные факты, послужившие основой для создания теорий строения дэс
- •4.2.2. Теория строения дэс Гельмгольца – Перрена
- •4.2.3. Теория строения дэс Гуи – Чэпмена
- •4.2.4. Современная теория строения дэс Штерна
- •4.3. Электрокинетический потенциал
- •4.3.1. Определение электрокинетического потенциала из электрокинетических явлений
- •4.3.2. Практическое значение электрокинетических явлений
- •4.4. Строение коллоидных мицелл
- •4.4.1. Примеры мицелл гидрофобных золей в природе
- •Вопросы и задания для самоконтроля
- •Глава 5 устойчивость и коагуляция лиофобных дисперсных систем
- •5.1. Основные понятия и определения
- •5.1.1. Факторы агрегативной устойчивости лиофобных систем
- •5.2. Коагуляция
- •Стадии коагуляции
- •5.2.1. Кинетика коагуляции. Теория кинетики быстрой коагуляции Смолуховского
- •5.2.2. Коагуляция золей электролитами
- •Эмпирические правила электролитной коагуляции
- •5.3. Теория устойчивости лиофобных дисперсных систем длфо
- •5.3.1. Расклинивающее давление
- •Составляющие расклинивающего давления
- •5.3.2. Энергия электростатического отталкивания
- •5.3.3. Энергия молекулярного притяжения
- •5.3.4. Потенциальные кривые взаимодействия частиц
- •5.4. Закономерности коагуляции гидрофобных золей электролитами
- •5.4.1. Особые явления при коагуляции
- •Коагуляция смесью электролитов
- •5.4.2. Примеры коагуляции. Образование почв
- •5.4.3. Физико-химические методы очистки сточных вод
- •Вопросыи задания для самоконтроля
- •Глава 6 структурно-механические свойства дисперсных систем
- •6.1. Типы структур
- •6.2. Реологические свойства дисперсных систем
- •6.2.1. Вязкость жидких дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 7 оптические свойства дисперсных систем
- •7.1. Рассеяние света в дисперсных системах
- •7.2. Поглощение света в дисперсных системах
- •7.3. Окраска дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 8 молекулярно-кинетические свойства дисперсных систем
- •8.1. Осмос
- •8.2. Диффузия
- •8.3. Броуновское движение
- •8.4. Седиментационное равновесие
- •8.5. Седиментационный анализ
- •Вопросы и задания для самоконтроля
- •Глава 9 краткая характеристика основных дисперсных систем
- •9.1. Системы с жидкой дисперсионной средой
- •9.1.1. Суспензии и золи
- •Классификация суспензий
- •Получение суспензий
- •Значение суспензий
- •9.1.2. Эмульсии
- •Классификация эмульсий
- •Агрегативная устойчивость эмульсии и природа эмульгатора
- •9.1.3. Пены
- •9.2. Системы с газообразной дисперсионной средой
- •9.2.1. Аэрозоли
- •Классификации аэрозолей
- •Агрегативная устойчивость аэрозолей. Коагуляция
- •Методы разрушения аэрозолей
- •9.3. Системы с твердой дисперсионной средой
- •Вопросыи задания для самоконтроля
- •Перечень используемой литературы
- •Коллоидная химия
- •В авторской редакции
- •Отпечатано в Издательстве тпу в полном соответствии с качеством предоставленного оригинал-макета
3.2.2. Эмпирическое уравнение адсорбции Фрейндлиха
Представления, развитые Лэнгмюром, в значительной степени идеализируют и упрощают действительную картину адсорбции. На самом деле поверхность большинства адсорбентов неоднородна, молекулы адсорбата взаимодействуют друг с другом на поверхности адсорбента, и адсорбция часто не заканчивается образованием мономолекулярного слоя. В этом случае уравнение изотермы адсорбции усложняется.
Фрейндлих предположил, что масса адсорбированного газа, приходящаяся на единицу массы адсорбента должна быть пропорциональна его равновесному давлению, возведенному в какую-то дробную степень. Другими словами, чем выше давление или чем больше концентрация растворенного вещества, тем больше вещества будет адсорбироваться на поверхности, однако пропорциональность должна носить не прямой, а степенной характер.
Эмпирическое уравнение Фрейндлиха для адсорбции имеет вид:
![]() , (3.16)
, (3.16)
где А – удельная адсорбция; р – равновесное давление; b и n – константы, определяемые опытным путем.
Константа b по своему физическому смыслу – значение адсорбции при равновесной концентрации адсорбата, равной единице (при С = 1, А = b). Эта константа для различных адсорбционных систем изменяется в пределах 2÷2,5. Показатель 1/n характеризует степень отклонения изотермы адсорбции от прямой линии (1/n ≈ 0,2–0,7).
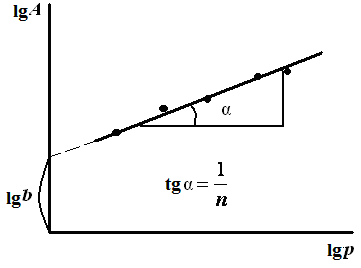
Константы уравнения Фрейндлиха из опытных данных определяют графически. Для этого уравнение (3.16) логарифмируют:
|
Рис. 3.8. Изотерма адсорбции в координатах линейной формы уравнения Фрейндлиха |
Строят линейную зависимость в координатах lgA–lg p. Экстраполяция зависимости до оси ординат дает отрезок, равный lgb, тангенс угла наклона прямой равен:
|
3.2.3. Теория полимолекулярной адсорбции Поляни
|
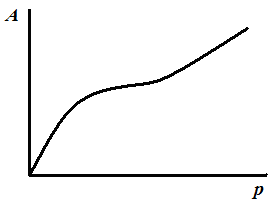
Рис. 3.9. S-образная изотерма адсорбции Поляни |
На практике, особенно при адсорбции паров, встречаются изотермы, правая часть которых круто поднимается вверх (S-образные), что свидетельствует о взаимодействии адсорбированных слоев молекул с адсорбатом, когда адсорбированные молекулы наслаиваются друг на друга. |
Для объяснения этого явления и описания S-образных изотерм адсорбции М. Поляни (и А. Эйкен) в 1915 г. предложил теорию полимолекулярной адсорбции, основанную на совершенно иных представлениях, чем теория Лэнгмюра.
Основные положения теории Поляни
1. Адсорбция обусловлена физическими силами (силами Ван-дер-Ваальса). Основной вклад вносят дальнодействующие дисперсионные силы аддитивные и не зависящие от температуры.
2. На поверхности адсорбента нет активных центров (энергетически однородная поверхность).
3. Адсорбционные силы действуют на больших расстояниях, что приводит к образованию полимолекулярного слоя. По мере удаления от поверхности действие адсорбционных сил уменьшается и на некотором расстоянии практически становится равным нулю.
4. Адсорбционные силы не зависят от температуры.
5. Практически все адсорбированное вещество на поверхности адсорбента находится в жидком состоянии.
В теории проводится аналогия между адсорбцией и конденсацией пара. Предполагается, что в результате взаимодействия с поверхностью газ сжимается до давления насыщения рS и переходит в жидкость. При этом возникает адсорбционный объем жидкости Vадс, который связан с величиной адсорбции соотношением:
Vадс = А·Vm, (3.19)
где А – значение адсорбции в моль; Vm – мольный объем адсорбата в конденсированном состоянии (объем 1 моль жидкого адсорбата).
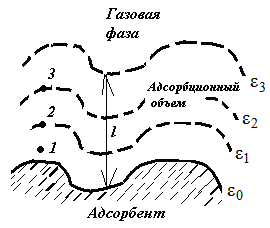
Адсорбционный объем Vадс (толщиной l) может быть представлен посредством ряда эквипотенциальных поверхностей (рис. 3.10), каждая поверхность соответствует определенному значению адсорбционного потенциала ε, который имеет максимальное значение у поверхности и минимальное – на границе адсорбционного слоя.
Адсорбционный потенциал – работа обратимого изотермического процесса по переносу 1 моль адсорбата из данной точки адсорбционного объема в газовую фазу (работа против действия адсорбционных сил).
Работа по переносу молекулы из точки 1 больше, чем из точки 2. следовательно: ε1 > ε2> ε3. Максимальный адсорбционный потенциал наблюдается вблизи поверхности адсорбента.
Рассматривая молекулы адсорбата как идеальный газ, можно записать, что адсорбционный потенциал равен работе расширения или сжатия идеального газа:
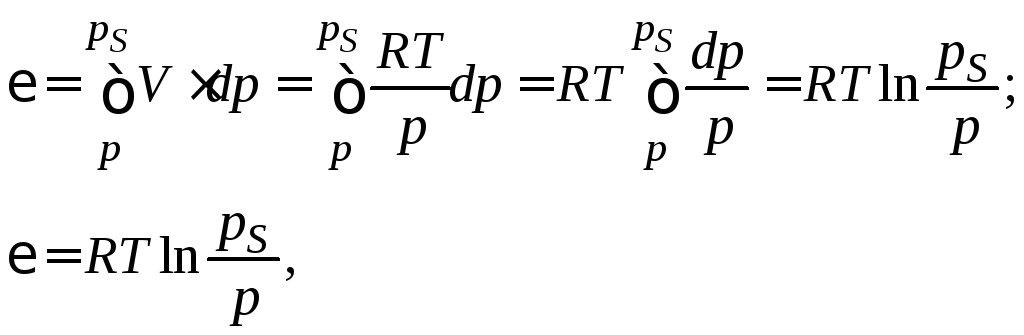 (3.20)
(3.20)
где рS – насыщенное давление газа (пара) при данной температуре (константа для каждого газа); р – равновесное давление в объемной фазе вдали от поверхности.
Зависимость адсорбционного потенциала (ε) от адсорбционного объема (Vадс) Поляни назвал характеристической кривой. Характеристическая кривая не зависит от температуры и индивидуальна и характерна для каждого вида адсорбента для сходных адсорбатов.
Характер характеристической кривой, построенной по экспериментальным данным (рис. 3.11), не зависит от температуры.
|
|
|
|
Рис. 3.10. Схематический разрез адсорбционного объема по теории Поляни |
Рис. 3.11. Характеристическая кривая |
Теория Поляни имеет большое практическое значение, т.к. позволяет рассчитывать изотермы адсорбции различных адсорбатов на одних и тех же адсорбентах при любой температуре.
Пусть
имеется экспериментальная зависимость
![]() для одного адсорбата при температуреТ1.
Необходимо рассчитать и построить
изотерму адсорбции для другого адсорбата
при температуре Т2.
Для этого:
для одного адсорбата при температуреТ1.
Необходимо рассчитать и построить
изотерму адсорбции для другого адсорбата
при температуре Т2.
Для этого:
1.
Построим характеристическую кривую
при температуре Т1.
Для этого рассчитаем значение
адсорбционного потенциала по уравнению
(3.20) (величина
![]() – константа для первого адсорбата) и
значение адсорбционного объема по
уравнению
– константа для первого адсорбата) и
значение адсорбционного объема по
уравнению![]() .
.
2.
Точки характеристической кривой
подставляем в уравнение (3.20) при
температуре Т2
и значении
![]() для другого адсорбата, и получаем
значенияр2.
Также рассчитываем значение адсорбции
А
по уравнению
для другого адсорбата, и получаем
значенияр2.
Также рассчитываем значение адсорбции
А
по уравнению
![]() ,
зная значение
,
зная значение![]() – константа для адсорбата.
– константа для адсорбата.
Адсорбционные потенциалы для разных адсорбатов на одном и том же адсорбенте находятся в постоянном соотношении. Это соотношение называется коэффициентом аффинности (близости, сродства):
![]()
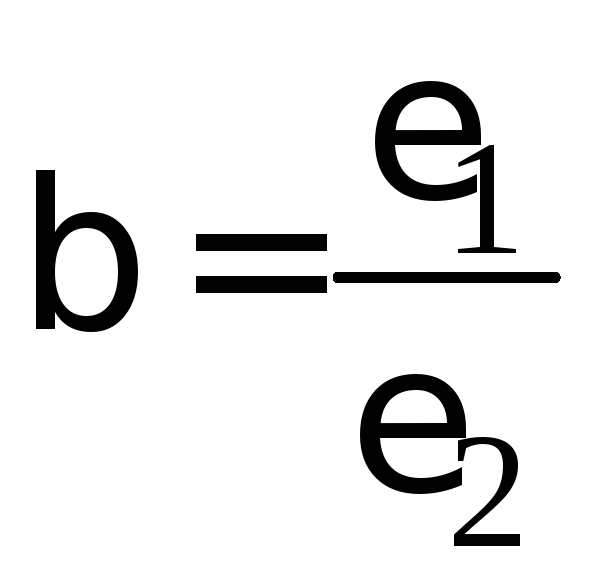 . (3.21)
. (3.21)
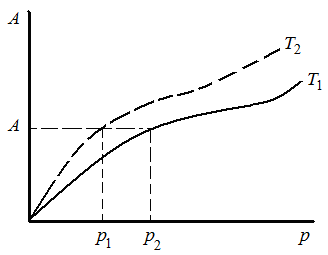
|
Рис. 3.12. Изотермы адсорбции Поляни при двух температурах |
Если имеется изотерма адсорбции и известно значение коэффициента аффинности для одного адсорбата, то можно построить изотерму адсорбции для другого адсорбата. Таким образом, теория Поляни, хотя и не дает аналитического выражения для изотермы адсорбции, однако позволяет вычислить адсорбцию для любой заданной температуры, если известна хотя бы одна изотерма при одной температуре и имеется характеристическая кривая конкретного адсорбента. |
Так как по теории Поляни практически все адсорбированное вещество находится на поверхности в жидком состоянии, то эта теория оказалась пригодной для описания адсорбции на пористых адсорбентах, в порах которых происходит конденсация пара.
Адсорбция паров на пористых сорбентах, удельная поверхность которых достигает сотен тысяч квадратных метров, имеет более сложный характер по сравнению с адсорбцией на непористых телах той же химической природы. Как правило, она сопровождается капиллярной конденсацией – конденсацией пара в порах при давлениях меньших, тем давление насыщенного пара адсорбата над плоской поверхностью.
Пример
3.2. При
изучении адсорбции сернистого ангидрида
SO2
(![]() )
на силикагеле при различных температурах
были получены следующие экспериментальные
данные:
)
на силикагеле при различных температурах
были получены следующие экспериментальные
данные:
T = 303 К
|
|
0 |
78 |
166 |
206 |
242 |
|
|
0 |
33,4 |
47,5 |
52,4 |
56,3 |
T = 313 К
|
|
0 |
147 |
200 |
244 |
280 |
|
|
0 |
38,75 |
44,55 |
48,55 |
51,85 |
1. Постройте изотерму адсорбции сернистого ангидрида при различных температурах, сделайте вывод о зависимости величины адсорбции от температуры.
2. Рассчитайте и постойте характеристическую кривую.
Решение:
1. По экспериментальным данным построим изотермы адсорбции сернистого ангидрида на силикагеле при различных температурах (рис. 3.13). Из графиков видно, что с увеличением температуры адсорбция уменьшается.
2. Для построения характеристической кривой рассчитаем адсорбционный объем и адсорбционный потенциал по уравнениям (3.19) и (3.20):
а) для расчета адсорбционного потенциала воспользуемся табличными значениями давления насыщенного пара (рS) сернистого ангидрида при различных температурах.
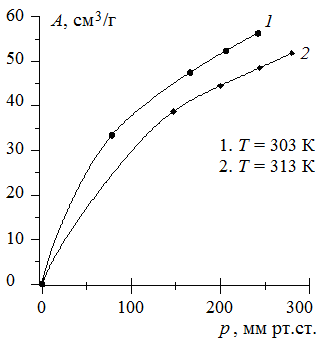
Рис. 3.13. Изотермы адсорбции сернистого ангидрида на силикагеле при различных температурах
Давление насыщенного пара (рS) сернистого ангидрида при различных температурах
|
Т, К |
303 |
313 |
|
|
349,6 |
471,2 |
Рассчитаем адсорбционный потенциал при Т = 303 К для р = 78 мм рт.ст. по уравнению (3.20):
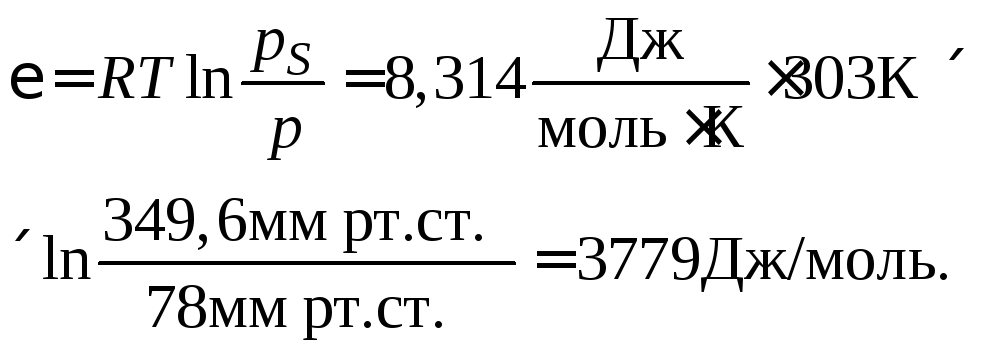
Аналогичный расчет проведем для других давлений при температурах 303 К и 313 К. Полученные результаты занесем в таблицы.
T = 303 К
|
|
78 |
166 |
206 |
242 |
|
|
3779 |
1876 |
1332 |
927 |
T = 313 К
|
|
147 |
200 |
244 |
280 |
|
|
3031 |
2230 |
1713 |
1354 |
б)
Для расчета адсорбционного объема (![]() ):
):
Пересчитаем величину адсорбции в размерность моль/г, для этого рассчитаем количество моль SO2, адсорбированного 1 г геля кремневой кислоты:
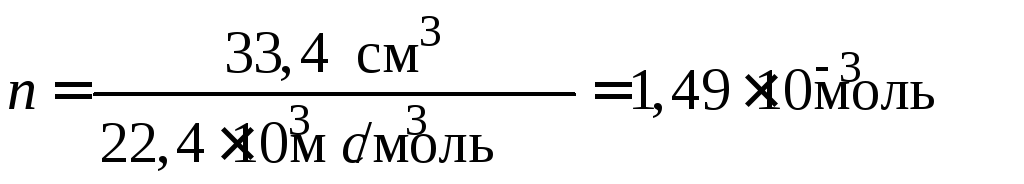 .
.
Рассчитаем мольный объем сернистого ангидрида:
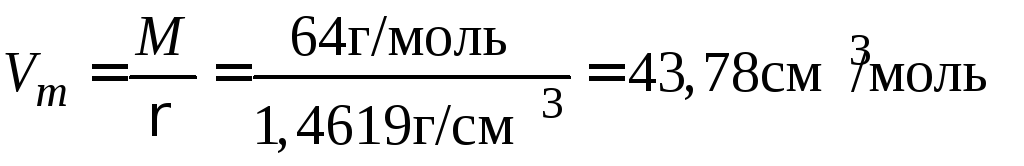 ,
,
где 64 г/моль – молярная масса SO2; 1,4619 г/см3 – плотность жидкого SO2.
Рассчитаем адсорбционный объем при Т = 303 К для А = 33,4 см3/г = =1,49·10–3 моль/г по уравнению (3.19):
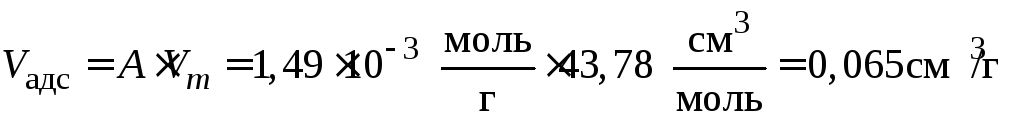 .
.
Аналогичный расчет проведем для других величин адсорбции при температурах 303 К и 313 К. Полученные результаты занесем в таблицы.
T = 303 К
|
|
33,4 |
47,5 |
52,4 |
56,3 |
|
|
0,065 |
0,093 |
0,102 |
0,110 |
T = 313 К
|
|
38,75 |
44,55 |
48,55 |
51,85 |
|
|
0,076 |
0,087 |
0,095 |
0,101 |
в) Занесем результаты расчетов адсорбционного объема и адсорбционного потенциала при двух температурах в таблицы:
T = 303 К
|
|
0,065 |
0,093 |
0,102 |
0,110 |
|
|
3779 |
1876 |
1332 |
927 |
T = 313 К
|
|
0,076 |
0,087 |
0,095 |
0,101 |
|
|
3031 |
2230 |
1713 |
1354 |
г) Строим характеристическую кривую.
Из рис. 3.14 видно, что все рассчитанные при разных температурах точки легли на одну кривую, следовательно, характеристическая кривая действительно не зависит от температуры, индивидуальна и характерна для каждого адсорбента.
Мы рассмотрели кратко две теории адсорбции – теорию мономолекулярной адсорбции Лэнгмюра и теорию полимолекулярной адсорбции Поляни, на первый взгляд исключающие друг друга. Возникает вопрос, какая из этих теорий более правильная? На это следует ответить, что обе теории ограничены в применении. В зависимости от природы адсорбента и адсорбата, от условий сорбции в одних случаях применима одна, а в других – другая теория адсорбции. Теория Поляни применима только к явлениям чисто физической адсорбции. Теория Лэнгмюра охватывает с известными ограничениями явления как физической, так и химической адсорбции. Однако теория Лэнгмюра не может быть применена для объяснения адсорбции на тонкопористых сорбентах, имеющих сужающиеся поры.
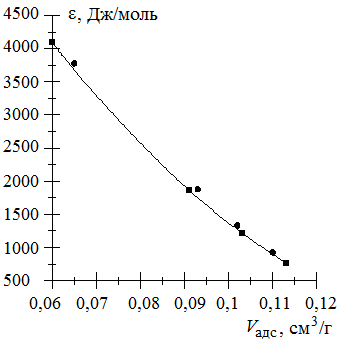
Рис. 3.14. Характеристическая кривая для силикагеля
В большинстве случаев мономолекулярный адсорбционный слой не компенсирует полностью избыточную поверхностную энергию, и влияние поверхностных сил может распространяться на второй, третий и последующие адсорбционные слои. Эта возможность реализуется, когда пары и газы адсорбируются при температурах ниже критической. В этом случае образуются полимолекулярные слои адсорбата на поверхности адсорбента. Полимолекулярную адсорбцию можно представить как результат вынужденной конденсации пара под действием поверхностных сил.