- •«Национальный исследовательский
- •Томский политехнический Университет»
- •Е.В. Михеева, н.П. Пикула, а.П. Асташкина
- •Коллоидная химия
- •Оглавление
- •Глава 1 дисперсные системы
- •1.1. Общая характеристика дисперсных систем
- •1.1.1. Признаки объектов коллоидной химии
- •1.1.2. Специфические особенности высокодисперсных систем
- •1.2. Классификации дисперсных систем
- •1.2.1. Классификация по размерам частиц дисперсной фазы
- •1.2.2. Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •1.2.3. Классификация по силе межфазного взаимодействия дисперсной фазы и дисперсионной среды
- •1.2.4. Классификация по подвижности частиц дф (по структуре)
- •1.2.5. Классификация по фазовой различимости
- •1.2.6. Классификация по топографическому признаку (по форме частиц)
- •1.3. Методы получения дисперсных систем
- •1.3.1. Диспергационные методы
- •1.3.2. Конденсационные методы
- •1.3.2.1. Физические конденсационные методы
- •1.3.2.2. Химические конденсационные методы
- •2. Реакции обмена
- •3. Реакции окисления
- •1.3.3. Метод пептизации
- •1.4. Методы очистки дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 2 термодинамика поверхностных явлений
- •2.1. Классификация поверхностных явлений
- •2.2. Свободная поверхностная энергия и поверхностное натяжение
- •2.2.1. Физический смысл поверхностного натяжения
- •2.2.2. Термодинамическое определение поверхностного натяжения
- •2.2.3. Единицы измерения поверхностного натяжения
- •2.3. Влияние различных факторов на величину поверхностного натяжения
- •2.3.1. Влияние химической природы вещества
- •2.3.2. Влияние температуры
- •2.3.3. Влияние природы граничащих фаз
- •2.3.4. Влияние природы и концентрации растворенного вещества
- •2.4. Межмолекулярные и межфазные взаимодействия
- •2.4.1. Когезия
- •2.4.2. Адгезия
- •2.4.3. Растекание одной жидкости по поверхности другой
- •2.4.4. Смачивание
- •2.4.4.1. Анализ уравнения Юнга
- •2.4.4.2. Флотация
- •2.5. Особенности искривленной поверхности раздела фаз
- •2.5.1. Уравнение Лапласа
- •2.5.2. Капиллярное давление. Течение жидкости в капиллярах
- •2.6. Методы определения поверхностного натяжения
- •2.6.1. Метод наибольшего давления пузырька газа (метод Ребиндера)
- •2.6.2. Сталагмометрический метод (метод счета капель)
- •2.6.3. Метод капиллярного поднятия жидкости
- •2.7. Влияние кривизны поверхности на давление насыщенного пара
- •2.7.1. Уравнения Томсона (Кельвина)
- •2.7.2. Капиллярная конденсация
- •2.7.3. Изотермическая перегонка
- •Вопросыи задания для самоконтроля
- •Глава 3 адсорбция
- •3.1. Основные понятия и определения
- •3.1.1. Количественные способы выражения величины адсорбции
- •3.1.2. Классификации адсорбции
- •1. Классификация по природе границы раздела
- •2. Классификация по типу взаимодействия адсорбата и адсорбента
- •3.1.3. Основные экспериментальные зависимости адсорбции
- •3.2.Адсорбция на границе твердое тело – газ
- •3.2.1. Теория мономолекулярной адсорбции Лэнгмюра
- •3.2.2. Эмпирическое уравнение адсорбции Фрейндлиха
- •3.2.3. Теория полимолекулярной адсорбции Поляни
- •3.2.4. Дальнейшие представления о многослойной адсорбции. Теория бэт
- •3.2.5. Адсорбция на пористых адсорбентах
- •3.2.6.Адсорбенты и их характеристики
- •3.3.Адсорбция на границе жидкость – газ
- •3.3.1. Фундаментальное уравнение адсорбции Гиббса
- •3.3.2. Свойства поверхностно-активных (пав) и поверхностно-инактивных (пив) веществ
- •3.3.3. Строение адсорбционного слоя на границе раствор–газ
- •3.3.4. Уравнение Шишковского
- •3.3.5. Поверхностная активность. Правило Дюкло – Траубе
- •3.3.6. Расчет гиббсовской адсорбции из изотермы поверхностного натяжения методом графического дифференцирования
- •3.3.7.Применение уравнения изотермы Лэнгмюра к адсорбции на границе жидкость–газ. Расчет молекулярных характеристик исследуемого пав
- •3.3.8. Мицеллообразование в растворах коллоидных пав
- •3.3.9. Классификации пав
- •3.3.10. Солюбилизация
- •3.3.11. Практическое значение пав
- •3.3.12. Проблемы биоразлагаемости промышленных пав
- •3.4.Адсорбция на границе твердое тело – раствор
- •3.4.1. Молекулярная адсорбция
- •3.4.2. Ионная адсорбция
- •3.4.3. Ионообменная адсорбция. Ионный обмен
- •Вопросыи задания для самоконтроля
- •Глава 4 электрические свойства дисперсных систем
- •4.1. Электрокинетические явления
- •4.1.1. Механизм образования двойного электрического слоя
- •1. Неравенство электрохимических потенциалов ионов в кристаллической решетке твердого тела и ионов в растворе
- •Адсорбционный механизм образования дэс
- •Механизм поверхностной диссоциации
- •2. Специфическая адсорбции ионов на поверхности твердой фазы
- •3. Ориентированная адсорбция поверхностно-активных веществ
- •4.2. Теории строения двойного электрического слоя
- •4.2.1. Экспериментальные факты, послужившие основой для создания теорий строения дэс
- •4.2.2. Теория строения дэс Гельмгольца – Перрена
- •4.2.3. Теория строения дэс Гуи – Чэпмена
- •4.2.4. Современная теория строения дэс Штерна
- •4.3. Электрокинетический потенциал
- •4.3.1. Определение электрокинетического потенциала из электрокинетических явлений
- •4.3.2. Практическое значение электрокинетических явлений
- •4.4. Строение коллоидных мицелл
- •4.4.1. Примеры мицелл гидрофобных золей в природе
- •Вопросы и задания для самоконтроля
- •Глава 5 устойчивость и коагуляция лиофобных дисперсных систем
- •5.1. Основные понятия и определения
- •5.1.1. Факторы агрегативной устойчивости лиофобных систем
- •5.2. Коагуляция
- •Стадии коагуляции
- •5.2.1. Кинетика коагуляции. Теория кинетики быстрой коагуляции Смолуховского
- •5.2.2. Коагуляция золей электролитами
- •Эмпирические правила электролитной коагуляции
- •5.3. Теория устойчивости лиофобных дисперсных систем длфо
- •5.3.1. Расклинивающее давление
- •Составляющие расклинивающего давления
- •5.3.2. Энергия электростатического отталкивания
- •5.3.3. Энергия молекулярного притяжения
- •5.3.4. Потенциальные кривые взаимодействия частиц
- •5.4. Закономерности коагуляции гидрофобных золей электролитами
- •5.4.1. Особые явления при коагуляции
- •Коагуляция смесью электролитов
- •5.4.2. Примеры коагуляции. Образование почв
- •5.4.3. Физико-химические методы очистки сточных вод
- •Вопросыи задания для самоконтроля
- •Глава 6 структурно-механические свойства дисперсных систем
- •6.1. Типы структур
- •6.2. Реологические свойства дисперсных систем
- •6.2.1. Вязкость жидких дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 7 оптические свойства дисперсных систем
- •7.1. Рассеяние света в дисперсных системах
- •7.2. Поглощение света в дисперсных системах
- •7.3. Окраска дисперсных систем
- •Вопросыи задания для самоконтроля
- •Глава 8 молекулярно-кинетические свойства дисперсных систем
- •8.1. Осмос
- •8.2. Диффузия
- •8.3. Броуновское движение
- •8.4. Седиментационное равновесие
- •8.5. Седиментационный анализ
- •Вопросы и задания для самоконтроля
- •Глава 9 краткая характеристика основных дисперсных систем
- •9.1. Системы с жидкой дисперсионной средой
- •9.1.1. Суспензии и золи
- •Классификация суспензий
- •Получение суспензий
- •Значение суспензий
- •9.1.2. Эмульсии
- •Классификация эмульсий
- •Агрегативная устойчивость эмульсии и природа эмульгатора
- •9.1.3. Пены
- •9.2. Системы с газообразной дисперсионной средой
- •9.2.1. Аэрозоли
- •Классификации аэрозолей
- •Агрегативная устойчивость аэрозолей. Коагуляция
- •Методы разрушения аэрозолей
- •9.3. Системы с твердой дисперсионной средой
- •Вопросыи задания для самоконтроля
- •Перечень используемой литературы
- •Коллоидная химия
- •В авторской редакции
- •Отпечатано в Издательстве тпу в полном соответствии с качеством предоставленного оригинал-макета
5.2.1. Кинетика коагуляции. Теория кинетики быстрой коагуляции Смолуховского
В качестве меры агрегативной устойчивости дисперсной системы можно рассматривать скорость ее коагуляции.
Скорость коагуляции – изменение частичной концентрации дисперсных частиц в единице объема в единицу времени.
Скорость коагуляции может быть самой разной в различных системах (от нескольких секунд до нескольких лет). Система тем более устойчива, чем медленнее она коагулирует.
Различают: быструю коагуляцию, при которой каждое столкновение частиц приводит к их слипанию (все соударения эффективны); и медленную коагуляцию, когда не все столкновения частиц являются эффективными.
Теория кинетики быстрой коагуляции однородных сферических частиц была разработана польским ученым М. Смолуховским в 1916 г.
Основные положения теории быстрой коагуляции Смолуховского:
частицы дисперсной фазы сближаются в результате броуновского движения, слипаются, образуют агрегат, который совершает дальнейшее броуновское движение как единое целое;
скорость сближения частиц определяется коэффициентом диффузии и средним расстоянием между частицами;
в каждом элементарном акте участвуют только две частицы дисперсной фазы;
все частицы имеют одинаковый размер и обладают одинаковой подвижностью, форму частиц считают сферической.
Смолуховский предположил, что в начальной стадии процесс коагуляции протекает как бимолекулярная реакция и описывается уравнением реакции второго порядка:
![]() . (5.1)
. (5.1)
После интегрирования уравнения (5.1) получаем выражения для расчета константы скорости процесса коагуляции, числа частиц и времени половинной коагуляции в любой момент времени:
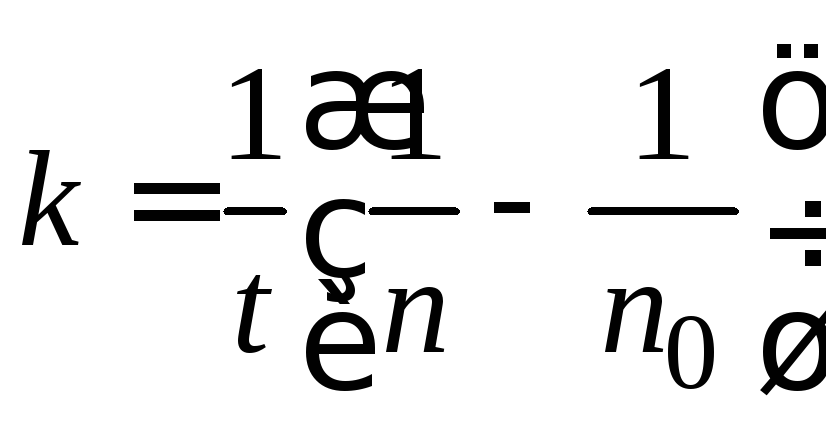 ; (5.2)
; (5.2)
 ;
(5.3)
;
(5.3)
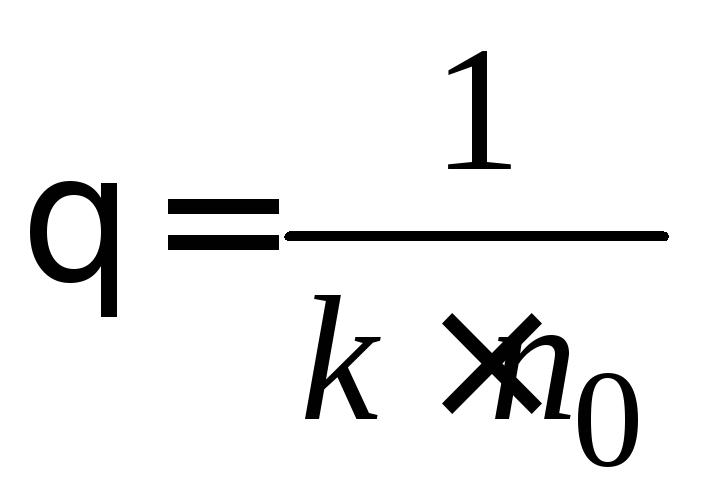 , (5.4)
, (5.4)
где
n0
– общее число частиц в единице объема
золя до коагуляции;
n
– число частиц к моменту времени t;
k
– константа скорости процесса коагуляции;
θ – временя половинной коагуляции,
время, в течение которого начальная
концентрация частиц уменьшится в два
раза
![]() .
.
|
Рис. 5.2. Взаимное притяжение частиц при d = 2r |
Теория быстрой коагуляции Смолуховского позволяет оценить критическое расстояние d, при котором становится возможным слипание двух дисперсных частиц. Рассмотрим самый простой случай – обе частицы представляют собой сферы одинакового радиуса r (рис. 5.2). |
Согласно теории Смолуховского, константа скорости коагуляции k зависит от интенсивности броуновского движения и определяется коэффициентом диффузии D и расстоянием между центрами дисперсных частиц d, на котором действуют силы притяжения между частицами:
![]() . (5.5)
. (5.5)
Подставим в уравнение (5.5) вместо коэффициента диффузии его значение из уравнения Эйнштейна:
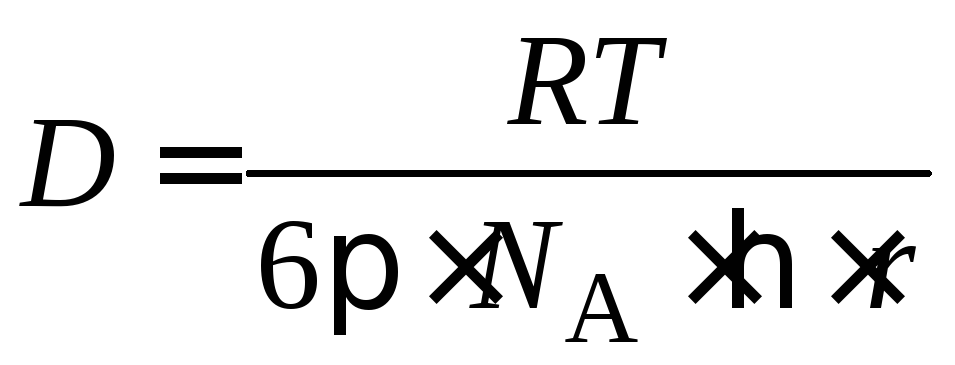 , (5.6)
, (5.6)
где
η –
вязкость дисперсионной среды; r
– радиус коагулирующих частиц;
![]() – число Авогадро;R
– универсальная газовая постоянная;
Т
– температура.
– число Авогадро;R
– универсальная газовая постоянная;
Т
– температура.
Константа скорости быстрой коагуляции k является постоянной для данной коллоидной системы и вычисляется по уравнению:
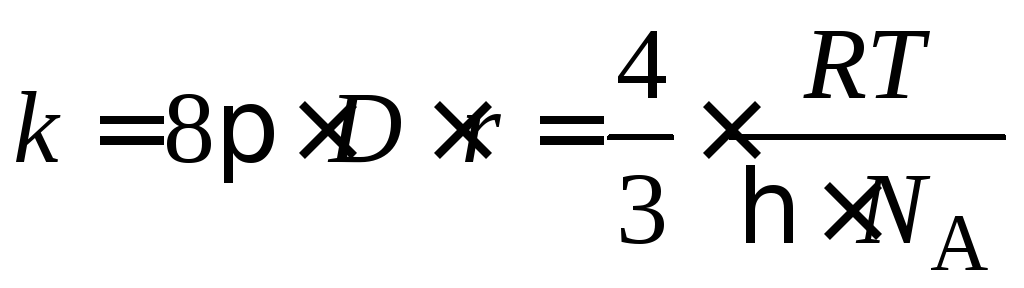 . (5.7)
. (5.7)
Тогда для времени половинной коагуляции уравнение примет вид:
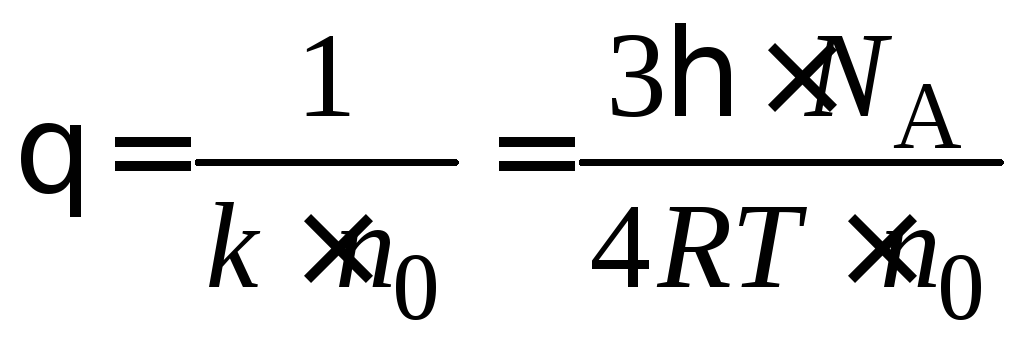 . (5.8)
. (5.8)
Из (5.7) следует, что величина константы скорости коагуляции не зависит от начальной концентрации золя и от размера частиц дисперсной фазы, k – постоянная только для данного золя, а зависит от температуры и вязкости дисперсионной среды. Вязкость жидкостей, как правило, уменьшается с повышением температуры, следовательно, константа скорости процесса коагуляции сильно зависит от температуры.
Время половинной коагуляции уменьшается с ростом концентрации дисперсной фазы. Таким образом, агрегативная устойчивость дисперсных систем увеличивается с возрастанием вязкости дисперсионной среды, понижением температуры и концентрации дисперсной фазы.
Если величина k, вычисленная из экспериментальных данных, не совпадает с величиной, полученной по уравнению (5.7) (kэксп<kтеор), то в системе протекает не быстрая, а медленная коагуляция.
Смолуховский предложил формулы, позволяющие определить, сколько частиц того или иного порядка (первичных, вторичных и т.д.) имеется в золе в момент времени t:
для общего числа частиц:
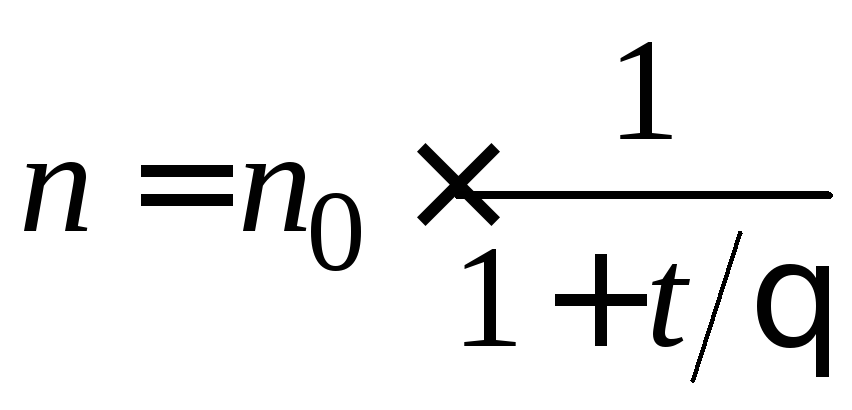 ; (5.9)
; (5.9)
для первичных частиц:
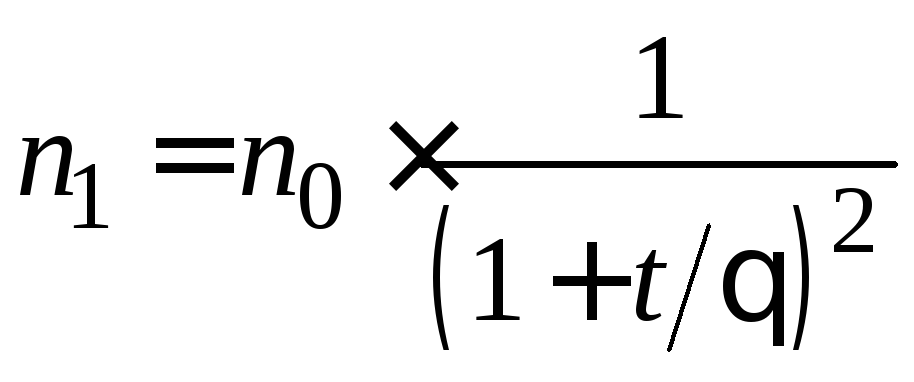 ; (5.10)
; (5.10)
для вторичных частиц:
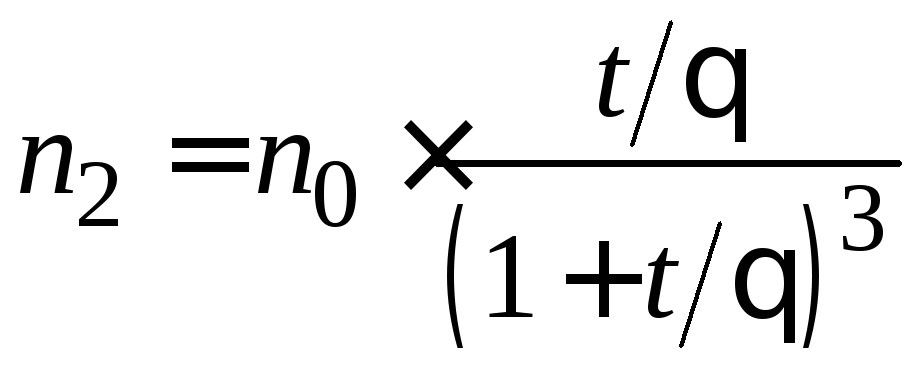 . (5.11)
. (5.11)
для частиц т-го порядка:
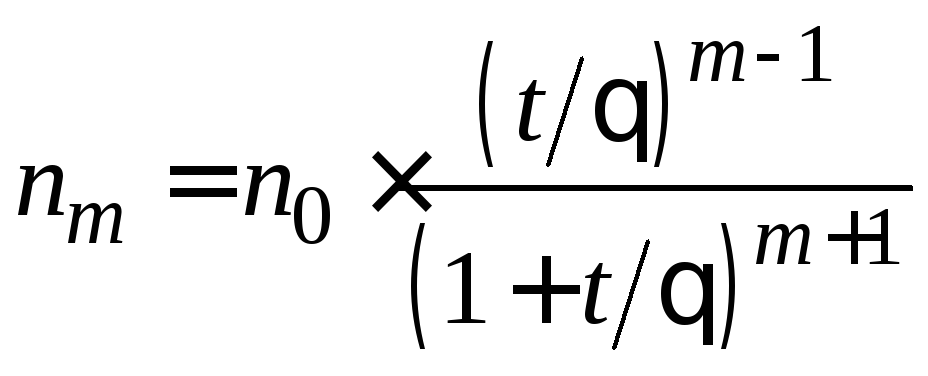 . (5.12)
. (5.12)
Графическая зависимость изменения числа частиц от времени коагуляции изображена на рис. 5.3.
|
Рис. 5.3. Изменение числа частиц во времени при быстрой коагуляции
|
Из рис. 5.3 видно, что функции распределения общего числа частиц n и частиц первого порядка n1 – монотонно убывающие, причем число первичных частиц n1 уменьшается быстрее, чем общее число частиц n, т.к. начинают появляться двойные, тройные и т.д. частицы. Для частиц высших порядков кривые проходят через максимум, высота которого уменьшается по мере увеличения размера частиц. |
Согласно теории Смолуховского, время половинной коагуляции не зависит от времени коагуляции. Чтобы проверить применимость теории по экспериментальным данным вычисляют θ для нескольких значений t по уравнению:
![]()
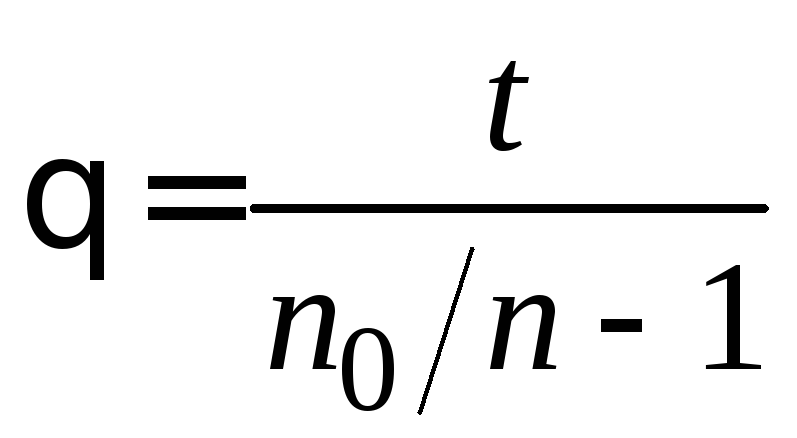 . (5.13)
. (5.13)
Если величина θ остается постоянной при различных значениях времени коагуляции, то в системе протекает быстрая коагуляция, для которой применима теория Смолуховского. Представления Смолуховского объясняют коагуляцию монодисперсных золей.
Представления Смолуховского объясняют коагуляцию монодисперсных золей. Теория коагуляции полидисперсных золей была разработана Мюллером. Мюллер показал, что частицы различных размеров коагулируются быстрее, чем частицы одинаковых размеров. При этом «большие» частицы играют роль центров коагуляции – коагуляция преимущественно происходит при столкновении малых частиц с большими. Таким образом, чем больше больших частиц, тем выше скорость коагуляции. Теория Мюллера объясняет автокаталитический характер коагуляции, скорость которой может постепенно возрастать со временем. Мюллер показал, что скорость коагуляции возрастает, если частицы имеют удлиненную форму. В этом случае на поступательное движение частиц дисперсной фазы накладывается еще и вращательное движение, увеличивающее вероятность столкновения частиц.
Пример 5.1. Во сколько раз уменьшится начальное число частиц n0 дыма мартеновских печей через 1, 10 и 100 с после начала коагуляции? Средний радиус частиц r = 2·10–8 м, массовая концентрация частиц в 1 м3 составляет 1·10–3 кг, плотность частиц ρ = 2,2·103 кг/м3. Константа скорости коагуляции k = 3·10–16 м3/с.
Решение:
1. Найдем объем дисперсной фазы:
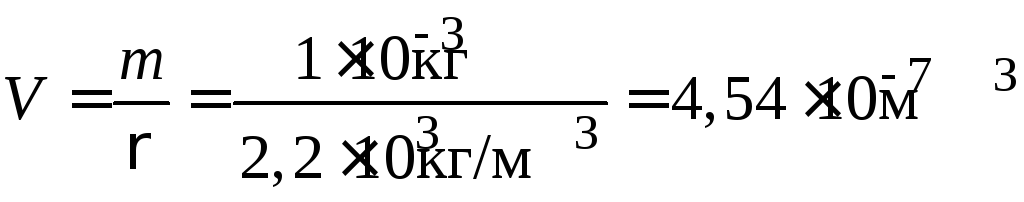 .
.
2. Вычислим объем одной частицы, предполагая, что частицы имеют форму шара:
![]() .
.
3. Вычислим начальное число частиц в 1 м3 до коагуляции:
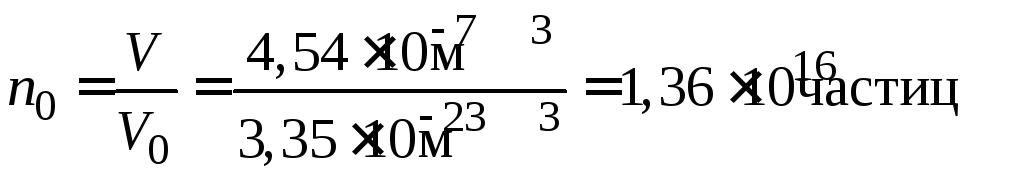 .
.
4. Из уравнения (5.3) следует, что общее число частиц n к моменту времени t равно:
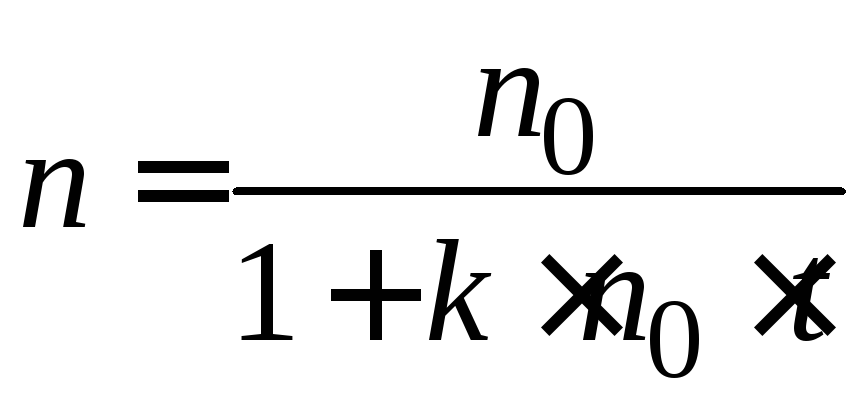 .
.
Отсюда,
начальное число частиц
![]() к моменту времениti
уменьшиться в
к моменту времениti
уменьшиться в
![]() раз:
раз:
![]() ;
;
![]() ;
;
![]() ;
;
![]() .
.
Начальное число частиц дыма мартеновских печей через 1 с уменьшится в 5 раз, через 10 с – в 42 раза, через 100 с – в 409 раз.
Пример
5.2. Начальное
число частиц золя
![]() составляет 5·108
частиц. Время половинной коагуляции θ
= 335 с.
Рассчитайте общее число частиц n
через: 100; 200; 250; 350 и 400 с после начала
коагуляции. Постройте график изменения
общего числа частиц от времени коагуляции
в координатах n = f(t).
составляет 5·108
частиц. Время половинной коагуляции θ
= 335 с.
Рассчитайте общее число частиц n
через: 100; 200; 250; 350 и 400 с после начала
коагуляции. Постройте график изменения
общего числа частиц от времени коагуляции
в координатах n = f(t).
Решение. Рассчитываем общее число частиц по уравнению (5.9):
 ;
;
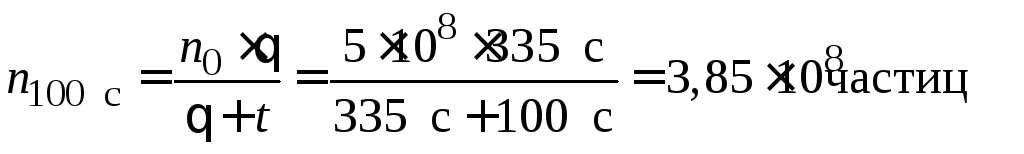 ;
;
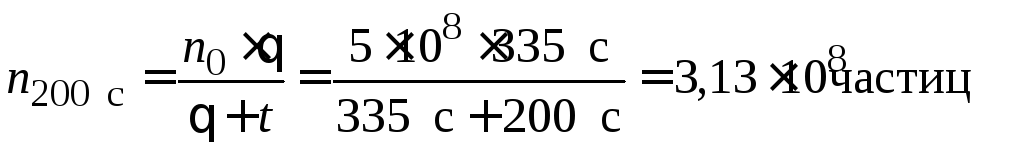 ;
;
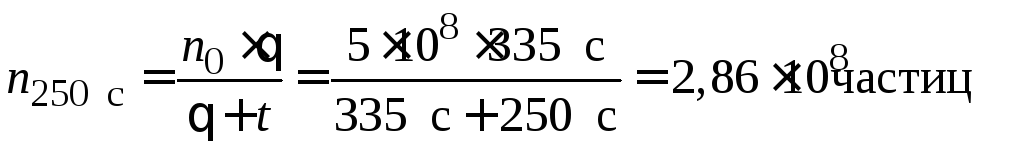 ;
;
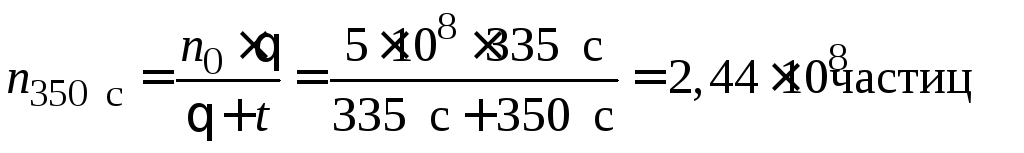 ;
;
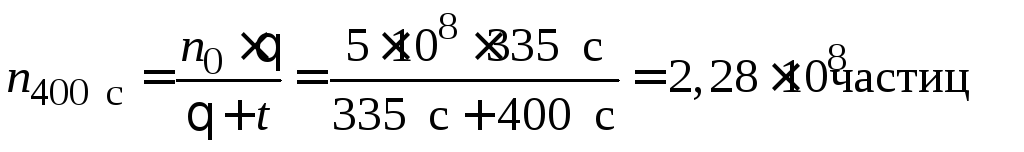
Построим график зависимости общего числа частиц от времени коагуляции в координатах n = f(t).
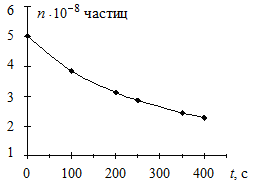
Рис. 5.4. Зависимость общего числа частиц от времени