
Мерзликин Н.В. Клиническая хирургия
.pdf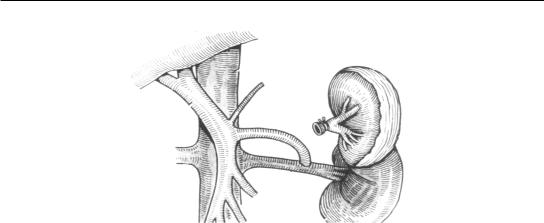
2. Хирургические заболевания печени и желчных путей
Рис. 128. Спленоренальный анастомоз
Из всех предложенных видов сосудистых анастомозов наибольшее признание полу- чил прямой порто-кавальный анастомоз, который некоторые хирурги считали классическим методом лечения портальной гипертензии. Преимущество порто-кавальных анастомозов перед другими видами операций доказывалось значительным снижением портального давления и исчезновением расширенных вен пищевода после наложения анастомоза.
С накоплением опыта и изучением отдаленных результатов были пересмотрены показания к применению порто-кавального анастомоза, а также подмечено, что при наложении порто-кавального анастомоза бок в бок наблюдается большой процент энцефалопатии и печеночной недостаточности с летальным исходом. Причина этого – ретроградный сброс крови из печени в анастомоз. В силу значительной разницы в сосудистом сопротивлении объем печеночного кровотока в этих условиях снижается, что и обусловливает прогрессирование печеночной недостаточности. Большинство хирургов стали применять анастомоз конец в бок. Со временем стало ясно, что и прямой порто-кавальный анастомоз, и центральный спленоренальный анастомоз не могут удовлетворить клиницистов в силу их отрицательного влияния на печень. Это обстоятельство послужило основанием к поискам новых вариантов анастомозов, не снижающих печеночного кровотока или заменяющих внутрипе- ченочный портальный кровоток артериальным.
В связи с этим представляют интерес предложения включения артериального кровотока в портальную систему печени (артериализация печени) при наложении порто-каваль- ного анастомоза. Было предложено артериализировать воротную вену у больных циррозом печени путем наложения анастомоза конец в бок между аортой и культей воротной вены (рис. 129). На сегодня предложено несколько вариантов артериализации печени: через селезеночную артерию (селезеночная артерия анастомозируется с умбиликальной веной конец в конец или накладывается анастомоз между селезеночной артерией и проксимальным концом воротной вены) и путем наложения анастомоза между подвздошной артерией и проксимальным концом воротной вены через аутотрансплантат из подкожной вены бедра.
Клинический опыт артериализации печени еще недостаточен и не позволяет высказать определенного мнения. Вопрос о важности мезентериальной или артериальной крови для ее функции и процессов регенерации остается открытым.
181
Клиническая хирургия
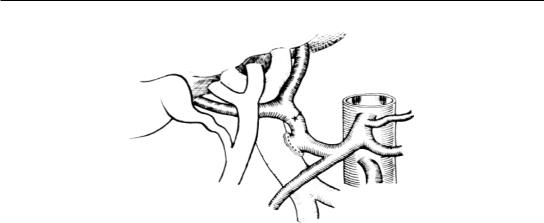
Рис. 129. Артериопортальный анастомоз
Неудовлетворенность прямыми порто-кавальными анастомозами ввиду их отрицательного влияния на печень привела к созданию новых вариантов анастомозов по принципу селективной декомпрессии с сохранением мезентериального притока к печени. Предложен метод локальной декомпрессии портальной системы путем наложения дистального спленоренального анастомоза в двух вариантах: спленоренальный анастомоз бок в бок с последующим пересечением проксимального конца селезеночной вены и пересечение селезеночной вены и вшивание дистального ее конца в бок почечной вены.
Операции, направленные на уменьшение притока крови в портальную систему (спленэктомия, перевязка артерий). В этой группе операций основное место занимает спленэктомия.
Считается, что увеличенная селезенка, обладая сократительной способностью, может вызвать динамическую портальную гипертензию с кровотечением из желудоч- но-кишечного тракта. Установлено влияние спленэктомии на ослабление или полное исчезновение аутоиммунной агрессии у больных циррозом печени. Однако показания к ее применению должны быть строго обоснованы в каждом конкретном случае.
Примерно в то же время, что и спленэктомия, была предложена перевязка селезеноч- ной артерии. Последняя позволяет разгрузить портальное кровообращение и выключить селезенку как патологическое депо крови, при этом сохраняются венозные пути для коллатерального оттока портальной крови через вены в сращениях вокруг селезенки. Перевязка селезеночной артерии, по мнению ведущих отечественных хирургов в области хирургии портальной гипертензии, заслуживает внимания не как самостоятельное вмешательство, а в сочетании с другими операциями. Она может быть применена в комбинации с оментопексией при циррозе печени, внепеченочной портальной гипертензии, в случаях массивного сращения селезенки с окружающими тканями и резко выраженной васкуляризации этих сращений, при перемещении селезенки в забрюшинное пространство и других операциях.
Операции, направленные на прекращение связи вен желудка и пищевода с венами портальной системы (резекция проксимального отдела желудка и пищевода, операция Таннера, перевязка вен желудка и пищевода и др.) предложены и в основном применяются для остановки кровотечения из варикозных вен пищевода.
182

2. Хирургические заболевания печени и желчных путей
Наиболее известной и распространенной операцией этого типа является операция Таннера, который предложил поперечно рассекать кардиальный отдел желудка с последующим сшиванием его. Автор считает, что этой операцией достигается полный разрыв между венами портальной системы и верхней полой веной. Независимо от Таннера М.А. Топчибашев применил рассечение стенки кардиального отдела до слизистой оболочки с прошиванием расширенных вен подслизистого слоя с последующим сшиванием стенки желудка. Наиболее радикальным средством разобщения вен пищевода и желудка является резекция нижней трети пищевода и верхней части желудка с наложением гастроэзофагоанастомоза.
Операции, направленные на усиление регенерации печени и внутрипеченочного артериального кровообращения (резекция печени, невротомия печеночной артерии, артерио-портальные анастомозы). В этой же группе операций заслуживает внимания денервация общей печеночной артерии (удаление адвентициальной пластинки). По мнению авторов операции, она дает хорошие результаты при хронических гепатитах. Соче- тание ее с перевязкой селезеночной артерией усиливает гипотензивный эффект.
В последние годы установлено, что применение частичной резекции цирротически измененной печени вызывает усиление регенерации паренхиматозных элементов и более интенсивное обратное развитие цирроза.
Трансплантация печени. Единственной на сегодня радикальной операцией при синдроме портальной гипертензии и циррозах печени является операция трансплантации пе- чени. Она считается одной из наиболее сложных в современной трасплантологии как в техническом плане, так и в плане реанимационно-анестезиологического обеспечения.
Изъятие органа производится только при работающем сердце после констатации смерти мозга донора. Печень пересаживается в ортотопической позиции. При заборе органа у донора печень удаляют вместе с участком нижней полой вены и почечной артерии, а также общим желчным протоком. При имплантации печени накладывают анастомозы между нижними полыми венами, печеночными артериями и воротными венами донора и реципиента, а также формируют холедохоеюноанастомоз.
Трансплантацию печени осуществляют после подбора донора по обычному алгоритму определения совместимости. После операции проводится обычная схема иммуносупрессии.
183

Клиническая хирургия
3. ХИРУРГИЧЕСКИЕ ЗАБОЛЕВАНИЯ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
3.1. Острый панкреатит
Острый панкреатит – это воспалительно-некротическое поражение поджелудочной железы в результате ферментативного аутолиза или самопереваривания.
Под острым панкреатитом понимают различные по этиологии деструктивные поражения поджелудочной железы вначале преимущественно аутолитического характера, к которым затем присоединяется воспаление. Эти поражения могут прогрессировать с развитием некроза, самостоятельно разрешаться, рецидивировать в пределах одного и того же патологического состояния. Острый панкреатит может быть самостоятельным заболеванием, а может быть осложнением других заболеваний и повреждений.
Острый панкреатит стоит на третьем месте среди острых хирургических патологий органов брюшной полости – острого аппендицита и острого холецистита.
Вопросы диагностики и лечения острого панкреатита являются одной из актуальных проблем хирургии. Это объясняется трудностями диагностики, свое-образным клиническим течением, опасностью развития смертельных осложнений, а также разногласиями в показаниях и методике оперативного лечения. В последнее время отмечено несомненное учащение заболеваемости острым панкреатитом, особенно среди лиц молодого возраста, что связано в первую очередь с приемом алкоголя.
Этиология. Острый панкреатит как самостоятельное заболевание является полиэтиологическим, но монопатогенетическим заболеванием. Любая причина, вызывающая гиперсекрецию панкреатического сока и затруднение его оттока (развитие гипертензии в панкреатических протоках, заброс в протоки цитотоксических и активирующих панкреатические ферменты веществ, прямое повреждение секретирующих панкреацитов), может привести к развитию острого панкреатита. Существует несколько теорий возникновения острого панкреатита: теория общего канала, обтурационная, алиментарная, сосудистая, интоксикации, аллергическая и другие.
Рассмотрим наиболее значимые этиологические факторы острого панкреатита.
1. Заболевания желчных путей. Одним из ведущих этиологических факторов острого панкреатита, в том числе и деструктивного, признаны заболевания желчных путей (рис. 130). Возможность развития некротического панкреатита на почве рефлюкса инфицированной желчи в протоки поджелудочной железы при обтурации большого сосочка двенадцатиперстной кишки была доказана еще в 1901 г. E. Opie. Это наблюдение послужило краеугольным камнем для построения теории общего канала, когда совместное впадение общего желчного и панкреатического протоков в ампулу фатерова соска создает условия для затекания желчи в протоки поджелудочной железы и развития острого панкреатита при
184
3. Хирургические заболевания поджелудочной железы
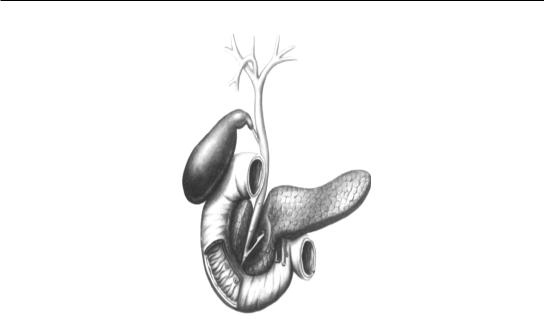
Рис. 130. Билиарно-панкреатическая система
наличии препятствия в зоне большого дуоденального сосочка. В норме давление в протоке поджелудочной железы (1,1–2,45 кПа) выше, чем в общем желчном протоке (0,98–1,37 кПа), что предупреждает попадание в него желчи.
Исследованиями многих авторов установлено, что анатомические отношения, создающие условия для билиарно-панкреатического рефлюкса, могут быть выявлены у 65–80% больных, однако камни, ущемленные в большом дуоденальном сосочке, выявляются только у 3–5% больных, оперируемых по поводу острого панкреатита. При этом следует учитывать, что помимо стойкой непроходимости БДС, камни желчных путей могут вызывать и преходящую, рецидивирующую блокаду сосочка, приводящую к длительному спазму сфинктера Одди и в условиях общего канала к развитию острого панкреатита.
К числу факторов, способствующих развитию описанного выше механизма, могут быть отнесены множественные мелкие камни желчного пузыря в сочетании с нали- чием расширенного пузырного протока.
В последние годы все большее внимание привлекает развитие микрохоледохолитиаза в патогенезе папиллоспазма, палиллостеноза и вторичного панкреатита. Микролиты не обнаруживаются при операции ни пальпаторно, ни проведением рентгеноконтрастных исследований, однако их можно обнаружить при анализе кала у лиц, перенесших приступ острого панкреатита.
Так, Neoptolemos (1989) сформулировал теорию персистирующего холедохолитиаза в развитии панкреатита. Автор выделяет две фазы развития патологического процесса: в первой фазе микролиты постоянно раздражают ампулу фатерового сосочка, что вызывает спазм сфинктера Одди и рефлюкс желчи в протоки поджелудочной железы, а это, в свою очередь, ведет к ее отеку; во второй фазе более крупные камни блокируют отток активизированного панкреатического секрета, что приводит к развитию панкреонекроза.
185

Клиническая хирургия
2. Заболевания желудочно-кишечного тракта. Вторичное поражение поджелудочной железы наиболее характерно для заболеваний двенадцатиперстной кишки. Основным механизмом включения железы в патологический процесс является проникновение в панкреатические протоки кишечного содержимого, которое активирует протео- и липолитические ферменты поджелудочной железы.
Рефлюкс дуоденального содержимого в панкреатические протоки обычно реализуется при наличии ряда условий, в частности при повышении давления в просвете двенадцатиперстной кишки и нарушении эвакуации из нее. Однако одного повышения давления в двенадцатиперстной кишке для возникновения рефлюксного панкреатита недостаточно, поскольку имеется ряд механизмов, предохраняющих попадание кишеч- ного содержимого в протоки поджелудочной железы. К их числу относят замыкающую функцию печеночно-поджелудочной ампулы, наличие складки слизистой оболочки в трансмуральном участке главного панкреатического протока, значительный градиент давления между системой панкреатических протоков и двенадцатиперстной кишкой.
Панкреатит, связанный с рефлюксом содержимого двенадцатиперстной кишки, может возникнуть при наличии недостаточности БДС (гипотония сфинктера) и дуоденостазе (хроническая дуоденальная непроходимость, вызванная механическими нарушениями или функциональными поражениями двенадцатиперстной кишки).
К числу механических факторов, приводящих к развитию дуоденостаза, могут быть отнесены кольцевидная поджелудочная железа, стенозирующие опухоли, рубцовые изменения и сдавление двенадцатиперстной кишки в зоне двенадцатиперстно-то- щего перехода брыжеечными сосудами (артериомезентериальная непроходимость). Органический дуоденостаз может быть проявлением синдрома приводящей петли после резекций желудка по Бильроту-2.
Значение потери функции сфинктерного аппарата большого дуоденального сосочка в условиях дуоденального стаза наглядно проявляется у больных, у которых в условиях дуоденального стаза производят операцию папиллосфинктеротомии или наложения холедоходуоденоанастомоза. Дуоденальное содержимое беспрепятственно проникает в протоковую систему поджелудочной железы, желчные пути и вызывает развитие острого панкреатита, холангита.
Среди заболеваний двенадцатиперстной кишки существенная роль в развитии панкреатита принадлежит околососочковым дивертикулам. При впадении главного панкреати- ческого и желчного протоков в полость дивертикула могут возникать спазм и атония сфинктера Одди и нарушение оттока панкреатического секрета на почве дивертикулита.
Воспаление поджелудочной железы также может быть связано с осложнениями язвенной болезни желудка и двенадцатиперсной кишки, особенно с возможностью пенетрации язвы задней стенки желудка в поджелудочную железу.
3. Алкоголизм и нарушения питания. Алкоголизм может вызывать развитие как острого, так и хронического панкреатита. Механизм действия алкоголя на поджелудоч- ную железу до конца не выяснен. Принято считать, что он не оказывает прямого цитотоксического влияния на поджелудочную железу, что действует он опосредованно и при этом обладает выраженным стимулирующим фактором гиперсекреции.
186

3. Хирургические заболевания поджелудочной железы
Для стимуляции секреции не обязателен прием алкоголя через рот, такое же действие оказывает спирт, введенный внутривенно. Наиболее распространено представление о том, что в патогенезе алкогольного панкреатита имеют значение два фактора: чрезмерная стимуляция алкоголем внешнесекреторной функции поджелудочной железы и задержка оттока ее секрета с повышением внутрипротокового давления.
Первый обусловлен раздражением спиртом слизистой двенадцатиперстной кишки, что приводит к повышенной продукции стимуляторов панкреатической и желудочной секреции – секретина, панкреозимина, гистамина и гастрина. В то же время воздействие алкоголя на стенки желудка стимулирует образование соляной кислоты, которая в свою очередь стимулирует выделение секретина.
Второй фактор – нарушение эвакуации панкреатического секрета – обусловлен прежде всегорефлекторнымспазмомсфинктераОддивответнараздражениеслизистойдвенадцатиперстной кишки, следствием чего является повышение интрапанкреатического давления.
К факторам, способствующим поражению поджелудочной железы, следует также отнести гиперкалорийное питание, богатое жирами и белками. При систематическом употреблении алкогольных напитков и обильном питании происходит накопление липидов в ацинарных клетках с последующим нарушением структуры этих клеток, их дегенерацией, атрофией и развитием фиброза.
4.Травма и операция. Проникающие, закрытые и интраоперационные ранения поджелудочной железы и ее протоков различного калибра часто осложняются развитием острого панкреатита.
Травма поджелудочной железы относится к числу тяжелых и трудных для диагностики и лечения повреждений, сопровождающихся довольно высокой летальностью
èвысоким риском развития осложнений не только в раннем, но и в отдаленном послеоперационном периоде. Одной из причин этого является за-брюшинное расположение органа и тесный контакт его с анатомически важными образованиями. Травма головки наиболее часто сопровождается сочетанными повреждениями двенадцатиперстной кишки, общего желчного протока, БДС.
5.Нарушения кровообращения. Острые и хронические нарушения кровообращения с расстройствами микроциркуляции на фоне гипертонического криза, артериальной гипертензии, при циркуляторных шоках различного происхождения, атеросклеротической окклюзии чревного ствола, тромбозе и эмболии сосудов приводят к развитию ишемического острого панкреатита.
6.Заболевания самой поджелудочной железы. Особое внимание следует обратить на развитие острого панкреатита на фоне развития непроходимости панкреатического протока, вызванного хроническим панкреатитом, а также сдавлением панкреатического протока опухолями. У пациентов со злокачественными опухолями могут также наблюдаться метастазы в поджелудочную железу.
7.Посттрансплантационные и постперфузионные острые панкреатиты. Данный особый вид панкреатита развивается после операций на сердце в условиях искусственного кровообращения, а также после трансплантации сердца и различных паренхиматозных органов. Механизм развития подобных осложнений пока плохо изучен.
187

Клиническая хирургия
8. Окклюзионный острый панкреатит развивается после пломбировки протоков поджелудочной железы с лечебной целью, острый панкреатит может также развиться после различных инвазивных методов исследований поджелудочной железы (выполнение ЭРХПГ).
Патогенез. Основной теорией патогенеза острого панкреатита является ферментативная. Доказательством этой теории служит экспериментальное получение острого панкреатита введением ферментов поджелудочной железы как в протоки, так и в ткань железы. Возникают изменения, свойственные острому панкреатиту, в виде серозного, а затем геморрагического отека межуточной ткани, некроза паренхимы, жирового некроза и лейкоцитарной инфильтрации.
В зависимости от места введения ферментов (внутрь протоков, в ткань железы, в забрюшинную клетчатку или внутрибрюшинно) патологические изменения возникают не только в самой железе в виде очаговых или распространенных изменений, но и в брюшине, в забрюшинной клетчатке, печени и других системах и органах. Тяжесть этих изменений находится в прямой зависимости от характера и количества введенного субстрата.
Экспериментальные исследования подтверждают реальность ферментативной теории патогенеза острого панкреатита, поскольку отмечается резкое повышение активности ферментов поджелудочной железы в крови, моче, лимфе грудного лимфати- ческого протока в ранние сроки заболевания. Источником повышения активности панкреатических ферментов в различных жидкостях организма является сама пораженная поджелудочная железа, а путями распространения активизированных ферментов в кровяное русло – лимфатические сосуды, воротная вена и портокавальные анастомозы.
Активизация собственных ферментов в поджелудочной железе (трипсин, калликреин, эластаза, липаза, фосфолипаза и др.) начинается с выделения из поврежденных клеток железы цитокиназы. Под действием цитокиназы трипсиноген переходит в трипсин. Под влиянием трипсина из различных клеток освобождается серотонин. Активизированный трипсином панкреатический калликреин действует на кининоген, создает высокоактивный пептид, который способен быстро превращаться в брадикинин. Брадикинин может образовываться и непосредственно из кининогена. Таким образом, возникает целая группа биологически активных веществ (трипсин, калликреин, кинины, гистамин, серотонин и др.). При остром панкреатите самыми ранними и типичными изменениями являются повреждения сосудов и нарушение кровотока на уровне микроваскулярного русла, связанные с действием вазоактивных веществ. При этом происходят изменения просвета сосудов, проницаемости сосудистой стенки и характера кровотока, особенно капиллярного.
По данным электронной микроскопии прежде всего подвергается воздействию эндотелиальная выстилка внутренней оболочки сосудов, а позднее страдают и другие слои стенки сосудов, что приводит к резкому повышению проницаемости сосудистой стенки и паралитическому состоянию сосудов.
Существенные нарушения микрогемоциркуляции возникают и в других органах (печень, почки и др.), но несколько позднее.
Повреждение эндотелия, резкое замедление кровотока, вплоть до полного стаза, и повышение свертывающей функции крови служат причиной раннего образования тром-
188

3. Хирургические заболевания поджелудочной железы
бов прежде всего в мелких венозных сосудах. Гистологические исследования показали, что тромбоз мелких сосудов поджелудочной железы обнаруживается у 50,7% больных, погибших в первые 7 дней заболевания.
Âусловиях нарушенного местного кровообращения, изменения тканевого метаболизма возникают очаги некроза паренхимы поджелудочной железы. Этому способствует тромбообразование в сосудах, которое наиболее характерно для геморрагических форм панкреатита.
По мере последующей гибели клеток паренхимы железы появляется все большее количество активных ферментов, которые вызывают еще большее нарушение кровообращения в железе и появление новых очагов омертвения ацинарной ткани. Гибнет не только паренхима (железистая ткань) поджелудочной железы, но и жировая ткань. Возникают паренхиматозный и жировой некрозы.
Паренхиматозный некроз, т.е. некроз ацинозных клеток, по своему происхождению является ишемическим и связан с действием протеолитических ферментов (эластаза и др.) и целой группы биологически активных веществ (калликреин, кинин, гистамин, серотонин, плазмин и др.), которые образуются под их влиянием. Этот вид некроза относится к разделу колликвационного и сопровождается относительно слабой перифокальной лейкоцитарной реакцией. Мертвые ткани паренхимы железы обладают свойством быстро расплавляться, образуя гноевидную серую массу с большим содержанием протеолитических ферментов, а также рассасываться и вызывать явления выраженной интоксикации.
Жировой некроз вызывается непосредственным действием на жировую ткань железы липолитических ферментов (липазы, фосфолипазы) и в наибольшей степени развивается в условиях лимфостаза, который по мере развития панкреатита нарастает. Жировой некроз относится к разделу сухого (коагуляционного). Он вызывает резко выраженную перифокальную лейкоцитарную реакцию, отчего объем и плотность железы при распространенных очагах стеатонекроза увеличиваются. Ткани, подвергшиеся жировому некрозу, в асептических условиях не расплавляются и не служат источником интоксикации, но при наличии большой массы протеолитических ферментов (тканевых
èмикробных) легко секвестрируются.
Âклинической практике обычно встречаются смешанные виды некроза, но чаще с преобладанием того или другого. При выраженных геморрагических панкреатитах в железе более выражен паренхиматозный, а при рецидивирующих формах и липоматозе поджелудочной железы – жировой некроз.
Помимо вышеперечисленных некрозов, можно выделить некрозы асептические и инфицированные. При остром панкреатите значительно чаще встречаются асептические виды некроза, которые относительно легко инфицируются.
Для острого панкреатита характерно фазовое развитие местного патологического процесса. При прогрессирующих формах панкреатита первоначальная фаза серозного, а затем геморрагического отека сменяется фазой паренхиматозного и жирового некроза, после чего наступает фаза расплавления и секвестрации омертвевших участков поджелудоч- ной железы и забрюшинной клетчатки.
189

Клиническая хирургия
Таким образом, эти три фазы и создают три периода развития болезни. Если периоду высокой гиперферментемии соответствуют распространенные сосудистые изменения в поджелудочной железе и других органах и анатомических образованиях (сальник, брюшина, печень, почки, тонкая и толстая кишка и др.), то во время нормализации активности панкреатических ферментов в крови характерным для острого панкреатита, по данным В.И-
. Филина, является реактивное воспаление (второй период), за которым следует репаративный процесс (третий период).
Традиционное представление об остром панкреатите как об изолированном поражении поджелудочной железы следует считать глубоко ошибочным. При остром некротическом панкреатите выраженные патологические изменения возникают не только в самой поджелудочной железе (собственно панкреатит), но и в забрюшинной клетчатке вокруг железы (парапанкреатит), сальниковой сумке (оментобурсит), брюшине (перитонит), сальнике (оментит) и в других образованиях (брыжейка тонкой кашки, круглая связка печени, пече- ночно-дуоденальная связка и др.). Такое распространение патологического процесса в брюшной полости и забрюшинном пространстве обусловлено действием ферментов поджелудочной железы и других биологически активных веществ.
При распространении гнойного парапанкреатита поражается вся левая или правая половина забрюшинного пространства с захватом даже тазовой забрюшинной клетчатки. Наиболее характерной чертой гнойного поражения забрюшинной клетчатки является очень большая частота секвестрации некротических очагов.
Под оментобурситом понимают воспаление брюшины, выстилающей стенки сальниковой сумки.
У больных острым панкреатитом могут развиваться три вида перитонита: ферментативный, асцит-перитонит, гнойный перитонит. У тучных людей массивные жировые некрозы большого сальника приводят к возникновению инфильтративно-некроти- ческого и гнойно-некротического оментита, а сальниковых отростков и связок – эпиплоита и лигаментита.
О распространенном характере поражения в брюшной полости при остром панкреатите свидетельствует обнаружение очагов жирового некроза в брыжейках тонкой и толстой кишки, сальнике, забрюшинной клетчатке боковых каналов.
При тяжелых формах геморрагического панкреатита в связи с генерализованным воздействием на сосудистое русло биологически активных веществ очень быстро возникают значительные расстройства кровообращения на всех уровнях – тканевом, органном и системном. Циркуляторные расстройства во внутренних органах (легкие, сердце, печень, почки и др.) приводят к дистрофическим, некробиотическим и даже явным некротическим изменениям, после чего возникает вторичное воспаление.
При остром панкреатите значительная экссудация в ткани и полости, многократная рвота, глубокиефункциональныеизменениявовнутреннихорганахявляютсяпричинамивыраженных обменныхнарушений.Притяжелыхформахболезнистрадаютвсевидыобмена:водно-электро- литный, углеводный, белковый, жировой.
Нарушение электролитного состава крови характерно для тяжелых форм панкреатита, выраженность его определяется временем от начала заболевания. При геморра-
190
