
Мерзликин Н.В. Клиническая хирургия
.pdf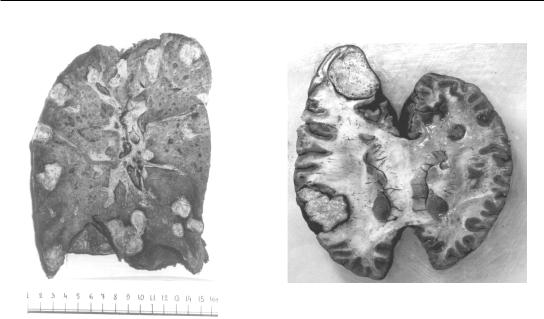
2. Хирургические заболевания печени и желчных путей
Рис. 89. Метастазы альвеококка в легкие |
Рис. 90. Метастазы альвеококка в мозг |
стазы) делают альвеококкоз похожим по своему течению и характеру поражения на злокачественные опухоли печени. Разница только во времени. Альвеококковый паразитарный узел растет значительно медленнее ракового узла.
Поскольку паразитарная опухоль альвеококка питается за счет питательных веществ хозяина, на периферии паразитарного узла царит бурная жизнь – быстрый рост и размножение паразитарных пузырьков. В центре же из-за недостатка питания часть паразитарных элементов альвеококка погибает и разлагается, образуя полость – паразитарную каверну, достигающую порой значительных размеров. В ряде случаев, когда паразитарная каверна достаточно велика и близко подходит к краям паразитарной опухоли, под влиянием незна- чительной травмы может произойти ее прорыв в соседние полости. Известны прорывы полостей распада в брюшную, грудную полости, в полость перикарда и в бронхиальное дерево. Это заканчивается гибелью больного от осложнений заболевания.
Распространение альвеококкоза в мире достаточно ограничено. Он встречается в Тироле и Баварии (ФРГ), на юге Франции в области Юрских гор, на Аляске, острове Ребун и севере Японии (о. Хоккайдо); на территории бывшего СССР – в Закавказье (Армения, Азербайджан), Киргизии (область Кочкорской котловины), Башкирии, в Западной Сибири, Кировской области, на Чукотке, Камчатке и в Якутии. Наибольшее число больных (до 1000 человек) зарегистрировано в Якутии, где в 70-е гг. ХХ в. заболеваемость достигала 11 на 1000 населения в год.
Классификация альвеококкоза предложена Б.И. Альперовичем (1967), который различает альвеококкоз печени и внепеченочные локализации альвеококка. Последние являются крайней редкостью и практического значения почти не имеют.
Клинически альвеококкоз печени разделяют на следующие стадии: 1) бессимптомную;
121

Клиническая хирургия
2)неосложненного течения;
3)осложнений, среди которых различают:
–прорастание в соседние органы (диафрагму, почки, поджелудочную железу и т.д.);
–портальную гипертензию;
–механическую желтуху;
–желчно-бронхиальные свищи;
–метастазы в легкие и головной мозг;
–прорывы полостей распада в брюшную, плевральную полости, перикард;
–типичные формы-маски (от прорастания в желудок и др.).
Клиническое течение и проявление альвеококкоза зависит в первую очередь от стадии процесса и характера патологоанатомических изменений.
При бессимптомной стадии паразитарный узел в печени практически ничем себя не проявляет, за исключением незначительных признаков сенсибилизации организма за счет начинающейся аллергизации, выраженной особенно у детей: крапивница, кожный зуд, зуд кончика носа. В крови в это время может развиться эозинофилия. Узел, располагающийся чаще всего в IV сегменте печени, может быть выявлен при тщательной пальпации, профилактическом осмотре или при ультразвуковом исследовании.
На стадии неосложненного течения появляются выраженные клинические проявления заболевания. Больные жалуются на чувство тяжести в правом подреберье, тупые боли в эпигастрии и незначительные диспепсические явления. При осмотре, особенно у детей, можно выявить деформацию грудной клетки («эхинококковый горб»), но этот симптом встречается достаточно редко. Важным патогномоничным симптомом альвеококкоза является обнаружение в зоне печени каменистой плотности «опухоли», смещаемой при дыхании, слегка болезненной при пальпации. Этот важный симптом описан Н.М. Любимовым (1899), а важность его обнаружения при альвеококкозе под- черкивал томский профессор В.М. Мыш. На этой стадии отмечаются изменения лабораторных данных, иммунологических реакций. Специальное исследование позволяет уточнить диагноз.
При осложненной форме заболевания к местным симптоиаи – каменистой плотности опухоли в печени или флюктуации в центре ее – присоединяется ряд проявлений этих осложнений, нередко маскирующих картину основного заболевания. Так, при прорастании или сдавлении ворот печени у больного развивается механическая желтуха (желтушное окрашивание склер и слизистых, обесцвеченный кал, темная моча, повышение билирубина сыворотки крови) или портальная гипертензия (асцит, пищеводные и прямокишечные кровотечения, «корона Медузы» – расширение вен брюшной стенки). Образование паразитарных каверн большого размера при их инфицировании протекает как гнойник в печени. Прорыв паразитарных каверн в брюшную полость клини- чески проявляется как вялотекущий перитонит, прорыв в плевральную полость – как плеврит, в полость перикарда – как перикардит, прорыв полости распада в бронхиальное дерево клинически проявляется симптомами желчно-бронхиального свища (отделение большого количества мокроты желчного характера, усиление отделения желчной мокроты после приемов пищи и в положении лежа, прогрессирующее истощение).
122

2. Хирургические заболевания печени и желчных путей
Диагностика. Результаты лабораторных исследований при альвеококкозе достаточно характерны для очаговых поражений печени: ускорение СОЭ, изменение белковых фракций (уменьшение альбуминов плазмы, увеличение гамма-глобулинов); при осложнениях и нарушениях функции печени – возрастание трансаминаз (АЛТ и АСТ) и увеличение уровня билирубина сыворотки как прямой, так и непрямой его фракций.
Реакция Казони с эхинококковым антигеном положительна в 90% случаев, поскольку альвеококк по своим биологическим и антигенным свойствам достаточно близок к эхинококку. Разведение антигена для реакции Казони увеличивает достоверность исследования (Альперович, 1967). Применяются и другие иммунологические реакции, которые мы считаем необязательными и не всегда информативными.
Диагностика альвеококкоза достаточно легка при условии знания врачом эпидемиологических данных и клиники заболевания. Проживание в определенной местности, общение по роду деятельности с дикими животными и клинически определяемая каменистой плотности «опухоль» в печени (симптом Любимова) позволяют достоверно поставить диагноз, а специальные методы исследования – точно его верифицировать.
Наиболее ценным инструментальным методом диагностики является ультразвуковое исследование (Ярошкина, 1992). Оно позволяет увидеть плотное эхонегативное образование с неровными контурами в толще долей печени, отвечающее контурам паразитарного узла, или обнаружить паразитарную каверну в толще узла с толстыми неровными стенками. С помощью этого метода можно не только выявить характер поражения печени, но и определить его топографию и взаимоотношения с элементами ворот органа и нижней полой веной, что определяет объем и характер предстоящей операции (рис. 91).
При лапароскопии в случаях, когда паразитарный узел выходит на поверхность печени в доступных осмотру зонах, можно визуально определить характер процесса и даже взять биопсию для гистологического уточнения диагноза. Метод достаточно информативен, но не позволяет установить размеры распространения опухоли в толще печени и ее операбельность, поскольку величина паразитарной опухоли на деле всегда превосходит определяемую при лапароскопическом исследовании (рис. 92).
Реогепатография (изучение печеночного кровотока) выявляет наличие ослабленного кровотока в зоне паразитарного узла.
Рентгеновское исследование дает большой материал для диагностики альвеококкоза. Еще в 1930-е гг. рентгенологи Fridrich и Л.Б. Линденбратен отметили, что при альвеококкозе имеется важный рентгенологический симптом – участки очажков обызвествления в тени печени в виде известковых брызг. Это визуализированные обызвествленные пузырьки паразита, которые погибли во время развития последнего. По данным Б.И. Альперовича, этот симптом наблюдается примерно в 50% случаев. Снимок должен быть мягким и достаточно качественным (рис. 93).
Контрастирование системы воротной вены с помощью спленопортографии или трансумбиликальной портогепатографии при неосложненном альвеококкозе позволяет определить дефект наполнения в зоне паразитарного узла. Сосуды воротной системы огибают паразитарную «опухоль», а мелкие ветви в зоне паразитарного узла отсутствуют (рис. 94).
123
Клиническая хирургия
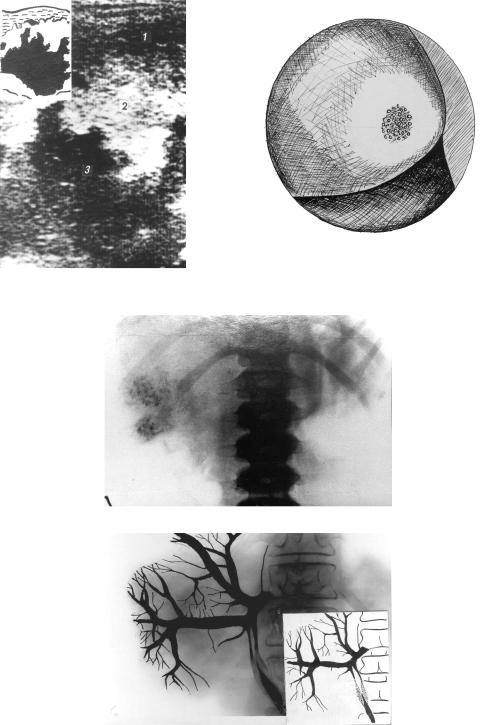
Рис. 91. УЗИ. Полость распада |
Рис. 92. Лапароскопия. |
|
Узел альвеококка в печени |
Рис. 93. Гепатограмма. Известковые брызги
Рис. 94. Портогепатограмма при альвеококкозе
124

2. Хирургические заболевания печени и желчных путей
При осложненном альвеококкозе, когда в процесс вовлекаются крупные ветви воротной вены или основной ее ствол, данная картина четко прослеживается на портогепатограммах.
При артериальной ангиографии печени удается отметить уменьшение сосудистого рисунка в зоне паразитарного узла, выпрямленность артерий и ампутацию мелких ветвей в зоне их поражения.
При компьютерной томографии (КТ) и спиральной компьютерной томографии в зоне печени можно выявить очаговую тень соответственно контурам паразитарного узла и при серийных срезах диагностировать наличие паразитарной каверны в толще узла. Установить взаимоотношения узла с элементами ворот печени удается только при ангиографическом исследовании или ультразвуковом сканировании при условии высокой квалификации исследователя.
Лечение альвеококкоза на сегодня достаточно хорошо разработано в основном за счет исследований отечественных ученых – И.Л. Брегадзе, его школы, Б.И. Альперовича и Ю.М. Дедерера. Эффективного лекарственного средства для лечения альвеококкоза в настоящее время не существует. Попытки рентгенотерапии также не увенчались успехом. Только хирургическое лечение, в ряде случаев дополненное другими методами, позволяет излечить больного или существенно облегчить его состояние.
Â1896 г. Bruns успешно произвел операцию резекции печени при альвеококкозе и удалил паразитарную опухоль вместе с участком печени. Аналогичную операцию впервые
âРоссии успешно осуществил томский профессор В.М. Мыш. В 1912 г. он прооперировал гимназистку 14 лет. Это была первая в мире успешная резекция печени у ребенка.
Â1894 г. А.А. Бобров оперировал врача из Якутии по поводу альвеококкоза. Во время операции была вскрыта паразитарная каверна, стенки которой оператор подшил к краям раны. Впоследствии он неоднократно выскабливал паразитарную ткань через рану и в конце концов добился почти полного излечения больного. Это была первая паллиативная операция альвеококкоза в мировой практике. К настоящему времени в мире сделано более тысячи таких операций. Более половины из них выполнил Б.И. Альперович.
Все хирургические вмешательства при альвеококкозе делятся на две группы: радикальные и паллиативные.
Наиболее радикальным вмешательством является резекция печени, которая осуществляется так же, как при злокачественной опухоли, в пределах здоровых тканей органа. Эта операция приносит больному полное излечение и восстановление трудоспособности. Самой успешной из существующих методик является методика резекции печени Б.И. Альперовича. Профессор Альперович произвел самое большое в мировой практике количество резекций печени по поводу альвеококкоза, причем с минимальной смертностью (рис. 95). К сожалению, резекция печени при этом заболевании возможна только в 25–30% случаев, поскольку оно протекает с малыми клиническими проявлениями и больные обращаются к врачу обычно в осложненной стадии болезни, когда резекция неосуществима или чрезвы- чайно рискованна. В этом случае приходится прибегать к паллиативным операциям.
Среди паллиативных операций наиболее «радикальной» является паллиативная резекция печени. По общим правилам производится резекция участка печени с парази-
125
Клиническая хирургия
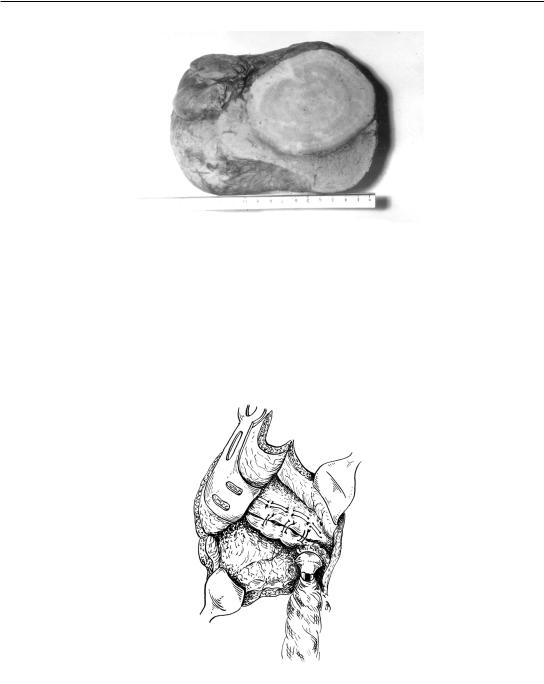
Рис. 95. Резекция печени при альвеококкозе. Препарат
тарным узлом. Небольшая пластинка паразитарной ткани на воротах печени или на стенке нижней полой вены оставляется. Поскольку альвеококкоз – не рак, данная операция достаточно эффективна, особенно если на оставшиеся участки паразитарной ткани воздействовать паразитоцидными веществами – спиртом, трипафлавином или сверхнизкими температурами, которые губят паразитарную ткань. Эта операция как по непосредственным, так и отдаленным результатам приближается к радикальному вмешательству – резекции печени (рис. 96).
Рис. 96. Схема паллиативной резекции печени с криодеструкцией
При наличии неоперабельного процесса – очень большой паразитарной опухоли с большой полостью распада и поражением ворот печени, – следует прибегнуть к такой паллиативной операции, как марсупиализация паразитарной каверны. После лапаротомии пос-
126

2. Хирургические заболевания печени и желчных путей
ледняя вскрывается. Из нее удаляют гной и секвестры (участки омертвевшей ткани паразита). Часть стенок полости иссекается, а края оставшейся полости подшивают к краям раны брюшной стенки. Рана тампонируется, при этом за счет инфицирования часть паразитарной ткани омертвевает и отторгается. Заживает рана вторичным натяжением; возможно воздействие на ткань паразита химическими веществами, а еще лучше – сверхнизкими температурами с целью вызвать гибель паразита и его отторжение в рану.
При очень большой неоперабельной паразитарной опухоли без распада возможно частичное удаление паразитарной ткани – кускование паразита с целью его частичного удаления и создания условий для дальнейшего лечения через рану (когда края созданной полости подшиты к краям раны). Последняя операция наименее перспективна, но иногда применяется с целью хоть как-то помочь больному. При механической желтухе возможно осуществление желчеотводящей операции для облегчения состояния больного.
Следует несколько остановиться на криохирургическом лечении альвеококкоза.
Âсемидесятые годы прошлого столетия в клинике Б.В. Петровского О.Б. Милонов с сотрудниками в эксперименте на хлопковых крысах установил, что паразит при альвеококкозе погибает при температуре ниже 80°С. В СССР криовоздействие при альвеококкозе пече- ни впервые было осуществлено Б.И. Альперовичем в 1972 г. За прошедшие 30 лет им разработан целый ряд методов криохирургических вмешательств с помощью оригинальной аппаратуры: криоскальпеля, виброкриоскальпеля и криодеструктора. Эти инструменты позволяют сочетать эффективное воздействие сверхнизких температур с ультразвуком и вибрацией, которые усиливают терапевтическое воздействие холода. С помощью этих инструментов успешно проведены криорезекции, а также паллиативные резекции печени, когда на оставленные участки паразитарной ткани в опасных зонах (область ворот органа и нижней полой вены) осуществляется криовоздействие, губительное для паразита; криодеструкция паразитарной ткани при операциях кускования паразита и марсупиализации, когда на альвеококковую ткань воздействуют сверхнизкими температурами, ускоряющими гибель паразитарных элементов и отторжение их в рану.
Все паллиативные операции не излечивают больных, но могут весьма существенно продлить их жизнь; паллиативные же резекции с криодеструкцией оставшихся уча- стков печени позволяют практически излечить больного. При альвеококкозе возможно также производить повторные вмешательства и удалять метастазы паразита из головного мозга и легких.
Âпоследние годы в печати появились работы экспериментаторов, которые получили положительный эффект от воздействия на альвеококк мебендазола и его производных.
Âсвязи с этим целесообразно после операций по поводу альвеококкоза назначать больным этот препарат для предупреждения рецидивов.
Профилактика альвеококкоза представляет трудную задачу. Если при эхинококкозе промежуточные и окончательные хозяева паразита могут подвергаться воздействию людей, то при альвеококкозе как промежуточные, так и окончательные хозяева паразита проживают в условиях дикой природы и малодоступны для воздействия человека.
Âсвязи с этим проводится в основном индивидуальная профилактика альвеококкоза в виде строгого соблюдения правил личной гигиены. Наиболее подвержены зара-
127

Клиническая хирургия
жению альвеококкозом работники звероферм. От них требуется соблюдение особых мер предосторожности (работа в специальных рукавицах, фартуках, обязательная дезинфекция рук после кормления животных и ухода за ними и т.д.). Забой животных на зверофермах должен производиться только в специально отведенных местах под контролем ветеринарной службы с соблюдением мер предосторожности со стороны обслуживающего персонала.
2.6. Хирургические осложнения описторхоза
По данным ВОЗ, свыше 10% населения земного шара инвазирована различными трематодами. Весьма актуальной в практической медицине является проблема описторхоза.
Описторхоз – паразитарное заболевание, возбудитель которого – небольшой гельминт описторхис (Opisthorhis fellineus) из класса трематод. Впервые он обнаружен итальянским ученым Rivolta в 1884 г. в печени кошек и назван «кошачьим сосальщиком». У человека этот паразит был обнаружен в 1891 г. профессором Томского университета К.Н. Виноградовым и получил название сибирской двуустки.
Â2001 г. в СибГМУ прошла международная конференция, посвященная 110-летне- му периоду изучения описторхоза (болезнь Виноградова). В нашей стране есть природные описторхозные очаги. Самым крупным из них считается очаг в Западной Сибири – ОбьИртышский бассейн, где заболеваемость населения достигает 80–87%, а в некоторых районах Томской области – 90%. Затем следует очаг бассейна Днепра и его притоков, третьим очагом считаются Пермская область и Волго-Камский район. В Западной Европе это заболевание распространено в бассейне реки Неман, встречается в Австралии, Германии, Венгрии, Голландии, Польше, Румынии, Франции, Италии, Швеции и т.д. В Таиланде имеет место аналогичное паразитарное заболевание – клонорхоз, вызываемое родственным сибирской двуустке гельминтом.
Патогенез. Взрослые особи листовидной формы, длиной от 4 до 13 мм и шириной от 1 до 3 мм. Паразитируя в желчных протоках, реже – в желчном пузыре и протоках поджелудочной железы, описторхисы оказывают разнообразное влияние на организм человека (рис. 97). Патогенез описторхоза – процесс сложный и еще не изученный до конца. В возрасте 1 месяца личинки достигают половой зрелости и начинают выделять яйца. Степень инвазивности колеблется от нескольких особей до десятков тысяч. Нарастание интенсивности инвазии происходит путем повторного заражения.
Âпатогенезе описторхоза выделяют две фазы: раннюю, или острую, и позднюю, или хроническую. Острый описторхоз длится от нескольких дней до 4–8 недель и более. Острая фаза протекает по типу аллергического заболевания с резко выраженной
эозинофилией, в основе которой – сенсибилизация организма антигенами паразитов. Описторхисы выделяют вещества, аналогичные гемагглютининам человека α, β, р, n. Эти гемагглютинины в крови определенной групповой принадлежности больного ведут к гемагглютинации и гемолизу, повышенной проницаемости стенок сосудов, циркуляторным расстройствам, дезорганизации соединительной ткани. Иммунопатологичес-
128

2. Хирургические заболевания печени и желчных путей
Рис. 97. В просвете расширенного внутрипеченочного желчного протока – описторхисы. Выражен аденоматоз стенки протока. Гематоксилин-эозин х70
кая реакция лежит в основе поражений слизистых оболочек органов пищеварения, эндотелия сосудов, ЦНС, а также играет определенную роль в поражении внутрипеченоч- ных желчных ходов. Ранняя стадия описторхоза протекает практически бессимптомно.
Хроническаяфазаначинаетсясмоментаоткладыванияяицописторхисамииможетдлиться 10–20 лет и даже более. Степень морфофункциональных изменений зависит от длительности и интенсивности инвазии. Недостаточная эффективность профилактических мер и дегельминтизации, неэффективность ее при осложненных формах, выраженность патоморфологических изменений органов обитания гельминтов приводят к хронизации процесса.
При хроническом течении описторхоза встречаются осложненные формы заболевания, требующие хирургических методов лечения.
Изучению патоморфологии органов паразитирования, патогенеза и клиники осложнений хронического описторхоза посвящены труды многих отечественных ученых: Н.А. Зубова, А.М. Третьякова, Р.В. Зиганьшина, В.Я. Глумова, А.А. Кульчиева и других, в том числе и работы, выполненные под руководством Б.И. Альперовича: А.Ю. Ревского, А.Г. Соколовича, В.Я. Митасова, В.К. Абушахманова, Н.А. Бражниковой, В.Ф. Цхай.
Патоморфология органов паразитирования изучалась нами на 254 трупах в возрасте от 16 до 91 года в разные годы. В 1980-е гг. описторхоз был выявлен у 13,4% умерших, а в 1990-е – уже у 18,3%, т.е. несмотря на появление новых антигельминтных препаратов, частота инвазии не снизилась, что связано, по-видимому, с реинвазией. Кроме того, наблюдалось увеличение и степени инвазии. Если в первый период массивная инвазия была отмече- на у 26% умерших, то во второй – у 42%. При массивной степени инвазии развиваются тяжелые патоморфологические изменения, приводящие к смерти. У 17% умерших описторхоз учтен как основная причина смерти.
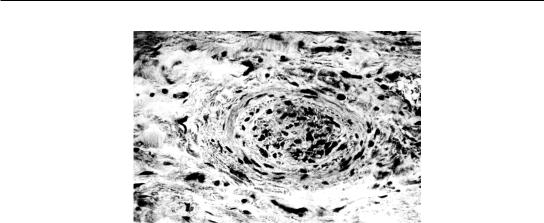
В основе патологического процесса лежат пролиферативные изменения внутри- и внепеченочных желчных протоков с определенной стадийностью течения. В раннем периоде развиваются аденоматозные процессы, а в позднем – склероз (рис. 98). В местах физиологических сужений склеротические процессы приводят к образованию стриктур пузырного протока, дистальной части холедоха и БДС. Стриктуры сопровождаются механичес-
129
Клиническая хирургия
Рис. 98. Стриктура пузырного протока. Гематоксилин-эозин х600
ким холестазом. Последний усиливается обтурацией желчных протоков описторхисами и продуктами их жизнедеятельности («описторхозным детритом»), а также перихоледохеальным лимфаденитом, свойственным описторхозу.
Хронический холестаз приводит к развитию подкапсульных и внутрипеченочных холангиоэктазов, кист печени, является источником инфицирования билиарного тракта, а значит, холециститов, холангитов, холангитических абсцессов со всеми гнойными проявлениями этих осложнений вплоть до развития билиарного сепсиса.
Аналогичные изменения возникают и в поджелудочной железе, что обусловлено не только паразитированием гельминтов в протоках железы (редко), их токсическим действием, но и нарушением оттока панкреатического сока при стриктурах дистальной части холедоха и БДС, рефлюксом желчи в протоки железы. Морфологические изменения характеризуются продуктивным каналикулитом с оча- говым или внутридольковым склерозом и нарушением дольчатого строения железы, особенно в области головки. В паренхиме наблюдаются атрофия ацинусов, реже кровоизлияния и некрозы. Ретенционная каналикулоэктазия лежит в основе образования кист поджелудочной железы (рис. 99).
Все эти изменения создают условия для развития как острого, так и хронического панкреатита. В свою очередь, описторхозный панкреатит на фоне склеротических изменений дистальной части холедоха и БДС способствует развитию протяженных стриктур дистального отдела общего желчного протока и нарушению пассажа желчи в двенадцатиперстную кишку.
Описторхозная инвазия вызывает и поддерживает воспалительно-пролиферативные изменения не только в желчных протоках, но и в паренхиме и межуточной ткани печени, что в сочетании с холестазом приводит к склерозу, а в ряде случаев и к циррозу (рис. 100). Хроническая описторхозная инвазия оказывает угнетающее влияние на Т-иммунную систему, создает благоприятный фон для первичного рака печени. Дистрофические и некроти- ческие изменения слизистой желчных и панкреатических протоков с патологической интенсивной регенерацией эпителия и образованием аденоматозных структур на фоне склероза соединительной ткани, атипизм эпителия являются основой формирования холангиогенного рака печени, желчных путей и БДС, поджелудочной железы.
130
