
- •Б.Я. Брянский, т.А. Калинина
- •1.1. Основные понятия химической термодинамики 7
- •1. Конспект теоретического материала
- •1.1. Основные понятия химической термодинамики
- •1.1.1. Термодинамическая система
- •1.1.2. Состояния, свойства термодинамической системы.
- •1.2.1. Уравнение состояния термодинамической системы. Нулевой
- •1.2.2. Идеальный газ и его уравнение состояния
- •1.2.3. Реальный газ и его уравнения состояния
- •В критической точке одному давлению соответствует не три объёма, а один (см. Рис.1). Следовательно, для этой точки кубическое уравнение принимает следующий вид:
- •1.3. Первый закон термодинамики
- •1.3.1. Функции состояния и формы обмена энергией
- •1.3.2. Содержание первого закона термодинамики
- •1. При поглощении теплоты система увеличивает внутреннюю энергию и совершает работу:
- •2. При уменьшении внутренней энергии система выделяет теплоту и совершает работу:
- •1.3.3. Расчёт работы
- •1.3.4. Расчёт теплоты. Теплоёмкость
- •1.3.5. Адиабатический процесс
- •1.4. Начальные понятия термохимии
- •1.4.1. Тепловой эффект химической реакции с точки зрения
- •1.4.2. Стандартные молярные энтальпии (смэ) реакций и фазовых
- •1.5. Термохимические расчёты
- •1.5.1. Расчёт стандартной энтальпии реакции через стандартные энтальпии образования участников реакции
- •1.5.2. Расчёт стандартной энтальпии реакции через стандартные энтальпии сгорания участников реакции
- •1.5.3. Расчёт стандартной энтальпии реакции через энергии связей участников реакции
- •1.5.4. Расчёт стандартной энтальпии решётки (цикл Борна-Габера)
- •1.5.5. Расчёт стандартной энтальпии гидратации и
- •1.5.6. Расчёт энтальпии реакции при произвольной температуре
- •1.5.7. Связь энтальпии реакции с изменением внутренней энергии
- •1.6. Энтропия и второй закон термодинамики
- •1.6.1. Энтропия и её статистический смысл
- •1.6.2. Второй закон термодинамики
- •1.6.3. Расчёты изменения энтропии в равновесных процессах
- •1.7. Применение второго закона термодинамики к неизолированным изотермическим системам
- •1.7.1. Энергии Гельмгольца и Гиббса
- •1.7.2. Расчёт энергии Гиббса реакции
- •1.7.3. Термодинамические потенциалы. Соотношения Максвелла
- •1.8. Закон действующих масс
- •1.8.1. Химический потенциал. Фундаментальное уравнение Гиббса
- •1.8.2. Вывод закона действующих масс
- •1.8.3. Принцип Ле Шателье – Брауна
- •2. Лабораторные работы по термохимии
- •2.1. Общие замечания.
- •2.2. Определение постоянной калориметра
- •2.3. Лабораторная работа 1. Определение парциальной мольной энтальпии растворения вещества
- •Порядок выполнения работы
- •Контрольные вопросы
- •2.4. Лабораторная работа № 2. Определение теплоты реакции нейтрализации сильной кислоты сильным основанием
- •Порядок выполнения работы
- •Контрольные вопросы
- •2.5. Лабораторная работа № 3. Определение теплоты диссоциации слабой кислоты
- •Порядок выполнения работы
- •1. Определяют постоянную калориметра (см. П.2.1).
- •3. Определение теплоты реакции нейтрализации (Qнейтр) проводят по методике предыдущей лабораторной работы или используют табличные данные (по указанию преподавателя).
- •8. Рассчитывают теплоту реакции нейтрализации соляной кислоты гидроксидом натрия (Qнейтр) по методике предыдущей работы, либо используют справочные данные.
- •Контрольные вопросы
- •2.6. Лабораторная работа № 4. Определение теплоты гидратообразования соли
- •Порядок выполнения работы
- •Контрольные вопросы
- •2.7. Лабораторная работа № 5. Определение теплоты реакции окисления щавелевой кислоты перманганатом калия
- •Порядок выполнения работы
- •Контрольные вопросы
- •2.8. Лабораторная работа № 6. Определение теплоты испарения органических жидкостей
- •Порядок выполнения работы
- •Контрольные вопросы
- •5. Рассчитайте изменение внутренней энергии при испарении 1 моль органической жидкости, теплоту испарения которой вы определили экспериментально.
- •3. Рекомендации к практическим занятиям
- •3.1. Рекомендации для успешного решения задач
- •3.2. Материалы к практическим занятиям
- •3.2.1. Уравнения состояния идеальных и реальных газовых систем
- •3.2.2. Первый закон термодинамики. Вычисление внутренней энергии,
- •3.2.3. Тепловой эффект химической реакции. Закон Гесса. Зависимость теплового эффекта от температуры. Формула Кирхгофа
- •3.2.4. Второй закон термодинамики. Вычисление изменения энтропии в различных процессах. Расчёт абсолютной энтропии веществ
- •3.2.5. Термодинамические потенциалы. Соотношения Максвелла
- •3.2.6. Закон действующих масс. Расчёт равновесного состава
- •3.2.7. Уравнение изотермы химической реакции
- •3.2.8. Зависимость константы равновесия от температуры. Уравнения
- •3.2.9. Методы расчета константы равновесия и энергии Гиббса реакции
- •4. Методические рекомедации и справочные материалы
- •4.1. Основные правила работы при проведении лабораторных работ по термохимии
- •4.2. Основные правила построения и оформления графиков
- •4.3. Рекомендации по применению международной системы единиц си
- •4.4.Таблицы физико-химических данных
- •Литература
- •Дополнительная
- •Часть 1 Издательство ОмГу
- •644077, Г. Омск, пр. Мира, 55а, госуниверситет
2. Лабораторные работы по термохимии
2.1. Общие замечания.
Термохимия - это раздел химической термодинамики, в котором изучаются тепловые эффекты, сопровождающие различные физико-химические процессы – химические реакции, фазовые переходы и др.
Определение тепловых эффектов проводят на основании калориметрических измерений, в ходе которых определяют изменение температуры (t1) во время протекания изучаемого процесса, а затем рассчитывают тепловой эффект по уравнению теплового баланса
Q = (m1c1+m2c2+…)t1,
где mi и ci -масса и теплоёмкость исследуемого вещества и участвующих в теплообмене частей калориметра.
Выполняя лабораторные работы по определению тепловых эффектов различных процессов на основании калориметрических измерений, следует правильно и аккуратно оформлять отчёт о проделанной работе. Отчёт должен содержать:
- дату выполнения работы и её название;
- цель работы и задание, полученное от преподавателя;
- список используемых реактивов, посуды и аппаратуры;
- краткое содержание работы, уравнения реакций и формулы, которые используются для расчётов;
- результаты взвешиваний и измерения объёмов;
- использованные справочные данные;
- показания измерительных приборов, если они использовались в работе;
- таблицы с записью температур в ходе калориметрического опыта;
- графики и результаты графических определений;
- вычисления по приведённым уравнениям с подставленными числовыми данными; результаты вычислений;
- сопоставление экспериментально полученных результатов со справочными величинами или рассчитанными на основании справочных данных; расчёт относительной ошибки определения, вывод по работе.
При подготовке к выполнению лабораторной работы необходимо познакомиться с лекционным материалом по теме работы, теоретическими материалами, приведёнными в данном пособии, а также в учебниках, рекомендованных в методических указаниях к каждой работе. Внимательно ознакомьтесь с порядком выполнения эксперимента, проведите все необходимые предварительные расчёты, выпишите справочные данные, постарайтесь ответить на контрольные вопросы.
Основная аппаратура. Калориметрические измерения проводят в специальном приборе – калориметре. Важнейшими составными частями калориметра являются: калориметрический сосуд с жидкостью (вода, раствор соли, кислоты и т.д) и защитная оболочка, уменьшающая теплообмен с окружающей средой. Способы изолирования калориметров от теплового воздействия различны, но чаще всего применяются калориметры с изотермической оболочкой, которые позволяют учесть теплообмен его с окружающей средой и вычислить изменение температуры, соответствующее опыту без теплообмена. В крышке калориметра имеются отверстия для ввода в калориметрический сосуд исследуемого вещества, датчика температуры и мешалки.
В данном практикуме используются два вида калориметрических установок с изотермической оболочкой – учебно- лабораторный комплекс (УЛК) «Химия» для термохимических измерений, снабжённый термодатчиком, позволяющим измерять температуру калориметрической жидкости с точностью до 0,0020, и калориметр, в котором для определения изменения температуры используется термометр Бекмана. При использовании в работе УЛК «Химия» инструкцию для работы с ним следует получить у лаборанта.
Устройство и установка термометра Бекмана Изменение температуры в ходе калориметрического опыта можно фиксировать при помощи термометра Бекмана, позволяющего определять изменения температуры Δt с точностью до 0,002 оС. Термометр имеет запасной резервуар со ртутью, что позволяет проводить измерения Δt в довольно широком диапазоне температур. Термометр должен быть настроен на определённый температурный интервал непосредственно перед проведением калориметрических измерений.
П еред
установкой термометра проверяют его
показания при условиях проведения
опыта. Например, необходимо, чтобы в
воде комнатной температуры столбик
термометра находился между 20
и 30 его
шкалы. Для этого погружают термометр в
стакан с дистиллированной водой комнатной
температуры. Если уровень ртути в
капилляре находится между 20
и 30 ,
то термометр не требует установки.
еред
установкой термометра проверяют его
показания при условиях проведения
опыта. Например, необходимо, чтобы в
воде комнатной температуры столбик
термометра находился между 20
и 30 его
шкалы. Для этого погружают термометр в
стакан с дистиллированной водой комнатной
температуры. Если уровень ртути в
капилляре находится между 20
и 30 ,
то термометр не требует установки.
Е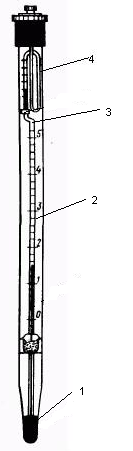 сли
окажется, что уровень ртути находится
выше 30 ,
то термометр должен быть установлен.
Для этого рабочий резервуар термометра
нагревают рукой. При этом ртуть заполнит
не только весь капилляр термометра, но
и войдёт в верхнюю часть запасного
резервуара, образуя капельку, которую
нужно стряхнуть в запасной резервуар
(рис.1). Для этого правой рукой берут
термометр за верхнюю часть, а левой
легко ударяют по пальцам правой. Снова
проверяют установку термометра, помещая
рабочий резервуар в стакан с дистиллированной
водой. Если ртуть в капилляре окажется
выше от-
сли
окажется, что уровень ртути находится
выше 30 ,
то термометр должен быть установлен.
Для этого рабочий резервуар термометра
нагревают рукой. При этом ртуть заполнит
не только весь капилляр термометра, но
и войдёт в верхнюю часть запасного
резервуара, образуя капельку, которую
нужно стряхнуть в запасной резервуар
(рис.1). Для этого правой рукой берут
термометр за верхнюю часть, а левой
легко ударяют по пальцам правой. Снова
проверяют установку термометра, помещая
рабочий резервуар в стакан с дистиллированной
водой. Если ртуть в капилляре окажется
выше от-
Рис.2.1. Термометр Бекмана: 1-рабочий резервуар, 2- шкала, 3- капилляр, 4- запасной резервуар
метки 30, то описанную выше процедуру следует повторить до достижения положения ртути в капилляре между 20 и 30. Если в запасной резервуар переведено слишком много ртути (её уровень установился ниже 20), то следует добавить ртуть из запасного резервуара в рабочий.
Для этого лучше всего держать термометр в наклонном положении так, чтобы запасной резервуар был ниже рабочего резервуара. Следует нагреть последний рукой и, когда ртуть заполнит весь капилляр, лёгким встряхиванием добиться передвижения ртути из нижней части запасного резервуара в верхнюю и слияния её со ртутью в капилляре. Затем, изменив наклон термометра таким образом, чтобы запасной резервуар находился выше рабочего, охладить последний струёй водопроводной воды. Когда из запасного резервуара перейдёт нужное количество ртути (ориентировочно) в рабочий резервуар, термометр нужно поставить вертикально и способом, описанным выше, разорвать столбик ртути. Снова проверить установку термометра, поместив его в стакан с водой.
Варьируя оба эти приёма, легко установить термометр в нужной части шкалы. Термометр Бекмана содержит большое количество ртути, поэтому обращение с ним требует большой осторожности.
