
- •522 Список літератури
- •Розвиток тимчасових і постійних зубів
- •Розвиток тимчасових зубів
- •Розвиток постійних зубів
- •Будова дентину
- •Будова цементу
- •Анатомічна будова тимчасових зубів
- •Анатомічна будова постійних зубів
- •Нижня щелепа
- •Фізичні методаї діагностики
- •Методи дослідження кісткової тканини щелепно-лицевої ділянки
- •Лабораторні методи дослідження
- •Захисні механізми ротової порожнини
- •Клініка, діагностика і диференційна діагностика карієсу тимчасових зубів
- •Карієс тимчасових зубів на стадії формування кореня
- •Карієс тимчасових зубів на стадії сформованого кореня
- •Клініка, діагностика, диференційна діагностика карієсу постійних зубів
- •Лікування карієсу у дітей Лікування карієсу тимчасових зубів
- •Лікування карієсу постійних зубів
- •Стоматологічні пломбувальні матеріали, що застосовуються в дитячій
- •Терапевтичній стоматологи
- •Стоматологічні цементи
- •Композиційні пломбувальні матеріали
- •Стоматологічні адгезиви (бонд-системи, або праймер-адгезивні системи)
- •Стоматологічні амальгами
- •Профілактика карієсу у дітей
- •Некаріозні ураження зубів
- •"Тетрациклінові" зуби
- •Флюороз (ендемічний флюороз)
- •Природжені вади розвитку твердих тканин зубів
- •Пульпіт тимчасових і постійних зубів Структура та функції пульпи
- •Пульпіт тимчасових зубів Етіологія і патогенез пульпіту у дітей
- •Класифікація пульпіту у дітей
- •Клінічна симптоматика пульпіту тимчасових зубів
- •Пульпіт постійних зубів Етіологія, патогенез, класифікація
- •Мал. 60. Класифікація пульпіту кмі (о.С. Яворська, л.І.Урбанович, 1961) 269
- •Клініка, діагностика і диференційна діагностика пульпіту постійних зубів у дітей
- •Лікування пульпіту постійних зубів у дітей
- •Періодонтит тимчасових і постійних зубів
- •Структура і функції періодонта
- •Етіологія і патогенез періодонтиту тимчасових і постійних зубів у дітей
- •Клініка періодонтиту тимчасових зубів
- •Клініка періодонтиту постійних зубів
- •Ендодонтія тимчасових зубів
- •Вибір методу лікування періодонтиту тимчасових зубів
- •Лікування гострого періодонтиту тимчасових зубів
- •Лікування хронічного періодонтиту тимчасових зубів
- •Ендодонтичні наконечники та інструменти для обробки кореневих каналів
- •Лікування гострого періодонтиту постійних зубів у дітей
- •Травматичні ушкодження зубів
- •Тактика під час лікування травм
- •Постійних зубів у дітей і. Пошкодження твердих тканин зуба та пульпи
- •II. Пошкодження тканин пародонта
- •III, IV. Пошкодження кістки, ясен, слизової оболонки
- •Травми тимчасових зубів у дітей
- •Ускладнення після травми тимчасових та постійних зубів
- •Анатомічні та морфологічні особливості тканин пародонта
- •Класифікація хвороб пародонта
- •Пародонтит
- •Генералізований пародонтит
- •Ідіопатичні хвороби з прогресуючим лізисом тканин пародонта (пародонтоліз)
- •Хвороби слизової оболонки ротової порожнини у дітей Особливості будови слизової оболонки ротової порожнини в дитячому віці
- •Класифікація хвороб слизової оболонки ротової порожнини
- •Пошкодження слизової оболонки ротової порожнини
- •Вірусні хвороби слизової оболонки ротової порожнини
- •Прояви гострих вірусних та інфекційних захворювань на слизовій оболонці ротової порожнини
- •Грибкові хвороби слизової оболонки ротової порожнини
- •Алергічні хвороби слизової оболонки ротової порожнини
- •Зміни слизової оболонки ротової порожнини при деяких системних захворюваннях
- •Зміни слизової оболонки ротової порожнини при специфічних хворобах
- •Хвороби губів (хейліти)
- •Стоматогенне вогнище інфекції та вогнищевозумовлені хвороби
- •Список літератури
Захисні механізми ротової порожнини
Розвиток будь-яких патологічних змін у ротовій порожнині завжди супроводжується реакцією різних ланок її захисту. Уявлення всієї складності цієї системи дозволяє глибше зрозуміти механізм розвитку хвороб зубів, тканин пародонта та слизової оболонки ротової порожнини. Ротова порожнина має багатокомпонентну систему захисту від патогенних чинників навколишнього середовища. Захисні міханізми ротової порожнини умовно поділяються на дві великі групи - неспецифічні та імунні, які у свою чергу поділяються на специфічні і неспецифічні, гуморальні та клітинні. Їх функція тісно інтегрована для досягнення найважливішої мети — забезпечення цілості тканин ротової порожнини, а також і всього організму.
Неспецифічні механізми захисту ротової порожнини. Неспецифічні механізми захисту ротової порожнини складаються із гетерогенних захисних компонентів, які функціонально поєднані. До них належать поведінка, умовно і безумовно рефлекторна реакція, бар'єрна функція покривного епітелію. Ці реакції об'єднуються відповідною функціональною системою цілості організму.
Ротова порожнина як початковий відділ травного тракту виконує багато функцій, які можуть бути потенційно пов'язані з порушенням цілості тканини ротової порожнини або організму в цілому. Тому часто ротова порожнина використовується організмом як активний засіб отримання інформації про навколишеє середовище через систему механо-, термо- хеморецепторів язика, губів, слизової оболонки щік, піднебіння, періодонта та ін. При можливому порушенні цілості тканин, пов'язаних зі зміною в навколишньому середовищі, організм формує захисні реакції поведінки. Такими реакціями можуть бути уникнення подразника, відхилення голови, зімкнення щелеп, уникнення місць, що здаються небезпечними, тощо.
До механізмів захисту ротової порожнини відносять виділення слини слинними залозами — салівацію, яка в основному реалізується через умовно чи безумовнорефлекторну дію нервової системи. Сильне подразнення термо-, механо- чи хеморецепторів, а також дія
8
9712
113
на ноцицептори у разі втрати цілості тканин призводять до виділення великої кількості слини, бідної на ферменти і яка виконує наступні завдання — сприяє швидкому видаленню несприятливих речовин із ротової порожнини, нормалізує температуру, нейтралізує хімічно несприятливі чинники (кислоти, луги). Крім того, слина має велику кількість відновних матеріалів (макро-мікроелементи для зубів), ферментів, регулюючих факторів (фактор росту епітелію), імунних елементів тощо. Крім того, в слизовій оболонці ротової порожнини рефлекторно може змінюватись кровопостачання для активації біохімічних, імунологічних, відновних процесів у зонах ушкодження.
Однією із важливих захисних функцій неспецифічного захисту ротової порожнини є бар'єрна. Бар'єри умовно ділять на зовнішні та внутрішні. До зовнішніх належать покривний епітелій ротової порожнини, до внутрішніх — мікроциркуляторне русло власне слизової оболонки ротової порожнини, пульпи зуба, яке регулює надходження з крові в органи і тканини необхідних енергетичних, пластичних ресурсів і своєчасний відтік продуктів клітинного обміну, що забезпечує стійкість складу, фізико-хімічну та біологічну якість тканин ротової порожнини.
Бар'єрна стійкість слизової оболонки насамперед залежить від стану її епітелію, що являє собою активно-функціонуючу перешкоду для мікробів, токсинів, інших хімічних речовин. Завдяки наявності внутрішньоклітинних лізо- фагосом, а також продукції гліко протеїдів, ферментів, що чинять несприятливий вплив на бактерійні клітини, епітелій, крім чисто механічного захисту, виконує також активну антибактеріальну функцію (Я. С.Шварцман іспівавт., 1978). Крім того, на деяких ділянках ротової порожнини (ясна, тверде піднебіння, дорсальна поверхня язика) розмноження мікроорганізмів обмежене через постійне злущування епітелію.
Значення бар'єрної функції епітелію залежить від кількості шарів епітеліальних клітин. Так, наприклад, найміцніший бар'єр міститься на дорсальній поверхні язика, найслабший у зубо-ясенній борозні, що компенсується іншими біологічними захисними механізмами цієї ділянки (переміщення рідини, фагоцитоз тощо).
Важливу роль у неспецифічному захисті граь антагонізм нормальної мікрофлори ротової порожнини. Відомо, що стрептококи, які становлять понад 30% мікрофлори слизової оболонки, зубного на-
114
Захисні механізми ротової порожнини
льоту можуть пригнічувати функціонування інших видів бактерій. Str. Sangvis, mutans, salivarias разом із Lactobacillus acidophilus продукують мікросередовище життєдіяльності зі значно низьким рН, яка непридатна для Veillonella, Bacteroides, інших мікроорганізмів. Str. Mutans, str. mitior синтезують перекис водню, який пригнічує актиноміцети. Накопичення кількості мікроорганізмів може змінювати пропорцію кількості 0^-СОу стимулюючи заселення анаеробних видів мікроорганізмів, які у свою чергу пригнічують адгезію, кисло-тотвірну функцію стрептококів. Наприклад, бактероїди розщеплюють декстран, леван, мутан, глютан. Водночас нейсерії, актиноміцети утилізують полісахаридну продукцію стрептококів як енергетичний субстрат, таким чином позбавляючи самі стрептококи та інші види мікробів матриксу для адгезії. Вейлонели можуть використовувати молочну кислоту Str. Mutans у своєму метаболізмі, підвищуючи рН середовища. Лактобацили утворюють антибіотики: лактолін, лакто-цидин, ацидофілін, які пригнічують стрептокок і стафілокок.
Бактеріоцин, продукт Str. Mutans, відомий більше під назвою "мутаціон" активно діє на стрептококи з групи зеленящих, а також на актиноміцети. Цангіцини Str. Sangvis бактерицидне діють на Str. Mutans.
Деякі мікроби інгібують розмноження інших мікробів невідомим шляхом. Так, Str. Mitis пригнічує розмноження дифтерійної палички', гноєтворних стрептококів, золотистого стафілокока. Str. Salivarius діє бактеріостатичне на стрептококи групи А.
Ще одну функцію захисту, особливо від транзиторної мікрофлори, нормальна мікрофлора реалізує через блокування рецепторів покривного епітелію (А.Ройт ,1991).
Неспецифічні чинники гуморального та клітинного імунітету. Рідина ротової порожнини має виражену антибактеріальну та противірусну дію завдяки присутності в ній факторів неспецифічного імунного захисту. Вони секретуються клітинами слизової оболонки, залозистих утворень ротової порожнини, глотки, нейтрофілами та макрофагами. До них належать лізоцим, комплемент, пропердин, бета-лізини, бактерициди та багато інших гуморальних речовин, що мають виражені неспецифічні інгібуючі, інактивуючі, лізируючі та інші властивості, які згубно впливають на мікроорганізми.
8*
115
Велика питома вага у продукції лізоциму, який потрапляє в ротову рідину ротової порожнини, надається нейтрофільним гранулоцитам. Слина має високу концентрацію лізоциму порівняно з іншими біологічними рідинами. Лізоцим, лізируючи глікопептиди клітинної стінки, в основному грампозитивних бактерій, забезпечує кисне-вонезалежний механізм неспецифічного захисту. Він може також лізирувати глікопептиди грамнегативних бактерій після зняття ліпідного шару комплементом або катіонними білками (А.Ройт, 1991). Крім неспецифічної антимікробної дії, лізоцим значною мірою активує специфічні механізми протиінфекційного захисту, будучи си-нергістом антитіл.
Лактоферин, прототип трансферину сироватки крові, також бере активну участь у захисті органів ротової порожнини від збудників різних інфекцій і водночас контролює функціонування нормальної мікрофлори (R.R.Amold, 1980). Захисна дія даного білка основана на конкуренції з мікроорганізмами за приєднання заліза. У разі надлишку заліза вірулентність деяких видів мікроорганізмів (стрептокока, стафілокока, мікроорганізмів роду Candida) різко зростає. Походження лактоферину в ротовій порожнині дітей вивчене мало.
Вагоме значення у формуванні неспеїщфічної протиінфекцій-ної резистентності слизової оболонки ротової порожнини, особливо противірусної, має інтерферон. Варто відзначити, що, будучи медіатором сенсибілізованих лімфоцитів, інтерферон може модулювати специфічні імунні реакції, зокрема, пригнічувати реакції гіперчутли-вості уповільненого типу. Відомо щонайменше 14 а-інтерферонів, які синтезуються лімфоцитами, у той час як фібробласти, епітелій та інші клітини продукують р-інтерферони. Активовані лімфоцити (цитотоксичні лімфоцити, кілери, хелпери), а, ймовірно, і макрофаги синтезують у-інтерферони. При вірусній інфекції клітини продукують у-інтерферон і секретують його до міжклітинного простору, де він зв'язується зі специфічними рецепторами сусідніх незаражених клітин.
Зв'язаний інтерферон здійснює противірусну активність таким чином. У клітині, на яку вплинув інтерферон, депресуються щонайменше два гени, і починається синтез двох ферментів — протеїнкіна-зи та ендонуклеази, що призводить до зниження трансляції, а також деградації матричної РНК як вірусу, так і хазяїна. Таким чином, кінцевий результат дії інтерферону полягає у створенні бар'єра з неінфіко-
116
Захисні механізми ротової порожнини
ваних клітин навколо осередку вірусної інфекції, що обмежує її поширення. Особливо висока концентрація у-інтерферону виявляється в зоні ураження після надходження туди з лімфатичних вузлів великої кількості специфічних цитотоксичних лімфоцитів, які знищують усі уражені вірусом клітини. Найважливіша роль у-інтерферону тоді, коли вірус є слабким індуктором інтерферонів а і (3. Варто відзначити, що у-інтерферони відіграють значну роль саме у боротьбі з вірусами, але не у запобіганні вірусній інфекції, у-інтерферони також посилюють згубну функцію нормальних кілерів. у-інтерферон, що виділяється Т-хелперами, стимулює внутрішньоклітинне перетравлення макрофагами мікроорганізмів, наприклад, роду Candida. Останнім часом з'явилися дані про інтерферони як фактори, що, будучи антагоністами онкобілка, інгібують проліферативну активність клітин, в яких відбулися мутаційні зміни.
До чинників неспецифічного захисту слизової оболонки ротової порожнини належить також комплемент (С) — складний комплекс білків (близько 20), які формують каскадні системи (подібно системі згортання крові, утворення кінінів, фібринолізу), забезпечуючи швидке багаторазове посилення імунної відповіді на первинний антигенний сигнал. Комплемент у ротовій порожнині наявний переважно в ясенній рідині у формі СЗ, С4, С5 та активується в основному альтернативним шляхом, зумовлюючи запальну реакцію та пошкодження тканин пародонта (Р.А.Томпсон, 1983).
Крім наведених чинників неспецифічного захисту, важлива протекторна роль належить таким ферментам слини, як амілаза, лужна та кисла фосфатаза, РНК-аза, ДНК-аза, протеолітичні ферменти та інгібітори протеолізу (К-М.Веремеєнко і співавт., 1976; Л.О.Хомен-ко, 1980). Слина представлена майже повним набором ферментів, здатних руйнувати всі види простих біологічних субстратів (білки, жири, вуглеводи).
У ротовій порожнині клітинні реакції неспецифічного захисту відбуваються переважно полінуклеарними нейтрофілами та макрофагами (АЛ.Шугар і співавт., 1980). Макрофаги представлені у власному шарі слизової оболонки гістіоцитами, в той час як нейтрофіли, будучи мобільними фагоцитами, у великій кількості виявляються в ясенній борозні, менше — в слині.
Полінуклеарні нейтрофіли у ясенній борозні є основним типом
117
клітин. Вони становлять від 91 до 98,6% усіх вільних клітин ясенної рідини (A.L Sonis et al., 1981).Варто відзначити постійність міграції нейтрофільних лейкоцитів через зубо-ясенну борозну до ротової порожнини і основне їх захисне навантаження в даній ділянці. Кількість мігруючих клітин збільшується не лише під час запальних процесів, але й під час фізіологічного навантаження на зуби, що треба враховувати при проведенні профілактичних заходів. Фагоцитарна функція в основному здійснюється за допомогою специфічних антитіл і комплементу. На фагоцитах ясенної рідини виявлені рецептори до IgG, IgM і комплементу (С). Крім ясенної борозни, полінуклеарні нейтрофіли містяться у власне слизовому шарі, переважно у судинах. Частина їх мігрує до пласту епітеліальних клітин багатошарового плоского епітелію слизової оболонки ротової порожнини, виконуючи контролюючу функцію разом із малими лімфоцитами та макрофагами (р.а.томпсон, 1983; Van Dyke et al., 1993).
Гістіоцити (осілі макрофаги) на відміну від циркулюючих макрофагів крові — це клітини, які довго живуть і функція яких зводиться до боротьби з тими бактеріями, вірусами та найпростішими, які здатні існувати всередині клітин хазяїна. Гістіоцити, що пасивно перебувають у слизовій оболонці ротової порожнини, активуються у процесі розвитку запалення. Вони мають підвищений вміст гідролаз, посилено секретують нейтральні протеази, здійснюють фагоцитоз. Проте багато облігатних внутрішньоклітинних паразитів перетравлюються макрофагами лише після впливу на них (у-інтерферону, що виділяється стимульованими лімфоцитами (хелперами) (А.Ройт, 1991).
Активовані макрофаги відіграють також певну роль як ініціатори розвитку хронічного запалення. Активований макрофаг здатний секретувати понад 60 різноманітних чинників, залучених до хронічних запальних реакцій і здатних знищити практично будь-який фа-гоцитований мікроб і клітини, які набули властивості "чужих".
Якщо організм хазяїна неспроможний знищити мікроб, що внутрішньоклітинне розмножується, то внаслідок хронічного Т-залеж-ного запалення в зоні скупчення антигенів відбувається нагромадження великої кількості гістіоцитів, які виділяють фіброгенні чинники, іцо активують фібробласти. Таким чином, стимулюється утворення грануляційної тканини і формування гранульоми. Гранульо-
118
Захисні механізми ротової порожнини
ма що виникає представляє собою спробу організму обмежити поширення персистуючої інфекції (В.В.Сєров і співавт., 1981).
Неспецифічність мікро- та макрофагального захисту є відносним поняттям, зважаючи на участь специфічних гуморальних (анти-тілозалежних) та клітинних (лімфокіни) механізмів кооперації.
Специфічні чинники гуморального і клітинного імунітету. Формування гуморальної специфічної захисної відповіді на антиген забезпечує В-ланка імунної системи. У разі взаємодії з антигеном В-лімфоцити проліферують і диференціюються через бластну форму на плазматичні клітини, які є активними продуцентами специфічних антитіл різних класів (IgM, IgG, IgA, IgE, IgD).
Основним гуморальним чинником місцевої антиінфекційної резистентності слизової оболонки ротової порожнини с IgA-антитіла, зокрема секреторні (S IgA). Джерелами S IgA слини с плазматичні клітини малих і великих слинних залоз та власне слизової оболонки ротової порожнини. Біологічна роль S IgA різноманітна. S IgA інгібує зв'язування мікроорганізмів з поверхнею епітеліальних клітин слизової оболонки ротової порожнини, таким чином запобігаючи їх проникненню углиб тканин. Участь S IgA слини в перешкоджанні прикріплюванню мікробів до поверхні зубів остаточно не з'ясована, хоча їх кількість у зубній бляшці достатньо велика. S IgA антитіла здатні інгібувати прикріплення грибів та вірусів до поверхні епітелію. S IgA слини можуть змінювати метаболізм бактерій, обмежувати утворення колоній, знижувати вірулентність збудників інфекцій, пригнічувати нейрамідазну активність стрептококів, зв'язуватися з деякими екзотоксинами. Порушення бар'єрної функції S IgA може бути причиною багатьох алергічних захворювань, розвитку клітинних імунних реакцій з пошкодженням слизової оболонки. S IgA слини, будучи основним компонентом "першої лінії захисту", має також важливе значення в регуляції нормальної мікрофлори ротової порожнини, її розселенні та надходженні до тканин. Недостатність S IgA слини може спричинити порушення взаємовідношення між мікрофлорою ротової порожнини, особливо її умовно-патогенними формами, і макроорганізмом. Це проявляється збільшенням кількості мікроорганізмів, посиленняїй їх агресивних властивостей та появою форм, які рідко трапляються у здорових осіб або не зустрічаються взагалі. Слід відзначити, що система місцевого специфічного імунітету,
119
яка реалізується через S IgA-антитілоутворення, є загальною для слизових оболонок організму, відносно автономною і регулюється Т-клітинним імунітетом.
Кількість IgG і особливо IgM в слині є незначною, тим часом як в ясенній рідині вони разом із сироватковим IgA представляють всю масу імуноглобулінів, відповідаючи такій же приблизно концентрації їх у сироватці крові. Даний факт свідчить про відмінність поверхневого імунітету слизової оболонки ротової порожнини і зубо-ясенної борозни.
Велика кількість IgG, IgM, комплементу, нейтрофільних лейкоцитів у зубо-ясенній борозні створює стійкий захист від інвазії мікроорганізмів у цій ділянці. Будь-який розлад у цій системі захисту сприяс можливим кількісним і якісним змінам мікрофлори в зубних нашаруваннях з наступним розвитком запально-деструктивного процесу у пародонті.
IgE представлені у власне слизовій оболонці. Фіксуючись на тканевих базофілах, вони виконують роль гуморальної лінії захисту слизової оболонки ротової порожнини шляхом синтезу біологічно активних речовин. Мікроорганізми або їх продукти метаболізму, здатні порушити лінію захисту, створену S IgA, зв'язуються зі специфічними IgE на поверхні тканевих базофілів, унаслідок чого останні отримують сигнал про звільнення вазоактивних амінів та хе-мотаксичних чинників. Це у свою чергу сприяє надходженню сюди циркулюючих у крові IgG, комплементу, нейтрофілів та еозинофілів, створюючи можливість як активного захисту, так і тканевого пошкодження. Слід відзначити більш низьку концентрацію IgE в слизовій оболонці ротової порожнини порівняно з дихальною трубкою або кишечником. Кількість IgE різко зростає при атотях, у тому числі в слизовій оболонці ротової порожнини, губів.
Тимус залежні клітинні реакції імунітету здійснюються Т-лімфо-цитами, популяція яких досить неоднорідна і представлена спеціалі-зованими за функціями клітинами: Т-супресорами, Т-хелперами, Т-юлерами, цитотоксичними лімфоцитами та ін.
У ротовій порожнині Т-лімфоцити місіягься на поверхні епітелію ясенної борозни. В інших ділянках вони виконують свою функцію в Lamina propria слизової оболонки. Слід підкреслити, що тканини ясен найбільш насичені тимусзалежними лімфоциіами. Незва-
120
Захисні механилш ротової порожнини
жаючи на відсугність Т-лімфоцитів у слині, їх роль у механізмах про-тиінфекційної резистентності ротової порожнини досить значна і здійснюється Т-клітинною регуляцією секреторного імунітету. Відзначається превалювання Т-хелперів у лімфоїдних накопиченнях підслизових шарів інших слизових оболонок, у тому числі і ротової порожнини, які посилюють IgA-антитілоутворення, та Т-супресорів, які пригнічують синтез Ig G та Ig M. Превалювання Т-хелперів для IgA-антшілоутворення в підслизовому шарі має важливе біологічне значення. Посилення секреції SIgA-антитіл на прониклий антиген сприяє фіксації його на поверхні слизової оболонки і запобігає розвитку інших імунологічних реакцій з можливим пошкодженням тканин.
Останнім часом встановлено, що захист слизових оболонок здебільшого пов'язаний з існуванням так званої лімфоїдної тканини, асоційованої зі слизовими оболонками (MALT). Ця тканина являє собою дифузне накопичення лімфоцитів, плазматичних клітин і фагоцитів (у тому числі і в ротовій порожнині) або ж організовану тканину з добре оформленими фолікулами (язичкові, піднебінні, глоткові мигдалики, пейєрові бляшки тонкого кишечника, апендикс);
(BJ.Underdownetal., 1986).
У зв'язку із встановленням факту існування загального місцевого імунітету для слизових оболонок та наявності MALT отримана відповідь на запитання, яким чином відбувається стимуляція антигеном специфічного антитілоутворення.
Наприклад, стрептокок, потрапляючи в крипти піднебінних мигдаликів або в пейєрові бляшки і зазнаючи за допомогою лімфоїдних клітин та макрофагів низки перетворень, індукує В-лімфоцити на специфічне антитілоутворення. Останні через грудну протоку надходять до кровотоку і поширюються по всьому організму. Потрапляючи в слинні або інші залози (зокрема, молочну залозу матерів, які годують груддю), до печінки, вони диференціюються на плазматичні клітини, які продукують специфічні до стрептокока антитіла. При проходженні через епітелій формується димер IgA, до якого приєднується секреторний чинник, котрий захищає молекулу IgA від ферментативного лізису. З'являючись із секретом залози, антитіла специфічно зв'язуються зі "співродичами" того самого стрептокока, інгібуючи їх патогенні властивості. Те саме відбувається у дифузно
121
розташованій лімфоідній тканині, в тому числі і у власне слизовій оболонці ротової порожнини. Таким чином, здійснюється захист слизової оболонки на всьому протязі травного тракту, що має велике профілактичне значення як для захисту, так і для формування нормальної мікрофлори, особливо на перших місяцях життя (BJ.Underdown etal.,1986).
Ураховуючи згадане вище, набуває великого значення функціонування лімфоглоткового кільця у профілактиці захворювань ротової порожнини, а також важливість функціонування місцевого імунітету інших слизових оболонок організму (травного тракту, дихальної системи тощо) в контексті можливих патологічних змін у ротовій порожнині.
Висвітлення поверхневого захисту ротової порожнини буде неповним, якщо не згадати про важливу роль малих лімфоцитів, які містяться в слизових оболонках. Вони регулюють швидкість мітозу клітин базального шару, їх дозрівання, а також зроговіння та злущування покривного епітелію (BJ.Underdown et al.,1986).
Отже, практично всі ланки імунної системи людини беруть участь в етіології та патогенезі захворювань ротової порожнини. Знання механізмів розвитку цих процесів дозволяє цілеспрямовано впливати на них під час лікування стоматологічних хвороб, а також під час проведення профілактичних заходів.
Карієс зубів у дітей
Карієс зубів (caries dentis) — це патологічний процес, що розвивається після прорізування зубів і характеризується демінералізацією та руйнуванням твердих тканин зубів з наступним утворенням дефекту у вигляді каріозної порожнини. Згідно з номенклатурою ВООЗ для оцінки ураженості зубів карієсом використовують три основних показники: поширеність, інтенсивність і приріст інтенсивності карієсу.
Поширеність карієсу — це співвідношення кількості осіб (у відсотках), які мають каріозні, пломбовані і видалені зуби, до загальної кількості обстежених. Поширеність карієсу у різні вікові періоди неоднакова Ця закономірність вщображена у віковій кривій карієсу (мал. 25). Каріозні ураження діагностуються у дітей віком від 1-1,5 року. У віці до 7-9 років поширеність карієсу зростає до 95-100%, у дітей 11-12 років знижується до 70-80% унаслідок фізіологічної зміни зубів і формування постійного прикусу. Починаючи з 13-14, років поширеність карієсу знову зростає.
Інтенсивність карієсу (індекс карієсу) — кількість каріозних пломбованих і видалених зубів у одного обстеженого. У дітей із тимча-
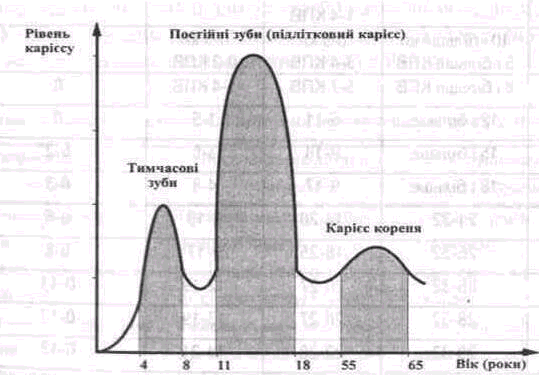
Мал. 25. Вікові періоди високого та низького приросту карієсу зубів
123
совим прикусом індекс карієсу позначають як "кп" (каріозні, пломбовані), тому що видалені тимчасові зуби не підлягають обліку. У дітей зі змінним прикусом індекс карієсу позначають як КПВ+кп (врахову-югься уражені карієсом як тимчасові, так і постійні зуби). У дітей із постійним прикусом індекс карієсу позначається як КПВ (каріозні, пломбовані, видалені).
Показники інтенсивності карієсу у дітей варіюють у зв'язку із впливом значної кількості як зовнішніх, так і внутрішніх чинників (табл. 18). Тому ВООЗ запропонувала враховувати інтенсивність карієсу у 12-річних дітей як основу для оцінки стану твердих тканин зубів. У цих дітей виділяють п'ять рівнів інтенсивності карієсу: дуже низь-
Таблиця 18. Оцінка інтенсивності карієсу зубів за віком (за умови зниженого вмісту фтору в питній воді)
Вік, роки |
Рівень карієсу |
|||
Дуже високий |
Високий |
Низький |
Стійкі до карієсу |
|
2 |
3 і більше |
2 |
0 |
0 |
3 |
6 |
2-5 |
1 |
0 |
4 |
9 |
3-8 |
2 |
0 |
5 |
9 і більше кп 1КПВ |
4-8 |
1-3 |
|
7 |
10 і більше кп |
7-9 кп 1-4 КПВ |
1-6 КП |
0 |
9 |
10 і більше кп 5 і більше КПВ |
6-9 кп 3-4 КПВ |
0-5 кп 0-2 КПВ |
0 |
11 |
8 і більше КПВ |
5-7 КПВ |
1-4КПВ |
0 |
13 |
12 і більше |
6-11 |
1-5 |
0 |
15 |
15 і більше |
9-14 |
3-8 |
0-2 |
17 |
18 і більше |
9-17 |
4-8 |
0-3 |
19 |
21-32 |
14-20 |
7-13 |
0-6 |
20-24 |
26-32 |
18-25 |
9-17 |
0-8 |
25-29 |
28-32 |
20-27 |
12-19 |
0-11 |
30-34 |
28-32 |
20-27 |
13-19 |
0-12 |
35-39 |
29-32 |
22-28 |
14-21 |
0-13 |
40-44 |
32 |
22-32 |
14-21 |
0-13 |
124
Карієс зубів у дітей
кий (0-1,1); низький (1,2-2,6); середній (2,7-4,4); високий (4,5-6,5); дуже високий (6,6 і вище).
Як показник іітгенсивності карієсу поряд з індексом карієсу, що враховує уражені і видалені зуби, застосовується індекс, який враховує кількість уражених карієсом поверхонь зубів — КПп. Для визначення цього індексу підраховується кількість уражених карієсом або запломбованих поверхонь зубів. Цей індекс точніше відображує динаміку каріозного процесу, що особливо важливо при визначенні ефективності профілактичних заходів.
Для оцінки саме цих процесів (динаміки розвитку карієсу та ефективності його профілактики) застосовується показник приросту інтенсивності-карієсу. Для цього визначають інтенсивність карієсу (за індексом карієсу зубів або за індексом карієсу поверхонь) у однієї і тієї ж особи або контингенту через певний період (1-3-5 років). Різниця у значенні показника між другим і першим обстеженнями становить приріст інтенсивності карієсу.
Етіологія і патогенез. З початку розвитку стоматології налічується понад 400 теорій походження карієсу. Найвідомішими з них є хіміко-паразитарна теорія Міллєра (1884), фізико-хімічна теорія Д.А.Ентіна (1928), трофічна теорія І.ГЛукомського (1948), теорія А.Е.Шарпенака (1949), концепція зустрічних дій на пульпу зуба АЛ.Рибакова (1971). Проте жодна із цих теорій не дає вичерпної відповіді на всі питання щодо етіології і патогенезу карієсу зубів.
У табл. 19 подано деякі чинники загального та місцевого характеру, які спричинюють виникнення карієсу у дітей.
Таблиця 19. Загальні та місцеві причини виникнення карієсу у дітей
Загальні карієсогенні чинники |
Місцеві карієсогенні чинники |
Порушена резистентність зубних тканин |
Неповноцінне харчу |
Патогенна мікрофлора |
Неповноцінна |
вання; |
зубного нальоту; |
структура; |
низький вміст фтору в |
зміна кількісного та |
відхилення у хімічному |
питній воді; |
якісного складу слини; |
складі; |
соматичні ахворювання |
вживання харчових про |
спадкова схильність до |
дитини; |
дуктів з великим вмістом |
карієсу |
екстремальні впливи |
рафінованих вуглеводів |
|
125
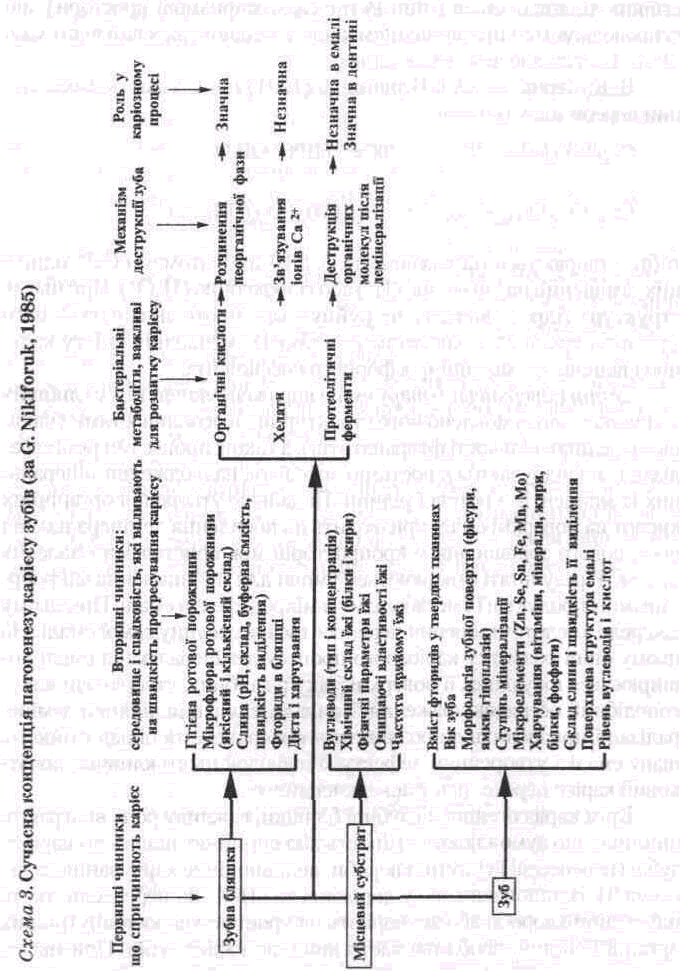
За сучасними уявленнями, розвиток карієсу відбувається внаслідок складної взаємодії зовнішніх і внутрішніх чинників, що реалізується в системі мікроорганізм — слина — структура емалі (мал. 26).
Дію цих чинників легше з'ясувати, якщо нормальний стан емалі розглядати як динамічну рівновагу між постійними процесами де- і ремінералізацп. У тому разі, коли в зубних тканинах процеси деміне-ралізації переважають над ремінералізацією, виникає ділянка демі-нералізаціі у вигляді каріозної плями. Подальше прогресування процесу деміїїералізації емалі і дентину призводить до утворення каріозної порожнини.
Відомо, що розвиток карієсу зубів пов'язаний з мікрофлорою, серед якої провідну роль відіграють стрептококи, особливо Str. mutans. Етіологічна роль мікроорганізмів у розвитку карієсу зубів доведена в експериментах на гнотобіотичних тваринах, у яких карієс не виникав незважаючи на тривале перебування на карієсогенній дієті. Уведення в карієсогенну їжу звичайної мікрофлори з ротової порожнини людини незмінне призводило до розвитку карієсу в експериментальних тварин.
Карієсогенну дію мікроорганізмів пов'язують з утворенням ними зубної бляшки. Вона є конгломератом, основу якого становлять мікроорганізми, фіксовані на полісахаридній стромі, що різною мірою насичена мінеральними речовинами. Зубна бляшка щільно прилягає до поверхні зуба і розташовується над пелікулою — тонкою органічною плівкою, що вкриває емаль зуба. Зубна бляшка у більшості людей містить такі самі основні види мікроорганізмів у різному співвідношенні (табл. 20). При цьому на долю стрептококів (mutans,
Таблиця 20. Мікрофлора зубної бляшки (за Ch. Moutoun, 1993)
Вид мікроорганізмів |
Відсоток від загальної КІЛЬКОСТІ |
Частота виділення, % |
Стрептококи |
17-38 |
100 |
Грам (+) палички |
22-52 |
100 |
Neissena |
0-2 |
99 |
Грам (-) анаеробні палички |
1-13 |
94 |
Fusobactena |
0-17 |
98 |
Veilonella |
0-7 |
55 |
126
salivarius, mitis, sangvis) припадає близько 40% від загальної кількості мікроорганізмів бляшки. Найбільш карієсогенним е Str. mutans, який виробляє молочну кислоту тільки з глюкози, розщеплює маніт і сорбіт, утворює глікан із сахарози. Втрата здатності виробляти глікан веде до втрати вірулентності Str. mutans.
Утворення зубної бляшки відбувається в певній послідовності:
1) прикріплення бактерій до пелікули; 2) утворення зовнішньоклі-тинної структури (матриксу); 3) ріст бактерій та утворення зубного нальоту.
Існують різні механізми прикріплення бактерій до пелікули. LM.Silverstone (1980) вказує на наявність таких етапів у цьому процесі:
адсорбція мікромолекул;
хімічне прикріплення мобільних бактерій;
зворотна фіксація бактерій на поверхні;
незворотна їх фіксація;
розвиток вторинної мікрофлори.
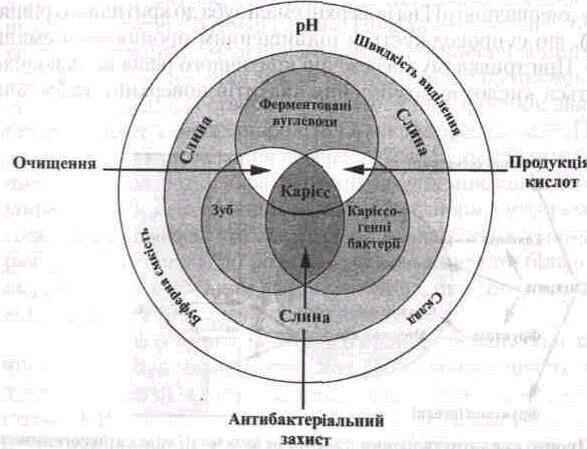
Мал. 26. Діаграма Keyes (1962), що відображує взаємодію між трьома основними етіологічними чинниками карієсу зубів
127
Цьому питанню приділяють велику увагу тому, що зменшення фіксації бактерій дозволить знизити карієсогенний потенціал на поверхні зуба.
Утворення матриксу пов'язане з діяльністю мікроорганізмів. Матрикс складається з двох компонентів: білків, переважно похідних від глікопротеїнів слини, і бактеріальних екстрацелюлярних полісахаридів (в основному полімерів вуглеводів).
Зі стовщенням і "дозріванням" у пористій і проникній для слини "молодій" зубній бляшці створюються анаеробні умови, які змінюють її мікробний склад. Утворення зубної бляшки значною мірою пов'язане з утилізацією бактеріями залишків їжі, що затримуються на поверхнях зубів. Найбільше бактерії використовують речовини, які легко проникають у бляшку: сахарозу, глюкозу, фруктозу, мальтозу, лактозу. Особливе значення надасться декстрану, тому що поряд зі значними адгезивними властивостями, потрібними для фіксації та росту зубної бляшки, цей полісахарид погано розчиняється і досить стійкий до мікроорганізмів.
Гліколіз вуглеводів (сахарози, глюкози, фруктози) сприяє локальному зменшенню рН на поверхні емалі зуба до критичного рівня (рН=5,0), що супроводжується підвищенням проникності емалі (мал. 27). При тривалому збереженні критичного рівня іонів водню відбувається кислотне розчинення апагитів поверхні в найменш
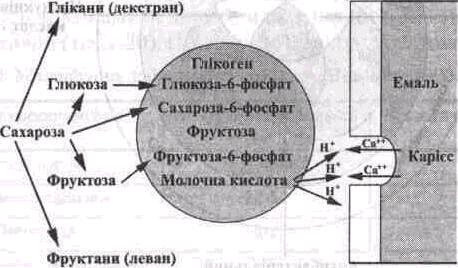
Мал. 27. Процес кислотоутворення внаслідок взаємодії між карієсогенними бактеріями та вуглеводами (сахароза). Переважання процесів демінералізації емалі в разі недостатності локальних механізмів нейтралізації кислот (за Ch. Moutoun,1993)
128
Карієс зубів у дітей
стійких ділянках емалі (лінії Ретціуса, міжпризмові простори), що супроводжується проникненням кислот у підповерхневий шар емалі з його наступною демінералізацією.
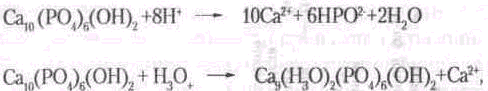
тобто угворюється гідроксіапатит не з 10, а з 9 атомами Са2^ один з них заміщений на іон водню (Н^ або гідроксонію (HgO^). При цьому структура гідроксіапатиту не руйнується, проте знижується його здатність протидіяти кислотам у зв'язку із зменшення вмісту кальцію і відповідно кальцій-фосфорного коефіцієнта.
Зміни поверхневого шару емалі виражені менше, ніж у глибших її ділянках, що зумовлено його структурними особливостями (наявністю великої кількості фторапатитів), а також процесами ремінера-лізації, які відбуваються постійно внаслідок надходження мінеральних компонентів з ротової рідини. Подальше утворення органічних кислот на поверхні емалі призводить до посилення демінералізації і поступового збільшення мікропросторів між кристалами емалевих призм. У результаті створюються умови для проникнення мікроорганізмів і продуктів їх метаболізму в мікродефекти емалі. При цьому джерело кислотоутворення переноситься всередину самої емалі. На цьому етапі розвитку каріозного процесу демінералізація емалі поширюється як уздовж її поверхні, так і в глибину, утворюючи конусоподібний осередок ураження. Тривале існування ділянки демінералізації призводить до розчинення поверхневого, більш стійкого, шару емалі з утворенням дефекту. Унаслідок цього клінічно початковий карієс переходить у поверхневий.
Крім карієсогенної дії зубної бляшки, важливу роль відіграють чинники, що зумовлюють стійкість або сприйнятливість до карієсу зубів (перенесені і супутні хвороби, неповноцінне харчування та ін.;
схема 3). Встановлено, що у дорослих та дітей, які перенесли гострі інфекційні хвороби або ж хворіють на хронічні хвороби внутрішніх органів і систем, особливо часто виникає карієс зубів. При цьому
129
130
ступінь ураженості карієсом не пов'язаний з тими чи іншими особливостями перенесеної або супутньої хвороби. Для різних хвороб, що супроводжуються підвищеною сприйнятливістю до карієсу, загальним с те, що вони характеризуються змінами у стані імунологічної реактивності організму. Ці зміни полягають насамперед у зниженні кількості та функціональної активності клітинних і гуморальних захисних чинників як у сироватці крові, так і в ротовій рідині Основним гуморальним чинником місцевої антиінфекційної резистентності слизової оболонки ротової порожнини є IgA, зокрема секреторні (S IgA). Вони перешкоджають адгезії мікроорганізмів до поверхні слизової оболонки ротової порожнини, а також до твердих тканин зубів. Крім того, S IgA слини можуть змінювати метаболізм мікроорганізмів, обмежувати утворення колоній, знижувати вірулентність збудників інфекції.
Розвиток карієсу зубів пов'язують із зменшенням кількості або відсутністю S IgA у слині. Проте ця точка зору поділяється не всіма дослідниками. Суперечливість даних щодо ролі S IgA в патогенезі карієсу пов'язана з тим, що система секреторного антитілоутворення лабільна і залежить від багатьох чинників місцевого та загального характеру (стать, вік, кліматичні умови тощо).
Хронічні хвороби внутрішніх органів і систем супроводжуються також змінами фізико-хімічних властивостей слини, зменшенням її захисного і ремінералізуючого потенціалу.
Стійкість зубів до карієсу визначається також складом і властивостями емалі. Структура емалі як тимчасових, так і постійних зубів зумовлюється насамперед генетичними чинниками, проте значною мірою залежить і від повноцінності процесів мінералізації емалі (як внутрішньощелепної, так і в ротовій порожнині). Відомо, що мінералізація тимчасових зубів практично повністю відбувається у внутрі-шньоутробний період, тому вирішальне значення має стан здоров'я матері у період вагітності. На стійкість тимчасових зубів до карієсу суттєво впливають токсикози вагітних, порушення вуглеводного обміну, хвороби щитоподібної залози, травного тракту, вірусні хвороби, хронічна гіпоксія та ін. У тимчасових зубах дітей, які народилися від матерів із зазначеною патологією у період вагітності, карієс виникає майже відразу після їх прорізування.
На одонтогенез тимчасових зубів, а отже, на структуру емалі
131
впливають такі чинники, як недоношеність вагітності, хвороби новонароджених і дітей 1-го року життя. Результати поляризаційно-оптичного і рентгеноструктурного аналізів тимчасових зубів свідчать, що при фізіологічному перебігу вагітності спостерігається повноцінна мінералізація їх емалі. При токсикозах вагітних (нефропатія, водянка, прееклампсія та ін.) в емалі тимчасових зубів у дітей виявляються окремі ділянки з неповноцінною мінералізацією. Ці ділянки зберігаються і в ранньому дитинстві, навіть у неушкоджених тимчасових зубах у вигляді гіпомінералізованих зон.
На мінералізацію постійних зубів у дітей, крім здоров'я матері, суттєво впливає і стан здоров'я самої дитини, тому що цей процес відбувається переважно в перші роки життя дитини. Характер і повноцінність харчування, супутні хвороби, функціональний стан травного тракту, вміст фтору в питній воді та інші чинники можуть відігравати вирішальну роль у формуванні карієс-резистентних або сприйнятливих до карієсу твердих тканин зубів.
Встановлено (В.Р.Окушко та снівавт., 1989), що розчинність емалі зубів залежить від функціонального стану пульпи, зі змінами якого пов'язують стійкість зубів до карієсу. Такі властивості емалі, як її значна твердість і низька розчинність, забезпечуються лише за умови збереження високої функціональної активності пульпи. Можливо, що розбіжності у функціональному стані ііульпи на різних етапах розвитку тимчасових і постійних зубів зумовлюють особливості розвитку і перебігу карієсу у дітей.
Функціональна активність пульпи значною мірою пов'язана із соматичним станом дитини. Хронічні хвороби внутрішніх органів і систем організму можуть призвести до зниження функціональної активності пульпи, підвищуючи таким чином сприйнятливість емалі до карієсу та зумовлюючи агресивність його перебігу.
Слина формує середовище, в якому після прорізування зуби знаходяться постійно.
Слина виконує багато функцій: вона бере участь у процесах самоочищення ротової порожнини і зубів; має певну буферну ємкість, іцо дозволяє нормалізувати рівень рН у ротовій порожнині в разі його зниження; є перенасиченим розчином щодо вмісту іонів кальцію і фосфору, а тому є джерелом надходження цих та інших іонів до емалі, забезпечуючи процеси мінералізації та ремінералізації.
132
Стійкість зубів до карієсу безпосередньо пов'язана зі складом і властивостями слини. У осіб, сприйнятливих до карієсу, спостерігається зменшення швидкості виділення слини, відхилення в її мінеральному складі та зниження антибактеріальних властивостей. Подібні зміни виявляються в слині при патологічних станах, неповноцінному харчуванні та за інших умов, коли зуби піддаються інтенсивному ураженню карієсом.
Класифікація. У дитячій стоматології послуговуються загальноприйнятою класифікацією карієсу, яка характеризує ураження зубів за характером перебігу, глибиною та локалізацією.
І. За локалізацією: фісурний (caries fissuralis); апроксимальний
(caries aproxsimalis); пришийковий (caries cervicalis); поєднаної
локалізації (щічної, губної, язикової поверхонь).
II. За глибиною ураження: початковий (caries incipiens); поверхневий (caries superficialis); середній (caries media); глибокий (caries profunda).
III. За характером клінічного перебігу: гострий (caries acuta);
хронічний (caries chronica).
IV. За послідовністю виникнення: первинний (caries primaria);
вторинний, або рецидивуючий (caries secundaria, seu recidiva). Поряд з характеристикою каріозного ураження в одному окремо взятому зубі запропоновано (Т.Ф.Виноградова, 1978) оцінювати активність каріозного процесу в організмі в цілому. При цьому автор виділяє три ступеня активності хвороби: І — компенсований карієс;
II — субкомпенсований, III — декомпенсований (табл. 21).
Розподіл дітей на групи відповідно до ступеня активності каріозного процесу має важливе значення в організації стоматологічного
Таблиця 21. Оцінка інтенсивності каріозного процесу (за Т. Ф. Виноградовою, 1978)
Вік дитини, роки |
Показники інтенсивності карієсу залежно від ступеня активності |
||
І — компенсована форма (КПВ+кп) |
II — субкомпенсована форма (КПВ+кп) |
III — декомпенсована форма (КПВ+кп) |
|
7-Ю |
До 5 зубів |
До 4 зубів |
До 6 зубів |
11-14 |
6-8 зубів |
5-8 зубів |
7-9 зубів |
15-18 |
Більше ніж 8 зубів |
Більше ніж 8 зубів |
Більше ніж 9 зубів |
133
обслуговування дитячого населення, зокрема під час проведення санаційних і профілактичних заходів. Слід враховувати, що глибина карієсу у дітей є умовною величиною, яка залежить не тільки від розмірів каріозної порожнини, а й від об'єму пультової камери. Чим "молодший" зуб, тим більший об'єм його пультової камери і тим порівняно глибшим є карієс.
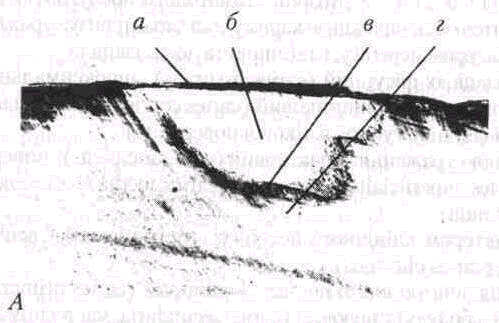
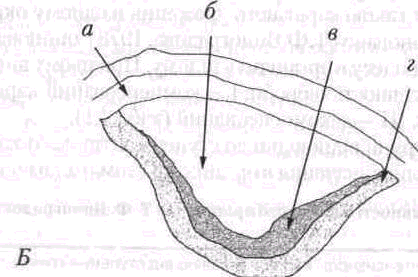
Малюнок 28. Поперечний розріз осередка початкового карієсу (saL. M. Silverstone, 1981).
й — поверхневий шар; б— тіло ураження; в — темна зона; / — зона гіпермі-нералізованої емалі.
А — вигляд у поляризаційному мікроскопі; Б — схематичне зображення па-томорфологічних зон в емалі.
134
Патологічна морфологія карієсу зубів. У стадії білої плями, або початкового карієсу, при поляризаційній мікроскопії виявляється осередок ураження емалі у вигляді трикутника, основа якого поверненадо зовнішньої поверхні емалі (С.М. Studevant, 1995;
мал. 28). У ньому розрізняють чотири зони: 1-ша — поверхнева зона, 2-га — тіло ураження, 3-тя — темна зона, 4-та — прозора зона.
Прозора зона розташована найглибше. Це зона гіпермінералізо-ваної емалі. У ній пори і пустоти розташовані вздовж емалевих призм. Об'єм пор у прозорій зоні становить 1%, що в 10 разів вище, ніж в інтактній емалі.
Темна зона називається так тому, що не пропускає поляризоване світло. У ній є велика кількість найдрібніших мікропросторів, заповнених повітрям або газоподібними речовинами, що і с причиною поглинання поляризованого світла. Об'єм пор у темній зоні становить від 2 до 4%. Відзначається втрата кристалічної структури емалі. Ширина темної зони залежить від інтенсивності процесів ремінера-лізації, при цьому вона може збільшуватися.
Тіло ураження — найбільша за об'ємом зона з ознаками явної де-мінералізації. Об'єм пор становить від 5% на периферії до 25% у центрі зони. У ній можуть містититись бактерії, тому що розмір мікропросторів в емалі достатній для проникнення їх углиб. Розчинення емалі відбувається вздовж ліній Речціуса, оскільки простори вздовж них відносно мало мінералізовані.
Поверхнева зона майже не уражена карієсом. Об'єм пор у ній невеликий порівняно з тілом ураження (меііше У/о), а мікрорентге-нологічно вона не відрізняється від неушкодженої емалі.
Поверхня інтактної емалі гіпермінералізована внаслідок постійного контакту зі слиною, а підвищений вміст іону фтору в поверхневому шарі емалі робить її більш стійкою до каріозного ушкодження порівняно з розташованими глибше шарами. Проте прогресування каріозного процесу призводить до утворення в поверхневому шарі емалі конусоподібних дефектів, крізь які бактерії можуть надходити усередину емалі.
Численні електронно-мікроскопічні дослідження емалі на різних етапах розвитку каріозної плями виявили порушення орієнтації кристалів гідроксіапатиту, зміну їх форми та розміру, утворення нетипових для нормальної емалі кристалів.
135
При початковому карієсі спостерігаються також зміни в пульпі зуба: дезорганізація шару одонтобластів, зміни їх паростків і гомогенізація цитоплазми, а також жирові переродження клітин сполучної тканини і зміни позаклітинної речовини пульпи.
При поверхневому і середньому карієсі виявляються деструктивні та реактивні зміни емалі і дентину.
Емалево-дентинне сполучення найменш стійке до каріозного ураження, тому карієс у цьому місці швидко поширюється і каріозне вогнище в дентині має V-подібний вигляд з вершиною, спрямованою в бік пульпи (С.М. Studevant, 1995; мал. 29). Цим можна пояснити швидке поширення карієсу в зубах у дітей по площині (так званий площинний карієс тимчасових зубів).
Пульпово-дентинний комплекс реагує на каріозне ураження посиленням мінералізації дентину з метою блокування дентинних канальців. Ця реакція є результатом посилення функціональної активності одонтобластів у відповідь на процеси демінералізації. Розрізняють 3 типи реагування дентину на каріозний процес: 1) реакція на тривалий, повільно прогресуючий процес із низьким рівнем кислотної демінералізації; 2) реакція на помірно-інтенсивний процес;
3) реакція на активний, швидко прогресуючий каріозний процес із високим рівнем кислотної демінералізації.

Мал. 29. Схематичне зображення карієсу жувальної поверхні (за С. М. Studevant, 1995). Емаль на жувальній поверхні видається інтактною, тому що каріозна порожнина має точковий вхідний отвір у фісурі. У каріозній порожнині міститься велика кількість стрептококів і лактобацил. Верхні шари дентину інфіковані ними. Нижні шари дентину ще не інфіковані, але значно демінералізовані. Замісний (репаративний) дентин починає формуватися відповідно до зони ураження
136
Визначальним чинником у здійсненні захисних перетворень у дентині с житгєздатна пульпа з достатнім рівнем мікроциркуляції та кровообігу.
У разі повільного перебігу карієсу пульпа може відновлювати демінералізований дентин шляхом ремінералізації інтертубулярно-го дентину. Дентин, що містить більшу кількість мінеральних речовин порівняно з інтактним, називається склерозованим. Він є бар'єром для поглиблення каріозного процесу, тому що дентинні канальці в ньому майже повністю заблоковані.
Другий тип реагування дентину визначається при помірному прогресуванні каріозного процесу. При цьому в дентині міститься значна кількість патогенних чинників, таких як мікроорганізми, продукти їх життєдіяльності, гідролітичні ферменти, залишки бактеріальних клітин, що можуть призводити до дегенерації і загибелі одонтобластів та їх відростків у зоні ураження і спричинити подразнення пульпи. Зруйновані дентинні канальці формують так звані мертві шляхи в дентині. У пульпі під дією речовин, що надходять через ці шляхи з дентину, утворюються вторинні або так звані замісні одон-тобласти (з недиференційованих мезенхімальних клітин). Ці клітини продукують репаративний (реактивний) дентин з боку пульпи відповідно до каріозного осередку (мал. ЗО). Цей дентин відрізняється від вторинного дентину, що його продукують одонтобласти пульпи протягом усього життя. Найчастіше структура репаративного дентину ірегулярна і аморфна. Дентинні канальці в ньому розташовані без певної орієнтації.
Третій тип реагування дентину виявляється при гострому, швидко прогресуючому карієсі з високим рівнем кислотоутворення. Якщо сила дії руйнівних чинників значно перевищує захисні можливості дентину та пульпи, в такому разі неминуче відбувається інфікування і запалення пульпи.
У дентині каріозного зуба розрізняють 5 зон патоморфологіч-них змін, які більш чітко простежуються при повільному прогресуванні карієсу, тобто при хронічному його перебігу.
Перша зона, розташована найглибше — це зона нормального ден-тину.У ній є дентинні канальці з відростками одонтобластів, у каналь-цях немає кристалів і бактерій.
137
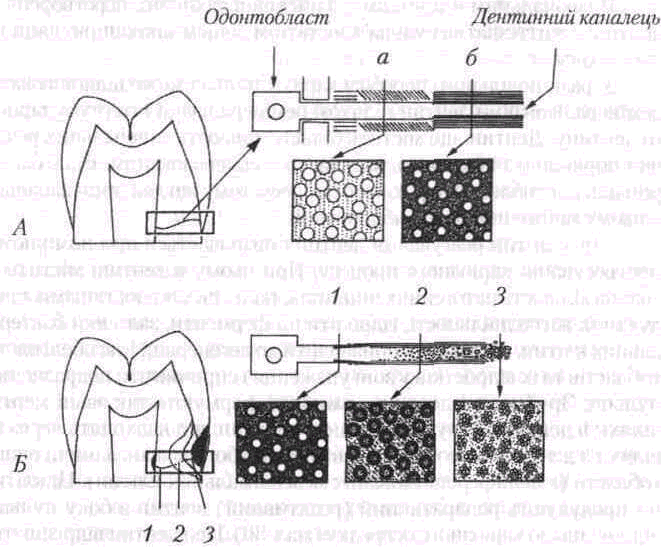
Мал. ЗО. Схематичне зображення інтактного каріозного дентину (за С. М. Studevant, 1995). А. — інтактний дентин:
й — припульповий дентин характеризується широкими дентииними каналь-цями, відсутністю перитубулярного дентину, слабкою мінералізацією інтер-тубулярного дентину; б — у шарах дентину, розташованих далі від пульпи, дентинпі канальці вужчі, вони оточені перитубулярним дентином, інтертубу-лярний дентин рівномірно мінералізований. Б — каріозний дентин:
1 — зона нормального дентину, що розташований біля пульпи. Характеризується деяким звуженням дентинних канальців унаслідок процесів гіпермі-нералізації; 2 — зона ушкодженого каріозного дентину. Характеризується втратою мінеральних речовин інтертубулярним та перитубулярним дентином. Проте бактерії в ньому відсутні. Накопичення кристалів мінеральних речовин відбувається у просвіті дентинних канальців. Це зона прозорого дентину; 3 — зона інфікованого каріозного дентину. Характеризується значною кількістю мікроорганізмів у дентинних канальцях і руйнуванням органічних структур дентину . ,.,„
loo
Друга зона — напівпрозорий дентин. Це зона демшералізацп інтертубулярного дентину і початку формування дуже тонких кристалів у просвіті канальців Помітні ушкодження відростків одонто-бластів, проте бактерій у канальцях немає.
Третя зона — прозорий дентин. Цей шар дентину характеризується подальшою втратою мінеральних речовин інтертубулярним дентином і відкладенням великих кристалів у просвіті канальців. Він м'якший порівняно з інтактним дентином. Бактерій немає. Колагенові волокна зберігають свою структуру, тому можливе самовіднов-лення цього дентину при живій пульпі.
Четверта зона — це зона дентину з порушеною гістологічною структурою. Характеризує гься розширенням і викривленням дентинних канальців, які заповнені великою кількістю мікроорганізмів. У ньому дуже мало мінеральних речовин, а колагенові волокна повністю зруйновані.
П'ята зона — інфікований дет ин. Це зона зруйнованого дентину, просякнутою великою кількістю бактерій. Структура дентину не визначається, оскільки відсутні мінеральні речовини і колагенові волокна.
При середньому карієсі відбуваються певні зміни в пульпі. Шар одонтобластів стоншений, вакуолізований. Під електронним мікроскопом в одонтобластах виявляються збільшені мітохондрп і слаб-корозвинена ендоплазматична сітка.
При глибокому карієсі, особливо у разі його гострого перебігу, відсугні зона прозорого (склерозованого) дентину і зона інтактного дентину. Дентин дна каріозної порожнини значно демінералізований з різним ступенем дегенеративних змін органічної речовини При цьому в пульпі виявляються значні зміни, які багагьма авторами ототожнюються із початковими фазами запалення (гіперемія пульпи).
139
