
- •Аналитическая химия и физико-химические методы анализа
- •Часть I содержит вопросы качественного анализа катионов и анионов.
- •Синий осадок «берлинской лазури»
- •Классификация анионов
- •Анализ качественного состава раствора
- •Предварительные испытания
- •Осадок PbCrO4 легко растворяет в растворах щелочей:
- •Хроматографический качественный анализ
- •Работа № 2 Качественное определение ионов железа, меди, кобальта и никеля в молоке методом тонкослойной хроматографии
- •Работа № 3 обнаружение анионов дробным методом
- •Вопросы для самопроверки
- •Часть II. К о л и ч е с т в е н н ы й а н а л и з
- •Работа № 4 Определение содержания серной кислоты
- •Перманганатометрия
- •Перманганатометрия работа№ 5 Определение содержания железа (II) в растворе соли Мора
- •Приготовление первичного стандартного раствора щавелевой
- •Установление концентрации раствора перманганата калия
- •Определение содержания железа (II) в растворе соли Мора
- •Иодометрия
- •Иодометрия работа № 6 Определение содержания меди (II) в растворе медного купороса
- •Приготовление первичного стандартного раствора дихромата калия.
- •Установление концентрации раствора тиосульфата натрия
- •3. Определение содержания Cu(II) в растворе медного купороса
- •Осадительное титрование
- •Аргентометрия
- •Работа № 7
- •Определение содержания NaCl в в растворе
- •(Обратное титрование по Фольгарду)
- •Работа № 8 Определение жесткости воды
- •Приготовление первичного стандартного раствора MgSo4
- •Вопросы для самопроверки
- •Часть III. Физико-химические методы анализа
- •Работа 9.1. Определение рН вина, сока (активной кислотности)
- •Работа № 9.2. Потенциометрическое определение титруемой кислотности вина (сока)
- •Ионометрический метод анализа
- •Работа № 10 Определение нитратов в экстрактах пищевого сырья
- •Работа № 11 определение содержания кислоты в растворе Приборы и материалы
- •Выполнение работы
- •Техника определения
- •Вопросы для самопроверки
- •Оптические методы анализа Спектральный анализ
- •Работа № 12 Определение содержания хрома и марганца на стилоскопе
- •Выполнение работы
- •Отождествление спектральных линий с помощью дисперсионной кривой
- •Полуколичественный спектральный анализ
- •Полуколичественный спектральный анализ
- •Количественный спектральный анализ
- •Работа № 13 Определение содержания ионов натрия, калия и кальция пламенно-фотометрическим методом
- •Выполнение работы
- •Приготовление эталонных растворов
- •Фотоэлектроколориметрический метод анализа
- •Работа № 14 Фотоколориметрические определение железа в белых винах
- •Выполнение работы
- •Построение градуированной кривой
- •Анализ вина
- •Люминесцентный анализ Флуориметрический метод
- •Работа № 15 определение витамина в2 (рибофламина) в драже или таблетках флуориметрическим методом
- •Построение градуировочной кривой
- •Измерение флуоресценции на флуориметре эф – зма
- •Расчет содержания рибофлавина в таблетках
- •Рефрактометрический анализ
- •Величину n2(отн.) называют относительным коэффициентом преломления второй среды по отношению к первой. Показатель преломления по отношению к вакууму называют абсолютным показателем преломления:
- •Работа № 16 Определение сухих веществ в сахарном сиропе на рефрактометре
- •Выполнение работы
- •Построение градуировочной кривой
- •Концентрация сухих веществ с%
- •Хроматографический количественный анализ
- •Работа № 17 Анализ смеси полисахарида и нитрата кобальта методом гельхроматографии
- •Выполнение работы
- •Спектрометрический анализ полисахарида на спектрофотометре
- •Вопросы для самопроверки:
- •Литература
- •Дополнительная литература:
Выполнение работы
Приборы: 1. Коллектор хроматографических фракций с дозатором объема фракции по времени или по числу капель. 2. Перистальтический насос для перекачки (с заданной скоростью) выходящего из колонки элюента к коллектору. 3. Штатив для колонки. 4. Спектрофотометр. 5. Кондуктометр.
Посуда: 1. Стеклянная хроматографическая колонка, длиной 20-25 см, диаметром 1,5-2 см. 2. Резиновая пробка с ниппелем и зажимом.3. Стеклянный стакан на 200 см3.4. Стеклянная пипетка на 10 см3. 5. Промывалка для дистиллированной воды. 6. Пробирки к коллектору для сбора фракций – 20 шт.
Реактивы: 1. Адсорбент – набухший в воде полисахаридный гель, в объеме 100 см3. 2. 1% раствор AgNO3 в объеме ~ 5 см3. 3. Исследуемый образец водный раствор смеси полисахарида (голубого декстрана) и нитрата кобальта в объеме ~ 5 см3. 4. Фильтровальная бумага.
Гельхроматографическое разделение исследуемой смеси.
Вымытую стеклянную колонку плотно закрывают с нижнего конца резиновой пробкой с ниппелем в ней и устанавливают в штативе.
Во избежание просачивания геля пробирку изнутри накрывают кружочком фильтровальной бумаги. Вначале заполняют колонку на 1/3 высоты дистиллированной водой, а затем постепенно вливают из стакана набухший в воде гель адсорбента на 3 см. ниже верхнего отверстия и закрывают ниппель зажимом.
Подготовленный для разделения раствор смеси осторожно наносят пипеткой на обнажившийся верхний слой адсорбента и присоединяют к нижнему отверстию ниппеля полиэтиленовый шланг, идущий к перистальтическому насосу и далее к коллектору фракций.
Дождавшись полного впитывания нанесенного на адсорбент раствора через верхнее отверстие осторожно наносят пипеткой 2-3 см3 дистиллированной воды и включают насос на нужный режим элюирования. Затем верхнее отверстие колонки соединяют резиновым шлангом с резервуаром, наполненным дистиллированной водой и далее весь процесс идет уже автоматически.
Перемещение голубого кольца декстрана вниз по колонке хорошо заметно. Весь процесс разделения смеси полисахарид – нитрат кобальта при заданной скорости элюирования занимает 40-50 мин, за которые в коллектор собирается 15 фракций, т.е. 1 фракция за 3 минуты.
Каждую из фракций анализируют спектрофотометрически на присутствие полисахарида, и кондуктометрически на присутствие нитрата кобальта.
Спектрометрический анализ полисахарида на спектрофотометре
Включают прибор и выдерживают его 3 минуты для выравнивания силы тока до 300 микроампер, затем включают излучающую водородную лампу и дожидаются загорания (со щелчком). Затем открывают крышку кюветодержателя (объектив фотоэлемента закрыт), поворачивают рукоятку видов работ в положение “on” – “включено” (положение “off” – “выключено”) и выдерживают 10 минут. Рукояткой регулировки длины волны “wavelength” – устанавливают соответствующий образцу узкий интервал со значением “λ” = 280 нм. Выдвижными ручками регулируют установку системы из двух фотоэлементов (одного для УФ – диапазона, другого для видимого ИК диапазона). Рукояткой “Durk-current” стабилизируют ультрафиолетовое излучение выбранного диапазона (“темновой” ток), фиксируя стрелку нуль прибора в среднем положении. Затем измеряют оптическую плотность “D” раствора. Кювету с растворителем помещают в кюветодержатель, закрывают его крышку (объектив фотоэлемента открыт для измерения). Рукоятку видов работ переключают из положения “on” в положение “ x I”, а рукоятку отсчета “reading” в положение ноль. Рукояткой “щель” – “slit” (узкая полоса диапазона) вначале грубо переводят стрелку нуль – прибора в положение 0, а рукояткой чувствительности производят точную доводку стрелки шкалы до 0, снимая после этого со шкалы отсчета “reading” значение оптической плотности “D” образца. Затем последовательно анализируют фракции элюента из колонки и строят график изменения оптической плотности “D” (полисахарид) в ходе хроматографирования, откладывая на оси абсцисс номера фракции, а на оси ординат – оптическую плотность “D” (рис. 18). Из графика следует, что вещество, поглощающее ультрафиолетовое излучение с длиной волны “λ” = 280 нм, содержится во фракциях с № 6 по № 10.
Кондуктометрический анализ нитрата кобальта на кондуктометре ОК – 102/1.
Из-за чувствительности прибора к присутствию сильных электролитов электрод, состоящий из двух проводников – электродов, должен быть очищен от следов электролитов промыванием в дистиллированной воде. Затем измеряют поочередно электропроводность хроматографических фракций с разным содержанием нитрата кобальта и строят график (рис. 18).
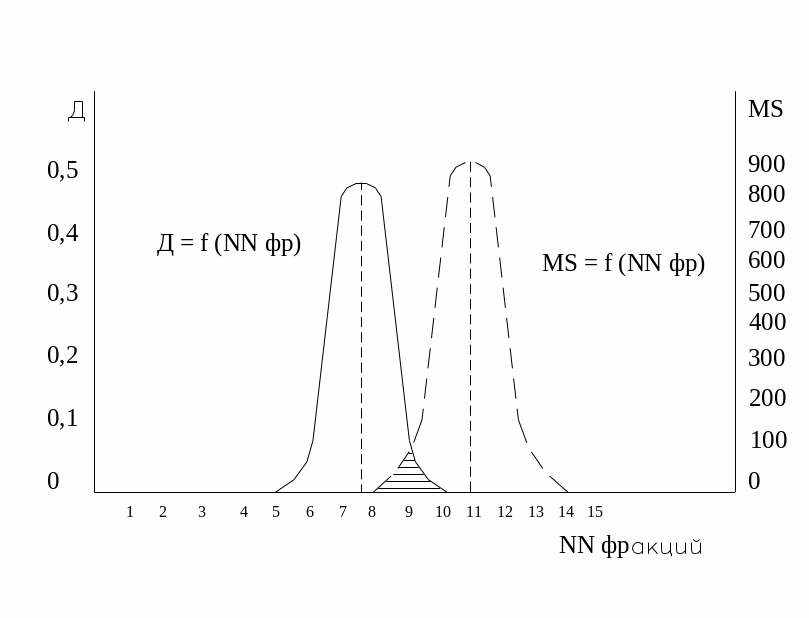
Рис. 18. Совмещенные графики оптической плотности и электропроводности (пунктиром) серии хроматографических фракций
Из графика следует, что фракции № 1-4 содержат чистый растворитель, фракции № 5-8 содержат лишь полисахарид, фракции № 10-12 содержат лишь Co(NO3)2, фракция № 9 содержит смесь обеих веществ (неполнота разделения).
