
- •Аналитическая химия и физико-химические методы анализа
- •Часть I содержит вопросы качественного анализа катионов и анионов.
- •Синий осадок «берлинской лазури»
- •Классификация анионов
- •Анализ качественного состава раствора
- •Предварительные испытания
- •Осадок PbCrO4 легко растворяет в растворах щелочей:
- •Хроматографический качественный анализ
- •Работа № 2 Качественное определение ионов железа, меди, кобальта и никеля в молоке методом тонкослойной хроматографии
- •Работа № 3 обнаружение анионов дробным методом
- •Вопросы для самопроверки
- •Часть II. К о л и ч е с т в е н н ы й а н а л и з
- •Работа № 4 Определение содержания серной кислоты
- •Перманганатометрия
- •Перманганатометрия работа№ 5 Определение содержания железа (II) в растворе соли Мора
- •Приготовление первичного стандартного раствора щавелевой
- •Установление концентрации раствора перманганата калия
- •Определение содержания железа (II) в растворе соли Мора
- •Иодометрия
- •Иодометрия работа № 6 Определение содержания меди (II) в растворе медного купороса
- •Приготовление первичного стандартного раствора дихромата калия.
- •Установление концентрации раствора тиосульфата натрия
- •3. Определение содержания Cu(II) в растворе медного купороса
- •Осадительное титрование
- •Аргентометрия
- •Работа № 7
- •Определение содержания NaCl в в растворе
- •(Обратное титрование по Фольгарду)
- •Работа № 8 Определение жесткости воды
- •Приготовление первичного стандартного раствора MgSo4
- •Вопросы для самопроверки
- •Часть III. Физико-химические методы анализа
- •Работа 9.1. Определение рН вина, сока (активной кислотности)
- •Работа № 9.2. Потенциометрическое определение титруемой кислотности вина (сока)
- •Ионометрический метод анализа
- •Работа № 10 Определение нитратов в экстрактах пищевого сырья
- •Работа № 11 определение содержания кислоты в растворе Приборы и материалы
- •Выполнение работы
- •Техника определения
- •Вопросы для самопроверки
- •Оптические методы анализа Спектральный анализ
- •Работа № 12 Определение содержания хрома и марганца на стилоскопе
- •Выполнение работы
- •Отождествление спектральных линий с помощью дисперсионной кривой
- •Полуколичественный спектральный анализ
- •Полуколичественный спектральный анализ
- •Количественный спектральный анализ
- •Работа № 13 Определение содержания ионов натрия, калия и кальция пламенно-фотометрическим методом
- •Выполнение работы
- •Приготовление эталонных растворов
- •Фотоэлектроколориметрический метод анализа
- •Работа № 14 Фотоколориметрические определение железа в белых винах
- •Выполнение работы
- •Построение градуированной кривой
- •Анализ вина
- •Люминесцентный анализ Флуориметрический метод
- •Работа № 15 определение витамина в2 (рибофламина) в драже или таблетках флуориметрическим методом
- •Построение градуировочной кривой
- •Измерение флуоресценции на флуориметре эф – зма
- •Расчет содержания рибофлавина в таблетках
- •Рефрактометрический анализ
- •Величину n2(отн.) называют относительным коэффициентом преломления второй среды по отношению к первой. Показатель преломления по отношению к вакууму называют абсолютным показателем преломления:
- •Работа № 16 Определение сухих веществ в сахарном сиропе на рефрактометре
- •Выполнение работы
- •Построение градуировочной кривой
- •Концентрация сухих веществ с%
- •Хроматографический количественный анализ
- •Работа № 17 Анализ смеси полисахарида и нитрата кобальта методом гельхроматографии
- •Выполнение работы
- •Спектрометрический анализ полисахарида на спектрофотометре
- •Вопросы для самопроверки:
- •Литература
- •Дополнительная литература:
Измерение флуоресценции на флуориметре эф – зма
1. Помещают в измерительную камеру пробирку с раствором IV. Проверяют настройку на нуль и нажав клавишу заслонки, устанавливают рукояткой стрелку на 80 делений.
2. Вынимают пробирку IV и, последовательно помещая в камеру пробирки I, II, III, IV, V и VII, измеряют интенсивность их лиминисценции дважды. Флуориметр должен работать не более 30 минут, после чего его выключают для охлаждения.
3. По величинам интенсивности стандартных растворов I, II, III, IV строят градуировочный график, имеющий прямолинейный характер.
4. Используя его определяют содержание рибофлавина в контрольном растворе (пробирка V). При удовлетворительных результатах (ошибка не должна превышать 2-3%) приступают к определению его в таблетках.
5. Проводят гашение люминесценции рибофлавина, предварительно повторив измерение растворов VI и VII. Для гашения восстанавливают рибофлавин гидросульфитом натрия. Добавляют в пробирки по 0,5 г гидросульфита, закрывают пробкой и перемешивают 30 сек.
6. Проверяют настройку прибора по стандартному раствору IV и снова измеряют свечение в прбирках VI и VII. Если стрелка прибора отклонилась на 0,5-1 деление, считают полученную ранее величину интенсивности правильной. При значительном отклонении стрелки его учитывают при содержании вещества.
Расчет содержания рибофлавина в таблетках
Содержание рибофлавина в мкг находят по градуировочному графику и, взяв среднее значение из двух определений, рассчитывают содержание В2 в таблетках (драже) по формуле:
Qрибофлавина = хмкг · 10-6 ·100см3,
где хмкг – количество В2 в 1 см3,
10-6 – фактор пересчета микрограмм в граммы
Рефрактометрический анализ
Рефрактометрия – исследование преломления света при прохождении луча через границу раздела прозрачных однородных сред и заключается в измерении показателя (или коэффициента) преломления исследуемого раствора, связанного с его концентрацией.
При падении луча света на границу раздела двух прозрачных сред от поверхности раздела и частичное отражение света от поверхности раздела и частичное распространение света в другой среде.
Направление луча во второй среде изменяется в соответствии с законом преломления:
n2(отн.)
![]() (1)
(1)
Величину n2(отн.) называют относительным коэффициентом преломления второй среды по отношению к первой. Показатель преломления по отношению к вакууму называют абсолютным показателем преломления:
n2(абс.)
=
![]()
относительный показатель преломления равен отношению абсолютных показателей преломления:
n(абс) · sinα1 = n2(абс) · sinα2
Относительный показатель преломления по отношению к воздуху называют просто показателем преломления n:
nабс. = nабс.(возд.) · n , поэтому
при атмосферном давлении и комнатной температуре nабс. = 1,00027.
При увеличении угла падения наступает момент, когда угол преломления окажется равным 90° - луч света будет скользить по поверхности раздела сред. Такой угол называется углом полного внутреннего отражения, или предельным, критическим углом.
Очевидно, что в этом случае преломления не произойдет, и поскольку sin 90° = 1, формула (1) переходит в n2(отн.) = sinα1 (2).
Уравнение (2) показывает, что по условию полного внутреннего отражения можно рассчитать показатель преломления. Это соотношение используют в практике рефрактометрии.
Показатель преломления зависит от длины волны падающего света, температуры. Температуру и длину волны света, при которой производится измерение, обычно указывают у символа “n”.
Например,
запись n![]() означает, показатель преломления измерен
при
означает, показатель преломления измерен
при
25°C для желтой D – линии натрия с длиной волны 589 нм. Показатель преломления и плотность вещества изменяются симбатно, т.е. с ростом плотности происходит увеличение показателя преломления. Установлено, что функция показателя преломления f(n) прямо пропорциональна плотности вещества d: f(n) = r · d;
r – коэффициент пропорциональности назвали удельной рефракцией. При умножении r на молярную массу M получают молярную рефракцию R
R = Mr
Величина рефракции (R), не зависит от внешних условий (температуры, давления и т.д.) для расчета рефракции используют формулу Лорентца–Лоренца
R
=
![]()
В органической химии широко используют правило аддитивности молярных рефракций, где молярная рефракция соединения равна сумме атомных рефракций элементов, образующих это соединение, а рефракция смеси равна сумме молярных рефракций ее составных частей, например:
RCCl![]() = RC +
4RCl
или RAB
= RA +
RB,
т.е. R смеси (А + В + С) = RACA +
RBСВ + RCСC
= RC +
4RCl
или RAB
= RA +
RB,
т.е. R смеси (А + В + С) = RACA +
RBСВ + RCСC
При градуировке прибора сразу устанавливают связь между углом наклона зрительной трубы и показателем преломления жидкости по шкале; деление шкалы одновременно наблюдается в поле зрения трубы (в окуляре). Если ось зрительной трубы установлена по направлению лучей, ограничивающих предельный угол преломления (лучи 0 на рисунке), то поле зрения разделится на светлую и темную половину (рис. 15).
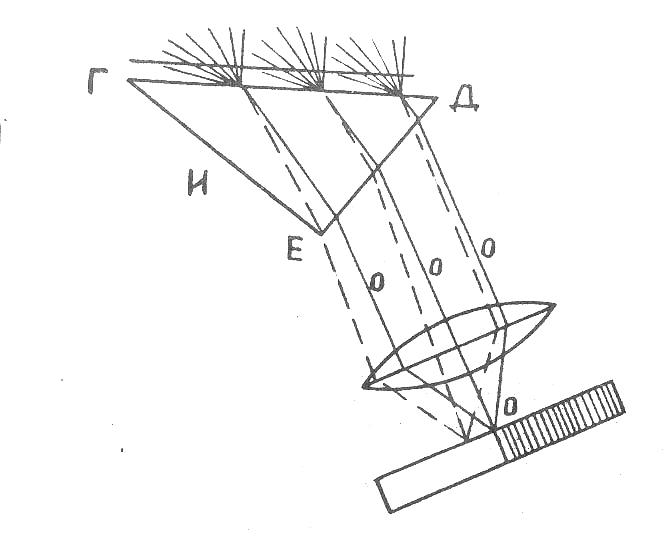
Рис. 15. Разделение поля зрения рефрактометра
на светлую и темную зоны
Положение границы раздела светлого и темного полей соответствует углу полного внутреннего отражения и связано с показателем преломления исследуемого вещества. В окуляр рефрактометра виден кружок с перекрещивающимися линиями. Он служит для установления границы раздела. Изменяя положение окуляра передвижением его рукояткой вдоль продолговатой прорези в передней крышке корпуса, надо добиться, чтобы точка перекрестия совпала с границей раздела светлого и темного полей. В прорези укреплена шкала показателей преломления nD. Цена деления этой шкалы равна 0,001, десятитысячные доли могут быть отсчитаны на глаз. Справа от шкалы nD расположена дополнительная шкала – “процент сухих веществ” – с делениями от 0 до 95% и ценой наименьшего деления от 0,2 до 50% и 0,1 - свыше 50% “сухих веществ”.
В поле зрения видны одновременно граничная линия, деления шкал и три визирных штриха. При помощи рукоятки визирные штрихи совмещают с граничной линией и производится отсчет делений шкалы nD (или % “сухих веществ”) (рис. 16).
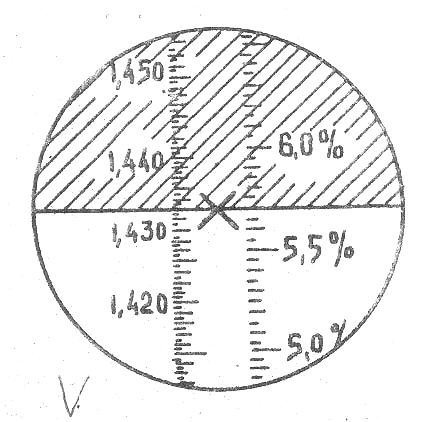
Рис. 16. Зрительное поле рефрактометра РЛ – 2 со шкалой показателей преломления и шкалой сухих веществ
