
- •Аналитическая химия и физико-химические методы анализа
- •Часть I содержит вопросы качественного анализа катионов и анионов.
- •Синий осадок «берлинской лазури»
- •Классификация анионов
- •Анализ качественного состава раствора
- •Предварительные испытания
- •Осадок PbCrO4 легко растворяет в растворах щелочей:
- •Хроматографический качественный анализ
- •Работа № 2 Качественное определение ионов железа, меди, кобальта и никеля в молоке методом тонкослойной хроматографии
- •Работа № 3 обнаружение анионов дробным методом
- •Вопросы для самопроверки
- •Часть II. К о л и ч е с т в е н н ы й а н а л и з
- •Работа № 4 Определение содержания серной кислоты
- •Перманганатометрия
- •Перманганатометрия работа№ 5 Определение содержания железа (II) в растворе соли Мора
- •Приготовление первичного стандартного раствора щавелевой
- •Установление концентрации раствора перманганата калия
- •Определение содержания железа (II) в растворе соли Мора
- •Иодометрия
- •Иодометрия работа № 6 Определение содержания меди (II) в растворе медного купороса
- •Приготовление первичного стандартного раствора дихромата калия.
- •Установление концентрации раствора тиосульфата натрия
- •3. Определение содержания Cu(II) в растворе медного купороса
- •Осадительное титрование
- •Аргентометрия
- •Работа № 7
- •Определение содержания NaCl в в растворе
- •(Обратное титрование по Фольгарду)
- •Работа № 8 Определение жесткости воды
- •Приготовление первичного стандартного раствора MgSo4
- •Вопросы для самопроверки
- •Часть III. Физико-химические методы анализа
- •Работа 9.1. Определение рН вина, сока (активной кислотности)
- •Работа № 9.2. Потенциометрическое определение титруемой кислотности вина (сока)
- •Ионометрический метод анализа
- •Работа № 10 Определение нитратов в экстрактах пищевого сырья
- •Работа № 11 определение содержания кислоты в растворе Приборы и материалы
- •Выполнение работы
- •Техника определения
- •Вопросы для самопроверки
- •Оптические методы анализа Спектральный анализ
- •Работа № 12 Определение содержания хрома и марганца на стилоскопе
- •Выполнение работы
- •Отождествление спектральных линий с помощью дисперсионной кривой
- •Полуколичественный спектральный анализ
- •Полуколичественный спектральный анализ
- •Количественный спектральный анализ
- •Работа № 13 Определение содержания ионов натрия, калия и кальция пламенно-фотометрическим методом
- •Выполнение работы
- •Приготовление эталонных растворов
- •Фотоэлектроколориметрический метод анализа
- •Работа № 14 Фотоколориметрические определение железа в белых винах
- •Выполнение работы
- •Построение градуированной кривой
- •Анализ вина
- •Люминесцентный анализ Флуориметрический метод
- •Работа № 15 определение витамина в2 (рибофламина) в драже или таблетках флуориметрическим методом
- •Построение градуировочной кривой
- •Измерение флуоресценции на флуориметре эф – зма
- •Расчет содержания рибофлавина в таблетках
- •Рефрактометрический анализ
- •Величину n2(отн.) называют относительным коэффициентом преломления второй среды по отношению к первой. Показатель преломления по отношению к вакууму называют абсолютным показателем преломления:
- •Работа № 16 Определение сухих веществ в сахарном сиропе на рефрактометре
- •Выполнение работы
- •Построение градуировочной кривой
- •Концентрация сухих веществ с%
- •Хроматографический количественный анализ
- •Работа № 17 Анализ смеси полисахарида и нитрата кобальта методом гельхроматографии
- •Выполнение работы
- •Спектрометрический анализ полисахарида на спектрофотометре
- •Вопросы для самопроверки:
- •Литература
- •Дополнительная литература:
Работа № 15 определение витамина в2 (рибофламина) в драже или таблетках флуориметрическим методом
Витамин В2, рибофлавин, содержится в мясе, рыбе, печени, молоке, яичном желтке и в растительных продуктах.
В организме человека витамин В2 участвует в углеводном и жировом обмене.
В аналитической химии используют рибофлавин в качестве абсорбционного флуоресцентного индикатора, наряду с эозином и флуоресцеином.
При восстановлении раствора рибофлавина гидросульфитом натрия происходит химическое гашение флуоресценции из-за превращения рибофлавина в бесцветное соединение.
Гашение флуоресценции при восстановлении рибофлавина используется при анализе его растворов, содержащих флуоресцеирующие примеси. Вначале измеряют суммарную интенсивность флуоресценции раствора, и после гашения свечения рибофлавина восстановлением NaHSO3 измеряют остаточное свечение примесей; по разности общего и остаточного свечения определяют свечение рибофлавина.
Количественное определение витамина В2 заключается в построении с помощью стандартных растворов градуировочной кривой в координатах: содержание рибофлавина в мкг (ось абсцисс) - интенсивность флуоресценции (ось ординат).
После определения по графику содержания рибофлавина в исследуемом растворе его проверяют на присутствие примесей путем гашения свечения рибофлавина гидросульфитом натрия и измерение остаточной флуоресценции.
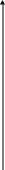 Y
Y





С
Используемый в Концентрационное
анализе диапазон гашение
концентраций флуоресценции
от
10-4
до 10-7
![]()
(при больших
концентрациях)
Рис. 14
Кривая зависимости интенсивности
флуоресценции от концентрации вещества.
Выполнение работы
Построение градуировочной кривой
Приготовление стандартных растворов
1. Отбирают мерной пипеткой 20 см3 раствора № 1, содержащего 20 мкг рибофлавина в 1 см3, помещают в мерную колбу на 100 см3, доводят дистиллированной водой до метки, закрывают пробкой и перемешивают. Исходный раствор № 2 содержит 4 мкг/см3 рибофлавина.
Для приготовления стандартных растворов в 4 мерные колбы на 100 см3 бюреткой отмеривают порции раствора №2 и доводят до метки дистиллированной водой:
№ колбы |
Раствор в см3 |
Содержание рибофлавина в мкг/см3 |
1 |
5,0 |
0,2 |
2 |
10,0 |
0,4 |
3 |
15,0 |
0,6 |
4 |
20,0 |
0,8 |
5 контрольный раствор |
х |
х выдает преподаватель |
3. Растворы перемешивают, переливают в измерительные пробирки и ставят в гнезде ящика для защиты от света.
4. Приготовляют раствор рибофлавина из таблетки, полученной от лаборанта. Для этого помещают таблетку в мерную колбу на 100 см3,добавляют горячей (70-80° C) дистиллированной воды до 2/3 объема и растворяют таблетку. Охлаждают колбу до комнатной температуры и заполняют дистиллированной водой до метки, закрывают пробкой и перемешивают. Отбирают пипеткой 3 см3 этого раствора в мерную колбу на 100 см3 № 6, добавляют дистиллированной воды до метки и перемешивают. Из колбы № 6 раствор переливают в пробирку № 6 и ставят в гнездо ящика.
