
- •Химическая технология неорганических веществ. Основные производства
- •Химическая технология неорганических веществ. Основные производства
- •Предисловие
- •Лекции №1-2 получение синтетического аммиака
- •1. Общие сведения.
- •1.1.Свойства аммиака.
- •1.2. Значение и применение аммиака.
- •2.Физико-химические основы синтеза аммиака.
- •3. Технологическая схема синтеза аммиака при среднем давлении.
- •4. Основные направления развития производства аммиака.
- •Лекции №3-4 химия и технология азотной кислоты.
- •1.Общие сведения.
- •1.1.Физические свойства Диаграммы состояния.
- •1.2. Химические свойства.
- •1.4. Применение азотной кислоты.
- •1.5. Способы получения азотной кислоты.
- •2. Получение неконцентрированной азотной кислоты из аммиака (химические уравнения и стадии).
- •3. Физико-химические основы процесса окисления аммиака.
- •3.1. Химические уравнения процесса окисления аммиака и их анализ.
- •3.2. Выбор оптимальных условий процесса окисления аммиака.
- •3.2.1. Катализаторы процесса окисления аммиака.
- •3.2.2. Скорость окисления аммиака.
- •3.2.3. Определение оптимальной температуры.
- •3.2.4. Определение оптимального давления процесса.
- •3.2.5. Состав газовой смеси.
- •4. Физико-химические основы процесса окисления нитрозных газов (no в no2).
- •5. Физико-химические основы процесса поглощения оксидов азота водой.
- •6. Очистка отходящих газов.
- •Лекция № 5 Получение неконцентрированной азотной кислоты в промышленности.
- •1. Основные операции и принципиальная схема.
- •2. Технологические схемы производства неконцентрированной азотной кислоты.
- •3. Принципиальная технологическая схема получения неконцентрированной азотной кислоты под повышенным давлением
- •Лекция № 6 Получение концентрированной азотной кислоты.
- •1. Общая характеристика методов получения концентрированной азотной кислоты.
- •2. Получение концентрированной азотной кислоты из разбавленных растворов.
- •3. Прямой синтез концентрированной азотной кислоты.
- •3.2. Основные стадии.
- •3.3. Технологическая схема производства концентрированной азотной кислоты прямым синтезом.
- •Лекция № 7 Химическая технология серной кислоты
- •1. Общие сведения.
- •1.1 Значение и применение серной кислоты.
- •1.2 Свойства серной кислоты.
- •1.3 Сырьевые источники.
- •1.4. Промышленные сорта серной кислоты.
- •1.5. Способы получения серной кислоты.
- •2. Производство серной кислоты.
- •2.1. Основные стадии производства серной кислоты.
- •2.2. Получение диоксида серы so2.
- •3. Получение so2 из флотационного колчедана.
- •3.1. Основные стадии получения диоксида серы.
- •3.2. Физико-химические основы процесса обжига флотационного колчедана.
- •3.3. Очистка обжигового газа от пыли.
- •3.4. Специальная тонкая очистка печного газа
- •3.5. Осушка обжигового газа.
- •3.6. Принципиальная схема производства.
- •Лекция №8 Получение диоксида серы из серы.
- •Технологические свойства серы.
- •2. Теоретические основы горения серы.
- •3. Схема установки для сжигания серы в распылённом состоянии.
- •3.6. Схема производства серной кислоты из серы.
- •Лекция № 9 физико-химические основы Контактного окисления диоксида серы
- •Анализ химического уравнения.
- •Выражение для константы равновесия.
- •Кинетическое уравнение.
- •4. Выбор оптимальных условий ведения процесса.
- •4.1. Влияние состава исходной газовой смеси.
- •4.2. Влияние температуры.
- •4.3. Влияние давления.
- •4.4. Катализаторы
- •Лекция №10 абсорбция. Очистка отходящих газов. Производство серной кислоты из сероводорода
- •1. Абсорбция триоксида серы.
- •2. Очистка отходящих газов.
- •3. Производство серной кислоты из сероводорода.
- •4. Основные направления совершенствования сернокислотного производства.
- •Лекция № 11 Электрохимические производства.
- •1. Общие сведения.
- •2. Теоретические основы электролиза.
- •3. Электролиз воды.
- •Лекция №12 Электролиз водного раствора хлорида натрия
- •Общие сведения.
- •2. Электрохимические процессы, протекающие при электролизе водного раствора хлорида натрия.
- •3. Промышленные электрохимические методы получения хлора.
- •4. Электролиз водных растворов хлоридов с применением стального катода.
- •4.1. Приготовление и очистка рассола.
- •4.2. Побочные процессы электролиза.
- •4.4. Технологическая схема производства водорода, хлора и щелочи.
- •4.5. Выпаривание электролитического щёлока.
- •5. Электролиз водного раствора хлорида натрия с ртутным катодом.
- •5.1. Физико-химические основы процесса.
- •5.2. Принципиальная схема электролиза с ртутным катодом.
- •Лекция №13 Производство хлористого водорода и соляной кислоты.
- •1. Свойства и применение хлористого водорода.
- •2. Способы производства хлористого водорода.
- •3. Теоретические основы синтеза хлористого водорода.
- •4. Абсорбция хлороводорода или получение соляной кислоты.
- •5. Схема получения хлороводорода и соляной кислоты.
- •6. Получение жидкого хлороводорода.
- •Лекция № 14 Химическая технология Получения нитрата аммония или аммиачной селитры
- •1. Общие сведения.
- •Физические свойства нитрата аммония.
- •1.2. Химические свойства нитрата аммония.
- •1.3. Технологические свойства.
- •1.4. Применение нитрата аммония.
- •1.5. Характеристика готового продукта.
- •2. Технология производства нитрата аммония.
- •2.1. Физико-химические основы процесса синтеза нитрата аммония.
- •2.2. Технологические схемы производства.
- •3. Техника безопасности в производстве аммиачной селитры.
- •Лекция № 15 Производство карбамида.
- •1. Общие вопросы.
- •1.1. Свойства карбамида.
- •1.2. Применение карбамида.
- •1.3. Сырьё.
- •2. Физико-химические основы процесса синтеза карбамида.
- •2.1. Химические уравнения и их анализ.
- •2.2. Оптимальный технологический режим процесса синтеза карбамида.
- •3. Промышленные схемы производства карбамида.
- •4. Технологическая схема производства карбамида с полным жидкостным рециклом и двухступенчатой дистилляцией плава.
- •5.Стриппинг-процесс.
- •Лекция №16 Производство кальцинированной соды или карбоната натрия.
- •Общие сведения.
- •2. Свойства и нахождение в природе карбоната натрия.
- •3. Получение кальцинированной соды по способу Леблана.
- •4.1. Химические реакции их анализ.
- •4.2. Основные операции (или стадии) производства кальцинированной соды.
- •4.3 Теоретические основы производства кальцинированной соды аммиачным способом.
- •4.4. Принципиальная технологическая схема производства кальцинированной соды по аммиачному способу
- •5. Получение гидрокарбоната натрия
- •Лекция № 17 производство гидроксида натрия или каустической соды химическим способом
- •1. Общие сведения.
- •2. Известковый способ производства гидроксида натрия
- •Химические реакции
- •Физико-химические основы процесса каустификации
- •Основные операции технологического процесса.
- •3.Ферритный способ производства гидроксида натрия.
- •3.1. Сырьё.
- •3.2. Химические реакции.
- •3.3. Основные стадии.
- •3.4. Расходные коэффициенты.
- •3.5. Совершенствование метода.
- •Элементы технологического расчёта реактора.
- •Список рекомендуемой литературы
- •Оглавление
- •650000, Кемерово, ул, Весенняя, 28.
- •650000, Кемерово, ул. Д.Бедного, 4а.
4.4. Принципиальная технологическая схема производства кальцинированной соды по аммиачному способу
На рисунке (Рис.34) представлена технологическая схема.
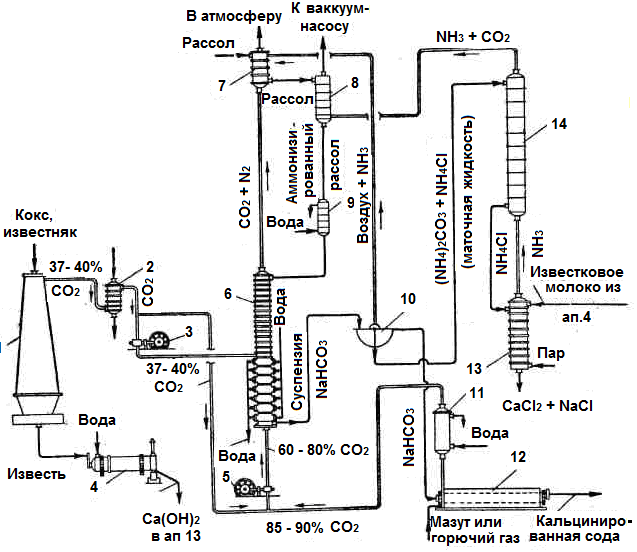
Рис.34. Принципиальная технологическая схема производства кальцинированной соды по аммиачному способу:
1 – известково-обжигательная печь; 2 – холодильник-газоочиститель; 3, 5 – компрессоры; 4 – аппарат для гашения извести; 6 – карбонизационная колонна; 7 – промыватель газов; 8 – абсорбер; 9 – холодильник аммонизированного рассола; 10 – вакуум-фильтр; 11 – холодильник-промыватель газа; 12 –содовая печь; 13 – дистиллер-смеситель; 14 – дистилляционная колонна.
Описание схемы.
1-я стадия. Очистка рассола
Предварительно приготавливают насыщенный раствор поваренной соли, который содержит 307 – 310 г/дм3 NaCl, затем его очищают от солей кальция и магния. Применяется, например, известково-содовая очистка.
Ионы кальция и магния образуют малорастворимые соединения и осаждаются из раствора:
Ca2+ + CO32- = CaCO3↓
Mg + Ca(OH)2 = Mg(OH)2↓ + Ca2+
2-я стадия. Аммонизация.
Эту стадию разделим на две:
А, протекающую в промывателе 7 и
Б, протекающую в абсорбере 8.
А. Предварительное насыщение рассола аммиаком и углекислым газом. Очищенный от солей кальция и магния рассол самотёком поступает в промыватель 7, где поглощает CO2 из газов, покидающих карбонизационные колонны 6, а также поглощает NH3 из газов, поступающих с вакуум-фильтров 10. Отработанный газ, содержащий в основном азот, удаляется в атмосферу.
Б. Собственно аммонизация. Рассол их промывателя газов 7 поступает в абсорбер 8, где поглощает NH3 и CO2, поступающие с газом из дистилляционной колонны 14. Газы, уходящие из абсорбера 8, направляются вакуум-насосом в промыватель 7, где они предварительно насыщают рассол.
3-я стадия. Карбонизация.
Аммонизированный рассол, предварительно охлаждённый в холодильнике 9, непрерывно поступает в верхнюю часть карбонизационной колонны 6, почти до верху заполненной жидкостью. Здесь происходит карбонизация рассола.
В карбонизационную колонну поступает газовая смесь, содержащая CO2.
Один поток газа, содержащий (37 – 40) % CO2, – это газ, полученный в известково-обжиговой печи по уравнению (4.3):
CaCO3 = CaO + CO2
и очищенный в аппарате 2.
Другой поток – газ содовых печей, содержащий (85 – 90) % CO2. В содовых печах CO2 получается по уравнению (4.2):
2NaHCO3 = Na2CO3 + CO2 + H2O
Концентрация смешанного газа при двух вводах в карбонизационную колонну – (60 – 80) % CO2. При одном вводе – примерно 50 % CO2.
В большинстве случаев, как на Рис. 35, имеется два ввода в карбонизационную колонну: первый ввод в нижнюю часть карбонизационной колонны – газ содовых печей; второй ввод в верхнюю часть – газ только известковых печей.
В карбонизационной колонне протекает основная реакция превращения NaCl и CO2 в NaHCO3 по уравнению (4.1):
NaCl + NH3 +CO2 = NaHCO3↓ + NH4Cl
Из верхней части карбонизационной колонны газ, содержащий некоторое количество CO2, поступает в промыватель 7, где CO2 поглощается свежим рассолом.
4-я стадия. Фильтрование и промывка осадка.
В карбонизационных колоннах 6 образуется суспензия кристаллического гидрокарбоната натрия в растворе хлорида аммония и не прореагировавшего хлорида натрия. Кроме того, в растворе содержатся соли аммония NH4HCO3 и (NH4)2CO3. Эта суспензия подаётся в вакуум-фильтр 10 для отделения гидрокарбоната.
Осадок NаHCO3 промывается на вакуум-фильтре 10. Сырой гидрокарбонат (NаHCO3) подаётся затем на кальцинирование во вращающуюся содовую печь 12, а маточная жидкость – в дистилляционную колонну 14 на регенерацию аммиака.
5-я стадия. Кальцинирование.
Кальцинирование – это разложение с образованием соды, воды и диоксида углерода. Процесс протекает во вращающихся печах 12 по уравнению (4.2):
2NаHCO3 = Na2CO3 + CO2 + H2O
Кальцинированная сода из печи 12 поступает на склад и далее на упаковку.
6-я стадия. Регенерация аммиака.
Регенерация аммиака проводится в двух аппаратах. Эту стадию также разделим на две:
А – протекающую в дистилляционной колонне 14 и
Б – протекающую в дистиллере-смесителе 13.
А. Маточная жидкость (фильтрат) подаётся из вакуум-фильтров 10 в дистилляционную колонну 14, где происходит регенерация аммиака в результате разложения солей аммония. Разложение углеаммонийных солей идёт при нагревании газами, выходящими из аппарата 13. Из этого аппарата паром отгоняют аммиак, поэтому газ имеет температуру 70 – 80ºС, содержит аммиак и частично диоксид углерода.
Углекислые соли аммония разлагаются в дистилляционной колонне 14 при температуре 70 – 80ºС по уравнениям реакций (4.5а и 4.5б):
NH4HCO3 = NH3 + CO2 + H2O
(NH4)2CO3 = 2NH3 + CO2 +H2O
Б. Для разложения хлорида аммония жидкость из дистилляционной колонны 14 подаётся в дистиллер-смеситель 13, куда поступает известковое молоко, получаемое в аппарате 4 гашением извести по уравнению реакции (4.4):
СаО + Н2О = Са(ОН)2
В дистиллере-смесителе 13 протекает реакция, описываемая уравнением (4.5):
2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3 + 2H2O.
Аммиак, выделяющийся при разложении солей аммония, отгоняется паром, подаваемым в нижнюю часть аппарата 13.
Регенерированные в аппаратах 13 и 14 аммиак и диоксид углерода направляются в абсорбер 8 на поглощение рассолом.
Раствор, полученный после отгонки аммиака, содержит в основном хлорид кальция и не вступивший в реакцию хлорид натрия. Этот раствор называется дистиллерной жидкостью. Дистиллерная жидкость является отходом производства. Рациональное использование данного отхода имеет важное значение в производстве.
В результате разложения гидрокарбоната натрия в содовых печах образуется газ, содержащий 85 – 90 % СО2. Газ содовых печей проходит холодильник-промыватель 11, очищается там, затем поступает в компрессор 5 и смешивается с другим газом – промытым и охлаждённым газом известково-обжиговых печей 1.
Смешанный газ (60 – 80% СО2)компрессором 5 под избыточным давлением 0,3 МПа подаётся в нижнюю часть карбонизационной колонны.
Производство кальцинированной соды по аммиачному способу в промышленности осуществляется почти по одинаковому принципу. Различны лишь конструкция, внутреннее устройство, размеры и производительность отдельных аппаратов.
