
- •Химическая технология неорганических веществ. Основные производства
- •Химическая технология неорганических веществ. Основные производства
- •Предисловие
- •Лекции №1-2 получение синтетического аммиака
- •1. Общие сведения.
- •1.1.Свойства аммиака.
- •1.2. Значение и применение аммиака.
- •2.Физико-химические основы синтеза аммиака.
- •3. Технологическая схема синтеза аммиака при среднем давлении.
- •4. Основные направления развития производства аммиака.
- •Лекции №3-4 химия и технология азотной кислоты.
- •1.Общие сведения.
- •1.1.Физические свойства Диаграммы состояния.
- •1.2. Химические свойства.
- •1.4. Применение азотной кислоты.
- •1.5. Способы получения азотной кислоты.
- •2. Получение неконцентрированной азотной кислоты из аммиака (химические уравнения и стадии).
- •3. Физико-химические основы процесса окисления аммиака.
- •3.1. Химические уравнения процесса окисления аммиака и их анализ.
- •3.2. Выбор оптимальных условий процесса окисления аммиака.
- •3.2.1. Катализаторы процесса окисления аммиака.
- •3.2.2. Скорость окисления аммиака.
- •3.2.3. Определение оптимальной температуры.
- •3.2.4. Определение оптимального давления процесса.
- •3.2.5. Состав газовой смеси.
- •4. Физико-химические основы процесса окисления нитрозных газов (no в no2).
- •5. Физико-химические основы процесса поглощения оксидов азота водой.
- •6. Очистка отходящих газов.
- •Лекция № 5 Получение неконцентрированной азотной кислоты в промышленности.
- •1. Основные операции и принципиальная схема.
- •2. Технологические схемы производства неконцентрированной азотной кислоты.
- •3. Принципиальная технологическая схема получения неконцентрированной азотной кислоты под повышенным давлением
- •Лекция № 6 Получение концентрированной азотной кислоты.
- •1. Общая характеристика методов получения концентрированной азотной кислоты.
- •2. Получение концентрированной азотной кислоты из разбавленных растворов.
- •3. Прямой синтез концентрированной азотной кислоты.
- •3.2. Основные стадии.
- •3.3. Технологическая схема производства концентрированной азотной кислоты прямым синтезом.
- •Лекция № 7 Химическая технология серной кислоты
- •1. Общие сведения.
- •1.1 Значение и применение серной кислоты.
- •1.2 Свойства серной кислоты.
- •1.3 Сырьевые источники.
- •1.4. Промышленные сорта серной кислоты.
- •1.5. Способы получения серной кислоты.
- •2. Производство серной кислоты.
- •2.1. Основные стадии производства серной кислоты.
- •2.2. Получение диоксида серы so2.
- •3. Получение so2 из флотационного колчедана.
- •3.1. Основные стадии получения диоксида серы.
- •3.2. Физико-химические основы процесса обжига флотационного колчедана.
- •3.3. Очистка обжигового газа от пыли.
- •3.4. Специальная тонкая очистка печного газа
- •3.5. Осушка обжигового газа.
- •3.6. Принципиальная схема производства.
- •Лекция №8 Получение диоксида серы из серы.
- •Технологические свойства серы.
- •2. Теоретические основы горения серы.
- •3. Схема установки для сжигания серы в распылённом состоянии.
- •3.6. Схема производства серной кислоты из серы.
- •Лекция № 9 физико-химические основы Контактного окисления диоксида серы
- •Анализ химического уравнения.
- •Выражение для константы равновесия.
- •Кинетическое уравнение.
- •4. Выбор оптимальных условий ведения процесса.
- •4.1. Влияние состава исходной газовой смеси.
- •4.2. Влияние температуры.
- •4.3. Влияние давления.
- •4.4. Катализаторы
- •Лекция №10 абсорбция. Очистка отходящих газов. Производство серной кислоты из сероводорода
- •1. Абсорбция триоксида серы.
- •2. Очистка отходящих газов.
- •3. Производство серной кислоты из сероводорода.
- •4. Основные направления совершенствования сернокислотного производства.
- •Лекция № 11 Электрохимические производства.
- •1. Общие сведения.
- •2. Теоретические основы электролиза.
- •3. Электролиз воды.
- •Лекция №12 Электролиз водного раствора хлорида натрия
- •Общие сведения.
- •2. Электрохимические процессы, протекающие при электролизе водного раствора хлорида натрия.
- •3. Промышленные электрохимические методы получения хлора.
- •4. Электролиз водных растворов хлоридов с применением стального катода.
- •4.1. Приготовление и очистка рассола.
- •4.2. Побочные процессы электролиза.
- •4.4. Технологическая схема производства водорода, хлора и щелочи.
- •4.5. Выпаривание электролитического щёлока.
- •5. Электролиз водного раствора хлорида натрия с ртутным катодом.
- •5.1. Физико-химические основы процесса.
- •5.2. Принципиальная схема электролиза с ртутным катодом.
- •Лекция №13 Производство хлористого водорода и соляной кислоты.
- •1. Свойства и применение хлористого водорода.
- •2. Способы производства хлористого водорода.
- •3. Теоретические основы синтеза хлористого водорода.
- •4. Абсорбция хлороводорода или получение соляной кислоты.
- •5. Схема получения хлороводорода и соляной кислоты.
- •6. Получение жидкого хлороводорода.
- •Лекция № 14 Химическая технология Получения нитрата аммония или аммиачной селитры
- •1. Общие сведения.
- •Физические свойства нитрата аммония.
- •1.2. Химические свойства нитрата аммония.
- •1.3. Технологические свойства.
- •1.4. Применение нитрата аммония.
- •1.5. Характеристика готового продукта.
- •2. Технология производства нитрата аммония.
- •2.1. Физико-химические основы процесса синтеза нитрата аммония.
- •2.2. Технологические схемы производства.
- •3. Техника безопасности в производстве аммиачной селитры.
- •Лекция № 15 Производство карбамида.
- •1. Общие вопросы.
- •1.1. Свойства карбамида.
- •1.2. Применение карбамида.
- •1.3. Сырьё.
- •2. Физико-химические основы процесса синтеза карбамида.
- •2.1. Химические уравнения и их анализ.
- •2.2. Оптимальный технологический режим процесса синтеза карбамида.
- •3. Промышленные схемы производства карбамида.
- •4. Технологическая схема производства карбамида с полным жидкостным рециклом и двухступенчатой дистилляцией плава.
- •5.Стриппинг-процесс.
- •Лекция №16 Производство кальцинированной соды или карбоната натрия.
- •Общие сведения.
- •2. Свойства и нахождение в природе карбоната натрия.
- •3. Получение кальцинированной соды по способу Леблана.
- •4.1. Химические реакции их анализ.
- •4.2. Основные операции (или стадии) производства кальцинированной соды.
- •4.3 Теоретические основы производства кальцинированной соды аммиачным способом.
- •4.4. Принципиальная технологическая схема производства кальцинированной соды по аммиачному способу
- •5. Получение гидрокарбоната натрия
- •Лекция № 17 производство гидроксида натрия или каустической соды химическим способом
- •1. Общие сведения.
- •2. Известковый способ производства гидроксида натрия
- •Химические реакции
- •Физико-химические основы процесса каустификации
- •Основные операции технологического процесса.
- •3.Ферритный способ производства гидроксида натрия.
- •3.1. Сырьё.
- •3.2. Химические реакции.
- •3.3. Основные стадии.
- •3.4. Расходные коэффициенты.
- •3.5. Совершенствование метода.
- •Элементы технологического расчёта реактора.
- •Список рекомендуемой литературы
- •Оглавление
- •650000, Кемерово, ул, Весенняя, 28.
- •650000, Кемерово, ул. Д.Бедного, 4а.
Лекция №10 абсорбция. Очистка отходящих газов. Производство серной кислоты из сероводорода
ВОПРОСЫ
Абсорбция триоксида серы.
Очистка отходящих газов.
Производство серной кислоты из сероводорода.
Основные направления совершенствования сернокислотного производства.
1. Абсорбция триоксида серы.
Третья стадия получения серной кислоты – это взаимодействие SО3 с водой:
SО3 + Н2О = Н2SО4; ∆H<0.
Анализ этого уравнения. Реакция взаимодействия триоксида серы с водой – это реакция:
– практически необратимая,
– быстрая,
– экзотермическая,
– протекающая одновременно в жидкой и паровой фазах.
Особенность этой реакции заключается в том, что реакция протекает одновременно в жидкой и в газовой фазе. Поэтому в газовой фазе образуется устойчивый туман
SО3(г.) + Н2О(пар) = Н2SО4(туман),
который плохо поддаётся улавливанию.
Следовательно, вода не может быть использована в качестве поглотителя.
Более подходящим поглотителем является 98,3%-я серная кислота, так как данной концентрации отвечает самое низкое давление паров воды над раствором. Поэтому степень поглощения триоксида серы в жидкой фазе при этой концентрации будет максимальной. Конечный продукт образуется не в виде тумана, а в виде моногидрата.
В промышленности моногидратом называют серную кислоту с концентрацией несколько меньшей 100% (98 %).
Дальнейшим насыщением получают олеум:
nSО3 + Н2SО4 = Н2SО4∙nSО3
Образующийся олеум – один из товарных продуктов производства серной кислоты. Разбавлением олеума получают серную кислоту необходимой концентрации.
Главное требование к процессу абсорбции – обеспечить возможно более полное поглощение триоксида серы, что должно снизить потери сырья и обеспечить снижение затрат на очистку отходящих газов.
Итак, оптимальная концентрация абсорбента – 98,3%-я серная кислота.
На полноту и скорость процесса абсорбции влияют и другие факторы.
Влияние температуры. Абсорбция сопровождается выделением тепла, а повышение температуры может существенно снизить эффективность абсорбции. Поэтому выделяющееся тепло необходимо отводить. Для этого абсорбционные башни снабжены охлаждающими элементами. Кроме того, для охлаждения орошение берут в избытке.
Скорость абсорбции увеличивается с увеличением давления и увеличением площади соприкосновения. Поэтому процесс ведут при повышенных давлениях в башнях с насадкой.
Очевидно, что после контактирования перед абсорбцией газ должен охлаждаться. В промышленных условиях газ охлаждают до температуры 65 – 80ºС, используя избыток орошения. Кроме того, для охлаждения, как уже было сказано, применяют охлаждающие элементы.
На рисунке (Рис.24) представлена упрощенная схема абсорбции триоксида серы и получения серной кислоты.
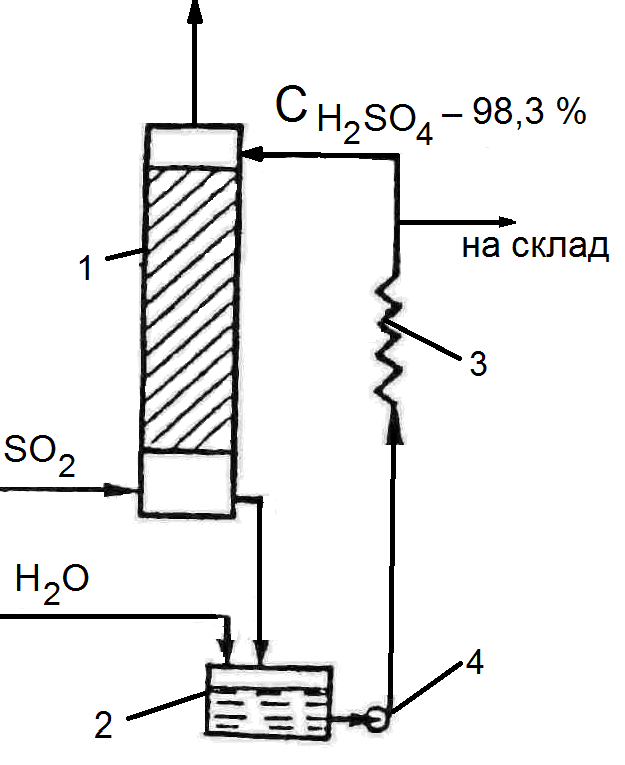
Рис. 24. Схема процесса абсорбции в производстве серной кислоты.
1 – абсорбер; 2 – сборник; 3 – холодильник; 4 – насос.
В абсорбционном отделении поглощение газа проходит в двух последовательно соединённых башнях:
– первая орошается 20%–м олеумом (олеумный абсорбер)
– вторая орошается 98,3%–й серной кислотой (моногидратный абсорбер).
Выделяющееся тепло абсорбции отводят в теплообменниках.
Поглотители берутся в большом избытке для лучшего отвода тепла.
Насыщение поглотителя триоксидом серы допускается не более 1%.
По мере заданного насыщения поглотители (олеум и моногидрат) разбавляются в соответствующих сборниках (олеумном и моногидратном) до исходной концентрации и вновь поступают на орошение в поглотительные башни. Предварительно часть олеума или моногидрата отводится на склад.
