
- •Химическая технология неорганических веществ. Основные производства
- •Химическая технология неорганических веществ. Основные производства
- •Предисловие
- •Лекции №1-2 получение синтетического аммиака
- •1. Общие сведения.
- •1.1.Свойства аммиака.
- •1.2. Значение и применение аммиака.
- •2.Физико-химические основы синтеза аммиака.
- •3. Технологическая схема синтеза аммиака при среднем давлении.
- •4. Основные направления развития производства аммиака.
- •Лекции №3-4 химия и технология азотной кислоты.
- •1.Общие сведения.
- •1.1.Физические свойства Диаграммы состояния.
- •1.2. Химические свойства.
- •1.4. Применение азотной кислоты.
- •1.5. Способы получения азотной кислоты.
- •2. Получение неконцентрированной азотной кислоты из аммиака (химические уравнения и стадии).
- •3. Физико-химические основы процесса окисления аммиака.
- •3.1. Химические уравнения процесса окисления аммиака и их анализ.
- •3.2. Выбор оптимальных условий процесса окисления аммиака.
- •3.2.1. Катализаторы процесса окисления аммиака.
- •3.2.2. Скорость окисления аммиака.
- •3.2.3. Определение оптимальной температуры.
- •3.2.4. Определение оптимального давления процесса.
- •3.2.5. Состав газовой смеси.
- •4. Физико-химические основы процесса окисления нитрозных газов (no в no2).
- •5. Физико-химические основы процесса поглощения оксидов азота водой.
- •6. Очистка отходящих газов.
- •Лекция № 5 Получение неконцентрированной азотной кислоты в промышленности.
- •1. Основные операции и принципиальная схема.
- •2. Технологические схемы производства неконцентрированной азотной кислоты.
- •3. Принципиальная технологическая схема получения неконцентрированной азотной кислоты под повышенным давлением
- •Лекция № 6 Получение концентрированной азотной кислоты.
- •1. Общая характеристика методов получения концентрированной азотной кислоты.
- •2. Получение концентрированной азотной кислоты из разбавленных растворов.
- •3. Прямой синтез концентрированной азотной кислоты.
- •3.2. Основные стадии.
- •3.3. Технологическая схема производства концентрированной азотной кислоты прямым синтезом.
- •Лекция № 7 Химическая технология серной кислоты
- •1. Общие сведения.
- •1.1 Значение и применение серной кислоты.
- •1.2 Свойства серной кислоты.
- •1.3 Сырьевые источники.
- •1.4. Промышленные сорта серной кислоты.
- •1.5. Способы получения серной кислоты.
- •2. Производство серной кислоты.
- •2.1. Основные стадии производства серной кислоты.
- •2.2. Получение диоксида серы so2.
- •3. Получение so2 из флотационного колчедана.
- •3.1. Основные стадии получения диоксида серы.
- •3.2. Физико-химические основы процесса обжига флотационного колчедана.
- •3.3. Очистка обжигового газа от пыли.
- •3.4. Специальная тонкая очистка печного газа
- •3.5. Осушка обжигового газа.
- •3.6. Принципиальная схема производства.
- •Лекция №8 Получение диоксида серы из серы.
- •Технологические свойства серы.
- •2. Теоретические основы горения серы.
- •3. Схема установки для сжигания серы в распылённом состоянии.
- •3.6. Схема производства серной кислоты из серы.
- •Лекция № 9 физико-химические основы Контактного окисления диоксида серы
- •Анализ химического уравнения.
- •Выражение для константы равновесия.
- •Кинетическое уравнение.
- •4. Выбор оптимальных условий ведения процесса.
- •4.1. Влияние состава исходной газовой смеси.
- •4.2. Влияние температуры.
- •4.3. Влияние давления.
- •4.4. Катализаторы
- •Лекция №10 абсорбция. Очистка отходящих газов. Производство серной кислоты из сероводорода
- •1. Абсорбция триоксида серы.
- •2. Очистка отходящих газов.
- •3. Производство серной кислоты из сероводорода.
- •4. Основные направления совершенствования сернокислотного производства.
- •Лекция № 11 Электрохимические производства.
- •1. Общие сведения.
- •2. Теоретические основы электролиза.
- •3. Электролиз воды.
- •Лекция №12 Электролиз водного раствора хлорида натрия
- •Общие сведения.
- •2. Электрохимические процессы, протекающие при электролизе водного раствора хлорида натрия.
- •3. Промышленные электрохимические методы получения хлора.
- •4. Электролиз водных растворов хлоридов с применением стального катода.
- •4.1. Приготовление и очистка рассола.
- •4.2. Побочные процессы электролиза.
- •4.4. Технологическая схема производства водорода, хлора и щелочи.
- •4.5. Выпаривание электролитического щёлока.
- •5. Электролиз водного раствора хлорида натрия с ртутным катодом.
- •5.1. Физико-химические основы процесса.
- •5.2. Принципиальная схема электролиза с ртутным катодом.
- •Лекция №13 Производство хлористого водорода и соляной кислоты.
- •1. Свойства и применение хлористого водорода.
- •2. Способы производства хлористого водорода.
- •3. Теоретические основы синтеза хлористого водорода.
- •4. Абсорбция хлороводорода или получение соляной кислоты.
- •5. Схема получения хлороводорода и соляной кислоты.
- •6. Получение жидкого хлороводорода.
- •Лекция № 14 Химическая технология Получения нитрата аммония или аммиачной селитры
- •1. Общие сведения.
- •Физические свойства нитрата аммония.
- •1.2. Химические свойства нитрата аммония.
- •1.3. Технологические свойства.
- •1.4. Применение нитрата аммония.
- •1.5. Характеристика готового продукта.
- •2. Технология производства нитрата аммония.
- •2.1. Физико-химические основы процесса синтеза нитрата аммония.
- •2.2. Технологические схемы производства.
- •3. Техника безопасности в производстве аммиачной селитры.
- •Лекция № 15 Производство карбамида.
- •1. Общие вопросы.
- •1.1. Свойства карбамида.
- •1.2. Применение карбамида.
- •1.3. Сырьё.
- •2. Физико-химические основы процесса синтеза карбамида.
- •2.1. Химические уравнения и их анализ.
- •2.2. Оптимальный технологический режим процесса синтеза карбамида.
- •3. Промышленные схемы производства карбамида.
- •4. Технологическая схема производства карбамида с полным жидкостным рециклом и двухступенчатой дистилляцией плава.
- •5.Стриппинг-процесс.
- •Лекция №16 Производство кальцинированной соды или карбоната натрия.
- •Общие сведения.
- •2. Свойства и нахождение в природе карбоната натрия.
- •3. Получение кальцинированной соды по способу Леблана.
- •4.1. Химические реакции их анализ.
- •4.2. Основные операции (или стадии) производства кальцинированной соды.
- •4.3 Теоретические основы производства кальцинированной соды аммиачным способом.
- •4.4. Принципиальная технологическая схема производства кальцинированной соды по аммиачному способу
- •5. Получение гидрокарбоната натрия
- •Лекция № 17 производство гидроксида натрия или каустической соды химическим способом
- •1. Общие сведения.
- •2. Известковый способ производства гидроксида натрия
- •Химические реакции
- •Физико-химические основы процесса каустификации
- •Основные операции технологического процесса.
- •3.Ферритный способ производства гидроксида натрия.
- •3.1. Сырьё.
- •3.2. Химические реакции.
- •3.3. Основные стадии.
- •3.4. Расходные коэффициенты.
- •3.5. Совершенствование метода.
- •Элементы технологического расчёта реактора.
- •Список рекомендуемой литературы
- •Оглавление
- •650000, Кемерово, ул, Весенняя, 28.
- •650000, Кемерово, ул. Д.Бедного, 4а.
3.2. Основные стадии.
Выделим основные стадии (или операции) получения концентрированной азотной кислоты из нитрозного газа:
1 – охлаждение нитрозных газов
2 – окисление NO в NO2 (уравнение 3.1)
3 – доокисление NO азотной кислотой (уравнение 3.2)
4 – охлаждение нитрозных газов
5 – получение нитроолеума (уравнение 3.3)
6 – разложение нитроолеума (уравнение 3.4)
7 – охлаждение
8 – получение жидкого N2O4 (уравнение 3.5)
9 – окисление тетраоксида кислородом (итоговое уравнение)
10 – десорбция избытка N2O4 из HNO3
11 – обезвреживание отходящих газов (эта операция выполняется после получения нитроолеума).
Составьте принципиальную схему получения концентрированной азотной кислоты методом прямого синтеза.
3.3. Технологическая схема производства концентрированной азотной кислоты прямым синтезом.
Технологическая схема производства концентрированной азотной кислоты прямым синтезом из жидких оксидов азота представлена на рисунке (Рис.14).
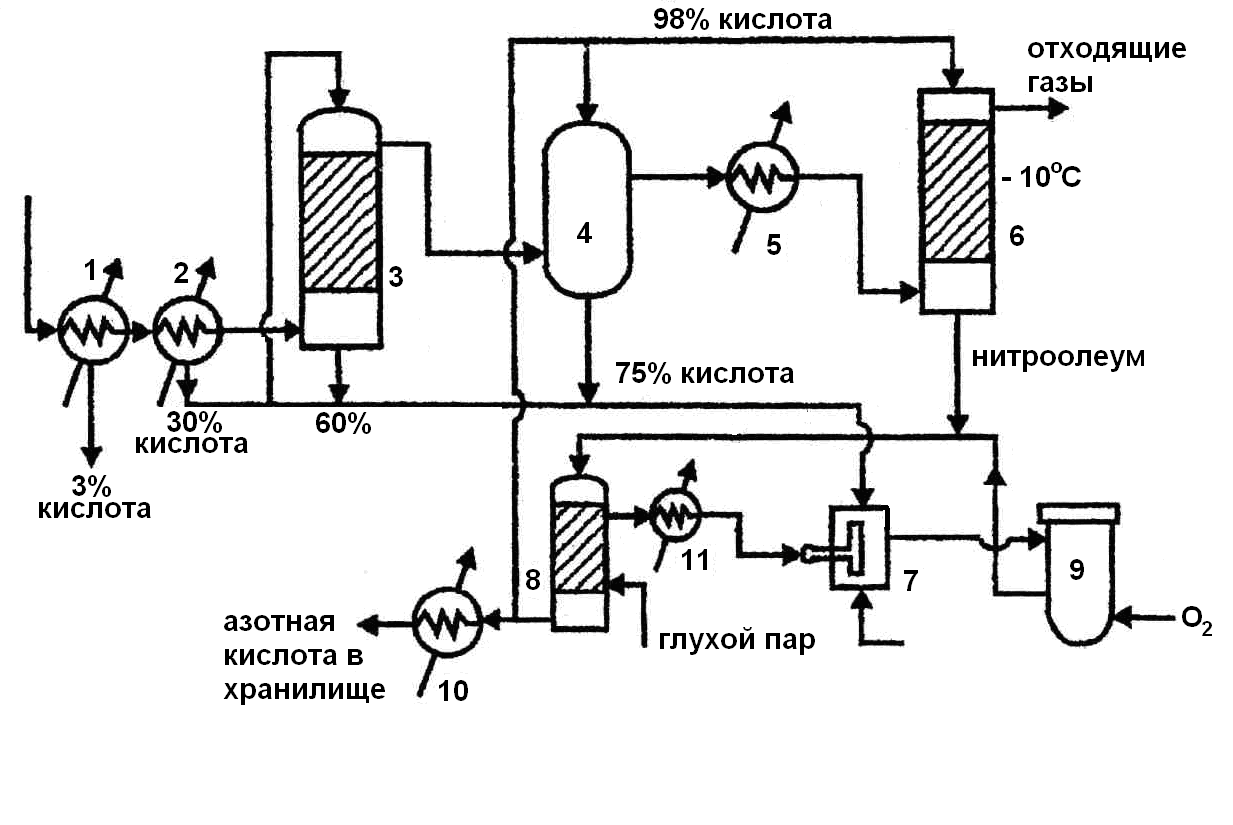
Рис.14. Технологическая схема производства концентрированной азотной кислоты прямым синтезом:
1 – скоростной холодильник; 2 – холодильник; 3 – окислительная башня; 4 – доокислитель; 5 – рассольный холодильник; 6 – абсорбционная колонна; 7 – смеситель; 8 – отбелочная колонна; 9 – автоклав; 10 – холодильник; 11 – холодильник-коденсатор.
Описание схемы.
Нитрозный газ поступает в скоростной холодильник 1, где охлаждается до 40 ºС, при этом образуется 3 %-я азотная кислота. Затем газ поступает в холодильник 2, при этом образуется 30%-я азотная кислота. Часть кислоты направляется в смеситель 7, другая часть – на орошение окислительной башни 3. Нитрозные газы поступают в окислительную башню 3, орошаемую азотной кислотой. При этом образуется 60%-я азотная кислота, часть которой направляется в смеситель 7, а часть - на окисление нитрозных газов в аппарат 4. Нитрозные газы из окислительной башни 3 поступают в доокислитель 4, орошаемый 98%-й азотной кислотой. Азотная кислота из доокислителя 4 направляется в смеситель 7, а нитрозные газы – в рассольный холодильник 5, где охлаждаются до (-10) ºС . Затем нитрозные газы поступают в абсорбционную колонну, орошаемую 98%-й азотной кислотой, для поглощения оксида азота (IV) и для получения нитроолеума. Непоглощенные газы из верхней части колонны направляются в систему очистки выхлопных газов, а образовавшийся нитроолеум подаётся в отбелочную колонну 8 для десорбции NO2. Отбеленная 98%-я азотная кислота охлаждается в холодильнике 10 и поступает в хранилище.
Газообразные концентрированные оксиды азота из отбелочной колонны охлаждаются и конденсируются в холодильнике-конденсаторе 11, который охлаждается рассолом до (-10)С. Затем они поступают в смеситель 7, где образуется смесь, состоящая из (68 – 80) % N2O4 , (26 – 10,5) % HNO3 и (6 – 9,5)% H2O.
Эта смесь подаётся в автоклав 9, туда же под давлением 5МПа поступает кислород. Образующаяся концентрированная азотная кислота отбирается из нижней части автоклава и, соединившись с нитроолеумом из абсорбционной колонны 6, подаётся в отбелочную колонну 8.
4. Перспективы развития азотнокислотного производства.
Развитие азотнокислотного производств возможно в следующих основных направлениях:
– создание систем высокой единичной мощности (до 4000тыс.т/год), работающих по комбинированной схеме;
– разработка высокоактивных избирательных неплатиновых катализаторов окисления аммиака;
– более полное использование энергии сжатых отходящих газов и теплоты химических реакций – создание полностью автономных энергетических схем;
– создание замкнутого оборота охлаждающей воды;
– решение проблемы очистки отходящих газов с использованием в качестве адсорбента силикагеля и цеолитов;
– более полное удаление остатков оксидов азота из отходящих газов с использованием в качестве восстановителя природного газа и аммиака.
