
- •Тема: гідроген
- •Проста речовина
- •Лабораторна робота № 1 одержання та властивості гідрогену.
- •Контрольні питання
- •Тема: лужні метали
- •Лабораторна робота № 2 властивості лужних металів та їх сполук.
- •Контрольні питання
- •Тема: елементи іі-а групи
- •Лабораторна робота № 3 властивості магнію, лужноземельних металів та їх сполук
- •Лабораторна робота № 4 визначення жорсткості води.
- •Контрольні питання
- •Тема: елементи ііі – а групи
- •Лабораторна робота № 5 властивості алюмінію та його сполук.
- •Контрольні питання
- •Тема: елементи іv – а групи
- •Лабораторна робота № 6 властивості карбону, силіцію та їх сполук.
- •Контрольні питання
- •Лабораторна робота № 7 властивості стануму, плюмбуму та їх сполук.
- •Контрольні питання
- •Тема: елементи V – а групи
- •Лабораторна робота № 8 властивості нітрогену, фосфору та їх сполук.
- •Контрольні питання
- •Лабораторна робота № 9 розпізнавання нітратних та фосфорних добрив.
- •Контрольні питання
- •Тема: халькогени
- •Лабораторна робота № 10 властивості сульфуру та її сполук.
- •Контрольні питання
- •Тема: галогени
- •Лабораторна робота № 11 одержання та властивості галогенів.
- •Контрольні питання.
- •Лабораторна робота № 12 властивості галогеноводневих кислот. Якісні реакції на галоген-іони.
- •Контрольні питання.
- •Тема: елементи підгрупи хрому
- •Лабораторна робота № 13 властивості хрому та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи мангану
- •Лабораторна робота № 14 властивості мангану та його сполук
- •Контрольні питання
- •Тема: елементи родини феруму
- •Лабораторна робота № 15 властивості феруму та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи купруму
- •Лабораторна робота № 16 властивості купруму та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи цинку
- •Лабораторна робота № 17 властивості цинку та його сполук. Визначення іонів ртуті
- •Контрольні питання
- •Список рекомендованої літератури
Лабораторна робота № 4 визначення жорсткості води.
Мета роботи: визначити тимчасову та загальну жорсткість природної води титриметричним методом
Прилади та реактиви: бюретки (25 мл), піпетки (100, 50 мл), колби конічні (250 мл), воротки для бюреток. Індикатори: метиловий оранжевий, еріохром чорний Т (0,2% розчин в етиловому спирті). Розчини: хлороводневої кислоти (0,1 н. титрований), буферний розчин (20 г хлориду амонію розчинити в дист воді, додати 100 мл 25% розчину аміаку і води до мітки в мірній колбі ємністю 1 л), ЕДТА (0,02 н. титрований: 3,7224 г ЕДТА розчинити в мірній колбі (1 л) в дист воді, розчин довести до мітки). Вода для аналізування
ДОСЛІД 1. Визначення тимчасової жорсткості води
Відміряти піпеткою 100 – 50 мл досліджуваної води і перенести її до конічної колби для титрування. Додати 2-3 краплі метилового оранжевого. В підготовлену заздалегідь бюретку налити 0,1 н. титрований розчин хлороводневої кислоти. Встановити рівень на нульове значення і по краплям приливати кислоту у воду до зміни забарвлення розчину від жовтого до оранжево-рожевого. Визначити об’єм хлороводневої кислоти, що пішла на титрування і записати до таблиці. Титрування повторити ще два рази, кожного разу доливаючи в бюретку кислоти до нульового ділення і ополіскуючи колбу для титрування. Розбіг у об’ємі кислоти при титруванні не повинен перевищувати 0,05 -0,1 мл. Результати записати в таблиці.
№ титрування |
Об'єм води V1, мл |
Об'єм розчину НCl, що пішов на титрування, мл |
Середній об'єм розчину НCl V2, мл |
Нормальність розчину НCl, NHCl |
1 |
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
|
Тимчасову жорсткість води розраховувати за формулою:

___________________________________________________________________________________________________________________________________________________________________________________________________________
ДОСЛІД 2. Визначення загальної жорсткості води
Заповнити бюретку титрованим розчином ЕДТА (0,02н.). Відміряти піпеткою 100 – 50 мл досліджуваної води і перенести її до конічної колби для титрування. Додати дистильованої води до загального об’єму 100 мл при необхідності та додати 5 мл буферного розчину для підтримки рН в межах 9-10 од. та 2-3 краплі еріохрому чорного, при цьому розчин забарвлюється у червоний колір. Перемішати розчин і одразу титрувати розчином ЕДТА до переходу червоного забарвлення до синього. Титрування повторити три рази, як в попередньому досліді. Результати записати в таблицю.
№ титрування |
Об'єм води V1, мл |
Об'єм розчину ЄДТА, що пішов на титрування V2, мл |
Нормальність розчину ЄДТА, NЄДТА |
1 |
|
|
0,02 |
2 |
|
|
0,02 |
3 |
|
|
0,02 |
Загальну жорсткість розрахувати за формулою:
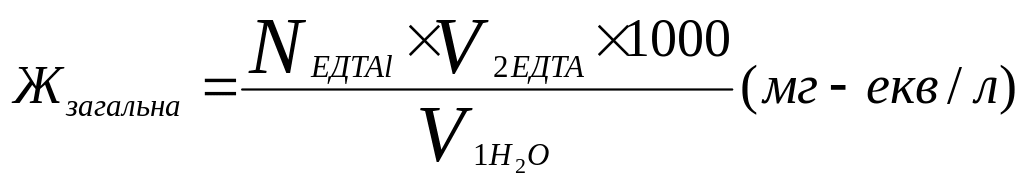
____________________________________________________________________________________________________________________________________________________________________________________________________________
Розрахувати постійну жорсткість, як різницю між загальною та тимчасовою жорсткістю.
________________________________________________________________________________________________________________________________________Зробити висновок до якого типу жорсткості відноситься досліджувана вода.
____________________________________________________________________________________________________________________________________________________________________________________________________________
