
- •Тема: гідроген
- •Проста речовина
- •Лабораторна робота № 1 одержання та властивості гідрогену.
- •Контрольні питання
- •Тема: лужні метали
- •Лабораторна робота № 2 властивості лужних металів та їх сполук.
- •Контрольні питання
- •Тема: елементи іі-а групи
- •Лабораторна робота № 3 властивості магнію, лужноземельних металів та їх сполук
- •Лабораторна робота № 4 визначення жорсткості води.
- •Контрольні питання
- •Тема: елементи ііі – а групи
- •Лабораторна робота № 5 властивості алюмінію та його сполук.
- •Контрольні питання
- •Тема: елементи іv – а групи
- •Лабораторна робота № 6 властивості карбону, силіцію та їх сполук.
- •Контрольні питання
- •Лабораторна робота № 7 властивості стануму, плюмбуму та їх сполук.
- •Контрольні питання
- •Тема: елементи V – а групи
- •Лабораторна робота № 8 властивості нітрогену, фосфору та їх сполук.
- •Контрольні питання
- •Лабораторна робота № 9 розпізнавання нітратних та фосфорних добрив.
- •Контрольні питання
- •Тема: халькогени
- •Лабораторна робота № 10 властивості сульфуру та її сполук.
- •Контрольні питання
- •Тема: галогени
- •Лабораторна робота № 11 одержання та властивості галогенів.
- •Контрольні питання.
- •Лабораторна робота № 12 властивості галогеноводневих кислот. Якісні реакції на галоген-іони.
- •Контрольні питання.
- •Тема: елементи підгрупи хрому
- •Лабораторна робота № 13 властивості хрому та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи мангану
- •Лабораторна робота № 14 властивості мангану та його сполук
- •Контрольні питання
- •Тема: елементи родини феруму
- •Лабораторна робота № 15 властивості феруму та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи купруму
- •Лабораторна робота № 16 властивості купруму та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи цинку
- •Лабораторна робота № 17 властивості цинку та його сполук. Визначення іонів ртуті
- •Контрольні питання
- •Список рекомендованої літератури
Контрольні питання
Як змінюється стійкість оксидів елементів ІVА групи при збільшенні порядкового номеру?
____________________________________________________________________
У якого з оксидів більш виразні основні властивості: а) SnO або PbO; б) SnO або SnO2.
____________________________________________________________________
Написати реакції, що підтверджують амфотерність гідроксиду Плюмбуму (ІV).
________________________________________________________________________________________________________________________________________
Написати реакцій отримання сульфідів Стануму (ІІ), Стануму (ІV), Плюмбуму (ІІ) з розчинів їх солей.
____________________________________________________________________________________________________________________________________________________________________________________________________________
Розставте коефіцієнти в рівнянні:
NaNO2 + PbO2 + H2SO4 → NaNO3 + PbSO4 + H2O
Тема: елементи V – а групи
|
r(A) |
I1, эВ |
Ео(Э3+/Э) |
Ступені окислення |
N |
0.71 |
14.5 |
- |
-3,0,+1,+2,+3,+4,+5 |
P |
1.10 |
10.5 |
- |
-3,0,+3,+5 |
As |
1.48 |
9.8 |
0.3 |
-“- |
Sb |
1.61 |
8.6 |
0.24 |
-“- |
Bi |
1.82 |
7.3 |
0.2 |
-“- |
До VА групи входять типові р-елементи Нітроген, фосфор, миш’як, сурма і вісмут. Атоми цих елементів мають на зовнішньому рівні п’ять електронів у конфігурації - s2p3. при збудженні атомів відбувається розпарювання s електронів і перехід одного з них на d-підрівень (за виключенням Нітрогену).
Молекула Нітрогену диатомна і за звичайних умов Нітроген не здатний вступати до реакцій, за виключенням літію. При нагріванні Нітроген реагує з багатьма металами і неметалами, утворюючи нітриди, а фосфор – фосфіди. Галогеніди Нітрогену - малостійкі сполуки; більш стійки оксигалогеніди Нітрогену - NOF, NOCI, NOBr, NO2F и NO2CI. З сіркою також не відбувається безпосередньої взаємодії Нітрогену; нітрогений Сульфур N4S4 отримується в результаті реакції рідкої Сульфуру з аміаком. При взаємодії розжареного коксу з Нітрогеном утворюється ціан (СN)2. В залежності від того, чи знаходиться Фосфор у надлишку або нестачі, утворюються сполуки фосфору (III) і (V), наприклад:
2P + 3Br2 = 2PBr3 або 2P + 5Br2 = 2PBr5
Нітрид Гідрогену – аміак в лабораторії отримують дією на солі амонію лугів або нагріванням кристалічних солей амонію з гідроксидом або оксидом кальцію. Аміак добре розчиняється у воді. Розчин аміаку – слабка основа.
NH3×H2O « NH4+ + OH- K=2×10-5
Встановлено, що більша маса аміаку знаходиться у водному розчині у вигляді гідратованих молекул NH3×пH2O і лише близько 0,4% розчиненого аміаку хімічно взаємодіє з водою. Аміак може вести себе як кислота NH3 « NH2- + H+, що дає соли: аміди - NaNH2; іміди - Na2NH; нітриди Na3N.
Фосфіди деяких металів можуть розкладатися водою з утворенням фосфіну PH:
Mg3P2 + 6H2O = 3Mg(OH)2 + 2PH3
PH3 – фосфін, добре розчинний у воді. Виявляє як основні так і кислотні властивості. Аміак та фосфін володіють лише відновними властивостями. Аміак окислюється Оксигеном до Нітрогену або, на платині в якості каталізатору до NO, відновлює метали (Купрум), реагує з Хлором. Фосфін на повітрі горить з утворенням оксиду фосфору (VI).
Солі амонію термічно нестійкі, проте характер розкладу залежить від кислоти, що утворює сіль. Як що кислота окисник, то відбувається реакція внутримолекулярного окислення:
(NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O
Як що, кислота не є окисником, то виділяється аміак і відповідна кислота:
NH4Cl = NH3 + HCl
При дії сильних лугів на солі амонію виділяється аміак, що служить якісною реакцією для визначення іонів амонію.
Найбільшу кількість оксидів має Нітроген: N2O, NO, N2O3, NO2, N2O5. Зі всіх оксидів лише N2O3 та N2O5 кислотні, решта – несолеутворюючи. N2O - легко розкладається, виділяючи Оксиген. NO і NO2 - молекули з неспареними електронами - радикали, можуть дімерізуватися.
2NO2 « N2O4 - реакція екзотермічна
N2O3 розчиняється у воді з утворенням слабкої нітрітної кислоти, що виявляє окисно-відновні властивості. Її солі нітрити отруйні і термічно більш стійки, ніж нітрати.
N2O5 – безбарвні кристали, що розкладаються до Оксигену та NO2. При розчиненні у воді утворює Нітрогену кислоту. Нітратна кислота – сильний окисник, ступень відновлення якого залежить від її концентрації та активності відновника. При великих концентраціях відновлення йде до NO2, при середніх - до NO, а при сильному розведенні - до молекулярного Нітрогену, NH4+. Чим вище концентрація HNO3, тим менш глибоко вона відновлюється. Чисте Ферум, Алюміній, хром не розчиняються у концентрованій нітратна кислоті в зв’язку з їх пасивацією. Деякі неметали (Сульфур, Фосфор, Карбон) окисляються нітратною кислотою. При цьому концентрована нітратна кислота відновлюється до оксиду (ІV), а розведена – до оксиду Нітрогену (ІІ).
З оксигеном Фосфор утворює лише оксиди - Р2О3 і Р2О5. Оксид Фосфору (ІІІ) отримують при повільному окисленні фосфору. За низьких температур склад оксиду має вигляд Р4О6, що вказує на упровадження Оксигену по зв'язку Р-Р в молекулі Р4, а потім до атомів Фосфору приєднується ще атоми Оксигену до кожного атому Фосфору. Оксиду фосфору (ІІІ) відповідає двохосновна фосфориста кислота (H3PO3) – сильний відновник, що має солі фосфіти.
О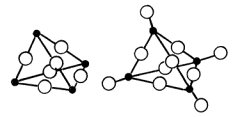 ксид
Фосфору (ІV) в газоподібному стані має
структуру Р4О10.
при розчиненні у холодній воді утворює
метафосфорну
кислоту
(HPO3),
а при інших температурах пірофосфорну
кислоту
(H4P2O7).
При кіп'ятінні метафосфорної кислот з
надлишком води утворюється трьохосновна
ортофосфорна
кислота
(H3PO4).
Всі одно заміщені солі цієї кислоти -
дигідрофосфати
розчинні у воді. З гідрофосфатів
та
фосфатів
розчинні лише солі лужних металів і
амонію. Розчини останніх мають лужну
реакцію, на відміну від дигідрофосфатів
в розчинах яких дисоціація дигідрофосфат-іону
переважає над гідролізом.
ксид
Фосфору (ІV) в газоподібному стані має
структуру Р4О10.
при розчиненні у холодній воді утворює
метафосфорну
кислоту
(HPO3),
а при інших температурах пірофосфорну
кислоту
(H4P2O7).
При кіп'ятінні метафосфорної кислот з
надлишком води утворюється трьохосновна
ортофосфорна
кислота
(H3PO4).
Всі одно заміщені солі цієї кислоти -
дигідрофосфати
розчинні у воді. З гідрофосфатів
та
фосфатів
розчинні лише солі лужних металів і
амонію. Розчини останніх мають лужну
реакцію, на відміну від дигідрофосфатів
в розчинах яких дисоціація дигідрофосфат-іону
переважає над гідролізом.
H
гідроліз
дисоціація
H 2PO4- H+ + HPO4-
На відміну від ортофосфорної кислоти, всі інші фосфорні кислоти – полімерні сполуки, що містять ланцюги: -РО3-О-РО3-.
