
- •Тема: гідроген
- •Проста речовина
- •Лабораторна робота № 1 одержання та властивості гідрогену.
- •Контрольні питання
- •Тема: лужні метали
- •Лабораторна робота № 2 властивості лужних металів та їх сполук.
- •Контрольні питання
- •Тема: елементи іі-а групи
- •Лабораторна робота № 3 властивості магнію, лужноземельних металів та їх сполук
- •Лабораторна робота № 4 визначення жорсткості води.
- •Контрольні питання
- •Тема: елементи ііі – а групи
- •Лабораторна робота № 5 властивості алюмінію та його сполук.
- •Контрольні питання
- •Тема: елементи іv – а групи
- •Лабораторна робота № 6 властивості карбону, силіцію та їх сполук.
- •Контрольні питання
- •Лабораторна робота № 7 властивості стануму, плюмбуму та їх сполук.
- •Контрольні питання
- •Тема: елементи V – а групи
- •Лабораторна робота № 8 властивості нітрогену, фосфору та їх сполук.
- •Контрольні питання
- •Лабораторна робота № 9 розпізнавання нітратних та фосфорних добрив.
- •Контрольні питання
- •Тема: халькогени
- •Лабораторна робота № 10 властивості сульфуру та її сполук.
- •Контрольні питання
- •Тема: галогени
- •Лабораторна робота № 11 одержання та властивості галогенів.
- •Контрольні питання.
- •Лабораторна робота № 12 властивості галогеноводневих кислот. Якісні реакції на галоген-іони.
- •Контрольні питання.
- •Тема: елементи підгрупи хрому
- •Лабораторна робота № 13 властивості хрому та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи мангану
- •Лабораторна робота № 14 властивості мангану та його сполук
- •Контрольні питання
- •Тема: елементи родини феруму
- •Лабораторна робота № 15 властивості феруму та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи купруму
- •Лабораторна робота № 16 властивості купруму та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи цинку
- •Лабораторна робота № 17 властивості цинку та його сполук. Визначення іонів ртуті
- •Контрольні питання
- •Список рекомендованої літератури
Лабораторна робота № 1 одержання та властивості гідрогену.
Мета роботи: ознайомитись з методами лабораторного отримання Гідрогену, його хімічними властивостями, дослідити окисно-відновні властивості перекису Гідрогену.
Прилади та реактиви: лабораторний штатив, пробірки, газовідвідні трубки, лучина, спиртівка. Цинк. Порошок оксиду Купруму (ІІ). Перманганат калію. Розчини: хлороводневої кислоти, йодиду калію, сульфатної кислоти, 3% пероксиду Гідрогену, нітрату ртуті (ІІ).
Техніка безпеки: Досліди, що супроводжуються виділенням газів проводити під тягою. При роботі не допускати попадання розчинів кислот та перекису Гідрогену на шкіру. При спаленні Гідрогену проявляти обережність. Суміш Гідрогену та Оксигену вибухонебезпечна.
ДОСЛІД 1. Отримання Гідрогену
Д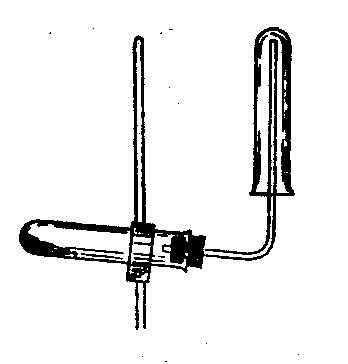 о
пробірки внести 5 крапель розчину
хлороводневої кислоти та шматочок
Цинку. Зачинити отвір пробірки пробкою
з газовідвідною трубкою. Коли реакція
буде проходити досить енергійно, піднести
до кінчика відвідної трубки гарячій
сірник та підпалити газ, що виділяється.
о
пробірки внести 5 крапель розчину
хлороводневої кислоти та шматочок
Цинку. Зачинити отвір пробірки пробкою
з газовідвідною трубкою. Коли реакція
буде проходити досить енергійно, піднести
до кінчика відвідної трубки гарячій
сірник та підпалити газ, що виділяється.
Завдання.
1. Написати рівняння реакції отримання Гідрогену, визначити окисника.
___________________________________________
2. Чи можливо для отримання Гідрогену з хлороводневої кислоти замінити Цинк іншим металом?
____________________________________________________________________
3. Написати рівняння горіння Гідрогену.
____________________________________________________________________
ДОСЛІД 2. Відновні властивості Гідрогену
Насипте скляною лопаточкою на дно сухої скляної пробірки порошок оксиду Купруму (ІІ) та закріпіть її у штативі горизонтально. Газовідвідну трубку з пробірки де утворюється Гідроген занурить до пробірки, що закріплена у штативі. Нагрівайте оксид Купруму (ІІ) слабким полум’ям горілки.
Завдання.
Написати рівняння реакції взаємодії Гідрогену з оксидом Купруму (ІІ).
__________________________________________________________________
За якою зовнішньою ознакою можливо встановити, що оксид Купруму перетворився у металічну мідь?
__________________________________________________________________
ДОСЛІД 3. Окисно-відновні властивості пероксиду Гідрогену
3.1. Окислення йодиду калію. До пробірки внести 3-4 краплі розчину йодиду калію, 1 краплю розчину сульфатної кислоти та 1 краплю 3%-го розчину пероксиду Гідрогену.
Завдання.
1. Написати рівняння реакції та вказати як змінюється колір розчину.
____________________________________________________________________
2. Які властивості виявляє пероксид Гідрогену в цій реакції?
___________________________________________________________________
3.2. Відновлення нітрату Ртуті (ІІ). До пробірки внести 3-4 краплі розчину та додати таку ж кількість розчину лугу до випадіння осаду оксиду ртуті (ІІ). Додати 4-5 крапель 3%-го розчину пероксиду Гідрогену та спостерігати зміну кольору осаду в зв’язку з утворенням часток металічної ртуті.
Завдання.
Написати рівняння реакції. Який газ виділяється?
____________________________________________________________________
ДОСЛІД 4. Каталітичне розкладення пероксиду Гідрогену
Внести до пробірки невелику кількість порошку перманганату калію та додати 2-3 краплі розчину пероксиду Гідрогену.
Завдання.
Написати рівняння реакції розкладення пероксиду Гідрогену.
___________________________________________________________________
До якого типу окисно-відновних реакцій вона відноситься? Який газ виділяється в реакції?
____________________________________________________________________
