
- •Тема: гідроген
- •Проста речовина
- •Лабораторна робота № 1 одержання та властивості гідрогену.
- •Контрольні питання
- •Тема: лужні метали
- •Лабораторна робота № 2 властивості лужних металів та їх сполук.
- •Контрольні питання
- •Тема: елементи іі-а групи
- •Лабораторна робота № 3 властивості магнію, лужноземельних металів та їх сполук
- •Лабораторна робота № 4 визначення жорсткості води.
- •Контрольні питання
- •Тема: елементи ііі – а групи
- •Лабораторна робота № 5 властивості алюмінію та його сполук.
- •Контрольні питання
- •Тема: елементи іv – а групи
- •Лабораторна робота № 6 властивості карбону, силіцію та їх сполук.
- •Контрольні питання
- •Лабораторна робота № 7 властивості стануму, плюмбуму та їх сполук.
- •Контрольні питання
- •Тема: елементи V – а групи
- •Лабораторна робота № 8 властивості нітрогену, фосфору та їх сполук.
- •Контрольні питання
- •Лабораторна робота № 9 розпізнавання нітратних та фосфорних добрив.
- •Контрольні питання
- •Тема: халькогени
- •Лабораторна робота № 10 властивості сульфуру та її сполук.
- •Контрольні питання
- •Тема: галогени
- •Лабораторна робота № 11 одержання та властивості галогенів.
- •Контрольні питання.
- •Лабораторна робота № 12 властивості галогеноводневих кислот. Якісні реакції на галоген-іони.
- •Контрольні питання.
- •Тема: елементи підгрупи хрому
- •Лабораторна робота № 13 властивості хрому та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи мангану
- •Лабораторна робота № 14 властивості мангану та його сполук
- •Контрольні питання
- •Тема: елементи родини феруму
- •Лабораторна робота № 15 властивості феруму та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи купруму
- •Лабораторна робота № 16 властивості купруму та його сполук
- •Контрольні питання.
- •Тема: елементи підгрупи цинку
- •Лабораторна робота № 17 властивості цинку та його сполук. Визначення іонів ртуті
- •Контрольні питання
- •Список рекомендованої літератури
Лабораторна робота № 6 властивості карбону, силіцію та їх сполук.
Мета роботи: отримання та дослідження властивостей кисневих сполук Карбону та Силіцію. Визначення явища адсорбції.
Прилади та реактиви. Спиртівка або сухе пальне, пробірки, скляна паличка, мікро колба, шпатель, піпетка, пробка, газовідвідна трубка. Лакмусовий папір. Карбон активований, мармур або крейда. Розчини: фуксину, хлороводневої, оцтової, конц. сульфатної кислот, гідроксиду кальцію, Карбонатів Натрію та калію, гідрокарбонату Натрію, хлоридів кальцію, стронцію, барію, силікату Натрію.
Техніка безпеки. Всі досліди, що супроводжуються виділенням оксиду Карбону(ІІ) і оксидів Нітрогену, проводити під тягою.
ДОСЛІД 1. Адсорбційна властивість Карбону
До пробірки налити 2-3 мл розчину фуксину і додати шпатель активованого Карбону. Пробірку зачинити пробкою і струшувати 2-3 хв. Дати розчину відстоятись.
Завдання.
Відмітити знебарвлення розчину і зробити висновок про адсорбційні властивості Карбону. Пояснити причини їх виникнення.
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
ДОСЛІД 2. Отримання оксиду карбону (IV) і визначення його властивостей
Зібрати прибор зображений на малюнку. В пробірку (мікро колбу) вмістити декілька кусочків мармуру або крейди і додати до ½ об’єму розчин хлороводневої кислоти. Швидко зачинити пробкою з газовідвідною трубкою, кінець якої опустити у пробірку. Для виявлення газу внести до пробірки запалену лучину.
Н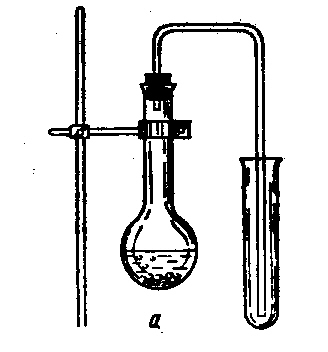 алити
до пробірки ¼ її ємкості вапнякової
води і пропустити вуглекислий газ до
утворення білого осаду. Продовжувати
пропускання СО2
до повного розчинення осаду.
алити
до пробірки ¼ її ємкості вапнякової
води і пропустити вуглекислий газ до
утворення білого осаду. Продовжувати
пропускання СО2
до повного розчинення осаду.
Завдання.
Написати рівняння взаємодії
а) мармуру з хлороводневої кислотою;
б) оксиду карбону (IV) з вапняковим молоком, враховуючи утворення карбонатів кальцію, а в надлишку СО2 – гідрокарбонату кальцію.
а)__________________________________________________________________
б)___________________________________________________________________
Зробити висновки про властивості вуглекислого газу
____________________________________________________________________________________________________________________________________________________________________________________________________________
ДОСЛІД 3. Відновні властивості карбону
До пробірки налити 2-3 краплі розчину концентрованої сульфатної кислоти та додати маленький кусочок Карбону. Закріпити пробірку у штативі та підігріти її на полум’ї спиртівки. Спостерігати виділення газу.
Завдання.
Визначити за запахом який газ виділяється та записати рівняння реакцій враховуючи, що Карбон окислюється до СО2. Яка речовина відновлюється?
________________________________________________________________________________________________________________________________________
ДОСЛІД 4. Отримання карбонатів лужноземельних металів та їх властивості
В дві пробірки налити 3-4 краплі розчину карбонату натрію та додати до першої розчин хлориду кальцію, до другої – хлориду барію. Дати осаду відстоятися, відібрати піпеткою надосадкову рідину, а до осадів додати розчин оцтової кислоти.
Завдання.
Відмітити колір утворених осадів і їх розчинення в оцтової кислоті. Написати рівняння всіх протікаючи реакцій.
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
ДОСЛІД 5. Гідроліз карбонатів
Нанести на червоний лакмусовий папір по краплині розчинів солей карбонатів натрію, калію та гідрокарбонату натрію. Відмітити колір паперу.
Завдання.
Визначити реакцію середовища, скласти рівняння гідролізу солей в молекулярному та іонно-молекулярному вигляді.
________________________________________________________________________________________________________________________________________Зробити висновок про силу вугільної кислоти.
____________________________________________________________________Чому гідрокарбонат натрію підлягає гідролізу в меншій мірі, ніж карбонат натрію?
________________________________________________________________________________________________________________________________________
ДОСЛІД 6. Отримання гелю кремнієвої кислоти
До пробірки налити конц. розчин силікату натрію і додати вдвічі менший об’єм розчину хлороводневої кислоти. Ретельно розмішати рідину скляною паличкою. Через деякий час утворюється колоїдна структура – драглі.
Завдання.
Скласти молекулярне та іонно-молекулярне рівняння взаємодії силікату натрію з хлороводневої кислотою.
________________________________________________________________________________________________________________________________________Зробити висновок про властивості кремнієвої кислоти.
________________________________________________________________________________________________________________________________________
ДОСЛІД 7. Отримання малорозчинних солей кремнієвої кислоти
До пробірки внести по 3-5 крапель розчинів солей: 1 – хлориду кальцію, 2 – нітрату кобальту, 3 – нітрату Плюмбуму, 4 – сульфату Купруму. Додати до кожної пробірки 2-3 краплі розчину силікату натрію. Відмітити колір осадів.
Завдання.
Скласти молекулярні та іонно-молекулярні рівняння відповідних реакцій.
1._______________________________________________________________________________________________________________________________________2._______________________________________________________________________________________________________________________________________3._______________________________________________________________________________________________________________________________________4._______________________________________________________________________________________________________________________________________
