
основы меаллургических процессов
.pdf
9.8.2. Влияние шероховатости
Какое существенное значение имеют пористые и шероховатые поверхности для процесса обезуглероживания, видно, например, из следующих опытов. Если при плавке стали в высокочастотной индукционной печи достичь путем увеличения мощности такой циркуляции, при которой жидкий шлак изолирует металл от стенок тигля, то газовыделение резко замедляется, а содержание углерода может стать в десятки или сотни раз больше равновесного.
При возобновлении контакта между сталью и огнеупорной футеровкой либо вследствие снижения мощности, подводимой к печи, либо в результате разрушения изолирующей прослойки шлака концом кварцевой палочки можно снова достичь интенсивного обезуглероживания.
Причина влияния рельефа пода заключается в том, что шероховатость изменяет угол смачивания, а пористость обусловливает сохранение зародышей газовой фазы.
Говоря о шероховатости, целесообразно ввести разграничение между макроскопическим краевым углом θ и микрокраевым углом θ0. Между ними существует следующая связь:
cos k cos |
|
|
S |
cos |
|
. |
(9.38) |
0 |
|
0 |
|||||
|
|
S0 |
|
|
|||
|
|
|
|
|
|
||
Здесь S и S0 – истинная и кажущаяся поверхности твердого тела; k – коэффициент шероховатости.
Иногда пользуются выражением:
1 |
|
|
k cos |
, |
(9.39) |
в котором cos – среднее значение косинуса крутизны микрорельефа. Соотношение (9.38) справедливо, когда высота и расстояние
между соседними гребнями микрорельефа малы по сравнению с капиллярной постоянной и радиусами микрокривизны мениска вблизи стенок. Необходимо, кроме того, чтобы сфера молекулярного действия обладала радиусом, меньшим такового для кривизны микрорельефа, и чтобы соблюдалось неравенство:
k cos 0 1.
191
Из уравнения (9.38) следует, что с ростом шероховатости увеличивается краевой угол, т.е. уменьшается смачиваемость. Последнее облегчает зарождение пузырька.
Таблица 9.2
Зависимость краевого угла от шероховатости поверхности
Содержание в стали, % |
Краевой угол θ, град., на |
|||
поверхности магнезита |
||||
|
|
|||
|
|
|
|
|
C |
Mn |
шероховатой |
гладкой |
|
|
|
|
|
|
1,14 |
0,13 |
150–153 |
139–135 |
|
|
|
|
|
|
0,15 |
0,50 |
162–170 |
124 |
|
|
|
|
|
|
0,16 |
0,50 |
151–157 |
121–126 |
|
|
|
|
|
|
В ряде случаев острые грани (гребни) шероховатой поверхности могут заметно снижать пересыщение, необходимое для образования зародыша пузырька.
9.8.3. Поры, смачиваемые жидким металлом
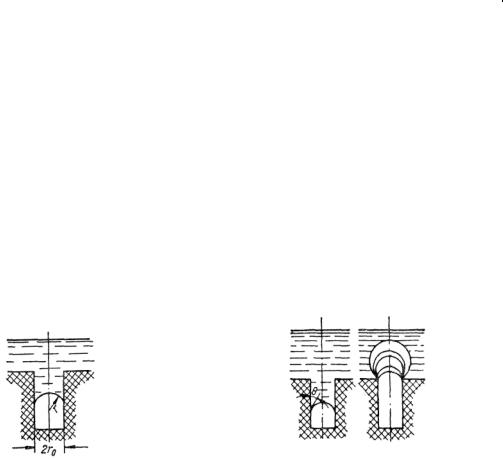
Когда жидкость находится в контакте с твердым телом, в порах которого содержится хотя бы небольшое количество газа, образование пузырьков сильно облегчается. При совершенной смачиваемости поверхность металла окажется не только выгнутой, но ее радиус кривизны r будет равен таковому для поры rп (рис. 9.10). Иначе говоря, газ, находящийся в объеме поры, является зародышем пузырька, который будет устойчивым, если rп rкр .
Рис. 9.10. Схема поры, частично заполненной жидкостью, смачивающей твердое тело
Рис. 9.11. Схема роста пузырька в поре, смачиваемой жидкостью
192
Таким образом, в случае совершенного смачивания поверхности твердого тела металлом, активными станут лишь те поры, радиус которых больше или равен критическому для пузырька. Сказанное относится, естественно, только к порам, не полностью заполненным сталью. Если же, в силу тех или иных обстоятельств, газ в них совершенно отсутствует, то такие поры при любых размерах неактивны.
Условия несколько изменяются, когда металл смачивает подкладку несовершенно (0 < θ < 90°). В этом случае
rп,кр rкр cos , |
(9.40) |
т.е. критический размер пор возрастает с ухудшением смачиваемости (с уменьшением угла θ).
Небольшие давления газа в пузырьке имеют место, очевидно, до тех пор, пока он находится в объеме поры. После его выхода в объем ванны условия роста становятся более благоприятными.
При этом отрыв пузырька будет происходить у вершины поры (рис. 9.11). Однако, в отличие от гладкой поверхности, где отрыв при θ<90 ° ведет к ликвидации зародыша, здесь, в порах, остается небольшое количество газа, облегчающее последующее формирование пузырьков.
9.8.4.Поры, не смачиваемые жидким металлом
Втех случаях, когда пористое твердое тело не смачивается жидким металлом, поверхность металла в поре будет выпуклой в сторону газовой фазы (θ > 90°). Такая кривизна обеспечивает лучшие условия газовыделения, чем те, которые имеются на плоской поверхности.
При θ > 90° давление газа в поре будет:
p |
|
p |
|
|
2 |
, |
(9.41) |
|
г |
внеш |
r |
||||||
|
|
|
|
|
||||
|
|
|
|
|
|
|
что меньше внешнего (pвнеш). В силу этого в пересыщенной системе будет происходить самопроизвольное разрастание объема газа в поре. Жидкость вытиснится из капилляра газом.
193

Рис. 9.12. Схема роста пузырька в поре, не смачиваемой жидкостью
Когда пограничная поверхность достигнет среза поры (рис. 9.12), она из выпуклой по отношению к газу (I, II) станет вогнутой (III) при том же краевом угле θ. Согласно уравнению 9.41, переход границы из положения I в положение II может осуществляться под действием капиллярных сил даже тогда, когда давление газа в поре меньше внешнего. Этого нет при передвижении границы из позиции II в позицию III, так как здесь поверхность раздела в начальный момент плоская.
Здесь рост пузырьков и переход поверхности в состояние с устойчивым краевым углом (θ > 90°) возможны лишь при пересыщении металла углеродом и кислородом, соответствующем плоской границе раздела.
Таким образом, для не смачиваемых подкладок центрами дегазации могут служить все не заполненные металлом поры. Если сталь в начале передела не была пересыщена газом, то последний может растворяться, переходя из пор в металл. Сталь будет заполнять капилляры, если их радиус удовлетворяет условию:
rп 2 cos . (9.42)
pвнеш
В результате этого подобные поры могут оказаться дезактивированными, т.е. не будут принимать участия в образовании пузырьков при последующем пересыщении металла.
Рост пузырька, сформировавшегося над порой, происходит в условиях постоянного угла θ путем постепенного расширения периметра контакта трех фаз (газ–подина–металл). Отрыв пузырька при θ > 90° осуществляется так же, как и на плоской поверхности, т.е. отделяется только верхняя часть пузырька. Его остаток (ножка) сохраняется на твердом теле и служит местом аккумуляции новых порций окиси углерода.
194
В заключение необходимо заметить, что оба рассмотренных случая (θ < 90° и θ > 90°) являются предельными. В процессе плавки величина θ не сохраняется постоянной. Так, например, для свеженаваренной футеровки, пористость которой близка в среднем к 6– 7%, краевой угол – тупой и колеблется от 108 до 128°. Здесь подавляющая масса пор является активной.
По мере ошлакования подины угол θ убывает и достигает значений, значительно меньших 90°. В этом случае активными становятся только те капилляры, радиус которых удовлетворяет выражению (9.40). В связи с этим выделение газа затрудняется и процесс обезуглероживания может замедляться.
Интенсивность кипения нередко повышается также и вследствие разрыхления верхнего слоя подины в результате реакции:
SiO2(тв) + 2C(мет) = Si(мет) + 2CO(газ)
9.9. Всплывание пузырьков
Всплывание пузырьков завершает процесс обезуглероживания. Оно выполняет при этом ряд весьма важных функций.
К ним, прежде всего, относится развитие фронта реакции в объеме ванны. Поднимающиеся пузырьки играют роль центров газообразования. Они растут за счет входящих в них молекул окиси углерода, а также растворенных в металле газов (N2, H2 и др.), являясь, таким образом, активными дегазаторами стали. Далее проходящие через шлак пузырьки реагируют с окислами железа, восстанавливая их до металла или ионов низшей валентности.
Они оказывают исключительно важное гидродинамическое воздействие на ванну, обусловливая ее сильное перемешивание. Этим самым резко увеличиваются коэффициенты массо- и теплопередачи, а также выброс капель металла в шлак и в атмосферу печи. Последнее имеет немаловажное значение для обезуглероживания и насыщения стали газами.
195
Глава 10 ОСНОВЫ ЛИКВАЦИОННЫХ И КРИСТАЛЛИЗАЦИОННЫХ
МЕТОДОВ РАФИНИРОВАНИЯ
10.1. Общая характеристика ликвационных явлений
Во многих металлургических процессах имеют место различного рода ликвационные явления, приводящие к разделению фаз. Под ликвацией (лат. – плавить, выплавлять) понимается нарушение однородности расплава, протекающее в жидком или затвердевающем металле. Гетерогенизация расплава обусловливается различием характера и величин сил взаимодействия между однородными и разнородными частицами составляющих расплавов.
Из гомогенного расплава при охлаждении и последующей выдержке при постоянной температуре происходит выделение одной или нескольких фаз в жидком или твердом виде, которые вследствие различия плотности с течением времени отделяются друг от друга. Таким образом, движущей силой ликвации в расплаве является гравитационное поле.
Несколько иного рода ликвация происходит при кристаллизации расплава, когда из однородной жидкой фазы выпадают частицы твердой фазы, обогащенные или обедненные вторым компонентом. В этом случае наиболее резко ликвационные явления проявляются в системах, для которых характерен большой температурный интервал кристаллизации, т.е. при наличии на диаграммах состояния широкой области между линиями ликвидуса и солидуса.
В процессе кристаллизации при формировании слитков или отливок ликвация носит обычно дендритный и зональный характер и является нежелательным явлением, так как сопровождается микро- и макронеравномерностью распределения примесей, что отрицательно сказывается на качестве металлопродукции.
Вместе с тем, ликвационные явления используются в качестве одного из методов рафинирования ряда цветных металлов. Эти методы предусматривают охлаждение рафинируемого расплава до определенной температуры и длительную выдержку при ней, при этом происходит выделение новой фазы, обогащенной примесью, и последующее ее отделение. Возможно проведение ликвационного процесса при охлаждении расплава, а также при нагреве твердого сплава. В последнем случае при так называемом зейгеровании происходит выплавление легкоплавкой структурной составляющей и
196
получение достаточно чистых от примесей кристаллов основного металла.
Явление разделения фаз, характерное для ликвационных методов рафинирования, имеет место и в ряде других металлургических процессов:
1)при окислительном рафинировании черновых металлов, при котором образуются частички оксидов примесей, переходящие из металлического расплава в шлаковую фазу;
2)при плавке на штейн и его переработке, при которой происходит разделение на металлическую, шлаковую и штейновую фазы;
3)при раскислении металлов, когда в результате присадки в кислородсодержащий расплав элементов-раскислителей образуется новая оксидная фаза – продукты раскисления;
4)при рафинировании металлов добавками серы (например, рафинировании свинца от меди) и при извлечении ценных примесей из расплавов присадками элементов, обладающих высоким химическим сродством к примесям (например, извлечение серебра и золота из свинца при помощи цинка) и др.
Во всех этих процессах, связанных с разделением фаз, на первой стадии происходит зарождение и рост новой фазы. Закономерности этих стадий были ранее рассмотрены применительно к термической диссоциации химических соединений. Эти закономерности остаются в значительной мере справедливыми и для вышеуказанных процессов. Последующими стадиями ликвационных процессов является укрупнение новой жидкой или твердой фазы и их отделение (т.е. всплывание или осаждение) из расплава.
10.2.Укрупнение новой фазы
Всоответствии с закономерностями гомогенного зарождения новой фазы устойчивы частицы, радиус которых превышает критический. Обычно образовавшиеся частицы новой фазы,
взвешенные в расплаве, имеют размер 10-7 см. Эти частицы представляют собой метастабильную, термодинамически неустойчивую фазу, поэтому испытывают естественное стремление к укрупнению. Укрупнение будет происходить за счет их столкновения, а также путем диффузионного роста частиц при наличии соответствующего пересыщения реагирующих веществ. Термодинамическая неустойчивость системы расплав – новая фаза обусловлена наличием избыточной энергии на поверхности раздела, поэтому движущей силой
197
укрупнения частиц новой фазы является межфазная энергия, сосредоточенная на поверхности расплав – новая фаза. Процесс укрупнения сопровождается уменьшением поверхности раздела, чему способствуют высокие значения межфазного натяжения.
Уменьшение энергии Гиббса на единицу поверхности ω при укрупнении двух частиц новой (A и B) фазы может быть оценено исходя из соотношения:
G |
A B |
|
A Me |
k |
B Me |
, |
(10.1) |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
где A B – удельная |
межфазная |
энергия |
на границе двух |
||||
контактирующих частиц A и B; A Me , B Me – то же на границе контакта
частица A или B – расплав; ω – поверхность включений; k – коэффициент, учитывающий неодинаковое изменение поверхности частиц A, B при их укрупнении.
Это соотношение справедливо как для слияния (коалесценции) жидких частиц, так и для слипания (коагуляции) твердых частиц. Явление укрупнения жидких частиц – коалесценция – это вполне естественный процесс, протекающий при их столкновении. При слиянии частиц, обычно имеющих сферическую форму, происходит уменьшение поверхности раздела, а следовательно, и снижение величины межфазной энергии на границе раздела фаз. Укрупнению жидких частиц способствуют высокие значения межфазного натяжения и соответственно малые величины вязкости расплава и частиц новой фазы. Скорость слияния ω двух капель одинакового размера пропорциональна межфазному натяжению и обратно пропорциональна вязкости и имеет вид:
|
|
|
|
|
, |
(10.2) |
|
k |
|
A Me |
|||
|
|
|
|
|
|
|
где η – динамическая вязкость; k – коэффициент.
При слиянии двух жидких частиц вначале происходит образование перешейка. Изменение радиуса перешейка a со временем η при слиянии двух соприкасающихся капель радиуса r описывается уравнением Я.И. Френкеля:
a2 |
3 |
|
r |
, |
(10.3) |
|
|
|
|||
|
|||||
|
2 |
|
|
|
|
198

где a – радиус кривизны перешейка; ζ – поверхностное натяжение; η – вязкость расплава.
В том случае, если сливаются капли с различными радиусами кривизны, то скорость слияния определяется меньшим радиусом. При различии значений вязкости расплава и капель новой фазы скорость коалесценции определяется вязкостью новой фазы.
Уравнение (10.3) дает достаточно хорошее совпадение расчетных и опытных данных при больших значениях вязкости новой фазы (более 0,7Па·с). При малых значениях вязкости сопротивление носит инерционный характер, и соотношение для радиуса перешейка имеет вид:
|
|
|
|
a2 k |
r / . |
(10.4) |
|
Явление укрупнения твердых частиц новой фазы, т.е. коагуляция, также является термодинамически возможным процессом. При коагуляции в результате столкновения происходит слипание частиц и последующее их спекание. Возможность протекания этого явления обусловлена тем, что в месте контакта двух частиц межфазная поверхностная энергия меньше, чем на поверхности раздела твердая частица – расплав. Таким образом, и при явлении коагуляции наблюдается стремление к уменьшению метастабильности системы, которая сопровождается снижением межфазной поверхностной энергии.
Вследствие несовершенства контакта при встрече двух твердых частиц, он может быть нарушен при малейшем движении металла, который образует прослойку (своего рода манжету) между частицами. Это обстоятельство обусловливает значительно меньшую скорость коагуляции (примерно в 105 раз) по сравнению с коалесценцией жидких частиц.
Жидкая манжета между частицами может быть удалена, следовательно, обеспечено достаточное слипание частиц при отрицательном значении изменения энергии Гиббса этого процесса, представленного следующим видом:
G 2 А газ A Me 0 . |
(10.5) |
Эта величина зависит от значения краевого угла смачивания θ расплавом поверхности твердой частицы. При θ > 90° обеспечивается слипание частиц и образование их скоплений; если θ < 90°, то процесс коагуляций термодинамически невозможен. Расчеты показывают, что
199

если краевой угол смачивания превышает 100°, турбулентный поток жидкого металла не может разорвать связь между контактирующими частицами и разобщить скопление частиц твердой фазы.
Скорость укрупнения твердых частиц определяется частотой и эффективностью их столкновения. Не каждая встреча частиц приводит
ких сцеплению. Столкновение и укрупнение частиц возможно:
1)в результате броуновского движения, т.е. под влиянием сил, действующих с одинаковой интенсивностью во всех направлениях (в этом случае происходит самопроизвольная или так называемая
перикинетическая коагуляция);
2)под воздействием направленного силового поля (гравитационного, электрического, концентрационного), в условиях естественной и принудительной конвекции (магнитного перемешивания, центробежных сил, температурного градиента). В этом случае имеет место так называемая ортокинетическая или
кинематическая коагуляция.
Перикинетический характер коагуляции свойственен частицам размерами 10-3–10-5 см, более крупные частицы не могут перемещаться под воздействием броуновских сил, т.е. по законам случайных блужданий. Если принять диффузионный механизм укрупнения частиц
радиусами r1 и r2, то скорость процесса выражается следующим уравнением:
1,2 4 r1,2D1,2n1n2 , |
(10.6) |
где r1,2 r1 r2 – расстояние между центрами частиц; D1,2 |
– константа |
массопереноса, представляющая собой сумму констант массопереноса частиц 1-го и 2-го типов; n1 и n2 – число частиц 1-го и 2-го типа в 1 см3 расплава.
Согласно С.И. Попелю, время η перикинетической коагуляции (т.е. время, необходимое для уменьшения концентрации частиц вдвое) зависит от вязкости расплава и исходной концентрации коагулирующих частиц, но не зависит от их размеров, т.е.
|
3 |
, |
(10.7) |
4kTn0 |
где n0 – начальное количество частиц в 1 см3 расплава; k – постоянная Больцмана.
200
