
- •Ответы к государственному экзамену по дисциплине "педиатрия" дня студентов лечебного факультета
- •1Ст-10-29%, 2ст.-30-49%, 3ст.- 50-99% , 4ст.-более 100%
- •Жаропонижающие препараты назначаются при повышении температуры тела выше 38°с:
- •Классификация
- •Лечебное питание назначается на срок не менее 1 года. Медикаментозное лечение
- •Особенности лечения гипомоторной джвп
- •Факторы риска. Особенности жкб у детей:
- •Лечение желчной коликипредусматривает:
- •1 Этап
- •2 Этап
- •3 Этап
- •I. Анамнестические:
- •II. Клинические:
- •III. Параклинические:
- •III. Параклинические:
- •Анатомическая сущность
- •I. Анамнестические:
- •II. Клинические:
- •III. Параклинические:
- •1. Инструментально – графические:
- •I. Клинические:
- •II. Параклинические:
- •3. Рентгенологические:
- •I. Клинические:
- •II. Параклинические:
- •1. Инструментально – графические:
- •2. Рентгенологические:
- •Варианты клинического течения
- •Ранние признаки хпн – полиурия, никтурия, анемия
- •9. Повышение ожсс.
- •I. Стероидная терапия:
- •II. Внутривенное высокодозное введение иммуноглобулина гамма.
- •III. Комбинированная терапия гкс и в/в иммуноглобулином:
- •IV. Анти-резус д иммуноглобулин:
- •V. Трансфузии тромбоцитов:
- •VI. Спленэктомия:
- •VII. Иммуносупрессивная терапия:
- •Причины.
- •Гипокальциемические судороги
- •Лечение гемолитической болезни новорожденных
- •I. Для гемолитических желтух характерно:
- •III. Для механических желтух характерно:
- •Лечение
- •2. Обеспечение влажности окружающей среды.
- •III. Лабораторная.
- •1. Дифтерия ротоглотки:
- •1. Типичная форма:
- •2. Атипичные формы:
- •1. Решение вопроса о госпитализации.
- •1. Специфические сложнения, обусловленные непосредственным действием вируса (гриппозной инфекцией):
- •Ведущие клинические синдромы оки:
- •Дифференциальный диагноз основных оки:
- •4. Псевдотуберкулез (скарлатиноподобная лихорадка):
- •3) Первичный туберкулезный комплекс:
- •4) Осложнения птб:
Гипокальциемические судороги
Гипокальциемицеские судороги (тетанические судороги, спазмофилия) – обусловлены снижением концентрации ионизированного кальция в крови.
Чаще встречаются у детей в возрасте от 6 месяцев до 1,5 лет при рахите (обычно весной), а также при гипофункции паращитовидных желез, при соматических заболеваниях, сопровождающихся длительной диареей и рвотой, и др.
Неотложная помощь:
1. При лёгких формах судорожных приступов назначить внутрь 5-10% раствор кальция хлорида или кальция глюконата из расчёта 0,1-0,15 г/кг в сут.
2. При тяжёлых приступах ввести парентерально:
- 10% раствор кальция глюконата в дозе 0,2 мл/кг (20 мг/кг) в/в медленно после предварительного разведения его раствором 5% глюкозы в 2 раза;
при продолжающихся судорогах 25% раствор магния сульфата 0,2 мл/кг в/м или 0,5% раствор седуксена 0,05 мл/кг (0,3 мг/кг) в/м.
Госпитализация после купирования судорог при необходимости в соматическое отделение. В постприступном периоде необходимо продолжить приём препаратов кальция внутрь в сочетании с цитратной смесью (лимонная кислота и натрия цитрат в соотношении 2:1 в виде 10% раствора по 5 мл 3 раза в сутки).
Острая сосудистая недостаточность у детей (обморок). Причины. Неотложная терапия.
Обморок (синкопальное состояние) – внезапная кратковременная потеря сознания с утратой мышечного тонуса вследствие переходящих нарушений мозгового кровообращения.
Наиболее частые причины обмороков у детей:
Синкопе вследствие нарушения нервной регуляции сосудов: вазовагальные, ортостатические, синокаротидные, рефлекторные, ситуационные, при гипервентиляционном синдроме.
2. Кардиогенные синкопе при:
брадиаритмиях (атриовентрикулярная блокада II-III степени с приступами Морганьи-Эдамса-Стокса, синдром слабости синусового узла);
- тахиаритмиях (пароксизмальная тахикардия, в том числе при синдроме удлинённого интервала QT, мерцательная аритмия);
механическом препятствии кровотоку на уровне сердца или крупных сосудов (стеноз аорты,гипертрофический субаортальный стеноз, недостаточность аортальных клапанов и др.).
3. Гипогликемические синкопе.
Цереброваскулярные и др.
Неотложная помощь:
Уложить ребёнка горизонтально, приподняв ножной конец на 40-500. Расстегнуть воротничок, ослабить пояс и другие детали одежды, оказывающие давление на тело. Обеспечить доступ свежего воздуха.
Использовать рефлекторные воздействия:
обрызгать лицо водой или похлопать по щекам влажным полотенцем;
дать вдохнуть пары нашатырного спирта.
При выходе из этого состояния дать выпить горячий сладкий чай.
При затянувшемся обмороке назначить:
10% раствор кофеина-бензоата натрия 0,1 мл/год жизни п/к или
раствор кордиамина 0,1 мл/год жизни п/к.
При выраженной артериальной гипотензии ввести 1% раствор мезатона 0,1 мл/год жизни в/в струйно.
При гипогликемическом состоянии ввести 20-40% раствор глюкозы 2 мл/кг в/в струйно.
При выраженной брадикардии и приступе Морганьи-Эдамса-Стокса провести первичные реанимационные мероприятия: непрямой массаж сердца, введения 0,1% раствора атропина 0,01 мл/кг в/в струйно.
Госпитализация при обморочном состоянии функционального генеза не показана, но если есть подозрение на органическую причину, необходима госпитализация в профильное отделение.
Острый лейкоз. Этиология. Классификация. Клиническая картина. Диагностика. Лечение.
Острые лейкозы - злокачественная пролиферация кроветворных клеток, возникающая вследствие соматической мутации в одной стволовой клетке, потомки которой формируют лейкемический клон.
Необходимым условием развития лейкемического клона является расстройство процессов клеточной дифференцировки и пролиферации с накоплением незрелых форм кроветворных клеток.
Этиология.
ионизирующая радиация;
химические вещества – бензин, тяжелые металлы, нефтяные продукты в развитии ОМЛ;
лекарства – использование алкилирующих препаратов в сочетании с радиотерапией повышают риск развития ОМЛ (как вторичных опухолей);
генетические нарушения:
однояйцевые близнецы: риск развития ОЛ повышается в 20 раз, если у одного из них есть лейкоз; как правило, лейкоз развивается в течение первых 5 лет жизни;
если у одного из родителей лейкоз, у детей риск развития лейкоза в 4 раза выше, чем в основной популяции;
хромосомные аномалии – синдром Дауна (риск развития лейкоза 1 : 95, интервал времени менее 10 лет), синдром Блума (1 : 8, возраст до 30 лет), анемия Фанкони (1 : 12, возраст до 16 лет); кроме того, синдром Кляйнфельтера и другие заболевания, связанные с изменением хромосом, характеризуются развитием ОМЛ;
вирусная теория лейкозов: ВЭБ – лимфома Беркитта, Т-клеточный лейкоз взрослых; ретровирус типа С – Т-клеточный лейкоз взрослых;
повышение частоты случаев лейкоза при следующих генетически обусловленных заболеваниях:
наследственная агаммаглобулинемия, синдром Швахман-Даймонда, Блекфана-Даймонда, синдром Костманна, синдром семейной моносомии 7, семейный синдром множественного рака с острым лейкозом, нейрофиброматоз.
Классификация лейкозов:
острый лимфобластный лейкоз (ОЛЛ) – 75%;
острый миелобластный лейкоз (ОМЛ) – 20%;
острый недифференцированный лейкоз (ОНДЛ) – менее 0,5%;
ОЛ смешанной линии (с коэкспрессией):
ОЛЛ с экспрессией 2 миелоидносвязанных Аг – 6% всех случаев ОЛЛ;
ОМЛ с экспрессией 2 лимфоидносвязанных Аг – 17: всех случаев ОМЛ;
ХМЛ – 3% (взрослая форма).
Морфологическая классификация (FAB):
ОЛЛ: L1, L2, L3:
L1 – малые лимфобласты с небольшим количеством цитоплазмы и нуклеолей (80% у детей); наиболее благоприятный;
L2 – более крупный лимфобласт с преобладанием нуклеолей (14%); неблагоприятный;
L3 – лимфобласты с базофильной цитоплазмой (1%); самый неблагоприятный: рецидив через 0,5 года после химиотерапии, выживаемость небольшая.
ОМЛ: М0, М1, М2, М3 – М3м, М4, М5 (М5а – М5b), M6, M7:
М0 – минимально дифференцированный ОМЛ (6% у детей);
М1 – ОМЛ без созревания (10%);
М2 – ОМЛ с созреванием (27%);
М3 – ОПЛ – промиелоцитарный (5%);
М3м – микрогранулярный промиелоцитарный;
М4 – острый миеломоноцитарный (21%);
М5: М5а – острый монобластный и М5b – острый моноцитарный (22% у детей);
М6 – острая эритролейкемия (3%);
М7 – острый мегакариобластный лейкоз (6%).
Иммунологическая классификация:
Для ОЛЛ:
ранний пре-В (54%) – commonB;
пре-В (25%);
транзиторный пре-В (4%);
В-клеточный зрелый (2%);
Т-клеточные (15%)
Для ОМЛ:
морфологическая (FAB) и иммунологическая совпадают.
Клиническая картина.
Общие симптомы включают:
температура в 60% случаев,
усталость – в 50%,
бледность – в 40%.
Симптомы, связанные с поражением костного мозга:
анемия: бледность, утомляемость, тахикардия, диспноэ, снижение Hb, эритроцитов;
нейтропения: температура, язвенно-некротический стоматит, инфекция;
тромбоцитопения: петехии, пурпура, экхимозы, кровоточивость из слизистых, редко – кровоизлияние в мозг.
Поражение лимфоидной системы:
лимфаденопатия (генерализованная), редко – поражение лимфоузлов средостения (синдром верхней полой вены);
спленомегалия;
гепатомегалия.
Экстрамедуллярное поражение (5%):
признаки и симптомы повышения внутричерепного давления – утренняя головная боль, рвота;
признаки и симптомы вовлечения паренхимы мозга в патологический процесс: гемипарезы, параличи черепных нервов, судороги, при вовлечении головного мозга – атаксия, гипотония, гиперрефлексия;
гипоталамический синдром: полифагия с чрезмерной прибавкой в весе, нарушение поведения;
несахарный диабет (при вовлечении заднего гипофиза);
поражение спинного мозга: боли в спине, ногах, слабость, потеря чувствительности конечностей, проблемы сфинктеров мочевого пузыря, прямой кишки;
кровоизлияние в ЦНС – осложнение, которое возникает чаще у пациентов с ОНДЛ, чем при ОЛЛ. Причины:
а) лейкостаз в сосудах головного мозга, ведущий к лейкотромбозу, инфарктам, геморрагиям;
б) тромбоцитопения и коагулопатия потребления.
Признаки поражения половой системы:
поражение яичек – у 10-23% больных мужского пола;
безболезненны;
скрытое поражение диагностируется у 10-33% пациентов при проведении билатеральной биопсии в течение первых 3 лет от начала лечения.
факторы риска вовлечения яичек в процесс:
Т-ОЛЛ;
лейкоцитоз > 20000;
наличие медиастинальной массы;
умеренная или выраженная гепатоспленомегалия или лимфаденопатия;
тромбоцитопения < 30000;
яичники у девочек вовлекаются в процесс редко.
Признаки поражения мочевой системы:
определяется у многих пациентов с помощью УЗИ;
иногда может проявляется гематурией, гипертензией или острой почечной недостаточностью.
Признаки поражения ЖКТ:
ЖКТ очень часто поражается при ОЛЛ;
наиболее частым проявлением является кровотечение из ЖКТ;
не имеет клинических проявлений, при терминальной стадии лейкоза возникает некротическая энтеропатия. Часто поражается толстый отдел кишечника – тифлит.
Признаки поражения костей и суставов:
костные боли – это наиболее частый признак поражения костей и наблюдается у 25% пациентов. Результат поражения лейкозным инфильтратом костей – периостит, инфаркты костей, замещение костных полостей бластными клетками.
Признаки поражения кожи:
поражение кожи часто возникает у больных неонатального периода при остром нелимфобластном лейкозе.
Признаки поражения ССС:
2/3 пациентов имеют признаки вовлечения сердечно-сосудистой системы в лейкозный процесс и диагностируются чаще на аутопсии, клинические признаки поражения ССС имеют место менее чем у 23% больных.
Признаки поражения легких:
признаки лейкозной инфильтрации и кровоизлияния.
Диагностика.
клинические проявления:
периферическая кровь:
нормоцитарная, нормохромная анемия;
число лейкоцитов: снижено, нормальное или повышено;
формула крови – бластоз (более 25%), лимфоцитоз;
тромбоцитопения (92% пациентов);
серьезные кровотечения возникают при уровне тромбоцитов < 25000;
морфологическое исследование костного мозга (костно-мозговая пункция);
цитохимическое исследование костного мозга:
миелопероксидаза, липиды, гликоген, неспецифические эстеразы (альфа-нафтилацетатэстераза и альфа-нафтилбутиратэстераза);
иммунофенотипирование бластных клеток;
молекулярно-биологическое исследование на протоонкогены (ПЦР);
цитогенетическое исследование;
ММТ – тест (на чувствительность к цитостатикам);
исследование на апоптоз;
рентгенография органов грудной клетки;
скелетограмма (при необходимости);
КТГ (органов грудной полости, брюшной полости, головы);
биохимические исследования:
электролиты, мочевина, мочевая кислота, печеночные пробы, билирубин и др.;
исследование ликвора:
биохимический состав и клетки;
спинномозговая жидкость имеет диагностическое значение при диагностике нейролейкоза;
а) повышение лейкоцитов свыше 5/мм3;
б) идентификация бластных клеток после центрифугирования;
в) окраска клеток;
гемостазиограмма:
снижение факторов коагуляции часто наблюдается при ОМЛ, включает гипофибриногенемию, фактор V, IX, X;
исследование функции ССС:
ЭКГ, УЗИ сердца;
исследование иммунологии:
уровень сывороточных иммуноглобулинов, уровень С3 и С4;
исследование вирусологического профиля:
титр АТ к вирусу ветряной оспы, ЦМВ, ВЭБ, АТ к вирусу простого герпеса, скрининг АТ гепатитов (HBV, HCV, HBV+HDV, HGV, HFV, HXV).
Стратегия лечения ОЛЛ:
Группы риска детей:
низкий фактор риска;
стандартный фактор риска;
высокий.
Группа низкого риска:
по иммунофенотипированию – незрелый В-клеточный ОЛЛ;
с гиперплоидией (более 50 хромосом);
с транслокацией (12; 21);
возраст от 1 до 9 лет;
с количеством лейкоцитов менее 50000/мм3.
Группа среднего риска:
все пациенты с Т-ОЛЛ имеют риск развития рецидива, исключая тех, у которых диагностирована ремиссия в индукционную фазу терапии;
пациенты с Т-ОЛЛ по иммунофенотипированию протимоциты (СД7+, СД2–, СД5–) имеют худший прогноз, чем пациенты с более зрелым Т-фенотипом.
Группа высокого риска – лейкозы В-клеточной линии при наличии:
гена BCR-ABL (ПЦР) или транслокации (9; 22);
гиперлейкоцитоза;
с плохим ответом на преднизолоновую профазу;
с транслокацией (4; 11); (11; 19); (1; 11) (у детей до года);
при отсутствии ответа на индукционную терапию (на 33 день).
Лечение:
Современная химиотерапия – это комбинированное, интенсивное лечение, которое проводится определенными циклами с интервалами различной продолжительности.
Задача индукционной терапии: максимально полное удаление лейкозных клеток, а поддерживающей терапии – контроль за вхождением в митотический цикл и делением покоящихся бластных клеток.
При ОЛ оценка эффективности проводится по:
динамике клинических проявлений;
темпам нормализации показателей периферической крови и КМ.
Основные принципы ПХТ:
максимально раннее начало комплексного лечения с момента установления точного диагноза;
проведение лечения в специализированных детских онкологических стационарах;
использование комбинаций цитостатических препаратов в адекватных дозах (расчет не на кг, а на м2) и режимах как в остром периоде, так и в ремиссии (лечение по протоколам);
проведение адекватного симптоматического лечения с применением компонентов гемотрансфузионной терапии (тромбоконцентрат, эритроцитарная масса, СЗП, факторы свертывания), антибактериальной терапии и др.
Цитостатический эффект препарата определяется:
фармакокинетикой препарата;
временем генерации опухолевых клеток;
влиянием препарата на переход клеток из одной фазы клеточного цикла в другую.
В программном лечении злокачественных новообразований крови и лимфоидной ткани выделяют следующие этапы:
индукция ремиссии;
консолидация;
поддерживающее лечение в периоде ремиссии (для ОЛЛ).
Этапу индуктивной терапии предшествует недельная циторедуктивная профаза (преднизолоном) с целью снижения объема опухолевой массы, предупреждения острого лизиса опухолевых клеток, определения чувствительности опухолевых клеток к ГКС.
Использование винкристина, преднизолона и L-аспарагиназы позволяет добиться полной ремиссии у 85-95% детей. За счет добавления антарциклинов удалось увеличить пятилетнюю выживаемость с 39 до 64%.
При лечении высокодозными блоками ПХТ добавляют Г-КСФ: он не влияет на пролиферацию опухолевых клеток, не снижает процент достижения ремиссии, уменьшает длительность аплазии.
ТКМ (трансплантация) не используется у детей с ОЛЛ стандартного риска. Аллогенная ТКМ применяется у больных с высоким риском – t(9; 22), t (4; 11). Пятилетняя безрецидивная выживаемость – 54%.
Терапия для группы низкого риска включает антиметаболиты + дексаметазон + винкристин; для стандартного риска – более интенсивная ПХТ; для высокого – блоки высокодозной терапии с трансплантацией периферической стволовой клетки.
Критерии доношенности и недоношенности. Определение. Понятие морфологической и функциональной зрелости (шкала Petruss,Dubovich).
ВОЗ: Недоношенным считается ребенок, родившийся в сроке гестации 37 и менее недель с массой 2500 г и менее и длиной 45см и менее.
В настоящее время в республике принят основной критерий недоношенности – гестационный возраст.
Недоношенный – ребенок, родившийся при сроке менее 37 полных недель беременности (до 260 дня).
Доношенный – ребенок, родившийся при сроке беременности от 37 до 42 недель, т.е. между 260 и 294 днями беременности.
Среди детей, имеющих массу при рождении менее 2500 г, до 1/3 – доношенные, а средняя масса тела ребенка на 37 неделе может составить около 3000 г.
Исходя из гестационного возраста выделяют 4 степени недоношенности:
I – 35-37 недель;
II – 32-34 недели;
III – 29-31 недели;
IV – 28 и менее
Зрелый новорожденный – ребенок по морфофункциональному состоянию готовый к внеутробной жизни при рациональной организации ухода и вскармливания. Зрелый ребенок хорошо удерживает температуру тела, у него есть сосательный, глотательный и другие рефлексы периода новорожденности, устойчивый ритм сердечных сокращений и дыхания, нормальная двигательная активность.
ВНЕШНИЕ морфологические признаки недоношенного ребенка:
Непропорциональное телосложение (длина головы колеблется от 1/4 до 1/3 роста). Преобладание мозгового черепа над лицевым. Швы и роднички открыты. Кости черепа тонкие, может быть конфигурация черепа (кости заходят одна на другую). Ядра окостенения в эпифизах обычно отсутствуют.
Яркая, темно-красная кожа, тонкая и глянцевая, как бы просвечивающаяся, слабая выраженность кожных складок на подошвах.
Лянуго – густой пушок, может быть на спине, лице, конечностях (только на разгибательных поверхностях).
Снижение подкожно-жирового слоя вплоть до полного отсутствия, склонность к отеку подкожно-жировой клетчатки.
Низко расположенный пупок.
Недоразвитие молочных желез (околососкового кружка и ткани), отсутствие гормонального криза.
Ногти тонкие, не всегда доходят до краев ногтевого ложа.
Мягкие хрящи ушных раковин.
Недоразвитие наружных гениталий.
Экзофтальм.
Мягкие кости черепа, открыты швы и малый родничок.
По совокупности морфологических признаков можно оценить зрелость ребенка.
Наиболее употребима шкала Petrussa (1971)
|
Признаки |
2 |
1 |
0 |
|
Ушная раковина |
Оформлена, твердая |
Только сверху завернута |
Бесформенная, мягкая |
|
Сосок(ореол) |
> 5 mm |
< 5 mm |
Розовая точка |
|
Большие половые губы |
> малых половых губ |
= малым половым губам |
< малых половых губ |
|
Яички |
В мошонке |
У входа в мошонку |
Не опущены |
|
Кожа |
Розовая |
Красная или отечная |
Тонкая, красная и отечная |
|
Исчерченность стоп |
Почти полностью |
Дистальная половина |
Дистально 1-2 черты |
Гестационный возраст = сумма баллов + 30.
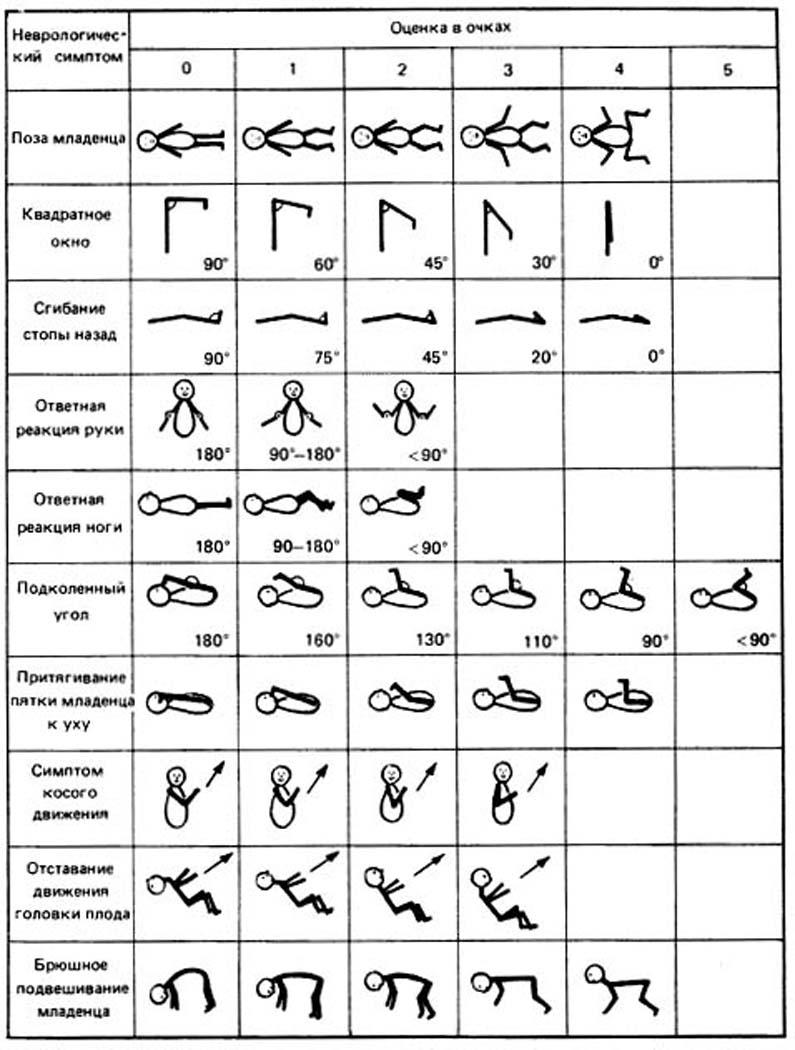
Шкала Дубовича – учитывает не только внешние, но и функциональные признаки незрелости, а именно нейромышечную зрелость
НЕЗРЕЛОСТЬ ОРГАНИЗМА НЕДОНОШЕННОГО РЕБЕНКА ЗАТРАГИВАЕТ ТАКЖЕ ФУНКЦИИ ЖИЗНЕННО ВАЖНЫХ ОРГАНОВ И СИСТЕМ: ЦНС, ССС , ДЫХАТЕЛЬНОЙ И ДР.
Нервная система: Особенности неврологического статуса недоношенных по сравнению с доношенными:
Меньшая двигательная активность, слабый крик.
Преобладание тонуса сгибателей над разгибателями без физиологического гипертонуса мышц. Флексорный гипертонус обычно появляется у них в 1-2 месяца жизни.
Снижение физиологических рефлексов, в том числе сосательного. У здоровых недоношенный с массой до 1500 г способность к сосанию появляется в течение 1-2 недель жизни, с массой от 1500 до 1000 г – на 2-3 неделе жизни, менее 1000 г – к месяцу жизни.
Несовершенство терморегуляции.
Дыхательная система: Первичные ателектазы легких, лабильность частоты (35-60) и глубины дыхания, частые апноэ.
Сердечно-сосудистая система: Лабильность частоты сердечных сокращений (140-180 в минуту), сосудистая дистония. Синдром Арлекина (описан в 1927 г).
Пищеварительная система: Снижение толерантности к пище, повышенная проницаемость сосудистой стенки.
Мочевыделительная система: Низкая фильтрационная и осмотическая функция почек.
Метаболизм: Гипопротеинемия, гипогликемия, гипокальциемия, гипербилирубинемия, метаболический ацидоз.
Иммунная система: Низкий уровень гуморального иммунитета и неспецифических факторов защиты (фагоцитоз, комплемент и др.).
Основные группы риска в развитии патологических состояний при рождении. Организация наблюдения за ними в родильном доме.
Для прогнозирования и предупреждения развития патологических состояний у новорожденных детей в раннем неонатальном периоде, проводится анализ здоровья матери, патологии течения беременности и родов, состояния ребенка в период ранней адаптации. Все патологические процессы, происходящие в организме беременной женщины, которые могут повлечь за собой нарушения в состоянии плода и новорожденного, принято называть факторами риска, В зависимости от факторов риска, для новорожденных выделяют группы риска:
|
Группа риска |
Факторы риска |
Мероприятия |
|
1. Острые инфекции в родах. Перенесенные инфекции во время беременности (особенно вирусные) в последнем триместре беременности. 3. Хронические очаги инфекции с обострениями во время беременности. 4. Носитель патогенного стафилококка. 5. Криминальное вмешательство. 6. Роды на дому. 7. Эндометрит в родах. 8. Длительный безводный период (более 5-6 ч.). 9. Лихорадка в родах. 10. Преждевременные роды. 11. Эндокринная патология (сахарный диабет, гипотиреоз).
|
родзал 1. Забор крови из сосудов пуповины - острофазоьые показатели (СРБ, общий белок и его фракции, церулоплазмин, серомукоид). 2. В первый час жизни посевы из наружного слухового прохода, содержимого желудка или ТБД, мекония, крови из пупочных сосудов на флору и чувствительность к антибиотикам. 3. Кровь из пупочных сосудов на иммуноглобулины А и М. 4. Бактериоскопия желудочного содержимого или ТБД. 5. Отослать плаценту на гистологическое и бактериологическое исследование. 6. Если нет противопоказаний со стороны матери или новорожденного, дача молозива в родзале. Палата новорожденных 1. Общий анализ крови, тромбоциты. 2. Динамика острофазовых показателей крови (СРБ, общий белок и его фракции, ДФА, церулоплазмин, серомукоид). 3. Термометрия через 4-6 часов первые три дня жизни. 4. Планирование введения иммуноглобулина человеческого из расчета 0,2-0,5 мл/кг. |
|
2. Риск развития гемолитической болезни новорожденных (ГБН) |
|
родзал
2. Обеспечить свободное истечение крови матери из сосудов пуповины. 3. Определить группу крови и резус-фактор новорожденного из пуповинной крови. 4. Провести забор крови из пуповины для лабораторного определения билирубина по фракциям, альбумина, прямой реакции Кумбса. 5. Первобеременным резус-отрицательным женщинам, родивших резус-положительных детей в/м в течение первых 3-х суток ввести антирезусную сыворотку. Палата новорожденных 1. Общий анализ крови, ретикулоциты, гематокрит, тромбоциты. 2. Исследование билирубина по фракциям в динамике с подсчетом его почасового прироста 3. При необходимости повторное проведение прямой реакции Кумбса или желатиновой пробы. 4. Определение глюкозы в крови. 5. При необходимости проведение непрямой реакции Кумбса (матери). 6. В первые сутки жизни - очистительная клизма дважды |
|
3. Риск интранатального поражения головного мозга |
1. Внутриматочная гипоксия плода, асфиксия новорожденного. 2. Оперативное родоразрешение (акушерские щипцы, вакуум-экстракция и т.д.). 3. Стремительные, быстрые, затяжные роды, потужной период менее 15 мин или более 1ч., безводный период более 12 часов. 4. Крупная масса плода (более 4 кг). 5. Аномальное положение плода (ягодичное, ножное, поперечное.). 6. Роды на дому. 7. Преждевременные роды. |
родзал 1. Кровь из пуповины на электролиты (натрий, калий, кальций, магний) 2. КОС. 3. Глюкоза в крови. Палата новорожденных 1. Общий анализ крови, гематокрит, тромбоциты 2. КОС, глюкоза в крови и электролиты в динамике. 3. Антигеморрагическая терапия (викасол, дицинон). 4. Охранительный режим 5. УЗИ головного мозга. 6. Осмотр окулиста |
|
4. Риск РАЗВИТИЯ ГИПОГЛИКЕМИИ |
1. Дети, родившиеся от матерей, больных сахарным диабетом. 2. Дети с нарушением внутриутробного роста (маловесные и маленькие к сроку гестации) и недостаточным питанием. 3. Недоношенные дети. 4. Новорожденные, родившиеся в гипоксии, асфиксии. 5. Меньший из близнецов. 6. Дети после операции заменного переливания крови. 7. Крупновесные дети (более 4000 г) для своего срока гестации. |
родзал 1. Реанимацию проводить с введением глюкозы только при наличии показателя глюкозы в крови новорожденного. 2. Новорожденным родившихся от матерей с сахарным диабетом, при реанимационных мероприятия использовать физиологический раствор. 3. Дача молозива в родзале при отсутствии противопоказаний со стороны матери и новорожденного. Палата новорожденных 1. Контроль за уровнем глюкозы в крови в течение первых 3-х суток жизни (правило троек или четверок). 2. Раннее прикладывание к груди с увеличением числа кормлений. Исходя из показателей глюкозы в крови ребенка, решать вопрос об оральном или парентеральном введении глюкозы. |
|
5. Риск РАЗВИТИЯ РЕСПИРАТОРНОГО ДИСТРЕСС-СИНДРОМА (РДС) |
1. Недоношенные дети, родившиеся в сроке гестации менее 35 недель. 2. Дети, перенесшие в/маточную гипоксию или асфиксию 3. Дети, родившиеся от матерей больных сахарным диабетом, гипотиреозом 4. Дети, родившиеся путем операции кесарева сечения. 5. Дети от матерей с гестозом. 6. Вторые из двоен. 7. Тяжелое течение ГБН. |
родзал 1. Профилактика РДС в дородовом периоде (глюкокортикоиды, мукосолван, этимезол, эуфиллин, лактин, бромгексин и т.д.) 2. Проведение пробы Клементса или пенного теста с околоплодными водами до рождения. 3. Эндотрахеальное введение сурфактанта (по показаниям). 4. Соблюдение температурного режима, не допускать переохлаждения ребенка. 5. Забор крови из пупочных сосудов на КОС. Палата новорожденных 1. Поместить ребенка в нагретый кувез. 2. В зависимости от степени тяжести РДС, решить вопрос о методе проведения оксигенотерапии (носовые катетеры, кислородная палатка, СДППД - Грегори, клапан Бенвенисте, назофаригеальные катетеры; ИВЛ). 3. Общий анализ крови, гематокрит в динамике. 4. КОС и электролиты в динамике. 5. Контроль в динамике за тяжестью РДС. |
|
6. Риск развития острого анемического синдрома |
1. Остальные геморрагии (спонтанные, при вскрытии околоплодного пузыря, фето-фетальная трансфузия и т.д.). 2. Плацентарные геморрагии (отслойка плаценты, парез плаценты во время операции кесарева сечения, гематомы плаценты и т.д.). 3. Послеродовые геморрагии (ВЧРТ, кефалогематомы, травмы паренхиматозных органов, геморрагическая болезнь новорожденных, коагулопатии, ДВС-синдром и т.д.) |
родзал 1. Пальцевое перекачивание крови по пуповине от матери к ребенку. 2. Определить группу крови и резус-фактор у ребенка. 3. По показаниям проведение реанимационных мероприятий по выведению ребенка из гиповолемического шока. Палата новорожденных 1. Общий анализ крови, гематокрит, тромбоциты (в 1-е сутки не менее 2-х раз). 2. Контроль за АД, ЦВД, ЧСС, ЧД, диурезом |
|
7. Риск развития геморрагического синдрома |
1. Дети с нарушением внутриутробного роста (маловесные и маленькие к сроку гестации) и недостаточным питанием.
3. Матери, страдающие сахарным диабетом. 4. Гестоз 5. Преждевременная отслойка плаценты. 6. Прием матерью медикаментов (салицилаты, антикоагулянты). 7. Внутриутробная гибель одного из близнецов. 8. Операция заменного переливания крови. 9. Внутриутробные инфекции, особенно вирусной этиологии. 10. Недоношенные дети 11. Переохлаждение ребенка. |
родзал 1. Не допускать охлаждения ребенка. 2. Определение группы крови и резус-фактора из пуповинной крови. Палата новорожденных 1. Общий анализ крови, тромбоциты, гематокрит. 2. Протромбиновый индекс. 3. По показаниям: фибриноген, плазминоген, время свертывания, длительность кровотечения, коагуляционный профиль. 4. Ввести викасол 1мг/кг. Назначить ангиопротекторы (дицинон, адроксон, этамзилат 0,1-0,2 мл/кг, аскорутин). |
|
8. Рискразвития гипербилирубинемии |
1. Дети от матерей, страдающих сахарным диабетом, гипотиреозом. 2. Недоношенные дети. 3. Дети, родившиеся в асфиксии. 4. При полицитемическом синдроме. 5. Наличие у детей кефалогематом, гематом, геморрагической сыпи. 6. Пренатальные и постнатальные инфекции. 7. Эксикоз. 8. Гипогликемия, гипопротеинемия. 9. Медикаменты, применяемые женщинами и новорожденными |
родзал Определение группы крови и резус-фактора, общего белка в пуповинной крови. Палата новорожденных 1. Общий анализ крови, гематокрит. 2. Определение уровня билирубина по фракциям в динамике. 3. Глюкоза в крови, общий белок, альбумин в динамике. 4. При высоких цифрах непрямого билирубина - прямая реакция Кумбса. |
Группы здоровья для новорожденных. Особенности диспансерного наблюдения за новорожденными в поликлинических условиях в зависимости от групп здоровья.
При выписке ребенка из родильного дома, неонатолог должен провести комплексную оценку его здоровья и определитьгруппу здоровья. В периоде новорожденности выделяют III основных группы здоровья:
I - здоровые дети, которые родились от здоровых родителей, с нормальным течением беременности и родов, с оценкой по шкале Апгар 8-9 баллов, не болевших в роддоме или имевшие пограничные состояния, которые не повлияли на состояние здоровья ребенка.
II - практически здоровые дети, но имеющие 1 или более фактора риска заболевания (поражение ЦНС, инфицирование, эндокринные или трофические расстройства). По степени выраженности риска, II группа здоровья разделяют на II A и II Б.
Группа здоровья IIA - практически здоровые новорожденные, не болевшие в роддоме, с минимальной степенью риска возникновения патологических процессов в позднем неонатальном периоде, это:
· дети, родившиеся от матерей с отягощенным биологическим и клиническим анамнезом;
· недоношенные I степени, при удовлетворительном течении раннего периода адаптации.
Группа здоровья IIБ - практически здоровые младенцы, но имеющие несколько групп риска, а также перенесшие заболевания в раннем неонатальном периоде, завершившиеся к моменту выписки из роддома.
III группу здоровья составляют больные дети с хроническими врожденными заболеваниями, тяжелыми пороками развития в фазе компенсации.
Новорожденные I группы здоровья наблюдаются участковым педиатром и осматриваются специалистами в обычные сроки.
Дети, группы здоровья IIА, осматриваются участковым педиатром не менее 4-х раз, а II Б 5 и более раз с обязательным осмотром зав. отделением. При необходимости проводятся лабораторные исследования: общий анализ крови, мочи, бактериологическое исследование, УЗИ.
Новорожденные III группы здоровья находятся на диспансерном наблюдении участкового педиатра и профильного специалиста.
Перинатальная и неонатальная смертность Определение. Показатели. Нозологическая структура Пути снижения.
Одним из важных показателей развития здравоохранения является показатель МЛАДЕНЧЕСКОЙ СМЕРТНОСТИ, который характеризует количество умерших детей от 0 до 1-го года жизни и рассчитывается по формуле:
число умерших детей на 1-ом году жизни X 1000
число родившихся живыми
За 2009 год младенческая смертность в нашей Республике составила 4,7 случаев на 1000 детей, родившихся живыми
Ее структура:
1 место - врожденные аномалии развития,
2 место - состояния возникающие в перинатальном периоде,
3 место - грипп, ОРВИ, пневмонии,
4 место - прочие заболевания.
В свою очередь младенческая смертность включает в себя НЕОНАТАЛЬНУЮ СМЕРТНОСТЬ от 0 до 28-и дней, которая рассчитывается по формуле:
число детей умерших от 0 до 28 дней X 1000
число родившихся живыми
Ранняя неонатальная смертность от 0 до 7-го дня жизни и рассчитывается по формуле:
число детей умерших от 0 до 7 дня X 1000
число детей родившихся живыми
Структура ранней неонатальной смертности выглядит следующим образом:
1 место - врожденные пороки развития;
2 место - СДР;
3 место - врожденные пневмонии;
4 место - внутриматочная гипоксия;
5 место - ВЖК;
6 место - инфекции и сепсис.
Поздняя неонатальная смертность с 7 до 28 дня.
Необходимо анализировать еще один показатель - ПЕРИНАТАЛЬНОЙСМЕРТНОСТИ, который рассчитывается по формуле:
число детей, родившихся мертвыми + число детей, умерших от 0 до 7 дняX 1000
число зарегистрированных новорожденных, родившихся живыми и мертвыми
В 2009 году – 4,5 случаев на 1000 живо- и мертворожденных
Пути снижения
Для снижения перинатальной, неонатальной и младенческой смертности необходимы:
интеграция служб акушеров-гинекологов, педиаторов, генетиков и реаниматологов. Т.е. преемственность в педиатрической, терапевтической и акушерско-гинекологической помощи.
Педиатрическая помощь в работе семейного врача включает:
антенатальную охрану плода своевременное выявление и лечение заболеваний, особенно хронических, у девочек-подростков – будущих матерей. Задача: к детородному возрасту максимально смягчить течение болезни. Особое внимание женщинам из групп риска.
динамическое наблюдение за детьми Своевременное квалифицированное наблюдение за детьми первого. При каждом посещении ребёнка оценивать его изическое и нервно-психическое развитие и при выявлени отклонений проводить мероприятия по их устранению
организацию рационального вскармливания всемерно пропагандировать естественное вскармливание, при необходимости своевременно переводить на искусственное, назначать фруктовые и овощные соки, витамины,
профилактику и лечение болезней и последующую реабилитацию
организацию осмотров детей врачами-специалистами, лабораторно-диагностических исследований, проведение профилактических прививок
подготовку детей к поступлению в дошкольные учреждения и школу
Каждое из этих направлений деятельности детально расшифровано на стр 19-20 Справочника СВ.
Иммунопрофилактика инфекционных заболеваний детально на стр 25-27. Если ребёнок всё же остался непривитым (противопоказания приведены там же), то врач и родители должны оберегать его от контактов с инфекционными болезнями.
Важную роль в решении вопросов играет перинатальный центр с хорошей материальной оснащенностью (в РБ – РНПЦ «Мать и дитя», 2 ГРД г.Минска).
Первичный и вторичный туалет новорожденного. Уход за кожей, остатком пуповины и пупочной ранкой в детской палате и в домашних условиях.
Первичный и вторичнй туалет новорожденного
После рождения головки ребенка отсасывают слизь из верхних дыхательных путей новорожденного с помощью электроотсоса или резинового баллона. Родившегося ребенка акушерка кладет на лоток, покрытый стерильной пеленкой, поставленный у ног матери. До отделения ребенка от матери из развернутого пакета для первичной обработки новорожденного берут пипетку и с помощью ватных тампонов (для каждого глаза отдельный), придерживая веки ребенка, закапывают в глаза, а девочкам и на наружные половые органы по 2-3 капли 30% раствора сульфацила-натрия (альбуцида), для профилактики гонобленореи. Затем накладывают на пуповину зажимы Кохера:
1-ый — на расстоянии 10 см от пупочного кольца;
2-ой — на расстоянии 8 см от пупочного кольца;
3-ий — как можно ближе к наружным половым органам женщины.
Участок пуповины между первым и вторым зажимами обрабатывают шариком с 95% этиловым спиртом и пересекают ножницами. Срез детской культи пуповины смазывают 1% раствором йодоната. Далее ребенка показывают матери, обращая внимание на пол ребенка и врожденные аномалии развития, если они есть. Новорожденного переносят в манипуляционно-туалетную для новорожденных при родовых палатах.
Акушерка моет руки под проточной водой с мылом, обрабатывает их одним из кожных антисептиков и приступает к вторичной обработке пуповины, используя пакет для вторичной обработки. С помощью стерильной марлевой салфетки отжимают пуповинный остаток от основания к периферии и протирают его марлевым шариком с 95% этиловым спиртом. Затем на расстоянии 1,5-2 см от пупочного кольца шелком № 6 (две ниточки) сильно завязывают пуповину, протягивая нитку от себя, а затем два раза перевязывают пуповину с другой стороны. Вместо ниток можно использовать специальные скобки. Стерильными ножницами пуповину отсекают на расстоянии 0,5-1 см от перевязки. При резус-отрицательной крови у матери, изосенсибилизации по системе АВО, объемной сочной пуповине, недоношенным и маловесным детям, новорожденным в тяжелом состоянии, когда сосуды пуповины могут понадобиться для проведения инфузионной и трансфузионной терапии, лигатуру накладывают на расстоянии 3-4 см от пупочного кольца. Тупфером, смоченным 5% раствором калия перманганата, обрабатывают срез культи, затем остаток пуповины и на расстоянии 1 см от пупочного кольца обрабатывают кожу, затем - шелковую нить. На культю накладывают стерильную марлевую повязку-треугольник.
Вслед за обработкой пуповины производят первичную обработку кожных покровов: стерильным ватным тампоном, смоченным стерильным растительным или вазелиновым маслом (60 мл) из индивидуального флакона, открытого перед обработкой ребенка, удаляют с головы и тела ребенка кровь, первородную смазку, слизь, меконий. Если ребенок сильно загрязнен меконием, его обмывают над тазом или раковиной под проточной теплой водой с детским мылом и ополаскивают струей теплого раствора калия перманганата 1 : 10000 (слаборозового цвета). После обработки кожу осушают стерильной пеленкой. Затем производят взвешивание ребенка, завернутого в другую стерильную пеленку, на весах (вес пеленки вычитают). Измерение ребенка осуществляют с помощью стерильной ленты. Рост ребенка измеряют от затылка до пяточных бугров, окружность головы - по линии, проходящей через лобные бугры и затылок в области малого родничка, грудь - по линии сосков и подмышечных впадин. На руки ребенка привязывают браслетки, а поверх одеяла повязывают медальон, на которых написаны фамилия, имя, отчество, номер истории родов матери, пол ребенка, массу, рост, час и дата его рождения. Ребенка помещают в индивидуальную кровать и в течение 2 часов ведут постоянное наблюдение за его состоянием. Через 2 часа после рождения ребенку проводят вторично профилактику гонобленореи. Ребенка переводят в отделение новорожденных; при переводе ребенка дежурный врач (акушерка) проверяет правильность документации, состояние пуповины и- расписывается в истории развития новорожденного, указав время перевода.
2. Уход за новорожденными в палатах новорожденных.
Ежедневный туалет новорожденного проводится утром, перед первым кормлением. Ребенка взвешивают, измеряют температуру тела, затем проводят обработку глаз от наружного угла глаза к внутреннему стерильными ватными шариками, смоченными физиологическим раствором. Для туалета носовых ходов используют жгутики, смоченные стерильным растительным маслом (жгутики вводят в носовые ходы на глубину 1-1,5 см). Затем протирают лицо ватными шариками (растворы как для глаз). После этого тампонами, смоченными в стерильном вазелиновом или растительном масле, обрабатывают естественные складки (сначала подмышечные, затем паховые).
При пеленании (перед каждым кормлением) детей подмывают под проточной водой в направлении спереди назад. Обработка остатка пуповины проводится ежедневно 3%-ным раствором перекиси водорода, затем сухой палочкой культю просушивают, после чего пуповинный остаток смазывают 5%-ным пермангонатом калия. После отпадения пуповинного остатка необходимо проводить обработку пупочной ранки этими же растворами до ее заживления.
3.Основные требования по уходу за новорожденными на дому.
При первом посещении ребенка врач должен тщательно собрать анамнез, проанализировать течение беременности и родов, наличие пограничных состояний или заболеваний в раннем неонатальном периоде. При осмотре ребенка оценивается состояние кожи и слизистых оболочек, его поведение, наличие и выраженность физиологических рефлексов, вид вскармливания, активность сосания, прибавка в массе, характер стула. Особое внимание следует обратить на состояние пупочной ранки, обязательно обучить мать ребенка технике ее обработки. Обычно заживление пупочной ранки происходит на 3-й неделе жизни (на 15-18 дни жизни). Длительно незаживающая пупочная ранка должна насторожить в отношении инфекций (омфалиты) или хирургической патологии (пупочный свищ).
• Ежедневный туалет. Туалет кожи, слизистых, пупочной ранки, подмывание ребенка осуществляются по тем же правилам, что и в палате новорожденных родильного дома. Полость рта обрабатывается только в случае молочницы. Ногти обрезаются маленькими ножницами с тупыми концами, которые предварительно обработаны 96-градусным спиртом.
• Пеленание. По желанию родителей можно с первых дней жизни использовать кофточки и ползунки. Но в случае, если ребенка решили пеленать, применяют метод свободного и широкого пеленания. Суть свободного пеленания заключается в одевании ребенку с первых дней жизни тонкой распашонки, а поверх нее - кофточки с зашитыми рукавами. При этом ручки ребенка остаются свободными, объем их движений увеличивается, что благотворно сказывается на нервно-психическом развитии, а также функции дыхания. Широкое пеленание необходимо для правильного формирования тазобедренных суставов. При этом способе бедра разведены в стороны и создаются условия для правильного формирования тазобедренных суставов. Для этого на подгузник кладут 2 фланелевые пеленки, сложенные прямоугольником 15х35 см, которые заворачиваются между ножек к животику ребенка так, чтобы бедра находились в разведенном состоянии.
• Купание. До 6 месяцев - ежедневно, затем можно купать через день. Температура воды должна быть 37-37,50С, продолжительность ванны 5-7 мин. Мыло для мытья тела используется 1-2 раза в неделю, область промежности моют с мылом ежедневно.
• Прогулки на свежем воздухе. Летом начинают сразу после выписки из стационара. Продолжительность первой прогулки - 15-20 мин, затем пребывание на улице увеличивают на 10-20 мин ежедневно. Весной и осенью продолжительность прогулки сокращается до 10-15 мин и длительность пребывания на свежем воздухе увеличивают на более короткий срок. В зимний период режим пребывания на свежем воздухе устанавливается индивидуально с учетом климата, состояния здоровья и особенностей ребенка.
Организация вскармливания доношенных и недоношенных новорожденных. Расчет питания Преимущества грудного вскармливания.
В 1989-1990 гг. Всемирной организацией здравоохранения была подготовлена крупномасштабная программа в поддержку грудного вскармливания, в цели и задачи которой входили пропаганда грудного вскармливания и создание в роддомах условий для успешного кормления новорожденных материнским молоком.
Суть программы изложена в 10принципах успешного грудного вскармливания:
1. Строго придерживаться установленных правил грудного вскармливания и регулярно доводить эти правила до сведения медицинского персонала и рожениц.
2. Обучать медицинский персонал необходимым навыкам для осуществления практики грудного вскармливания.
3. Информировать всех беременных женщин о преимуществах и технике грудного вскармливания.
4. Помогать матерям начинать грудное вскармливание в течение первого получаса после родов.
5. Показывать матерям, как кормить грудью и как сохранить лактацию, даже если они временно отделены от своих детей.
6. Не давать новорожденным никакой иной пищи или питья, кроме грудного молока, за исключением случаев, обусловленных медицинскими показаниями.
7. Практиковать круглосуточное нахождение матери и новорожденного рядом в одной палате.
8. Поощрять грудное вскармливание по требованию младенца, а не по расписанию.
9. Не давать новорожденным, находящимся на грудном вскармливании, никаких успокаивающих средств и устройств, имитирующих материнскую грудь (соски и др.).
10. Поощрять организацию групп поддержки грудного вскармливания и направлять матерей в эти группы после выписки из родильного дома или больницы.
Для выполнения данных принципов работа родильных домов должна быть организована так, чтобы обеспечить контакт матери и ребенка сразу после родов, совместное пребывание матери и ребенка, круглосуточный «свободный» режим кормления новорожденного. Первое прикладывание здоровых новорожденных к груди необходимо проводить в родзале в первые полчаса после родов. Для этого ребенка после перевязки пуповины выкладывают на живот матери и он сам «приползает» к груди и начинает сосать.
Преимущества раннего прикладывания к груди:
• происходит более раннее заселение кожи и кишечника ребенка нормальной микрофлорой;
повышается устойчивость новорожденного к инфекциям;
активнее стимулируется лактация у матери;
улучшается течение III-го периода родов и послеродового периода;
• быстрее устанавливается психоэмоциональный контакт между матерью и ребенком.
Преимущества совместного пребывания матери и ребенка:
• возможность постоянного контакта и доступа матери к новорожденному (круглые сутки);
возможность осуществлять кормление «по требованию»;
возможность наблюдать каждую реакцию ребенка;
легче проводить подготовку и обучение матери правилам ухода за ребенком;
укрепляется связь между матерью и новорожденным;
уменьшается риск больничных инфекций.
Преимущества грудного вскармливания:
1. Качество и соотношение белков, жиров и углеводов материнского молока идеально для усвоения организмом ребенка (оптимальная и сбалансированная пищевая ценность).
2. Женское молоко содержит биологически активные вещества и факторы иммунитета (ферменты, гормоны, иммуноглобулины, лизоцим), способствующие противоинфекционной устойчивости детей (защитная роль грудного молока).
3. Минеральные вещества (кальций, фосфор, микроэлементы) оптимально соответствуют потребностям ребенка, всасываются в 2 раза лучше, чем из коровьего молока (высокая усвояемость как микро- и макроэлементов, так и белков, жиров и углеводов).
4. Грудное молоко обеспечивает активное размножение в кишечнике новорожденных бифидо-флоры, т. е. благоприятно влияет на формирование биоценоза кишечника.
5. Для грудного молока характерны оптимальная температура и низкая осмолярность.
6. Грудное вскармливание адекватно регулирует формирование зубочелюстной системы.
7. При кормлении грудью устанавливается лучший психоэмоциональный контакт между матерью и ребенком, сильнее взаимная привязанность.
8. Грудное молоко - самая дешевая пища (экономический эффект грудного вскармливания).
9. у детей, находящихся на грудном вскармливании ниже риск развития язвенно-некротического энтероколита, синдрома внезапной смерти, аллергических заболеваний.
10. Исследованиями зарубежных авторов установлено, что у детей, которые находились на грудном вскармливании, реже наблюдаются гипертония, атеросклероз, сахарный диабет, лимфомы. Кроме того, для них характерны более высокие показатели умственного развития.
Принципы успешного грудного вскармливания касаются только здоровых новорожденных, родившихся от здоровых матерей. В случае болезни матери и/или ребенка, невозможности вскармливать грудью вопросы кормления решаются индивидуально.
Виды вскармливания новорожденных.
Формулы расчета питания у доношенных новорожденных
По терминологии ВОЗ выделяют следующие виды грудного вскармливания:
Полное грудное вскармливание (по отечественной терминологии - естественное вскармливание). При нем ребенок не получает ничего, кроме грудного молока или наряду с грудью матери получает соки или воду в объеме не более 1-2 глотков не чаще 1-2 раз в день.
Частичное грудное вскармливание (по отечественной терминологии приближается к термину «смешанное вскармливание»).
Выделяется III степени частичности:
1. «Высокий уровень» - грудное молоко составляет более 80 % суточного объема.
II. «Средний уровень» - грудное молоко составляет 20-79 % суточного объема.
III. «Низкий уровень» - грудное молоко составляет до 20 % суточного объема.
Знаковое или символическое грудное вскармливание - такое прикладывание к груди, при котором ребенок практически не получает пищи и которое проводится только как форма психологической защиты.
Необходимое количество молока рассчитывается по следующим формулам.
1. Формула Финкельштейна (применяется до 7-8 дня жизни): суточное количество молока составляет 70 мл х п (при массе до 3200 г), 80 мл х п (при массе более 3200 г), где п - день жизни.
2. Формула Зайцевой: суточное количество молока в миллилитрах составляет 2 % массы тела (в граммах) х п, где п - день жизни.
3. Количество молока на одно кормление: 3 мл х день жизни х массу тела в кг.
Количество молока на одно кормление: 10 мл х п, где п ~ день жизни.
5. С 10 дня до 2 месяцев жизни. Суточное количество молока (в мл) составляет 1/5 массы тела (в граммах).
Энергетический метод: Суточная калорийность пищи составляет в первые сутки - 30-35 ккал/кг массы тела ребенка, в последующие дни увеличивается ежедневно на 5 ккал в сутки. С 10-го дня жизни ребенок получает 100 ккал/кг в сутки, на 14 день жизни - 110-120 ккал/кг в сутки, в 1 месяц - 130140 ккал/кг в сутки.
Вскармливание недоношенных новорожденных
Анатомо-физиологические особенности ЖКТ у недоношенных
Сосательный и глотательный рефлексы и их координация до 32–34 недель гестации не развиты.
Объем желудка мал, тонус пилорического отдела преобладает над малоразвитым сфинктером кардиальной части желудка.
Секреция желудочного сока, способность кислотообразования и продукции пепсиногена снижены.
Активность перистальтики кишечника низкая, что приводит к вздутию живота, перерастяжению кишечника.
Расщепление белков неполное.
Активность лактазы снижена.
Функция поджелудочной железы даже у глубоконедоношенных детей находится на достаточном уровне.
Ферменты кишечника, участвующие в углеводном и белковом обмене, формируются на более ранних этапах, чем липолитические ферменты, в связи с чем у недоношенных часто отмечается повышенная экскреция фекального жира.
Сроки назначения первого кормления
Должны быть строго индивидуальными. Вопрос о первом кормлении ребенка решается с учетом его гестационного возраста и клинического состояния. Следует стараться начать энтеральное кормление как можно раньше. Слишком позднее первое кормление увеличивает первоначальную потерю массы тела, приводит к электролитным и метаболическим нарушениям, ацидозу.
Недоношенным детям, родившимся в большом сроке гестации (35–36 недель) в относительно удовлетворительном состоянии, целесообразно начинать первое кормление не позднее 2–3 часов после рождения.
У детей с гестационным возрастом менее 34 недель и массой менее 2000 г основные принципы вскармливания — осторожность и постепенность. Вместе с тем в ведущих центрах у стабильных детей с массой тела 1000–1500 г удается начинать энтеральное кормление в конце первых суток, менее 1000 г — со 2-го дня.
Перед началом первого кормления необходимо:
1) оценить клиническое состояние:
а) если ребенок перенес асфиксию с оценкой по шкале Апгар 1–5 баллов и ацидоз, то кормление необходимо отсрочить и назначить ребенку парентеральное питание и принять меры для коррекции нарушений;
б) частота дыханий должна быть не более 60 дыханий в минуту для кормления из соски и не более 60–80 дыханий в минуту — для зондового. Тахипноэ повышает риск аспирации;
2) убедиться в наличии перистальтики кишечника:
а) живот должен быть мягким, не вздутым, выслушиваться перистальтика;
б) должен отойти меконий;
3) провести пробу на толерантность к пище (если риск срыгиваний высок):
а) проводится физиологическим раствором (предпочтительнее), дистиллированной водой, 5 % раствором глюкозы;
б) количество раствора на одно кормление зависит от массы тела:
менее 1000 г — 1–2 мл;
1000–1500 г — 2–4 мл;
1500–2000 г — 4–5 мл;
в) проба может повторяться несколько раз (каждые 3 часа), пока не подтвердится, что функции ЖКТ не нарушены и кормление не вызывает аспирации и респираторных расстройств.
Расчет необходимого количества пищи
Определяется энергетическим (калорийным) методом:
– с 1 по 10 день жизни назначается по 10 ккал × m × n, где m — масса тела в кг, n — возраст ребенка в днях;
– с 11 по 20 день жизни калорийность увеличивается со 100 до 130 ккал/кг;
– с 21 дня до 1 месяца — со 130 ккал/кг до 140–150 ккал/кг.
Другие методы расчета питания недоношенным новорожденным:
формула Малышевой: 14 × m × n;
формула Зайцевой: 2 % от массы (в граммах) × n;
формула Ромеля: (n 10) масса в г/ 100;
на одно кормление 3 × m × n, где m — масса тела в кг, n — возраст ребенка в днях.
Приведенными формулами пользуются до 10–14 дня жизни.
Затем используется формула Хазанова:
с 2 до 4 недель суточный объем пищи составляет 1/6 массы тела в граммах;
с 4 недель — 1/5 массы тела.
Частота кормлений зависит от массы тела ребенка, его степени зрелости, общего состояния. Применяют 7–8-разовое кормление, но по показаниям частота может быть увеличена до 10 раз в сутки.
Способы вскармливания
1. Грудное. Возможно у недоношенных новорожденных 35–37 недель гестации при удовлетворительном состоянии. При грудном вскармливании необходимы систематические контрольные взвешивания до и после кормления.
2. Из соски. Применяется у недоношенных, родившихся после 33–34 недель беременности (сосательный рефлекс у которых снижен), при отсутствии у них нарушений в течении постнатальной адаптации.
3. Через зонд. Зонд вводят на длину, равную расстоянию от переносицы до мечевидного отростка, либо орогастрально (предпочтительнее), либо назогастрально (создает дополнительное сопротивление на пути прохождения воздуха, может провоцировать апноэ и брадикардию).
Показания для назначения зондового кормления:
срок гестации менее 32–33 недель;
отсутствие сосательного и глотательного рефлексов;
ИВЛ;
РДС 5 баллов;
подозрение на родовую травму;
появление стойкого цианоза при сосании;
дефекты твердого и мягкого неба.
Виды зондового кормления:
а) болюсное (прерывистое). Зонд используют для разовой порции молока, после чего сразу же удаляют. Молоко подается без усилий, медленно, под действием силы тяжести. Способ более физиологичный, чем капельное введение, т. к. способствует циклическому выбросу гормонов, что стимулирует рост и развитие ЖКТ;
б) пролонгированное (капельное, микроструйное). Зонд вводится на срок до 3–7 дней. Применяется обычно у детей с массой тела менее 1500 г, а также у более крупных в случае их тяжелого общего состояния с тенденцией к застою в желудке. Адаптированная смесь подается в желудок при помощи инфузионного насоса. В этом случае она предпочтительнее, чем материнское молоко, т. к. легче сохранить ее стерильность в течение всего времени введения.
При вскармливании через зонд перед каждым кормлением необходимо проверять остаточный объем желудка. Если он составляет более 10 % от объема предыдущего кормления, то порцию молока уменьшают на 50 % с последующим постепенным увеличением объема.
Показания для пересмотра схемы вскармливания:
срыгивания;
рвота;
вздутие живота.
Пограничные состояния периода новорожденности; простая и токсическая эритема, физиологическая убыль массы, транзиторная лихорадка, половой криз, мочекислый диатез. Тактика врача
Реакции или состояния, отражающие процессы приспособления организма новорожденного ребенка к внеутробному существованию называют переходными (транзиторными, физиологическими или пограничными) состояниями новорожденных. Они возникают на границе внутриутробного и внеутробного периодов и являются гранью между нормой и патологией, т. е. они являются физиологичными для новорожденных, но при определенных условиях (дефекты ухода, вскармливания, различные заболевания) могут становиться патологическими, т. е. пограничные состояния могут предрасполагать к заболеваниям. В раннем неонатальном периоде выделяют следующие фазы наибольшего напряжения адаптивных реакций:
I - первые 30 мин жизни (острая респираторно-гемодинамическая адаптация);
II - 1-6 ч (стабилизация и синхронизация основных функциональных систем);
III- 3--4-е сутки (напряженная метаболическая адаптация).
К пограничным состояниям периода новорожденности относятся:
1. Родовой катарсис - в первые секунды жизни младенец находится в состоянии летаргии.
2. Синдром «только что родившегося ребенка», в последующие 5-10 мин - происходит синтез огромного количества катехоламинов, действие внешних и внутренних раздражителей, в результате чего ребенок становится активным.
3. Транзиторная гипервентиляция, которая проявляется:
• активацией дыхательного центра под воздействием гипоксии, гиперкапнии и ацидоза, транзиторно возникающих во время родов. Ребенок делает первое дыхательное движение с глубоким вдохом и затрудненным выдохом, что приводит rрасправлению легких;
• заполнением легких воздухом и созданием функциональной остаточной емкости;
освобождением легких от жидкости и прекрашением ее секреции;
• расширением легочных артериальных сосудов и снижением сосудистого сопротивления в легких, увеличением легочного кровотока и закрытием фетальных шунтов.
4. Транзиторное кровообращение - в течение первых 2 дней жизни возможно шунтирование крови справа налево и наоборот, обусловленное состоянием легких и особенностями гемодинамики в БОJIЬШОМ круге кровообращения.
5. Транзиторная потеря первоначалъной массы тела - отмечается почти у всех новорожденных. Обусловлена потерей жидкости вследствие дефицита грудного молока, поздним временем прикладывания к груди, потерей жидкости с меконием и мочой. Максимальная убыль первоначальной массы тела у здоровых новорожденных составляет не более 4-6 % к 3-4 дню жизни. Восстановление массы тела после ее физиологической убыли у большинства детей (60-70 %) происходит к 6-7 дню.
6. Транзиторное нарушение терморегуляции:
• Транзuторная гипотермия - в первые 30 мин температура тела ребенка снижается на 0,1-0,3 °С в минуту и достигает около 35,5-35,8 °С, которая восстанавливается к 5-6 ч жизни. Это обусловлено особенностями компенсаторно-приспособительных реакций ребенка.
Пути потери тепла:
излучение (отдача тепла через стенки кувеза);
кондукция (контакт с холодной поверхностью);
конвенция (СКВОЗНЯК);
испарение (через поверхность тела, особенно если она влажная).
• Транзиторная гипертермия - возникает на 3-5 день жизни, температура тела может повышаться до 38,5-39,5 °С и выше. Основная причина обезвоживание, перегревание, недопаивание, катаболическая направленность обменных процессов.
7. Простая эритема - реактивная краснота кожи, возникающая после удаления первородной смазки или первой ванны. На 2 сутки эритема более яркая, к концу 1-й недели она исчезает, у недоношенных детей она может сохраняться до 2-3-х недель.
8. Токсическая эритема (ТЭ) - появление эритематозных пятен с серовато-желтоватыми папулами или пузырьками в центре на 2-5 день жизни, в следствии аллергоидной (80-85 %) - неиммунной (дегрануляция тучных клеток и выделение медиаторов аллергических реакций немедленного типа) или аллергической (15-20 %) реакции. По клиническим формам выделяют локализованную (ограниченную), распространенную и генерализованную ТЭ. ТЭ может носить острое или затяжное течение. Для острого течения характерно появление сыпи на 2-3 сутки жизни и исчезновение ТЭ к 5-7 дню. При затяжном течении время начала высыпаний вариабильно, от 1 суток до 3-4 дня жизни. Сыпь может сохраняться до 14 и более дней.
9. Транзиторная гипербилирубинемия (физиологическая желтуха).
Данное пограничное состояние среди доношенных новорожденных встречается в 60-70 %, недоношенных 90-95 %.
В основе генеза физиологической желтухи лежат особенности билирубинового обмена у новорожденных, которые проявляются:
1. Повышенным образованием непрямого билирубина (НБ) в результате:
а) укорочения длительности жизни эритроцитов, содержащих фетальный гемоглобин (НbF) до 70 дней;
б) физиологической полицитемии (НЫ20 г/л) при рождении;
в) несостоятельности эритропоэза;
г) дополнительных источников образования НБ из печеночного цитохрома и миоглобина, каталазы, пероксидазы;
д) преобладания процессов катаболизма.
2. Сниженной способностью к связыванию и транспортировке НБ в кровяном русле, вследствие гипоальбуминемии (l г альбумина связывает 0,85 мг НБ).
3. Снижением функции печени, которая проявляется:
а) сниженным захватом НБ гепатоцитами, в результате низкого уровня мембранного белка - легандина;
б) низкой способностыо К глюкуронированию из-за сниженной активности глюкуранилтрансферазы и низким уровнем глюкуроновой кислоты;
в) замедленной экскрецией конъюгированного билирубина из гепатоцита вследствие узости желчных протоков.
4. Поступлением НБ из кишечника через кишечно-печеночный шунт (Аранцев проток и слизистые кишечника) в кровяное русло через нижнюю полую вену, минуя v. porte, который образуется под воздействием фермента Р-глюкуронидазы.
5. Низким уровнем содержания бифидобактерий в кишечнике. Клинически транзиторная гипербилирубинемия проявляется иктеричностью кожных покровов на 2-3 сутки жизни и исчезает к 7-10 дню жизни. Характерно отсутствие волнообразного течения желтухи. Общее состояние у таких младенцев не нарушено, отсутствует гепатолиенальный синдром. Максимальный уровень билирубина в периферической крови на 3 сут не превышает 205 мкмоль/л, в пуповинной крови при рождении он составляет не более 50-60 мкмоль/л, почасовой прирост - ДО 5-6 мкмоль/л/час, суточный прирост билирубина 86 мкмоль/л, уровень прямого билирубина не более 25 мкмоль/л (10-15 % от общего билирубина).
Визуально желтушность кожных покровов у доношенных новорожденных появляется при уровне билирубина 60-80 мкмоль/л, недоношенных 100110 мкмоль/л. Желтуха характеризуется по интенсивности (субиктеричность, иктеричность, с лимонным или шафрановым оттенком) и распространенности (шкала Крамера - 5 степеней).
10. Половой (гормональный) криз проявляется нагрубанием грудных желез (65-70 %), милией, десквамативным вульвовагинитом, метроррагиями (5-]0 %) У девочек. В основе этого состояния лежат: гиперэстрогенный фон плода вследствие перехода гормонов от матери к плоду и быстрое их выведение на 1 неделе жизни. У недоношенных и незрелых новорожденных проявления гормонального криза наблюдаются реже.
11. Мочекислый инфаркт, который обусловлен повышенными процессами катаболизма, что приводит к усилению пуринового обмена с образованием мочевой кислоты, которая в виде кристаллов откладывается в почечных канальцах, и как следствие моча имеет желто-коричневый цвет. Время проявления - 1-я неделя жизни.
Недоношенные дети: частота и причины преждевременных родов. Анатомо-физиологические и нервно-психические особенности недоношенных детей
См. также вопрос №77.
Частота преждевременных родов составляет 5–13,6 %.
Причины недоношенности
Можно разделить на 3 группы.
Ι. Социально-экономические:
1) отсутствие или недостаточность медицинской помощи;
2) низкий уровень жизни и, соответственно, материальной обеспеченности и, как следствие, плохое питание матери, неудовлетворительные жилищно-бытовые условия;
3) уровень образования (влияет на образ жизни, особенности личности, материальное благополучие);
4) психические и физические травмы — потрясения, испуг, падение и ушиб беременной, подъем тяжестей;
5) профессиональные вредности, вредные привычки (курение, алкоголь, наркотики);
6) внебрачные роды (особенно при нежеланной беременности);
7) неблагоприятная экологическая обстановка.
ΙΙ. Социально-биологические:
1) юный или пожилой возраст (менее 18 и более 35 лет);
2) низкий рост, инфантильное телосложение;
3) многоплодные роды (около 20 % от всех недоношенных).
ΙΙΙ. Клинические:
1) инфантилизм половых органов, особенно в сочетании с гормональными расстройствами (недостаточность желтого тела, гипофункция яичников, истмико-цервикальная недостаточность) — до 16,6 % всех преждевременных родов;
2) предшествующие аборты и выкидыши (ведут к неполноценной секреции эндометрия, коллагенизации стромы, истмико-цервикальной недостаточности, повышению сократительной способности матки, развитию в ней воспалительных процессов: эндометрита, синехий);
3) соматические заболевания матери, особенно с признаками декомпенсации или обострения во время беременности (ревматизм, ревматический порок сердца, пиелонефрит, гипертоническая болезнь, анемия и др.) вызывают нарушение маточно-плацентарного кровотока, дегенеративные изменения в плаценте;
4) эндокринные заболевания (гиперфункция коры надпочечников, тиреотоксикоз, сахарный диабет);
5) острые инфекционные заболевания (роды на высоте лихорадки, а также в ближайшие 1–2 недели после выздоровления);
6) патология беременности — поздние гестозы, нефропатия, иммунологический конфликт в системе мать – плацента – плод, оперативные вмешательства во время беременности (особенно лапаротомия);
7) заболевания плода — внутриутробные инфекции, хромосомные болезни, пороки развития и др.;
8) экстракорпоральное оплодотворение.
Причины преждевременных родов можно разделить по другому принципу:
исходящие от матери;
со стороны плода;
связанные с особенностями течения беременности;
внешнесредовые.
Внешние признаки незрелости:
непропорциональное телосложение (голова относительно большая: длина ее колеблется от 1/4 до 1/3 длины тела, мозговой череп преобладает над лицевым; нижние конечности и шея короткие);
низкорасположенное место отхождения пуповины;
череп более круглый, кости его податливые, швы, малый и боковые роднички обычно открыты;
ушные раковины мягкие, плотно прилегают к черепу;
кожа тонкая и глянцевая, темно-красная, как бы просвечивающаяся, в области спины, плеч, на лбу, щеках, разгибательных поверхностях плеч и бедер имеется обильный первородный пушок (лануго);
подкожно-жировой слой истончен, отмечается склонность к отеку подкожно-жировой клетчатки;
ногти нередко не доходят до кончиков пальцев, ногтевые пластинки мягкие;
у мальчиков яички не опущены в мошонку (у крайне незрелых детей мошонка вообще недоразвита), у девочек половая щель зияет (вследствие недоразвития больших половых губ и относительной гипертрофии клитора).
Функциональные признаки незрелости:
Со стороны ЦНСхарактерны:
вялость, мышечная гипотония; слабый крик или писк;
слабость, быстрое угасание или отсутствие сосательного, глотательного и других физиологических рефлексов периода новорожденности; замедленная реакция на раздражители;
преобладание подкорковой активности (из-за незрелости коры головного мозга): движения хаотичны, могут отмечаться вздрагивания, тремор рук, клонус стоп;
несовершенство терморегуляции (сниженная теплопродукция и повышенная теплоотдача). Дети легко охлаждаются и перегреваются, у них нет адекватного повышения температуры на инфекционный процесс.
Со стороны дыхательной системы характерны:
лабильность частоты и глубины дыхания, поверхностный его характер;
респираторные паузы (апноэ) различной продолжительности (5–12 с); гаспсы (судорожные дыхательные движения с затрудненным вдохом);
во время сна или покоя могут наблюдаться: дыхание типа Биота (правильные чередования периодов апноэ с периодами дыхательных движений одинаковой глубины), дыхание типа Чейн-Стокса (периодическое дыхание с паузами и постепенным увеличением, а затем снижением амплитуды дыхательных движений);
большая лабильность частоты и глубины дыхания со склонностью к тахипноэ (36–72 в минуту, в среднем — 48–52).
Со стороны сердечно-сосудистой системы характерны:
преобладание симпатического отдела вегетативной нервной системы: любые раздражения вызывают учащение сердечных сокращений, повышение артериального давления;
лабильность частоты сердечных сокращений со склонностью к тахикардии (до 200 в минуту, в среднем — 140–160 уд./мин);
феномен эмбриокардии (ритм сердца, характеризующийся одинаковыми по продолжительности паузами между I и II тоном и между II и I тоном);
приглушенность сердечных тонов, в первые дни жизни возможны шумы вследствие часто встречающегося функционирования эмбриональных шунтов (боталлов проток, овальное окно);
более низкое АД в первые дни жизни (75/20 мм рт. ст. с повышением в последующие дни до 85/40 мм рт. ст.);
симптом Арлекина (или симптом Финкельштейна): в положении ребенка на боку наблюдается неравномерная окраска кожи: нижняя половина розового цвета, верхняя — белая, что обусловлено незрелостью гипоталамуса, который осуществляет контроль за состоянием тонуса капилляров кожи.
Со стороны других органов и систем:
пищеварительной: низкая протеолитическая активность ферментов желудочного сока, недостаточная выработка панкреатических и кишечных ферментов, желчных кислот, что приводит к снижению толерантности к пище; повышенная проницаемость кишечной стенки; предрасположенность к метеоризму и дисбактериозу; недоразвитие кардиального отдела желудка (склонность к срыгиваниям);
мочевыделительной: низкая фильтрационная и осмотическая функция почек;
эндокринной:снижение резервных возможностей щитовидной железы (склонность к транзиторному гипотиреозу);
иммунной:низкий уровень гуморального иммунитета и неспецифических факторов защиты.
У недоношенных новорожденных выявляются также следующие особенности метаболизма: склонность к гипопротеинемии, гипогликемии, гипокальциемии, гипербилирубинемии, метаболическому ацидозу.
Организация выхаживания, вскармливания и реабилитации недоношенных детей в родильном доме и в специализированных отделениях 2-го этапа.
Особенности течения периода новорожденности у недоношенных
Период новорожденности у недоношенных продолжается более 28 дней (до 1,5–3 месяцев). Например, если ребенок родился в сроке гестации 32 недели, то в 1 месяц жизни его гестационный возраст составит 32 + 4 = 36 недель.
Повышение мышечного тонуса в сгибателях у них обычно появляется в 1–2 месяца жизни.
У здоровых недоношенных с массой до 1500 г способность к сосанию появляется в течение 1–2 недель жизни, с массой от 1500 до 1000 г — на 2–3 неделе жизни, менее 1000 г — к месяцу жизни.
Физиологическая убыль массы тела продолжается дольше — 4–7 дней и составляет до 10–14 %, восстановление ее происходит к 2–3 неделе жизни.
У 90–95 % преждевременно родившихся детей наблюдается неонатальная желтуха, более выраженная и длительная, чем у доношенных.
Гормональный криз и токсическая эритема встречаются реже, чем у доношенных.
Большинство недоношенных детей догоняют своих сверстников к 1–1,5 годам, дети с очень низкой массой тела при рождении обычно отстают в физическом и нервно-психическом развитии до 2,5–3 лет. В 5–7 лет и 11–14 лет могут отмечаться нарушения гармоничности развития (задержка роста).
Этапность выхаживания недоношенных
Существуют три этапа выхаживания недоношенных детей:
Ι этап — специализированный родильный дом для преждевременных родов;
ΙΙ этап — отделения выхаживания недоношенных 2 этапа (40–45 коек на 1000 преждевременных родов в год);
ΙΙΙ этап — поликлиника (амбулаторно-поликлинический этап).
В некоторых случаях применяется двухэтапная система выхаживания недоношенных. Недоношенные новорожденные с массой тела более 2200–2300 г, способные поддерживать нормальную температуру тела и не имеющие отклонений в течении неонатального периода, могут быть выписаны из родильного дома домой под наблюдение участкового педиатра, минуя 2-й этап.
Необходимыми условиями выписки являются:
регулярная и достаточная прибавка массы тела;
хорошее заживление пупочной ранки;
нормальные анализы крови.
Недоношенного ребенка выписывают из родильного дома обычно на 7–8 сутки жизни.
Специализированный родильный дом для преждевременных родов
Создается с целью максимальной концентрации недоношенных детей в одном учреждении.
Это дает также возможность сконцентрировать в нем современную дорогостоящую аппаратуру и подготовить высококвалифицированные кадры, т. к. недоношенным новорожденным при ведении родов и выполнении реанимационных мероприятий требуется высокий уровень материального оснащения и практических навыков персонала.
Принципы выхаживания недоношенных в родильном доме
1. Создание комфортных условий постнатальной адаптации, дополнительный обогрев ребенка.
2. Организация адекватного питания при физиологической незрелости.
3. Обеспечение охранительного режима выхаживания.
4. Профилактика инфицирования.
5. Коррекция нарушений гемостаза, выделение групп риска с целью наиболее полного и эффективного обследования и лечения.
Особенности терморегуляции недоношенных новорожденных
Дети со сроком гестации 24–26 недель — пойкилотермные организмы. Они требуют окружающую температуру, равную или даже выше, чем температура их тела, чтобы сохранять тепло. Но даже при более поздних сроках гестации осмотр, пеленание, любые манипуляции у недоношенных детей связаны с риском их охлаждения. Именно поэтому преждевременно родившемуся ребенку следует обеспечить пребывание в термонейтральной зоне.
Термонейтральная зона — зона теплового режима, в которой организм затрачивает минимальное количество энергии для поддержания нормальной внутренней температуры тела.
Способность к терморегуляции зависит от:
гестационного возраста;
степени морфологической и функциональной зрелости;
массы тела;
постнатального возраста ребенка в днях;
общего состояния ребенка (наличия соматической и неврологической патологии).
При охлаждении ребенка температура его тела поддерживается за счет:
повышения потребления кислорода;
утилизации энергии (запасов глюкозы).
В результате охлаждения у недоношенного ребенка могут наблюдаться:
снижение уровня кислорода в крови;
развитие гипогликемии;
нарастание уровня непрямого билирубина;
развитие метаболического ацидоза;
усиление процессов липолиза.
Основным методом поддержания нормальной температуры тела у недоношенного ребенка является метод выхаживания в инкубаторах (кувезах).
Показания для помещения ребенка в кувез: нарушение терморегуляции, неспособность самостоятельно поддерживать температуру тела.
Обычно в кувезном выхаживании нуждаются дети:
с массой тела 2000 г и менее;
родившиеся в асфиксии;
с родовой травмой;
с РДС ΙΙ–ΙΙΙ степеней;
с отечным, аспирационным и другими синдромами.
Кроме температурного режима, инкубатор также дает возможность поддерживать внутри его:
определенную влажность (60–80 %), что позволяет снижать до минимума потери тепла испарением. Более высокая влажность повышает риск инфицирования у ребенка (необходимо использовать бактериостатики в камере увлажнителя и менять воду в нем каждые 24 часа). Низкая влажность повышает неощутимые потери жидкости и требует более высокую температуру в инкубаторе;
определенную концентрацию кислорода (до 30–33 %) путем «общей» подачи кислорода в кувез.
Ориентировочно необходимый ребенку температурный режим определяется по таблицам или формулам. Эти значения температур используются при предварительном обогреве кувеза перед помещением в него ребенка (стартовая температура).
Формулы расчета
На первой неделе жизни:
Т (С) = 36,6–0,34 × ГВ–0,28 × ПВ.
Старше 1 недели жизни:
Т (С) = 36–1,4 × МТ (кг)–0,03 × ПВ,
где: ГВ — это отклонение гестационного возраста ребенка от 30 недель (например, для ребенка, родившегося в 28 недель беременности, этот показатель равен «–2», а при 32 неделях — «+2»); ПВ — постнатальный возраст в днях; МТ — масса тела в кг.
В последующем температура воздуха в кувезе должна быть такой, чтобы обеспечить нормальную температуру тела ребенка.
Современные инкубаторы оснащены кожными и воздушными датчиками (сервоконтроль по принципу обратной связи).
Необходимо избегать колебаний воздуха при уходе за ребенком: по возможности не выкладывать его на пеленальный столик и все манипуляции проводить в кувезе, как можно реже открывать дверцу и окошки инкубатора.
Другие методы обогрева ребенка:
обогрев лучистым теплом;
обогреваемый матрасик;
грелки (на расстоянии 10–15 см от ног ребенка);
предварительно обогретое белье.
Эти методы могут применяться как переходный этап к переводу ребенка в открытую кроватку. Использовать их желательно тогда, когда температура воздуха в инкубаторе составит менее 30 С.
В палате для недоношенных детей должна поддерживаться температура воздуха не ниже 24–25 С, (до 28 С), влажность — не менее 55–60 %.
Длительность пребывания в кувезе недоношенного ребенка с массой 1200–1500 г обычно ограничивается 2–4 днями. При меньшей массе может составлять от 7–8 дней до нескольких недель. Каждые 3 дня необходимо менять инкубатор с целью профилактики инфицирования.
Вскармливание: см. вопрос №82
Профилактика инфицирования
Заключается прежде всего в строгом соблюдении санитарно-противоэпидемического режима (приказ № 178 МЗ РБ).
Методы профилактики инфицирования:
дача молозива в родзале;
вскармливание материнским молоком с добавлением лизоцима, антибиотиков;
регулярная смена кувезов, кислородных палаток, носовых катетеров (через 12 часов);
назначение антибиотиков и заместительной иммунотерапии недоношенным из высокой группы риска по развитию инфекционной патологии.
С целью своевременного выявления инфекции необходим бактериологический контроль:
мазок и посев на флору из наружного слухового прохода;
посев крови и мекония на стерильность.
Специализированное отделение для выхаживания недоношенных детей
Перевод недоношенных на 2-й этап выхаживания осуществляется обычно на 3 сутки жизни. Если ребенок нуждается в реанимационных мероприятиях, либо у него диагностируется инфекционная или хирургическая патология, то показан немедленный перевод в ОИТР, специализированное отделение выхаживания недоношенных 2-го этапа или хирургический стационар соответственно (при условии транспортабельности).
Длительность выхаживания на 2-м этапе колеблется от нескольких дней и недель до 1–3 месяцев.
Принципы работы отделений 2-го этапа выхаживания недоношенных детей. Аналогичны таковым в роддоме.
Организация палат:
палаты должны быть боксированными, оптимальная планировка — по зеркальному принципу, рассчитаны на 2–4 ребенка; площадь на одного ребенка — 6 м2;
заполнение палат проводят циклично (в течение 1–3 суток);
необходимо постоянно иметь свободные чистые палаты для изоляции заболевших детей.
Уход за ребенком является продолжением мероприятий, начатых на 1-м этапе.
Кроме того, на 2-м этапе проводится:
антропометрия:
взвешивание — ежедневно;
окружность головы — 1 раз в неделю;
остальные параметры — 1 раз в месяц;
купание (с 2 недель, ежедневно при наличии опрелостей либо через день), детей с массой менее 1000 г купают после 1 месяца жизни;
выкладывание на живот — показано как можно раньше. Начинают на жесткой поверхности, без подушки. Доказана даже целесообразность выхаживания недоношенных на животе (улучшается оксигенация, уменьшаются срыгивания);
массаж передней брюшной стенки — проводится ежедневно при достижении ребенком массы 1700–1800 г;
прогулки проводят на веранде с 3–4-недельного возраста (после достижения массы 1700–1800 г).
Выписка из отделений 2-го этапа возможна по достижении ребенком массы 1700 г. В отделениях 2-го этапа выхаживания г. Минска выписка осуществляется при достижении массы 2300–2500 г.
Перевод в Дом ребенка возможен по достижении массы 2000 г.
Задержка внутриутробного развития плода (маленький и маловесный к сроку гестации) определение, причины, критерии диагностики.
Согласно оценочным таблицам физического развития, новорожденные могут быть разделены на 4 группы:
1) с нормальным для своего гестационного возраста физическим развитием от Р10–Р90 и колебанием в пределах ±2G;
2) с низкой массой и длиной по отношению к гестационному возрасту (обусловлено замедленным внутриутробным ростом плода — ЗВУР), эти показатели будут ниже Р10 и более ―2G отклонений. К этой группе будут отнесены новорожденные:
маловесные для срока гестации — масса тела при рождении ниже Р10, длина больше Р10,
маленькие для срока гестации — масса тела и длина при рождении меньше Р10.
Частота рождения детей с нарушением внутриутробного роста составляет 30–40 %, увеличиваясь до 70 % в развивающихся странах. Смертность среди данной группы младенцев в 3–10 раз превышает таковую у новорожденных с нормальным развитием. Важно отметить, что около 10% случаев ЗВУР связано с патологическим кариотипом, еще в 10% - с врожденной инфекцией (цитомегаловирусной, краснухой, токсоплазмозом, сифилисом). В остальных случаях причиной данного состояния является маточно-плацентарная недостаточность.
В клинической практике выделяют 3 клинических варианта ЗВУР: гипотрофический (асимметричный); гипопластический (симметричный); диспластический — обычно проявление наследственной патологии с наличием пороков развития, нарушением телосложения, дизэмбриогенетических стигм.
По сроку возникновения – раннюю, характерную для асимметричного варианта ЗВУР, вследствие относительного уменьшения количества клеток; позднюю, как проявление симметричного варианта и характеризуется меньшими темпами гипертрофии клеток.
По степени тяжести: легкая - отклонение показателей физического развития ниже 10Р и до ―2G; среднетяжелое ниже 5Р до 3Р и от ―2G до ―3G; тяжелая - ниже 3Р и более ―3G с наличием стигм дизэмбриогенеза, пороков развития.
Новорожденные с нарушением внутриутробного роста имеют высокий риск возникновения таких острых состояний, как асфиксия в родах, мекониальная аспирация, легочное кровотечение, гипогликемия, гипокальциемия, метаболический ацидоз. Нарушение внутриутробного роста плода в 50 % случаев ведет к отставанию в физическом развитии в раннем возрасте, у 40 – 60 % детей — задержка интеллектуального развития, невропатические реакции.
К факторам, способствующим задержке роста плода и преждевременным родам, можно отнести:
социально-экономические (заработная плата, условия жизни, питание беременной, время ухода в декретный отпуск и др.);
социально-биологические (вредные привычки: курение, алкоголизм, наркомания; возраст родителей, профессиональные вредности и др.);
клинические — экстрагенитальная патология, эндокринные заболевания (сахарный диабет, гипотиреоз и др.), угроза прерывания беременности, гестоз, аномалии развития плаценты, пуповины и органов половой сферы, наследственные заболевания, многоплодная беременность, ВУИ, пороки развития плода, изоиммунологическая несовместимость, стрессовые ситуации.
3) новорожденные с недостаточным питанием (врожденная гипотрофия) — при этом масса и длина больше Р10 и колебанием их в пределах –2G, с клиническими проявлениями у таких детей трофических расстройств — недоразвитие или отсутствие подкожно-жировой клетчатки, снижение эластичности и тургора тканей, сухость и шелушение кожных покровов;
4) с крупной массой, превышая долженствующую к гестационному возрасту более Р90 и +2G.
Причем, крупновесные новорожденные могут быть с гармоничным или дисгармоничным развитием, которое определяют с помощью коэффициента гармоничности КГ= масса (кг) / площадь тела (длина в м3 ), при КГ от 22,5–25,5 дети гармоничные, КГ > 25,5 дисгармоничные с преобладанием массы над длиной тела, КГ < 22,5 дисгармоничные с преобладанием длины тела по отношению к массе.
Зрелость новорожденного ребенка определяется по совокупности морфологических (клинических) и функциональных признаков по отношению к гестационному возрасту, а также биохимическими показателями.
Маленький и маловесный к сроку гестации новорожденный: ведущие клинические синдромы в раннем неонатальном периоде, принципы выхаживания и лечения.
Гипотрофический вариант (асимметричный) встречается до 80% случаев и характеризуется снижением массы тела при рождении ниже 10Р без отставания в длине тела и окружности головы. Такие дети выглядят худыми, окружность живота меньше окружности головы за счет уменьшения размеров печени и истощения запасов гликогена, склонны к большой потере первоначальной массы тела и к более медленному ее восстановлению. Длительно сохраняется транзиторная желтуха, отсутствует гормональный криз. У этих младенцев часто отмечаются синдром гипервозбудимости, явления полицитемии, гипокальциемии, гипонатриемии, гипомагниемии, гипогликемии, гипербилирубинемии. Возможно проявления дыхательных и геморрагических расстройств. У большинства новорожденных с данным вариантом ЗВУР антенатальных поражений головного мозга нет.
Гипопластический вариант (симметричный) составляет 20 – 25%. Новорожденные имеют относительно пропорционально снижение всех параметров физического развития при рождении — ниже 10Р. Они выглядят пропорциально сложенными, но маленькими, у них могут быть единичные стигмы дизэмбриогенеза (не более 3 - 4). Соотношение между окружностью головы и груди не нарушено. Такие младенцы склонны к гипотермии, развитию полицитемии, гипогликемии, гипербилирубинемии, дыхательным расстройствам и наслоению инфекций.
Диспластический вариант — обычно проявление наследственной патологии с наличием пороков развития, нарушением пропорций тела, дизэмбриогенетических стигм (диагностическое значение имеет обнаружение пяти и более стигм одновременно). Для таких детей характерны тяжелые неврологические расстройства, обменные нарушения, склонность к анемизации и инфицированию. Новорожденные с данным вариантом ЗВУР подлежат медико-генетическому обследованию с кариотипированием.
Постнатальная адаптация детей с нарушением внутриутробного роста, низкой массой тела при рождении и недоношенных отличается следующими особенностями: незрелостью жизненно важных функциональных систем, их повреждением в антенатальном периоде или в периоде родов.
Принципы выхаживания и вскармливания данной группы новорожденных аналогичны недоношенным младенцам и включают следующие общие принципы:
1) проведение родов в специализированных стационарах с хорошо подготовленным медицинским персоналом и наличием медицинского оборудования для выхаживания таких новорожденных;
2) создание оптимального температурного режима в момент родов и после рождения;
3) обеспечение адекватной оксигенации;
4) обеспечение рационального питания;
5) профилактика гипербилирубинемии;
6) восполнение высоких потерь жидкости с учетом склонности к быстро возникающим перегрузкам, развитию гипернатриемии, острой почечной недостаточности, гиперосмолярности, отечного синдрома;
7) контроль за уровнем глюкозы и электролитов в сыворотке крови и моче;
8) контроль и коррекция нарушенного равновесия кислот и оснований крови;
9) антибактериальная терапия с первых дней жизни при наличии факторов риска внутриутробной или постнатальной инфекции.
Необходимо отметить, что для маловесных и маленьких для срока гестации новорожденных в клиническом плане наиболее характерны следующие клинические синдромы: энцефалопатический, геморрагический, анемический, респираторный, желтушный, кардиоваскулярный, диспептический, дистрофический.
Гемолитическая болезнь плода и новорожденного: определение, этиология, патогенез. Варианты клинического течения.
ГБН - врожденное заболевание, возникающее внутриутробно или в первые часы либо дни после рождения в результате изоиммунологического конфликта из-за несовместимости крови плода и матери по эритроцитарным антигенам.
Гемолитическая болезнь новорожденных обусловлена переходом из организма матери через плацентарный барьер антител, направленных против эритроцитов плода и ребенка, что приводит к их интенсивному разрушению.
Она является наиболее частой причиной желтухи и анемии у новорожденных.
Частота ГБН - 1: 250-300 родов.
В настоящее время идентифицировано более 100 эритроцитарных антигенов, способных вызвать сенсибилизацию организма и привести к образованию антител.
Как правило, эритроциты ребенка имеют какие-то отцовские антигены, отсутствующие у матери, но в большинстве случаев гемолитическая болезнь плода и новорожденного развивается вследствие несовместимости крови матери и плода по резус-фактору и его подтипам, системе АВО и реже по другим эритроцитарным антигенам - Келл, Даффи, Кид и др. ввиду их меньшей иммуногенности.
Причины и факторы риска развития гемолитической болезни новорожденных по системе резус.
Резус-фактор был открыт в 1940 году Виннером.
Причиной развития гемолитическая болезнь новорожденных, является беременность резус-отрицательной сенсибилизированной женщины резус-положительным плодом.
Факторы, способствующие сенсибилизации:
аборты,
выкидыши,
гемотрансфузии,
пересадка органов и тканей,
предыдущие беременности Rh-положительным плодом. Риск сенсибилизации при каждой такой беременности составляет примерно 10%.
Наличие ГБН у детей от предыдущих беременностей доказывает факт сенсибилизации женщины. Однако, несмотря на то, что резус-несовместимость матери и плода встречается в 9,5-13% браков, ГБН развивается у одного ребенка из 20-25, рожденных резус-отрицательными матерями. Это обусловлено рядом причин:
1. Защитной ролью плацентарного барьера. В норме во время беременности плацента пропускает не более 0,1-0,2 мл крови плода к матери, что у абсолютного большинства беременных не приводит к сенсибилизации организма. Для сенсибилизации необходимо примерно 0,5-5мл плодовой крови. Усиленное поступление эритроцитов плода к матери происходит к концу беременности, начиная с 37 недели и во время родов при отслойки плаценты. Объем поступления фетальных эритроцитов в этот момент составляет от 3 – 4 до 10 мл. Патологическое течение беременности (гестозы, эндокринные заболевания, угроза прерывания, экстрагенитальная патология, аномалии развития самой плаценты, инфекции) приводят к повышению проницаемости плаценты и, соответственно, к увеличению объема крови плода, поступающего к матери.
2. Защитным фактором является сопутствующая групповая несовместимость. При этом естественные групповые антитела (α,β) матери блокируют часть эритроцитов плода (т.к. они содержат либо А, либо В антиген) и тем самым уменьшают риск сенсибилизации организма матери к D-антигену.
3. Если резус-отрицательная женщина, родилась от гетерозиготной Rh-положительной матери, в этой ситуации развивается толерантность к D-антигену.
4. Если отец ребенка является гетерозиготным, риск развития заболевания снижается в 2-4 раза.
5. Около 20-35% Rh-отрицательных людей вообще не способны к ответу на D-антиген.
Патогенез гемолитической болезни новорожденных.
В патогенезе ГБН можно выделить 3 этапа:
1) первичная (скрытая) сенсибилизация матери;
образование иммунных антител при беременности сенсибилизированной женщины резус положительным плодом;
развитие иммунологического конфликта у плода.
При первичной сенсибилизации, обусловленной резус-несовместимостью, происходит образование антирезус-антител, являющихся IgМ. В случае продолжающегося поступления в кровоток матери эритроцитов плода, синтез антител переключается на образование IgG.
Характеристика антител:
IgМ - изогемаглютинины. Они являются полными, бивалентными, высокомолекулярными, непроницаемыми для плацентарного барьера. Способны в солевой среде агглютинировать, преципитировать и связывать комплемент.
IgG - гипериммунные, блокирующие антитела, 5% из которых являются гемолизинами. Они одновалентные, неполные, низкомолекулярные и свободно проходят через плаценту. Не дают агглютинацию в солевой среде, но способны умеренно склеиваться в коллоидной среде.
При последующей беременности сенсибилизированная женщина начинает получать единичные эритроциты плода. В ответ на поступление антигенов (Rh фактора, А или В) у нее активизируется иммунная память и начинают вырабатываться антитела (происходит одновременное образование IgG и М с преобладанием G). Снятие иммуносупрессорных механизмов приводит к синтезу большого количества антител. При нормально сформированной «здоровой» плаценте антитела к плоду во время беременности почти не поступают и накапливаются в кровотоке матери. Основное поступление антител в этом случае происходит во время родов.
Способствуют проникновению антител к плоду во время беременности следующие состояния, повреждающие плаценту:
токсикозы беременных;
угроза прерывания беременности;
экстрагенитальная патология у женщины;
фетоплацентарная недостаточность;
срок беременности (старение плаценты).
От времени проникновения антител к плоду и от их количества будет зависеть клиническая форма заболевания.
Собственно иммунологический конфликт может развиваться у плода (приводит к отечной, врожденной желтушной или анемической формам болезни) или у родившегося ребенка (развивается желтушная или анемическая формы).
При попадании антител в кровоток плода или новорожденного происходит реакция антиген – антитело. Неполные антиэритроцитарные антитела повреждают мембрану эритроцитов, что приводит к повышению ее проницаемости и нарушению обмена веществ в эритроците. Эти измененные эритроциты захватываются макрофагами ретикулоэндотелиальной системы и преждевременно гибнут. В результате образуется непрямой, токсичный билирубин, который, накапливаясь, приводит к развитию желтухи. Вследствие лизиса эритроцитов появляется и нарастает анемия. Усиливающаяся билирубиновая интоксикация и анемия приводят к поражению печени (с развитием гипопротеинемии, геморрагического синдрома), миокарда (может развиваться сердечная недостаточность), усилению проницаемости сосудов.
Тяжесть поражения и форма болезни зависят от:
степени повреждающего действия антител;
количества антител;
проницаемости плаценты;
времени проникновения антител к плоду;
длительности действия антител;
реактивности плода и его компенсаторных возможностей (усугубляют заболевание гипоксия, ацидоз, гипогликемия, гипоальбуминемия, незрелость).
Гемолитическая болезнь новорожденных приводит к развитию вторичного иммунодефицита вследствие:
повреждения клеток иммунной системы иммунными комплексами и непрямым билирубином;
снижения уровня комплемента, вследствие связывания его антителами;
блокирования макрофагальной системы иммунными комплексами;
уменьшения титра защитных антител (IgG), поступающих от матери к плоду.
Классификация гемолитической болезни новорожденных.
По этиологическому фактору (вид серологического конфликта):
а) по системе резус; б) по системе АВО; в)по антигенам других систем.
По срокам возникновения клинического синдрома:
а) внутриутробно; б) постнатально.
По клинико – морфологическим формам заболевания:
а) внутриутробная смерть плода с мацерацией; б) отечная; в) желтушная и г) анемическая формы.
По степени тяжести:
а) легкое; б) средней тяжести; в) тяжелое течение.
Осложнения:
а) ДВС-синдром; б) гипогликемия; в) билирубиновая энцефалопатия; г) синдром сгущения желчи; д) поражение печени, миокарда, почек.
Классификация ГБН по МКБ Х пересмотра.
I Водянка плода, обусловленная изоиммунизацией.
II Гемолитическая болезнь плода и новорожденного вследствие изоиммунизации (имеется в виду желтушная и анемическая формы).
III Ядерная желтуха, обусловленная изоиммунизацией.
Клиническая характеристика степеней тяжести ГБН.
Легкое течение ставится при уровне гемоглобина при рождении более 140г/л, билирубина пуповинной крови менее 60 мкмоль/л. В динамике болезни отмечаются умеренно выраженные клинико-лабораторные данные, требующие только консервативного лечения. Осложнения отсутствуют.
При среднетяжелом течении желтуха появляется в первые 5 часов жизни при резус-конфликте и в первые 11 часов жизни при АВО-конфликте. Уровень гемоглобина при рождении менее 140г/л. Динамика клинико-лабораторных данных требует заменного переливания крови.
При тяжелом течении уже при рождении отмечаются: выраженная желтуха (билирубин пуповинной крови более 85 мкмоль/л), тяжелая анемия (гемоглобин мене 100г/л). Течение болезни характеризуется наличием признаков билирубиновой интоксикации. Требуется 2 и более заменных переливаний крови.
Профилактика ГБН.
1. Планирование семьи.
2. Введение первобеременным и первородящим (не сенсибилизированным) женщинам, родившим резус-положительных детей, анти-резус-глобулин в первые 3 суток после родов.
3. Подсадка “кожного лоскута” мужа, беременной женщине.
4. Введение лимфовзвеси мужа, беременной женщине.
5. УЗИ мониторинг плода и определение титра антител у женщин которые находятся в группе риска по развитию ГБН плода и новорожденных для своевременного родоразрешения (в сроке 36-37 недель). Нельзя допускать перенашивания беременности.
Гемолитическая болезнь плода и новорожденного: основные звенья патогенеза отечной и желтушной форм болезни. Клинические проявления.
Особенности течения отдельных форм ГБН по резус-фактору.
Водянка плода (отечная форма ГБН).
Данная форма болезни развивается в результате длительного воздействия большого количества антител на незрелый плод в сроке 20-29 недель гестации.
Действие резус-антител на незрелые эритроциты плода приводит к их внутрисосудистому гемолизу с развитием гипербилирубинемии и гемолитической анемии. Образующийся непрямой билирубин связывается с альбумином и удаляется через плаценту, что и обуславливает отсутствие желтухи и развитие гипопротеинемии.
Вследствие гипопротеинемии снижается онкотическое давление в сосудистом русле, происходит транссудация жидкой части крови с развитием гиповолемии и отеков.
Гемолитическая анемия приводит к гемической гипоксии плода с характерными метаболическими нарушениями, которые обуславливают повышение проницаемости сосудов, развитие кровоизлияний, геморрагического синдрома.
Гемическая гипоксия также активизирует экстрамедуллярное кроветворение в печени и селезенке, что проявляется гепатоспленомегалий.
Активизация кроветворения проявляется также появлением в сосудистом русле незрелых форм эритроцитов (ретикулоцитов, нормо- и эритробластов).
Гиповолемия, отеки, анемия и гемическая гипоксия ведут сначала в централизации кровообращения, затем – к истощению компенсаторных возможностей гемодинамики и развитию сердечной недостаточности.
Клиника водянки плода. Ребенок рождается с выраженными общими отеками и увеличенным в размере животом (вследствие асцита, гепатоспленомегалии). При большой массе тела имеются признаки морфо-функциональной незрелости. Выявляются симптомы угнетения ЦНС (адинамия, атония, арефлексия). Характерны резкая бледность, геморрагические проявления. Границы относительной сердечной тупости расширены, часто наблюдаются признаки острой сердечной недостаточности. Дыхательные расстройства у этих больных обусловлены гипоплазией легкого, которое было внутриутробно поджато увеличенной печенью и часто развивающейся вследствие незрелости легких БГМ.
Данные лабораторных исследований.
1. В общем анализе крови – анемия (уровень гемоглобина обычно составляет 50 – 70г/л; содержание эритроцитов – 1 – 2×10¹²/л; ретикулоцитоз до 150‰; нормобластоз).
2. В биохимическом анализе крови – гипопротеинемия (о. белок ниже 40 – 45г/л).
3. В коагулограмме – низкий уровень прокоагулянтов.
Гемолитическая болезнь плода и новорожденного (желтушная и отечная формы).
Развивается вследствие попадания антител к плоду после 29 недель внутриутробного развития и/или в родах. От того, когда и в каком количестве антитела проникли к плоду или ребенку будет зависеть и форма болезни: врожденная или постнатальная, желтушная или анемическая.
Желтушная форма наиболее часто встречающаяся форма ГБН (в 90% случаев). Основной клинический признак – это раннее появление желтухи.
При врожденной форме желтуха выявляется уже при рождении, при внеутробной появляется в первые часы или сутки жизни. Чем раньше возникает желтуха, тем тяжелее протекает ГБН. Максимальной выраженности желтуха достигает на 2 – 4 дни жизни.
У больных отмечаются также умеренное увеличение печени и селезенки, умеренная анемия, пастозность тканей.
Анемическая форма встречается менее чем у 5% больных ГБН. При резус-конфликте она является следствием длительного поступления к плоду небольших количеств антител на фоне индивидуальных особенностей кроветворной системы плода (снижения регенераторных возможностей). Проявляется бледностью кожи и слизистых (анемия с рождения), нерезкой гепатоспленомегалией, может выслушиваться систолический шум. Желтуха отсутствует или незначительная.
Гемолитическая болезнь плода и новорожденного: клинические и лабораторные критерии диагностики.
Диагностика ГБН.
Пренатальная диагностика:
1) тщательный сбор акушерского анамнеза, выявление женщин из групп риска по ГБН (оценить количество беременностей и интервал между ними, имели ли место переливания крови, пересадка органов, наличие ГБН у предыдущих детей, осложнения настоящей беременности);
2) определение титра антител. Во время беременности проводится не менее 3-х раз: при постановке беременной на учет, в 18 – 20 недель гестации и далее по показанием в зависимости от наличия и титра антител (при росте титра – еженедельный контроль);
амниоцентез (исследование околоплодных вод). Если титр антител 1:16 – 1: 32, то в 26 – 28 недель гестации исследуют оптическую плотность околоплодных вод (повышается), содержание глюкозы, белка (повышены) эстрогенов (снижены).
4) УЗИ плода и плаценты в сроке 20-22, 24-26, 30-32, 34-36 недель. Можно выявить отечную форму ГБН (асцит, поза Будды), утолщение плаценты, гепатоспленомегалию.
Постнатальная диагностика:
1) выделение новорожденных группы риска развития ГБН;
2) оценка возможных клинических проявлений: (желтуха и/или бледность кожных покровов, отеки, гепатоспленомегалия, неврологическая симптоматика);
3) лабораторная диагностика:
определение группы крови и резус-фактора у новорожденных, родившихся от матерей с О (I) группой и Rh - отрицательной принадлежностью крови;
биохимический анализ крови: определение уровня билирубина в пуповинной крови (более 51-61 мкмоль/л), динамика уровня билирубина по его фракциям, определение почасового прироста билирубина (более 6 - 8 мкмоль/л), определение уровня гликемии;
общий анализ крови: отмечается снижение гемоглобина, эритроцитов, тромбоцитов, содержание ретикулоцитов более 7 ‰ , нормобластов более 50% , умеренный лейкоцитоз;
иммунологические исследования: прямая реакция Кумбса, выявляет наличие комплексов антиген – антитело. Исследуемым материалом являются эритроциты новорожденного, к которым добавляется антиглобулиновая сыворотка, которая способствует агглютинации имеющихся комплексов. При групповой несовместимости данная реакция положительная в первые 2-3 дня, Rh-конфликте - положительная с рождения; непрямая реакция Кумбса, свидетельствует о наличии свободных блокирующих антител- IgG, для этого используют сыворотку матери или больного ребенка, куда добавляют эритроциты известной антигенной структуры (групповой и резус принадлежности), затем через определенный промежуток времени производят отмывание эритроцитов с последующим добавлением антиглобулиновой сыворотки. Реакция положительная на 1-2 сутки.
Особенности патогенеза и клинических проявлений гемолитической болезни новорожденных при групповой несовместимости. Дифференциальный диагноз с резус-конфликтом.
Причины и факторы риска развития гемолитической болезни новорожденных по системе АВО.
В 1900 г. Ландштейнером было установлено, что человек имеет 4 группы крови. Группы крови наследуются по трем аллельным генам О, А, В. Ген А доминирует над генами О и В, ген В доминирует над геном О. Групповые антигены находятся на наружной поверхности мембраны эритроцитов и обнаруживаются уже на 5-6 неделе беременности. Антигены А и В содержатся не только на эритроцитах, но и во всех тканях плода, околоплодных водах и амниотической оболочке плаценты.
Поражение плода групповыми антигенами (по АВО-системе) наблюдается в 2 – 3 раза чаще, чем другими (1 на 140 родов). Обычно конфликт бывает при группе крови матери О(I) и группе крови плода А(II) или В(III).
Наиболее часто развитие ГБН наблюдается при наличии у матери О(I), а у плода А(II) групп крови. Это обусловлено большей активностью антигена А по сравнению с другими, а также более высоким титром и меньшей молекулярной массой α-агглютининов у лиц с О (І) группой крови.
Различают 2 типа групповых антител:
1) естественные, возникающие в процессе формирования организма;
2) иммунные, представляющие собой аглютинины и гемолизины. Иммунные антитела образуются вследствие скрытой сенсибилизации, которая происходит до наступления беременности (вакцинация, употребление в пищу животных белков, инфекционные заболевания, кишечные бактерии) или во время беременности (в результате иммунизации плодовыми антигенами А или В). Наличие скрытой сенсибилизации может привести к развитию ГБН по АВО-системе уже при наступлении первой беременности. Учитывая низкую молекулярную массу аглютининов и гемолизинов, они легко проникают через плаценту к плоду и приводят к развитию заболевания. Данный конфликт протекает легче, чем при Rh-несовместимости. Это обусловлено менее выраженной сенсибилизацией в результате следующих защитных механизмов:
1. Для сенсибилизации организм беременной женщины требуется большой объем крови плода.
2. Антигены А и В содержатся не только на эритроцитах, но и в околоплодных водах, плаценте, тканях плода, что способствует нейтрализации материнских антител.
3. Фетальные эритроциты, попавшие в организм беременной женщины, блокируются собственными изогемаглютининами.
Особенности клинических проявлений ГБН по АВО-системе.
Наиболее часто развивается при группе крови матери О(І) а ребенка А (ІІ).
Заболевание развивается чаще при первой беременности.
ГБН по АВО протекает легче, чем при резус-конфликте.
Отечной и врожденной желтушной форм болезни практически не бывает, т.к. антитела к плоду проникают только в родах.
Желтуха появляется позднее (на 2- 3 дни жизни), что обусловлено незрелостью рецепторов эритроцитов новорожденных к групповым антиэритроцитарным антителам.
Редко бывает увеличение печени и селезенки.
Чаще, чем при ГБН по резус-фактору, наблюдаются постнатальные анемические формы болезни с незначительной желтухой и развитием анемии на 2 – 3 неделях жизни
Практически не бывает грозных осложнений в виде ядерной желтухи, ДВС-синдрома.
Ядерная желтуха: определение, причины развития, клинические стадии и проявления, лечение, исход, профилактика
Ядерная желтуха – повреждение ядер основания мозга непрямым билирубином. Является грозным осложнением ГБН. Первые проявления поражения мозга билирубином отмечаются обычно на 3 – 4 сутки жизни, когда содержание непрямого билирубина в сыворотке крови достигает максимальных цифр (у доношенных новорожденных – более 400мкмоль/л). Чувствительность клеток мозга к токсическому действию билирубина у недоношенных, незрелых новорожденных, детей, перенесших асфиксию, родовую травму, РДС и другие тяжелые состояния намного выше и признаки билирубиновой интоксикации могут появляться у них при меньшем уровне билирубина.
Выделяют 4 фазы течения ядерной желтухи:
появление признаков билирубиновой интоксикации – вялости, гипотонии, гипорефлексии, патологического зевания, срыгиваний, рвоты, снижения активности сосания, монотонного крика.
Появление классических признаков ядерной желтухи (через 3 – 4 дня) Характерны длительные апноэ, брадикардия, адинамия, арефлексия быстро сменяющиеся спастической стадией (появляется опистотонус, ригидность затылочных мышц, спастичные «негнущиеся» конечности, кисти сжаты в кулачки). Периодически отмечается возбуждение, «мозговой» крик, симптом «заходящего солнца», судороги.
Период мнимого благополучия (на 3 – 4 неделях жизни). Происходит обратное развитие неврологической симптоматики: уменьшается спастичность, улучшается двигательная активность и выраженность безусловных рефлексов. Создается впечатление, что ребенок выздоравливает.
Период формирования неврологических осложнений (на 3 – 5 месяцах жизни). Возникают экстрапирамидные расстройства, нарушения моторики и слуха. Формируются:
хореоатетоз;
парезы, параличи;
снижение слуха вплоть до глухоты;
задержка психомоторного развития;
детский церебральный паралич (преимущественно гиперкинетическая форма).
Лечение: см. вопрос №93.
Принципы лечения гемолитической болезни новорожденных. Профилактика.
