
- •Тема 6: «Теплоемкость газов. Энтропия» 33
- •Тема 7: «Термодинамические процессы идеальных газов» 43
- •Тема 8: «Второй закон термодинамики» 57
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем» 71
- •Тема 10: «Водяной пар» 83
- •Тема 11. Истечение газов и паров 89
- •Тема 1: Основные понятия и определения
- •1.1. Основные термодинамические параметры состояния
- •4. Внутренняя энергия.
- •5. Энтальпия,
- •6. Энтропия,
- •1.2. Термодинамическая система
- •1.3. Термодинамический процесс
- •1.4. Теплота и работа
- •1.5. Термодинамическое равновесие
- •Контрольные вопросы
- •Тема 2: «Состояние идеального газа»
- •2.1. Основные законы идеальных газов
- •2.2. Уравнение состояния идеального газа
- •Тема 4: «Реальные газы»
- •4.1. Уравнение состояния Ван-дер-Ваальса
- •4.2. Уравнения м.П. Вукаловича и и.И. Новикова
- •Контрольные вопросы
- •Тема 5: «Первый закон термодинамики»
- •5.1. Внутренняя энергия
- •5.2. Работа расширения
- •5.3. Теплота
- •5.4. Аналитическое выражение первого закона термодинамики
- •5.5. Энтальпия
- •Контрольные вопросы
- •Тема 6: «Теплоемкость газов. Энтропия»
- •6.1. Основные определения
- •6.2. Удельная (массовая), объемная и мольная теплоемкости газов
- •6.3. Теплоемкость в изохорном и изобарном процессе
- •6.4. Молекулярно-кинетическая и квантовая теории теплоемкости
- •6.5. Истинная и средняя теплоемкости
- •6.6. Зависимость теплоемкости от температуры
- •6.7. Отношение теплоемкостей ср и сυ. Показатель адиабаты
- •6.8. Определение qp и qυ для идеальных газов
- •6.9. Теплоемкость смеси идеальных газов
- •6.10. Энтропия
- •Контрольные вопросы
- •Тема 7: «Термодинамические процессы идеальных газов»
- •7.1. Основные определения
- •7.2. Изохорный процесс
- •7.3. Изобарный процесс
- •7.4. Изотермический процесс
- •7.5. Адиабатный процесс
- •7.6. Политропные процессы
- •Контрольные вопросы
- •Тема 8: «Второй закон термодинамики»
- •8.1. Основные положения
- •8.2. Круговые термодинамические процессы (циклы)
- •8.3. Термический кпд и холодильный коэффициент циклов
- •8.4. Прямой обратимый цикл Карно
- •8.5. Обратный обратимый цикл Карно
- •8.6. Математическое выражение второго закона термодинамики
- •8.7. Изменение энтропии в обратимых и необратимых процессах
- •Контрольные вопросы
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем»
- •Характеристические функции
- •Физический смысл изохорно-изотермического и изобарно-изотермического потенциалов
- •Термодинамическое учение о равновесии
- •9.4. Общие условия равновесия термодинамической системы
- •Контрольные вопросы
- •Тема 10: «Водяной пар»
- •10.1. Основные понятия и определения
- •Контрольные вопросы
- •Тема 11. Истечение газов и паров
- •11.1. Первый закон термодинамики в применении к потоку движущегося газа
- •11.2. Работа проталкивания
- •11.3. Располагаемая работа
- •11.4. Адиабатный процесс истечения
- •11.5. Истечение из суживающегося сопла
- •11.6. Истечение идеального газа из комбинированного сопла Лаваля
- •Контрольные вопросы
4.2. Уравнения м.П. Вукаловича и и.И. Новикова
Уравнение Ван-дер-Ваальса при больших плотностях дает значительные ошибки, вызванные неточностями при его выводе, в частности не учетом физических явлений силовой ассоциации и диссоциации молекул.
Также опыты показали, что коэффициенты b и α в уравнении Ван-дер-Ваальса не являются постоянными величинами и зависят от температуры и давления.
При выводе своего уравнения авторы учли явления силовой ассоциации молекул под влиянием межмолекулярных сил взаимодействия.
При явлении ассоциации происходит объединение отдельных молекул в группы, состоящие из двух, трех, четырех одиночных молекул и более. Отдельные молекулы, входящие в группы сложных частиц, сохраняя свои индивидуальные свойства, не реализуют полностью всех степеней свободы.
Следовательно, под ассоциацией молекул понимается простое механическое объединение двух, трех, четырех молекул и более в одну сложную частицу, которая в некоторых отношениях ведет себя как самостоятельная газовая частица.
Совокупность однородных газовых частиц, образующихся в результате ассоциации молекул, можно рассматривать как обычный газ, а любой реальный газ рассматривать как смесь отдельных газов, частицами которых являются одиночные, двойные, тройные и т.д. группы молекул. Эти газы находятся в постоянном взаимодействии друг с другом, и каждый из них достаточно точно следует уравнению Ван-дер-Ваальса.
Применяя к подобным газам закон действующих масс, и считая, что ассоциация приводит к созданию групп из двух, трех и четырех молекул, М.П. Вукалович и И.И. Новиков получили уравнение состояния. В наиболее простой форме, когда учитываются лишь двойные комплексы, уравнение имеет вид:
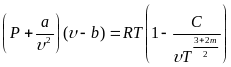
где
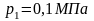 – постоянные
уравнения Ван-дер-Ваальса;
– постоянные
уравнения Ван-дер-Ваальса;
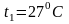 – постоянные,
определяемые на основании опытных
данных.
– постоянные,
определяемые на основании опытных
данных.
Контрольные вопросы
Чем отличаются реальные газы от идеальных?
Что называется коэффициентом сжимаемости?
Уравнение состояния реальных газов с вириальными коэффициентами.
Что положено в основу вывода уравнения Ван-дер-Ваальса?
Какой смысл имеет константа b уравнения Ван-дер-Ваальса?
Какая величина называется внутренним давлением газа?
Уравнение Ван-дер-Ваальса для 1 кг газа.
При каких условиях можно превращать газы в жидкое состояние?
В чем заключается силовая ассоциация молекул?
Что положено в основу вывода уравнения состояния М. П. Вукаловича и И.И. Новикова?
Тема 5: «Первый закон термодинамики»
Первый закон термодинамики является частным случаем всеобщего закона сохранения и превращения энергии применительно к тепловым явлениям, протекающим в термодинамических системах.
Закон сохранения и превращения энергии гласит, что в изолированной системе сумма всех видов энергии есть величина постоянная. Как следствие, энергия ниоткуда не появляется и никуда не исчезает, а лишь переходит из одного состояния в другое.
5.1. Внутренняя энергия
Под внутренней энергией газа понимается вся энергия, заключенная внутри тела или системе тел.
Внутренняя энергия включает в себя:
1. кинетическую энергию поступательного, вращательного и колебательного движения частиц;
2. потенциальную энергию взаимодействия молекул;
3. энергию электронных оболочек атомов;
4. внутриядерную энергию.
В большинстве теплоэнергетических процессов две последние составляющие остаются неизменными. Поэтому внутренняя энергия определяется как кинетическая и потенциальная энергия. При этом кинетическая энергия есть функция температуры, а потенциальная энергия зависит от среднего расстояния между молекулами, а, следовательно, от объема. Таким образом, внутренняя энергия это функция состояния тела:
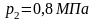
где
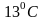 – постоянная интегрирования.
– постоянная интегрирования.
Величина U0 представляет собой нулевую энергию, или внутреннюю энергию при абсолютном нуле.
Как известно при 0 К тепловое движение молекул прекращается, но продолжается движение частиц внутри атомов. Например, движение электронов. Поскольку абсолютное значение внутренней энергии методами термодинамики установить невозможно, то при термодинамическом анализе системы используют изменение внутренней энергии в результате процесса, поэтому величина U0 не учитывается и принимается равной нулю.
Для идеальных газов в понятие внутренней энергии включают кинетическую энергию движения молекул и энергию колебательных движений атомов в молекуле.
Для реальных газов дополнительно потенциальную составляющую энергии, связанную с наличием сил взаимодействия между молекулами и зависящую от расстояния между ними.
Внутренняя энергия является аддитивным или экстенсивным параметром, так как ее величина зависит от массы тела. Удельная внутренняя энергия равна сумме энергий ее отдельных составляющих:
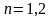
Изменение удельной внутренней энергии не зависит от характера или пути процесса, а определяется только начальным и конечным его состоянием:
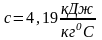
Этот факт наглядно демонстрирует рисунок 4.
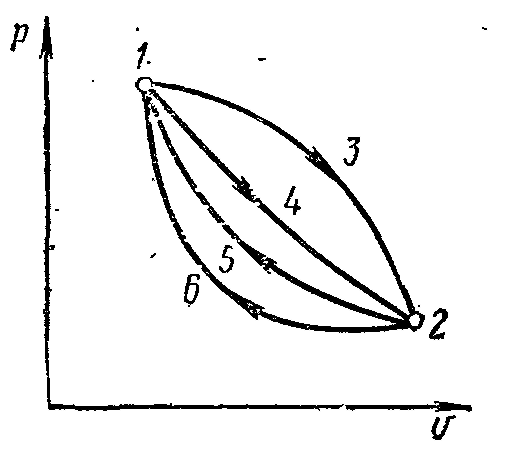
Рисунок 4.
Во всех процессах изменение внутренней энергии будет одно и то же.
В круговых процессах изменение удельной внутренней энергии равно нулю:
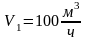
Утверждение, что удельная внутренняя энергия идеального газа является функцией только температуры справедливо с допустимой погрешностью и для реальных газов, если они находятся при высокой температуре и малом давлении.
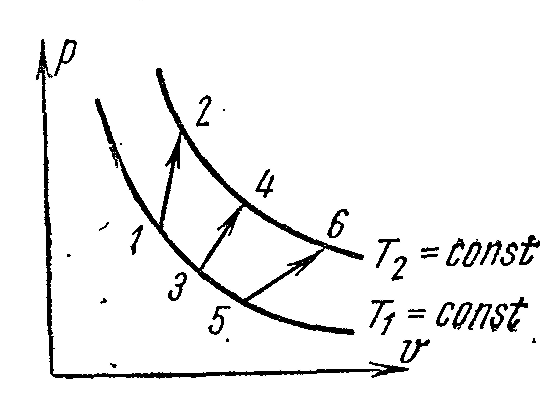
Рисунок 5.
Если на рυ-диаграмме (рис. 5) между изотермами Т1 и Т2 изобразить ряд произвольных процессов 1-2, 3-4, 5-6, которые имеют различные начальные и конечные объемы и давления, то изменение удельной внутренней энергии идеального газа будет одинаковым:
