
- •Тема 6: «Теплоемкость газов. Энтропия» 33
- •Тема 7: «Термодинамические процессы идеальных газов» 43
- •Тема 8: «Второй закон термодинамики» 57
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем» 71
- •Тема 10: «Водяной пар» 83
- •Тема 11. Истечение газов и паров 89
- •Тема 1: Основные понятия и определения
- •1.1. Основные термодинамические параметры состояния
- •4. Внутренняя энергия.
- •5. Энтальпия,
- •6. Энтропия,
- •1.2. Термодинамическая система
- •1.3. Термодинамический процесс
- •1.4. Теплота и работа
- •1.5. Термодинамическое равновесие
- •Контрольные вопросы
- •Тема 2: «Состояние идеального газа»
- •2.1. Основные законы идеальных газов
- •2.2. Уравнение состояния идеального газа
- •Тема 4: «Реальные газы»
- •4.1. Уравнение состояния Ван-дер-Ваальса
- •4.2. Уравнения м.П. Вукаловича и и.И. Новикова
- •Контрольные вопросы
- •Тема 5: «Первый закон термодинамики»
- •5.1. Внутренняя энергия
- •5.2. Работа расширения
- •5.3. Теплота
- •5.4. Аналитическое выражение первого закона термодинамики
- •5.5. Энтальпия
- •Контрольные вопросы
- •Тема 6: «Теплоемкость газов. Энтропия»
- •6.1. Основные определения
- •6.2. Удельная (массовая), объемная и мольная теплоемкости газов
- •6.3. Теплоемкость в изохорном и изобарном процессе
- •6.4. Молекулярно-кинетическая и квантовая теории теплоемкости
- •6.5. Истинная и средняя теплоемкости
- •6.6. Зависимость теплоемкости от температуры
- •6.7. Отношение теплоемкостей ср и сυ. Показатель адиабаты
- •6.8. Определение qp и qυ для идеальных газов
- •6.9. Теплоемкость смеси идеальных газов
- •6.10. Энтропия
- •Контрольные вопросы
- •Тема 7: «Термодинамические процессы идеальных газов»
- •7.1. Основные определения
- •7.2. Изохорный процесс
- •7.3. Изобарный процесс
- •7.4. Изотермический процесс
- •7.5. Адиабатный процесс
- •7.6. Политропные процессы
- •Контрольные вопросы
- •Тема 8: «Второй закон термодинамики»
- •8.1. Основные положения
- •8.2. Круговые термодинамические процессы (циклы)
- •8.3. Термический кпд и холодильный коэффициент циклов
- •8.4. Прямой обратимый цикл Карно
- •8.5. Обратный обратимый цикл Карно
- •8.6. Математическое выражение второго закона термодинамики
- •8.7. Изменение энтропии в обратимых и необратимых процессах
- •Контрольные вопросы
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем»
- •Характеристические функции
- •Физический смысл изохорно-изотермического и изобарно-изотермического потенциалов
- •Термодинамическое учение о равновесии
- •9.4. Общие условия равновесия термодинамической системы
- •Контрольные вопросы
- •Тема 10: «Водяной пар»
- •10.1. Основные понятия и определения
- •Контрольные вопросы
- •Тема 11. Истечение газов и паров
- •11.1. Первый закон термодинамики в применении к потоку движущегося газа
- •11.2. Работа проталкивания
- •11.3. Располагаемая работа
- •11.4. Адиабатный процесс истечения
- •11.5. Истечение из суживающегося сопла
- •11.6. Истечение идеального газа из комбинированного сопла Лаваля
- •Контрольные вопросы
8.4. Прямой обратимый цикл Карно
При осуществлении обратимого произвольного цикла количество источников теплоты можно уменьшить, если на определенных участках подводить и отводить теплоту при неизменной температуре, т.е. в изотермических процессах.
Предельный случай – вся теплота подводится и отводится изотермически. В этом случае потребуется всего два источника теплоты постоянной температуры: один теплоотдатчик и один теплоприемник.
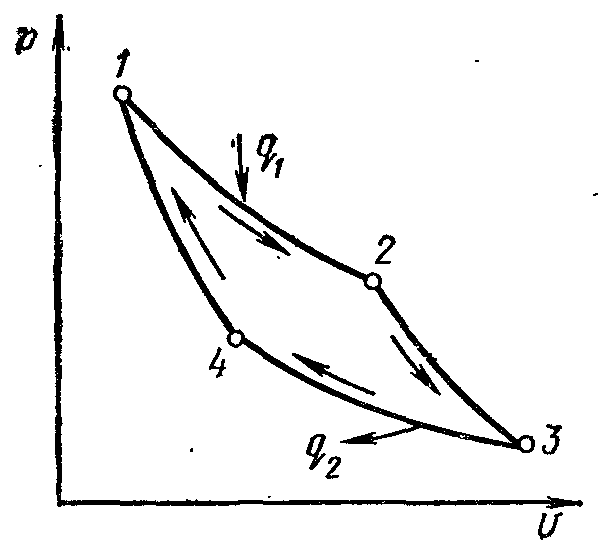
Рисунок 20 – Прямой обратимый цикл Карно в р,υ – координатах.
Осуществляется прямой обратимый цикл при таких условиях следующим образом.
Сначала в изотермическом процессе расширения теплота обратимо подводится к рабочему телу от теплоотдатчика с постоянной температурой.
Затем в обратимом адиабатном процессе расширения, в котором отсутствует теплообмен между рабочим телом и источниками теплоты, температура рабочего тела понижается до температуры теплоприемника.
Далее в обратимом изотермическом процессе при температуре теплоприемника происходит отвод теплоты от рабочего тела к нему.
Замыкающим цикл процессом должен быть опять обратимый адиабатный процесс, в котором при отсутствии теплообмена температура повышается до начальной и рабочее тело возвращается в первоначальное состояние.
Таким образом, обратимый цикл, осуществленный между двумя источниками постоянной температуры, должен состоять из двух обратимых изотермических и двух обратимых адиабатных процессов.
Для лучшего понимания представим тепловую машину, цилиндр которой может быть по мере надобности и абсолютно теплопроводным, и абсолютно нетеплопроводным.
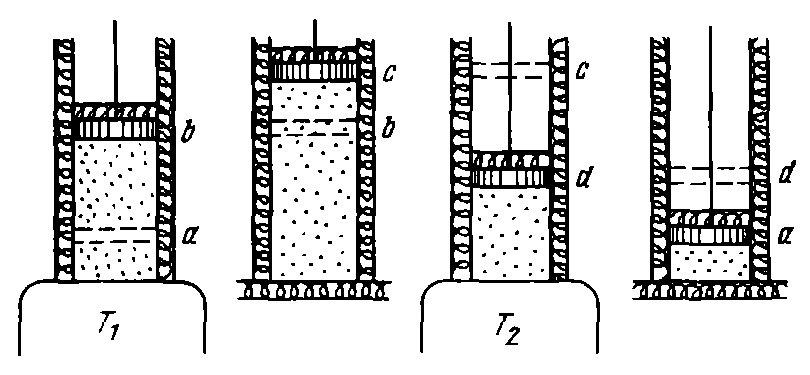
Рисунок 21.
Газ (рабочее тело) с начальными параметрами, характеризующимися точкой а (параметры рабочего тела р1, υ1, а температура Т1), помещен в цилиндр под поршень, причем боковые стенки цилиндра и поршень абсолютно нетеплопроводны, так что теплота может передаваться только через основание цилиндра (изотерма 12, рис. 20). Вводим цилиндр в соприкосновение с горячим источником теплоты. Расширяясь изотермически при температуре Т1 от объема υa до объема υb, газ забирает от горючего источника теплоту

Параметры точки 2: р2, υ2, Т1.
В точке b подвод теплоты прекращаем и ставим цилиндр на теплоизолятор. Дальнейшее расширение рабочего тела происходит адиабатно. Работа расширения совершается при этом только за счет внутренней энергии, в результате чего температура газа падает до Т2 (изотерма 23).
Параметры точки 3: р3, υ3, Т2.
Теперь возвратим тело в начальное состояние. Для этого сначала поместим цилиндр на холодный источник с температурой Т2 и будем сжимать рабочее тело по изотерме 34 (рис. 20), совершая работу l2 и отводя при этом к нижнему источнику от рабочего тела теплоту:
Затем снова поставим цилиндр на теплоизолятор и дальнейшее сжатие проведем в адиабатных условиях. Работа, затраченная на сжатие по линии 41, идет на увеличение внутренней энергии, в результате чего температура газа увеличивается до Т1.
Параметры точки 4: р4, υ4, Т2.
Таким образом, за весь цикл рабочему телу от теплоотдатчика было сообщено удельное количество теплоты q1 и отведено в теплоприемник удельное количество теплоты q2.
Термический КПД цикла:
Подставляя найденные значения q1 и q2 в уравнение для термического КПД и преобразуя получим:
Таким образом, термический КПД обратимого цикла Карно зависит только от абсолютных температур теплоотдатчика и теплоприемника. Он будет тем больше чем выше температура теплоотдатчика, и чем меньше температура теплоприемника.
Термический КПД всегда меньше 1, так как для получения КПД, равного единице необходимо, чтобы Т1=0 и Т2→∞, а это невозможно.
Термический КПД не зависит от природы рабочего тела и при Т1=Т2 равен нулю, т.е. невозможно теплоту превратить в работу если тела находятся в тепловом равновесии.
Термический КПД цикла Карно всегда больше КПД любого цикла, осуществимого в одном и том же интервале температур. Поэтому термических КПД любого цикла и КПД цикла Карно позволяет установить степень совершенства использования теплоты в машине, работающей по данному циклу.
В реальных двигателях цикл Карно не осуществляется. Однако на практике его значение велико, так как он служит эталоном для оценки степени совершенства любых циклов тепловых двигателей.
Обратимый цикл Карно, осуществленный в интервале температур Т1 и Т2, изображается на Т,s – диаграмме в виде прямоугольника 1234 (рис. 22).
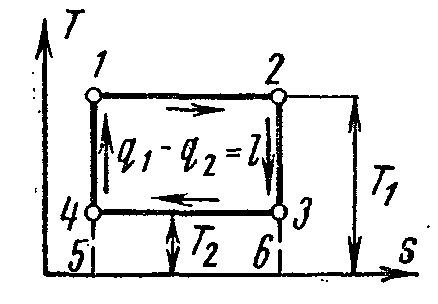
Рисунок 22 – Прямой обратимый цикл Карно в Т,s – координатах.
С помощью Т,s – диаграммы можно рассчитать термический КПД другим способом:
