
- •Тема 6: «Теплоемкость газов. Энтропия» 33
- •Тема 7: «Термодинамические процессы идеальных газов» 43
- •Тема 8: «Второй закон термодинамики» 57
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем» 71
- •Тема 10: «Водяной пар» 83
- •Тема 11. Истечение газов и паров 89
- •Тема 1: Основные понятия и определения
- •1.1. Основные термодинамические параметры состояния
- •4. Внутренняя энергия.
- •5. Энтальпия,
- •6. Энтропия,
- •1.2. Термодинамическая система
- •1.3. Термодинамический процесс
- •1.4. Теплота и работа
- •1.5. Термодинамическое равновесие
- •Контрольные вопросы
- •Тема 2: «Состояние идеального газа»
- •2.1. Основные законы идеальных газов
- •2.2. Уравнение состояния идеального газа
- •Тема 4: «Реальные газы»
- •4.1. Уравнение состояния Ван-дер-Ваальса
- •4.2. Уравнения м.П. Вукаловича и и.И. Новикова
- •Контрольные вопросы
- •Тема 5: «Первый закон термодинамики»
- •5.1. Внутренняя энергия
- •5.2. Работа расширения
- •5.3. Теплота
- •5.4. Аналитическое выражение первого закона термодинамики
- •5.5. Энтальпия
- •Контрольные вопросы
- •Тема 6: «Теплоемкость газов. Энтропия»
- •6.1. Основные определения
- •6.2. Удельная (массовая), объемная и мольная теплоемкости газов
- •6.3. Теплоемкость в изохорном и изобарном процессе
- •6.4. Молекулярно-кинетическая и квантовая теории теплоемкости
- •6.5. Истинная и средняя теплоемкости
- •6.6. Зависимость теплоемкости от температуры
- •6.7. Отношение теплоемкостей ср и сυ. Показатель адиабаты
- •6.8. Определение qp и qυ для идеальных газов
- •6.9. Теплоемкость смеси идеальных газов
- •6.10. Энтропия
- •Контрольные вопросы
- •Тема 7: «Термодинамические процессы идеальных газов»
- •7.1. Основные определения
- •7.2. Изохорный процесс
- •7.3. Изобарный процесс
- •7.4. Изотермический процесс
- •7.5. Адиабатный процесс
- •7.6. Политропные процессы
- •Контрольные вопросы
- •Тема 8: «Второй закон термодинамики»
- •8.1. Основные положения
- •8.2. Круговые термодинамические процессы (циклы)
- •8.3. Термический кпд и холодильный коэффициент циклов
- •8.4. Прямой обратимый цикл Карно
- •8.5. Обратный обратимый цикл Карно
- •8.6. Математическое выражение второго закона термодинамики
- •8.7. Изменение энтропии в обратимых и необратимых процессах
- •Контрольные вопросы
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем»
- •Характеристические функции
- •Физический смысл изохорно-изотермического и изобарно-изотермического потенциалов
- •Термодинамическое учение о равновесии
- •9.4. Общие условия равновесия термодинамической системы
- •Контрольные вопросы
- •Тема 10: «Водяной пар»
- •10.1. Основные понятия и определения
- •Контрольные вопросы
- •Тема 11. Истечение газов и паров
- •11.1. Первый закон термодинамики в применении к потоку движущегося газа
- •11.2. Работа проталкивания
- •11.3. Располагаемая работа
- •11.4. Адиабатный процесс истечения
- •11.5. Истечение из суживающегося сопла
- •11.6. Истечение идеального газа из комбинированного сопла Лаваля
- •Контрольные вопросы
1.2. Термодинамическая система
В любом явлении участвуют множество различных тел, связанных между собой. При термодинамическом изучении какого-либо явления в качестве объекта изучения выделяется группа тел, или единичное тело, или даже отдельные его части. Объект изучения называется термодинамической системой. Все, что окружает термодинамическую систему, называется окружающей средой.
Термодинамическая система – совокупность макроскопических тел, обменивающихся энергией как друг с другом, так и с окружающей средой.
Пример: газ, находящийся в цилиндре с поршнем – термодинамическая система, цилиндр и поршень окружающая среда.
Виды систем:
По степени обмена веществом и энергией:
1. изолированная – нет взаимодействия с окружающей средой. Пр.: термос;
2. закрытая – обменивается только энергией. Пр.: батарея;
3. открытая – обменивается с окружающей средой и веществом и энергией. Пр.: стакан, наполненный водным раствором соли.
По наличию границы раздела фаз:
Фаза – совокупность гомогенных частей гетерогенной системы, одинаковых по физическим и химическим свойствам, отделенная от других частей системы видимой поверхностью раздела. Фаза может быть твердой, жидкой и газообразной.
1. гомогенная – система, внутри которой нет поверхностей, разделяющих отличающиеся по своим свойствам части системы (фазы).
Пр.: идеальный газ или раствор поваренной соли.
Если во всех точках система имеет одинаковый состав и физические свойства одинаковы, то система называется физически однородной.
2. гетерогенная – система, внутри которой присутствует поверхность, разделяющая отличающиеся по свойствам части системы.
Пр.: вода и бензол, взвешенные частицы в жидкости, система из воды и льда.
1.3. Термодинамический процесс
Основные термодинамические параметры состояния р, υ и Т однородного тела зависят друг от друга и связаны соотношением:
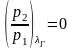 – уравнение
состояния.
– уравнение
состояния.
Если известно уравнение состояния, то для определения состояния простейших систем – однородных и постоянных по времени, по массе и по составу (состоящих из одной фазы и не изменяющихся химически) – достаточно знать две независимые переменные из трех:
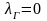
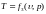
Если внешние условия меняются, то меняется и состояние системы. Совокупность изменений состояния термодинамической системы при переходе из одного равновесного состояния в другое называется термодинамическим процессом.
Равновесное состояния – состояние системы, в котором во всех ее точках давление, температура, удельный объем и другие физические параметры одинаковы.
Равновесный термодинамический процесс – процесс, проходящий через равновесные состояния.
Термодинамика в первую очередь рассматривает равновесные состояния и процессы изменения состояния термодинамической системы. Равновесный процесс осуществляется только в случае бесконечно медленного изменения параметров внешней среды или когда изменения параметров системы малы по сравнению со значениями этих параметров. Реальные процессы – неравновесные, поскольку под влиянием внешних условий они протекают с конечными скоростями и равновесное состояние не успевает устанавливаться.
С математической точки зрения уравнение состояния выражает некоторую поверхность – термодинамическая поверхность. Произвольно взятое равновесное состояние это точка на термодинамической поверхности, а совокупность этих точек при непрерывном изменений состояния – кривая, которая является графическим отображением равновесного процесса.
Параметры состояния системы могут быть:
1. экстенсивные – параметры, значения которых пропорциональны массе системы (объем, энергия, энтропия и др.);
2. интенсивные – параметры, не зависящие от массы системы (р, Т и др.)
Экстенсивные параметры подчиняются закону аддитивности, а интенсивные нет.
Измерение экстенсивной величины – это сравнение ее с другой, однородной с ней величиной, длина с длиной, объем с объемом.
Измерение интенсивной величины состоит в использовании объективной связи между изменением интенсивной и экстенсивной величины. Для изменения температуры используется термометр, который фиксирует интенсивную величину температуру путем измерения экстенсивной величины объема ртути.
