
- •Тема 6: «Теплоемкость газов. Энтропия» 33
- •Тема 7: «Термодинамические процессы идеальных газов» 43
- •Тема 8: «Второй закон термодинамики» 57
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем» 71
- •Тема 10: «Водяной пар» 83
- •Тема 11. Истечение газов и паров 89
- •Тема 1: Основные понятия и определения
- •1.1. Основные термодинамические параметры состояния
- •4. Внутренняя энергия.
- •5. Энтальпия,
- •6. Энтропия,
- •1.2. Термодинамическая система
- •1.3. Термодинамический процесс
- •1.4. Теплота и работа
- •1.5. Термодинамическое равновесие
- •Контрольные вопросы
- •Тема 2: «Состояние идеального газа»
- •2.1. Основные законы идеальных газов
- •2.2. Уравнение состояния идеального газа
- •Тема 4: «Реальные газы»
- •4.1. Уравнение состояния Ван-дер-Ваальса
- •4.2. Уравнения м.П. Вукаловича и и.И. Новикова
- •Контрольные вопросы
- •Тема 5: «Первый закон термодинамики»
- •5.1. Внутренняя энергия
- •5.2. Работа расширения
- •5.3. Теплота
- •5.4. Аналитическое выражение первого закона термодинамики
- •5.5. Энтальпия
- •Контрольные вопросы
- •Тема 6: «Теплоемкость газов. Энтропия»
- •6.1. Основные определения
- •6.2. Удельная (массовая), объемная и мольная теплоемкости газов
- •6.3. Теплоемкость в изохорном и изобарном процессе
- •6.4. Молекулярно-кинетическая и квантовая теории теплоемкости
- •6.5. Истинная и средняя теплоемкости
- •6.6. Зависимость теплоемкости от температуры
- •6.7. Отношение теплоемкостей ср и сυ. Показатель адиабаты
- •6.8. Определение qp и qυ для идеальных газов
- •6.9. Теплоемкость смеси идеальных газов
- •6.10. Энтропия
- •Контрольные вопросы
- •Тема 7: «Термодинамические процессы идеальных газов»
- •7.1. Основные определения
- •7.2. Изохорный процесс
- •7.3. Изобарный процесс
- •7.4. Изотермический процесс
- •7.5. Адиабатный процесс
- •7.6. Политропные процессы
- •Контрольные вопросы
- •Тема 8: «Второй закон термодинамики»
- •8.1. Основные положения
- •8.2. Круговые термодинамические процессы (циклы)
- •8.3. Термический кпд и холодильный коэффициент циклов
- •8.4. Прямой обратимый цикл Карно
- •8.5. Обратный обратимый цикл Карно
- •8.6. Математическое выражение второго закона термодинамики
- •8.7. Изменение энтропии в обратимых и необратимых процессах
- •Контрольные вопросы
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем»
- •Характеристические функции
- •Физический смысл изохорно-изотермического и изобарно-изотермического потенциалов
- •Термодинамическое учение о равновесии
- •9.4. Общие условия равновесия термодинамической системы
- •Контрольные вопросы
- •Тема 10: «Водяной пар»
- •10.1. Основные понятия и определения
- •Контрольные вопросы
- •Тема 11. Истечение газов и паров
- •11.1. Первый закон термодинамики в применении к потоку движущегося газа
- •11.2. Работа проталкивания
- •11.3. Располагаемая работа
- •11.4. Адиабатный процесс истечения
- •11.5. Истечение из суживающегося сопла
- •11.6. Истечение идеального газа из комбинированного сопла Лаваля
- •Контрольные вопросы
11.3. Располагаемая работа
Величина
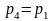 равная бесконечно малому приращению
внешней кинетической энергии рабочего
тела, называется элементарной
располагаемой работой.
равная бесконечно малому приращению
внешней кинетической энергии рабочего
тела, называется элементарной
располагаемой работой.
Эта энергия может быть использована для получения внешней полезной работы.
Для обратимого процесса течения газа
или
Равенство
показывает, что при движении рабочего
тела пот каналу знаки
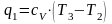 и
противоположны.
и
противоположны.
Если
 ,
то газ сжимается и его скорость
уменьшается:
.
,
то газ сжимается и его скорость
уменьшается:
.
Если , то газ расширяется и его скорость увеличивается: .
Располагаемую работу можно представить графически на рυ–диаграмме.
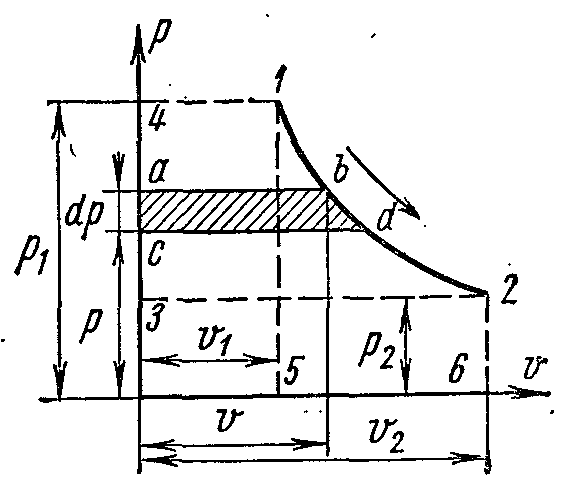
Рисунок 31.
На рисунке 31 изображен обратимый процесс расширения газа 1–2. Бесконечно малая располагаемая работу – υdp измеряется элементарной площадью abdc.
Очевидно вся располагаемая работа в процессе 1-2
Приращение кинетической энергии потокам газа представляет собой разность работ расширения потока газа и работы проталкивания ;
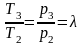 измеряется площадью
1234,
ограниченной линией процесса расширения
газа, абсциссами крайних точек и осью
ординат р.
измеряется площадью
1234,
ограниченной линией процесса расширения
газа, абсциссами крайних точек и осью
ординат р.
Если кривая 1-2 является политропой, то располагаемую работу находят по уравнению
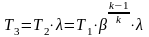
При адиабатном расширении идеального газа
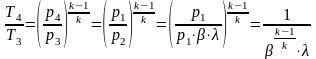
Сравнивая располагаемую работу при истечении (площадь 1234) с работой расширения газа (площадь 1265), получаем, что располагаемая работа в n раз больше работы расширения газа
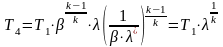
Из уравнения
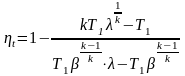 следует, что
следует, что
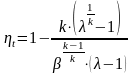
или
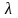
Располагаемая работа при истечении газа может быть получена за счет внешней теплоты и уменьшения энтальпии газа. Это уравнение справедливо как для обратимых, так и для необратимых процессов течения газа с трением.
При адиабатном течении из уравнения
или
При необратимом истечении газа располагаемая работа при том же перепаде давления меньше, так как энтальпия в конечном состоянии будет больше за счет полученной теплоты трения. Практически расчет ведется обычно для идеального (обратимого) процесса течения, а необратимость процесса учитывается эмпирическим коэффициентом, который всегда меньше единицы.
11.4. Адиабатный процесс истечения
Экспериментальные и теоретические исследования показывают, что в каналах даже при небольшой разности давлений газа и внешней среды получается достаточно большая скорость течения рабочего, тела. Так как длина канала небольшая, то теплообмен между стенками канала и газом при малом времени их прохождения настолько незначителен, что им можно пренебречь и процесс истечения считать адиабатным.
Скорость истечения газа при адиабатном процессе определяется из основного уравнения располагаемой работы:
или
Откуда
где
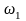 – начальная скорость газа;
– начальная скорость газа;
 – конечная скорость
газа при выходе из канала.
– конечная скорость
газа при выходе из канала.
В большинстве случаев начальная скорость газа по сравнению с конечной скоростью весьма мала, и в практических расчетах ею обычно пренебрегают.
Конечную скорость истечения определяют по уравнению:
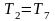
11.5. Истечение из суживающегося сопла
Располагаемую работу при адиабатном истечении идеального газа определяют по уравнению
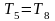
а скорость адиабатного истечения идеального газа по уравнению
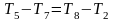
или

Скорость истечения газа зависит от состояния газа при входе в сопло и от давления р2 на выходе.
Массовый расход газа в килограммах в секунду при истечении определяется уравнением
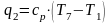
где
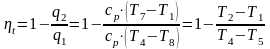 – площадь выходного сечения канала;
– площадь выходного сечения канала;
– скорость истечения;
– удельный объем газа в выходном сечении канала.
При адиабатном истечении идеального газа
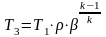
С учетом вышесказанного массовый расход идеального газа
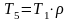
или
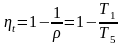
Массовый расход идеального газа зависит от площади выходного сечения канала, начального состояния газа и степени его расширения.
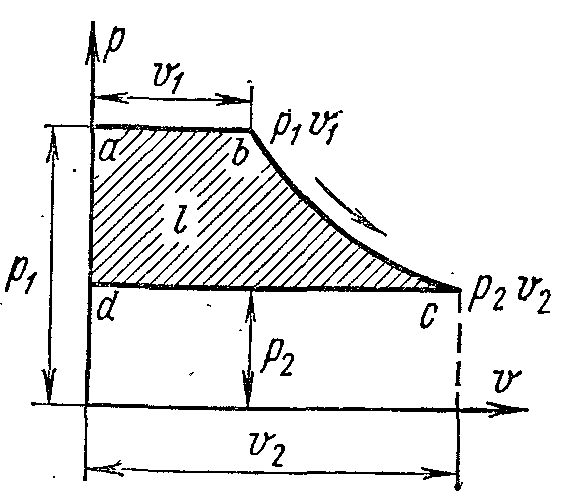
Рисунок 32.
Графически располагаемая работа при истечении газа изображается площадью abcd на рисунке 32.
