
- •Тема 6: «Теплоемкость газов. Энтропия» 33
- •Тема 7: «Термодинамические процессы идеальных газов» 43
- •Тема 8: «Второй закон термодинамики» 57
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем» 71
- •Тема 10: «Водяной пар» 83
- •Тема 11. Истечение газов и паров 89
- •Тема 1: Основные понятия и определения
- •1.1. Основные термодинамические параметры состояния
- •4. Внутренняя энергия.
- •5. Энтальпия,
- •6. Энтропия,
- •1.2. Термодинамическая система
- •1.3. Термодинамический процесс
- •1.4. Теплота и работа
- •1.5. Термодинамическое равновесие
- •Контрольные вопросы
- •Тема 2: «Состояние идеального газа»
- •2.1. Основные законы идеальных газов
- •2.2. Уравнение состояния идеального газа
- •Тема 4: «Реальные газы»
- •4.1. Уравнение состояния Ван-дер-Ваальса
- •4.2. Уравнения м.П. Вукаловича и и.И. Новикова
- •Контрольные вопросы
- •Тема 5: «Первый закон термодинамики»
- •5.1. Внутренняя энергия
- •5.2. Работа расширения
- •5.3. Теплота
- •5.4. Аналитическое выражение первого закона термодинамики
- •5.5. Энтальпия
- •Контрольные вопросы
- •Тема 6: «Теплоемкость газов. Энтропия»
- •6.1. Основные определения
- •6.2. Удельная (массовая), объемная и мольная теплоемкости газов
- •6.3. Теплоемкость в изохорном и изобарном процессе
- •6.4. Молекулярно-кинетическая и квантовая теории теплоемкости
- •6.5. Истинная и средняя теплоемкости
- •6.6. Зависимость теплоемкости от температуры
- •6.7. Отношение теплоемкостей ср и сυ. Показатель адиабаты
- •6.8. Определение qp и qυ для идеальных газов
- •6.9. Теплоемкость смеси идеальных газов
- •6.10. Энтропия
- •Контрольные вопросы
- •Тема 7: «Термодинамические процессы идеальных газов»
- •7.1. Основные определения
- •7.2. Изохорный процесс
- •7.3. Изобарный процесс
- •7.4. Изотермический процесс
- •7.5. Адиабатный процесс
- •7.6. Политропные процессы
- •Контрольные вопросы
- •Тема 8: «Второй закон термодинамики»
- •8.1. Основные положения
- •8.2. Круговые термодинамические процессы (циклы)
- •8.3. Термический кпд и холодильный коэффициент циклов
- •8.4. Прямой обратимый цикл Карно
- •8.5. Обратный обратимый цикл Карно
- •8.6. Математическое выражение второго закона термодинамики
- •8.7. Изменение энтропии в обратимых и необратимых процессах
- •Контрольные вопросы
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем»
- •Характеристические функции
- •Физический смысл изохорно-изотермического и изобарно-изотермического потенциалов
- •Термодинамическое учение о равновесии
- •9.4. Общие условия равновесия термодинамической системы
- •Контрольные вопросы
- •Тема 10: «Водяной пар»
- •10.1. Основные понятия и определения
- •Контрольные вопросы
- •Тема 11. Истечение газов и паров
- •11.1. Первый закон термодинамики в применении к потоку движущегося газа
- •11.2. Работа проталкивания
- •11.3. Располагаемая работа
- •11.4. Адиабатный процесс истечения
- •11.5. Истечение из суживающегося сопла
- •11.6. Истечение идеального газа из комбинированного сопла Лаваля
- •Контрольные вопросы
Контрольные вопросы
Дайте определение основным термодинамическим процессам.
Изобразите графически изохору, изобару, изотерму и адиабату в р,υ- и T,s-координатах.
Напишите уравнения основных процессов.
Напишите формулы соотношений между основными параметрами для каждого процесса.
Напишите формулы удельной работы изменения объема для каждого процесса.
Напишите формулы располагаемой (полезной) работы для каждого процесса.
При каком условии основные процессы идеального газа будут политропными?
Напишите уравнение политропы и укажите, в каких пределах изменяется показатель политропы.
Укажите значения показателя политропы для основных процессов.
По каким уравнениям вычисляется изменение энтропии.
Задача
Воздух массой 10 кг расширяется изотермически при температуре 400 ºС и давлении 800 кПа до конечного объема V2=5 м3. Определить начальный объем, конечное давление, работу расширения, изменение интальпии, энтропии и внутренней энергии.
Решение:
Начальный объем определяем из уравнения состояния
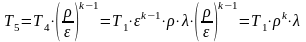
Конечное давление
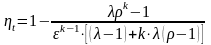 кПа
кПа
Работа расширения
Изменение энтропии
кДж/К
Энтальпия и внутренняя энергия идеального газа в изотермическом процессе неизменяются, так как di=0 и du=0.
Тема 8: «Второй закон термодинамики»
8.1. Основные положения
Первый закон термодинамики, являясь частным случаем всеобщего закона сохранения и превращения энергии, утверждает, что теплота может превращаться в работу, а работа – в теплоту, не устанавливая условий, при которых возможны эти превращения и не рассматривая вопроса о направлении теплового процесса.
Работа, как и все другие виды энергии, участвующие в каком-либо процессе, легко и полностью превращается в теплоту. Этот факт известен человеку с глубокой древности, когда тот добывал огонь трением двух кусков дерева. Процессы превращения работы в теплоту происходят в природе непрерывно: трение, удар, торможение и т.д., совсем иначе дело обстоит с переходом теплоты в работу. Такой переход возможен только при наличии разности температур между источником тепла и теплоприемником.
Таким образом, между преобразованием теплоты в работу и обратно существует глубокое различие. Существует закон позволяющий указать направление теплового потока и максимально возможный предел превращения теплоты в работу в тепловых машинах – это второй закон термодинамики, имеющий общее значение для всех тепловых процессов.
Формулировка закона гласит: тепловой двигатель без холодного источника теплоты, т.е. двигатель, полностью превращающий в работу всю полученную от горячего источника теплоту, называется вечным двигателем второго рода и его существование невозможно.
8.2. Круговые термодинамические процессы (циклы)
При подведении теплоты или изменении внутренней энергии рабочего тела, или в результате одновременного действия этих параметров получается определенное количество работы. При однократном расширении газа в цилиндре это количество работы является весьма ограниченным, поскольку наступает момент, когда температура и давление рабочего тела становятся равными температуре и давлению окружающей среды. В этот момент получение работы прекращается.
Для повторного получения работы необходимо в процессе сжатия возвратить рабочее тело в первоначальное состояние.
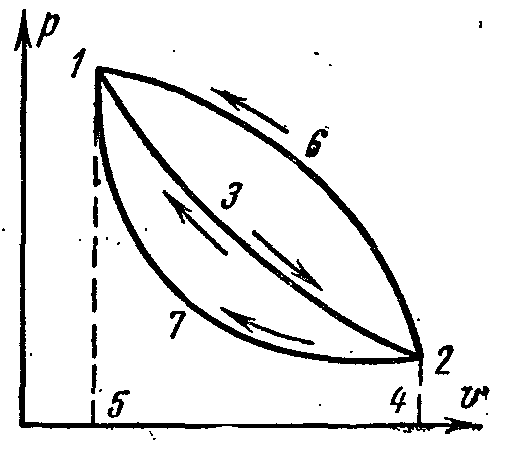
Рисунок 19 – Круговой процесс в Т,υ-координатах.
Из рисунка 19 следует, что при расширении рабочего тела по кривой 132, газ совершает работу, соответствующую площади пол кривой 51324. При достижении точки 2 рабочее тело должно быть возвращено в точку 1, чтобы оно снова могло произвести работу.
Процесс возвращения тела в начальное состояние может быть произведен тремя путями:
Кривая сжатия 231 совпадает с кривой 132. В таком процессе вся полученная при расширении работа (площадь 51324) равна работе сжатия (площадь 42315) и положительная работа равна 0;
Кривая сжатия 261 располагается над линией расширения 132. При этом на сжатие затрачивается больше работы (площадь 51624) чем на расширение (площадь 51324). Такой цикл называется обратным (по ним работают холодильные установки);
Кривая сжатия 271 располагается под линией расширения 132. В этом процессе работа расширения (площадь 51324) больше работы сжатия (площадь 51724). В результате положительная работа (площадь 13271) будет отдана во вне. Такой цикл называется прямым циклом (или циклом теплового двигателя).
Повторяя цикл неограниченное число раз можно получить любое количество работы.
Циклы бывают:
Обратимые (циклы, состоящие из обратимых равновесных процессов. Рабочее тело в таких циклах не должно подвергаться химическим изменениям);
Необратимые (циклы, в котором хотя бы один процесс является необратимым).
Результаты исследований идеальных циклов могут быть перенесены на работу реальных необратимых циклов с учетом поправочных коэффициентов.
