
- •Тема 6: «Теплоемкость газов. Энтропия» 33
- •Тема 7: «Термодинамические процессы идеальных газов» 43
- •Тема 8: «Второй закон термодинамики» 57
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем» 71
- •Тема 10: «Водяной пар» 83
- •Тема 11. Истечение газов и паров 89
- •Тема 1: Основные понятия и определения
- •1.1. Основные термодинамические параметры состояния
- •4. Внутренняя энергия.
- •5. Энтальпия,
- •6. Энтропия,
- •1.2. Термодинамическая система
- •1.3. Термодинамический процесс
- •1.4. Теплота и работа
- •1.5. Термодинамическое равновесие
- •Контрольные вопросы
- •Тема 2: «Состояние идеального газа»
- •2.1. Основные законы идеальных газов
- •2.2. Уравнение состояния идеального газа
- •Тема 4: «Реальные газы»
- •4.1. Уравнение состояния Ван-дер-Ваальса
- •4.2. Уравнения м.П. Вукаловича и и.И. Новикова
- •Контрольные вопросы
- •Тема 5: «Первый закон термодинамики»
- •5.1. Внутренняя энергия
- •5.2. Работа расширения
- •5.3. Теплота
- •5.4. Аналитическое выражение первого закона термодинамики
- •5.5. Энтальпия
- •Контрольные вопросы
- •Тема 6: «Теплоемкость газов. Энтропия»
- •6.1. Основные определения
- •6.2. Удельная (массовая), объемная и мольная теплоемкости газов
- •6.3. Теплоемкость в изохорном и изобарном процессе
- •6.4. Молекулярно-кинетическая и квантовая теории теплоемкости
- •6.5. Истинная и средняя теплоемкости
- •6.6. Зависимость теплоемкости от температуры
- •6.7. Отношение теплоемкостей ср и сυ. Показатель адиабаты
- •6.8. Определение qp и qυ для идеальных газов
- •6.9. Теплоемкость смеси идеальных газов
- •6.10. Энтропия
- •Контрольные вопросы
- •Тема 7: «Термодинамические процессы идеальных газов»
- •7.1. Основные определения
- •7.2. Изохорный процесс
- •7.3. Изобарный процесс
- •7.4. Изотермический процесс
- •7.5. Адиабатный процесс
- •7.6. Политропные процессы
- •Контрольные вопросы
- •Тема 8: «Второй закон термодинамики»
- •8.1. Основные положения
- •8.2. Круговые термодинамические процессы (циклы)
- •8.3. Термический кпд и холодильный коэффициент циклов
- •8.4. Прямой обратимый цикл Карно
- •8.5. Обратный обратимый цикл Карно
- •8.6. Математическое выражение второго закона термодинамики
- •8.7. Изменение энтропии в обратимых и необратимых процессах
- •Контрольные вопросы
- •Тема 9: «Характеристические функции и термодинамические потенциалы. Равновесие систем»
- •Характеристические функции
- •Физический смысл изохорно-изотермического и изобарно-изотермического потенциалов
- •Термодинамическое учение о равновесии
- •9.4. Общие условия равновесия термодинамической системы
- •Контрольные вопросы
- •Тема 10: «Водяной пар»
- •10.1. Основные понятия и определения
- •Контрольные вопросы
- •Тема 11. Истечение газов и паров
- •11.1. Первый закон термодинамики в применении к потоку движущегося газа
- •11.2. Работа проталкивания
- •11.3. Располагаемая работа
- •11.4. Адиабатный процесс истечения
- •11.5. Истечение из суживающегося сопла
- •11.6. Истечение идеального газа из комбинированного сопла Лаваля
- •Контрольные вопросы
1.4. Теплота и работа
При протекании термодинамического процесса тела, участвующие в нем обмениваются между собой энергией. В результате энергия одних тел уменьшается, других увеличивается.
Передача энергии может быть осуществлена двумя способами:
1.
Передача
энергии в форме теплоты (реализуется
при непосредственном контакте тел,
имеющих разную температуру. Энергия
передается от более нагретого тела к
менее нагретому. Количество переданной
энергии – теплота Q
или удельная теплота q
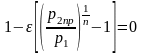 );
);
2.
Передача
энергии в форме работы (для
передачи энергии тело должно передвигаться
в силовом поле или изменять свой объем
под действием внешнего давления.
Количество переданной энергии – работа
L
или удельная работа l
 ).
).
В общем случае передача энергии в форме теплоты и работы может происходить одновременно. Количество теплоты и работы зависит от характера термодинамического процесса.
И теплота, и работа есть формы передачи движения от одних тел к другим, однако работа – макрофизическая форма передачи энергии, а теплота – микрофизическая, поскольку связана с передачей энергии на молекулярном уровне без видимого движения тел. Количество теплоты и работы есть мера энергии, переданной в форме теплоты и работы. Оба параметра зависят от характера процесса, а не определяются только его конечным и начальным состояниями.
1.5. Термодинамическое равновесие
Термодинамическое равновесие – когда состояние всех тел в системе длительное время не изменяется.
При термодинамическом равновесии передача теплоты от одних тел другим и механическое перемещение тел относительно друг друга невозможно, т.е. имеет место тепловое и механическое равновесие. При этом температура и давление системы равны температуре и давлению окружающей среды.
Без внешнего влияния выйти из состояния равновесия невозможно.
Контрольные вопросы
Какую взаимосвязь устанавливает техническая термодинамика?
На каких законах основывается термодинамика?
Какими параметрами характеризуется термодинамическое состояние системы и каково их содержание?
Что называется термодинамической системой?
Дать определение гомогенной и гетерогенной систем.
Что представляет собой термодинамический процесс, и каким он бывает?
В чем различие между абсолютным и (избыточным) давлением?
Как определяется высота столба жидкости для измерения давления?
Какие температурные шкалы приняты в России?
Что называется абсолютной температурой?
Определение удельного объема и плотности газа.
Какова связь между интенсивными параметрами состояния?
Что отображает уравнение состояния идеальных газов в пространстве?
Какими диаграммами изображается состояние вещества согласно термодинамической поверхности?
Зачем вводится в техническую термодинамику понятие об идеальном газе?
Характеристическое уравнение состояния для идеального газа?
На каких законах основан вывод уравнения состояния Клапейрона?
Размерность всех величин, входящих в уравнение Клапейрона?
Что называется молем (киломолем) газа?
На каких законах основан вывод уравнения Д.И. Менделеева?
Задача
Вычислить массу кислорода в баллоне объемом V=0,08 м3, находящемся при температуре t=27С. Давление газа по манометру pизб=1200 кПа, атмосферное давление по барометру 765 мм.рт.ст. при 25С.
Решение:
Приведем все заданные параметры к необходимым для подстановки в уравнение состояния единицам измерения.
воспользуемся
уравнением
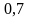 .
.
При измерении давления высотой столба жидкости необходимо учитывать измерение плотности жидкости в приборе в зависимости от температуры. При отклонении температуры жидкости в приборе от 0С следует ввести поправку. Для ртути можно использовать зависимость
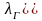
где p0 – атмосферное давление при температуре ртути 0С, мм.рт.ст;
p – атмосферное давление при температуре ртути t, С, мм.рт.ст.
В тех случаях, когда температура столба жидкости не указана, ее следует считать уже приведенной к 0С.
В
данном случае
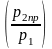 мм.рт.ст. или
мм.рт.ст. или
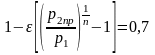 кПа.
кПа.
Абсолютное
давление в баллоне по формуле
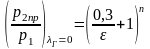 кПа=1301550
Па
кПа=1301550
Па
Температура Т=273+27=300К.
Газовая постоянная для кислорода
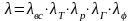
Масса кислорода
в баллоне исходя из уравнения
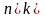 составит
составит
Ответ: 1,34 кг.
