
- •Хирургия аорты и магистральных сосудов Шалимов а.А. Дрюк н.Ф. Содержание
- •Методы реконструкции кровеносных сосудов и техника операций
- •Сосудистый шов
- •Способы дезоблитерации сосудов
- •Трансплантация сосудов
- •Паллиативные сосудистые операции
- •Хирургия грудной аорты и ее ветвей
- •Коарктация аорты
- •Классификация
- •Нарушения гемодинамики
- •Клиническая картина и диагностика
- •Лечение
- •Циркулярное протезирование
- •Аневризмы грудной аорты
- •Этиология
- •Клиническая картина и диагностика
- •Лечение
- •Расслаивающие аневризмы грудной аорты
- •Этиология
- •Патологическая анатомия
- •Клиническая картина и диагностика
- •Лечение
- •Окклюзионные поражения ветвей дуги аорты
- •Этиология
- •Клиническая картина и диагностика
- •Методы реконструкции ветвей дуги аорты
- •Окклюзионные поражения коронарных артерий (ишемическая болезнь сердца)
- •Этиология и патогенез
- •Хирургическая анатомия коронарных артерий
- •Состояние коронарных артерий у больных ишемической болезнью сердца
- •Клинические формы ишемической болезни сердца
- •Диагностика
- •Аневризмы брюшной аорты
- •Классификация
- •Клиническая картина и диагностика
- •Аневризмы, осложненные расслоением и разрывом стенок
- •Окклюзионные поражения почечных артерий (вазоренальная гипертония)
- •Этиология
- •Клиническая картина и диагностика
- •Дифференциальная диагностика
- •Хирургическое лечение вазоренальной гипертонии
- •Хронические окклюзии висцеральных артерий (висцерально-ишемический синдром)
- •Клиническая картина и диагностика
- •Сосудистые реконструктивные операции на висцеральных артериях.
- •Острая закупорка брыжеечных сосудов (инфаркт кишечника)
- •Клиническая картина и диагностика
- •Предоперационная подготовка
- •Хирургия периферических артерий хронические облитерирующие заболевания артерий конечностей
- •Облитерирующий эндартериит (облитерирующий тромбангиит, болезнь Винивартера — Бюргера).
- •Клиническая картина и диагностика
- •Классификация
- •Окклюзии брюшной аорты и подвздошных артерий
- •Хирургическое лечение
- •Сочетанные окклюзии аорто-подвздошного сегмента и бедренных артерий конечностей
- •Бедренно-подколенные окклюзии
- •Этиология
- •Окклюзия артерий подколенно-голеностопного сегмента
- •Хирургическое лечение
- •Особенности лечения облитерирующего эндартериита
- •Дифференциальные признаки облитерирующих заболеваний конечности
- •Реконструктивные операции на сосудах
- •Длительная внутриартериальная инфузия лекарственных веществ
- •Ампутация и некрэктомия
- •Хроническая артериальная недостаточность верхних конечностей
- •Этиология и классификация
- •Нейрососудистые компрессионные синдромы плечевого пояса
- •Болезнь и синдром рейно
- •Техника операций при хронической артериальной недостаточности верхних конечностей
- •Аневризмы периферических артерий
- •Классификация
- •Патологическая анатомия
- •Клиническая картина и диагностика
- •Хирургическое лечение
- •Принципы лечения больных после операций на периферических артериях
- •Экстренная хирургия артериальных сосудов
- •Эмболии и тромбозы бифуркации аорты и магистральных артерий
- •Этиология
- •Клиническая картина и диагностика
- •Лечение
- •Профилактика повторных эмболий
- •Травматические повреждения сосудов
- •Причины и классификация повреждений сосудов
- •Клиническая картина и диагностика
Клиническая картина и диагностика
Инфраренальные аневризмы. Бессимптомные аневризмы брюшной аорты чаще бывают малых размеров — до 4—7 мм в диаметре, не вызывают субъективных жалоб или проявляются скудной неспецифической симптоматикой. Скрытые аневризмы обычно выявляют случайно при обследовании больных с неясными абдоминальными симптомами, при аортографии, выполненной по поводу окклюзионных заболеваний сосудов, или обнаруживают на вскрытии умерших от причин, не связанных с аневризмой. Иногда сам больной может случайно обнаружить пульсирующее опухоле-
* Аневризмы, осложненные расслоением и разрывом стенки, рассмотрены нами в отдельном разделе (см. с. 134).
видное образование в области живота или ощущает пульсацию в животе, особенно в положении на животе, определяемое как «ощущение биения второго сердца».
Бессимптомные аневризмы составляют от 10 до 20% всех диагностированных аневризм брюшной аорты (Rob и Vollmar, 1959; Schatz и соавт., 1962). Раннее выявление этих форм имеет большое практическое значение в плане улучшения результатов лечения.
Типичные неосложненные или сочетанные аневризмы брюшной аорты характеризуются клиническими проявлениями, обусловленными сдавленней смежных органов и сочетанием с окклюзионными поражениями ветвей аорты или эмболией периферических артерий.
Наиболее частыми и типичными симптомами аневризм брюшной аорты являются боль в животе и наличие пульсирующего образования в брюшной полости, определяемого пальпа-торно или субъективно как ощущение пульсации в животе.
Боль отмечается чаще в левой половине живота, в области пупка, в спине и пояснично-крестцовой области. Характер ее может быть различной: тупая, ноющая, сильная пульсирующая или приступообразная по типу колики, которая может быть расценена как почечная и печеночная колика или панкреатит. Иногда боль становится невыносимой, усиливается при движении больных.
Пульсирующее образование в брюшной полости обнаруживается у 60—80% больных (Р. С. Ермолюк, 1968; Williams и соавт., 1972) обычно по срединной линии или в левой половине живота, имеет различные размеры, овальную или округлую форму, плотноэластическую консистенцию, неподвижное. В отличие от опухолей органов брюшной полости и забрюшин-ного пространства, которые могут передавать пульсацию аорты в одном направлении (так называемая передаточная пульсация), аневризмы аор- ты пульсируют во всех направлениях. Небольшие аневризмы, а также аневризмы значительных размеров у тучных больных не всегда обнаруживаются при пальпации. Опыт врача и целенаправленность исследования имеют немаловажное значение для их выявления.
Менее чем у V2 больных (А. А. Мартынов, 1972) над областью аневризмы и ниже ее выслушивают систолический шум, происхождение которого связано с завихрением и замедлением тока крови в полости аневризмы. При тромбозе аневризматического мешка, когда просвет его мало отличается от просвета аорты, систолический шум может отсутствовать.
Желудочно-кишечная симптоматика — снижение аппетита, спастическая боль, тошнота, рвота, хронические запоры — наблюдается более чем у половины больных и возникает вследствие атеросклеротической и тромботической обтурации или перегиба брыжеечных и чревной артерий (абдоминальный ишемический синдром), механической компрессии, смещения и перегиба двенадцатиперстной кишки и желудка аневризмой больших размеров, а также неврологическими вегетативными расстройствами в результате давления на парааортальные нервные сплетения. Почти у V4 больных отмечается потеря массы тела.
Урологические симптомы в виде приступообразной боли типа почечной колики, гематурии, дизуриче-ских расстройств возникают вследствие сдавления левого мочеточника и почки, а иногда — мочевого пузыря. При вовлечении в аневризматический процесс почечных артерий, чаще левой почки, может развиться почечная ишемическая гипертензия. В целом артериальная гипертензия наблюдается более чем у V2 больных аневризмой брюшной аорты (у 60%, А. В. Покровский, 1977).
Компрессия позвоночника, нервных корешков поясничного отдела спинного мозга может обусловливать
развитие выраженного ишиорадику-лярного синдрома с чувствительными и двигательными расстройствами со стороны нижних конечностей.
У 10—40% больных (А. А. Мартынов, 1972; Vollmar, 1967) наблюдаются симптомы ишемии нижних конечностей вследствие сочетанных атеросклеротических окклюзии подвздошных и бедренных сосудов, перегиба подвздошных артерий, эмболии периферических сосудов нижних конечностей тромбами из аневризмы.
Другие признаки атеросклероза имеются у большинства больных: поражение сосудов головного мозга, сердца, висцеральных и почечных артерий, облитерирующие поражения сосудов нижних конечностей.
У большинства больных целенаправленное клиническое исследование позволяет установить диагноз аневризмы брюшной аорты. Обзорная рентгене- и томография, особенно при исследовании в боковой и задней проекциях, являются ценными методами диагностики и позволяют не только поставить правильный диагноз, но и определить размеры аневризмы, ее локализацию, что имеет большое значение для планирования операции (А. В. Покровский и соавт., 1971; lyengar и соавт., 1973). Вследствие отложения кальция в стенке аорты на рентгенограммах определяются прерывистые линии контуров аневризмы. Указанные изменения лучше и чаще видны на снимках в боковой проекции; в прямой проекции наблюдается слияние тени аневризмы с позвоночником. При правильной экспозиции аневризмы обнаруживаются также при отсутствии кальцифика-ции ее стенки (Williams и соавт., 1972).
Косвенные
диагностические признаки могут быть
выявлены при внутривенной пиелографии
(смещение левого мочеточника кнаружи),
пневмо-ретроперитонеуме с последующей
рентгенографией, рентгенологическом
исследовании желудочно-кишечного тракта
с барием (оттеснение задней


Рис. 65. Аортограмма больного с аневризмой брюшной аорты:
а — сужение просвета аневризмы пристеночными тромбами, стенозирование левой почечной артерии; 6 — слабо контрастируется аневризматический мешок, заполненный тромбами
стенки желудка, деформация двенадцатиперстной кишки). Для диагностики аневризм используют также сканирование аорты с помощью технеция (пертехнетата — ТсМга), который вводят в вену. По нашим наблюдениям, этот метод является достаточно точным и простым. Перспективен для диагностики метод ультразвукового сканирования.
Большинство авторов (В. А. Кар-тавова и Л. О. Цакадзе, 1968; А. В. Покровский и соавт., 1971; Hall и соавт., 1970; lyengar и соавт., 1973, и др.) не считают аортографию обязательным исследованием при аневризме брюшной аорты и применяют ее лишь при определенных показаниях. Это объясняется тем, что обычные клинические и рентгенологические методы исследования позволяют в большинстве типичных случаев получить данные, достаточные для планирования операции, а также техническими трудностями (атеро-склеротические изменения, искривление и деформация сосудов) и риском осложнений (разрыв аневризмы, эмбо-
лия периферических артерий тромбо-тическими массами, почечная недостаточность). Кроме того, аортогра-фия не всегда позволяет выявить истинные размеры и локализацию аневризмы (у 13% больных, по данным May и соавт., 1968), а иногда по ангиографическим данным просвет аорты не отличается существенно от нормы в связи с массивным отложением тромбов в аневризматическом мешке (рис. 65), хотя истинные размеры аневризматического мешка могут быть большими. Поэтому при трактовке аортограмм следует обращать внимание не только на контрастное изображение самой аневризмы, но и на полутень, прилегающую к аневризме, обусловленную наличием пристеночных тромбов (И. X. Рабкин, 1977). Однако аортографию считают наиболее точным методом диагностики аневризм брюшной аорты, позволяющим также определить точную локализацию, протяженность, а также наличие сочетанного тромбоза, стеноза или аневризматического поражения ветвей брюшной аорты. Определение этих данных необходимо при выборе метода лечения.
Аортография показана при: 1) неясном диагнозе, бессимптомном течении, если на основании обычных клинико-рентгенологических методов исследования не представляется возможным подтвердить или исключить диагноз аневризмы; 2) подозрении на аневризму надпочечной локализации, высоко расположенных аневризмах у больных до 50 лет; 3) сочетанных окклюзионных поражениях подвздошных и бедренных артерий, а также висцеральных и почечных сосудов; 4) распространении аневризмы на ветви брюшной аорты.
Мы применяем аортографию у большинства больных, считая ее наиболее точным методом дооперационной диагностики аневризм. Однако при значительных технических трудностях применяем этот метод исследования в случае наличия указанных выше показаний. Отдаем предпочтение катетеризации бедренной артерии по Сель-дингеру при отсутствии признаков поражения бедренных и подвздошных артерий.
При вовлечении в атеросклероти-ческий процесс сосудов нижних конечностей используем ретроградное зондирование через подмышечную и плечевую артерии. При подозрении на поражение верхней брыжеечной и чревной артерий необходимо выполнять аортографию и в боковой проекции.
Дифференциальная диагностика. Разнообразие клинических признаков, особенно в случаях преобладания симптомов со стороны органов брюшной полости и забрюшинного пространства, а также скудная клиническая картина при бессимптомной аневризме вызывают иногда большие трудности в диагностике заболевания. Дифференциальный диагноз проводят с опухолями забрюшинного пространства (липома, липосаркома, лимфосаркома), желудка, кишечника, поджелудочной железы, почек, подковообразной или опущенной почкой,
окклюзией терминального отдела аорты, удлинением и девиацией аорты, особенно при гипертонической болезни, деформациях позвоночника. Решающее значение при этом имеют данные специальных методов обследования, в первую очередь рентгенологических, включая аортографию.
Прогноз заболевания в целом тяжелый. Лишь 7,6—36,4% больных живут свыше 5 лет после установления диагноза при спонтанном течении заболевания, без операции (Szilagyi и соавт., 1972; Bergan, Yao, 1974, и др.). Остальные умирают, причем большая половина (50—70%) — от разрыва аневризмы и кровотечения. Средняя продолжительность жизни больных с момента установления диагноза — 18—24 мес. Продолжительность жизни несколько больше при аневризмах менее 5 см в диаметре в случае отсутствия клинических проявлений. Однако малые размеры аневризмы не исключают возможности ее разрыва. Увеличение размеров аневризмы, нарастающая боль являются признаком прогрессирования аневризмы и опасности разрыва.
ЛЕЧЕНИЕ
Консервативных методов лечения этого заболевания не существует. Оперативное лечение в настоящее время является единственным способом, предотвращающим гибель больного от разрыва аневризмы. Такие паллиативные операции, как лигирование аорты, введение в аневризматический мешок различных металлических предметов с целью вызвать его тромбоз, окутывание аневризматического мешка различными тканями для укрепления стенки и другие, приводили к частым и тяжелым осложнениям. Методом выбора является радикальное лечение, то есть резекция аневризматического мешка с пластикой дефекта аорты и восстановлением магистрального кровотока. Методом выбора признана замена сегмента аорты гофрированными синтетическими сосудистыми протезами. Паллиативное вмешательство — укрепление стенки аневризмы снаружи синтетической тканью, а также аневризморрафия с образованием дубликатуры и укреплением брюшной аорты широкой фасцией бедра (метод Н. И. Краковского) — может быть рекомендовано тем больным, которым по тем или иным причинам невозможно сделать радикальную операцию.
Показания к операции. Хирургическое лечение принципиально показано всем больным с аневризмой брюшной аорты. Однако, учитывая тяжесть и опасность радикальной операции, а также пожилой или старческий возраст, наличие тяжелых сопутствующих заболеваний, необходим дифференцированный подход при определении показаний к операции. Задача состоит в оценке факторов риска и решении вопроса, может ли больной перенести наркоз и продолжительное травматичное хирургическое вмешательство, связанное с временным пережатием аорты и нарушением гемодинамики. Основными критериями при определении показаний к операции являются: размеры аневризмы, выраженность клинических симптомов, общее состояние больного с тщательной оценкой патологии и функции сердечно-сосудистой системы, почек, легких.
Вопросы показаний и противопоказаний к операции рассмотрены во многих работах (А. В. Покровский и соавт., 1971, 1977; Ф. Г. Углов, Л. О. Цакадзе, 1972; Bergan и Yao, 1974, и др.). Однако, по нашему мнению, невозможно дать схему, пригодную для всех случаев. Существуют принципиальные положения, касающиеся противопоказаний к операции, с которыми согласны большинство авторов: при неосложненной аневризме операция противопоказана больным со свежим инфарктом миокарда (менее 3 мес), острыми расстройствами мозгового кровообращения (давностью до 6 нед, А. В. Покровский, 1977), тяжелой легочной недостаточ-
ностью, недостаточностью кровообращения ПБ — III степени, выраженным нарушением функции печени, почечной недостаточностью с повышенным уровнем остаточного азота крови, сопутствующим злокачественным новообразованием, распространенной окклюзией подвздошных и бедренных артерий, включая глубокую бедренную артерию. При бессимптомных аневризмах малых размеров (до 5— 6 см в диаметре по рентгенологическим данным) у больных с высоким риском операции целесообразно воздержаться от хирургического лечения и продолжить динамическое наблюдение. Может быть целый ряд других относительных противопоказаний к операции. Необходимо тщательное обследование больного и квалифицированная оценка при участии хирурга и анестезиолога факторов риска, а также оценка опыта хирурга в лечении таких больных. Несомненно, плановые операции по поводу аневризмы брюшной аорты должны выполняться в специализированных клиниках.
Инфраренальные неосложненные аневризмы. Положение больного — на спине. Доступ осуществляют через широкую срединную лапаротомию от мечевидного отростка до лобка, что обеспечивает возможность манипуляций на инфраренальном участке брюшной аорты и на подвздошных артериях. Используют ранорасшири-тель. Вначале производят ревизию органов брюшной полости с целью выявления заболеваний, симулирующих аневризму и сопутствующих ей (опухоли, язва и др.). Тонкий кишечник отводят широким ретрактором вправо и кверху или выводят из брюшной полости (эвисцерация) и укутывают влажными полотенцами, особенно при наличии больших аневризм и у тучных больных. Предварительно, до эвисцерации, в корень брыжейки вводят раствор новокаина.
Задний листок брюшины рассекают над аневризмой и над общими подвздошными артериями. Пересекают трейцеву связку, двенадцатиперстную кишку и дистальную часть поджелудочной железы отделяют от аорты и смещают кверху ретрактором.
Следующий этап — тщательная ревизия аневризмы, сосудов и уточнение плана реконструктивной операции. Важно выяснить следующее: уровень верхнего полюса аневризмы, состояние и ширину участка аорты между почечными артериями и аневризмой, положение левой почечной вены, выраженность спаек в этой области и с нижней полой веной, состояние нижней брыжеечной артерии и выраженность сосудистых анастомозов с верхней брыжеечной артерией (дуга Риолана), а также состояние внутренних подвздошных артерий, от проходимости которых зависит кровоснабжение дистальной части толстого кишечника в случае прекращения кровотока по нижней брыжеечной артерии. Проверяют состояние бифуркации аорты и подвздошных сосудов в плане выявления аневризматического расширения их и окклюзионных поражений. В конечном счете решают вопрос о возможности выполнения радикальной операции — резекции аневризмы.
Следующий этап — выделение аорты выше аневризмы до уровня от-хождения почечных сосудов с таким расчетом, чтобы можно было наложить зажим ниже почечных сосудов. Левую почечную вену, расположенную поперечно на передней поверхности аорты, с помощью диссектора осторожно отделяют от аорты и берут на держалку. Нижнюю брыжеечную вену пересекают и перевязывают. После этого представляется возможным выделить верхний полюс аневризмы и аорту ниже отхождения почечных артерий и подвести под аорту катетер-держалку. Мобилизацию этого сегмента аорты осуществляют с помощью диссектора и манипуляций указательным пальцем. Необходимо помнить о возможности отхождения в этом участке аорты дополнительной ветви к нижнему полюсу почки и
поясничных артерий. У некоторых больных левая почечная вена может быть расположена кзади от аорты.
Затем выделяют и берут на турникеты общие подвздошные артерии. При этом особенно осторожно и тщательно выделяют правую общую подвздошную артерию с тем, чтобы не повредить лежащую под ней левую общую подвздошную вену, стенка которой часто плотно сращена с артерией. Вначале лучше выделить артерию дистальнее вены, а затем осторожно с помощью диссектора разделить сращения между веной и артерией. В случае ранения вены следует закрыть пальцем, а затем ушить отверстие атравматической иглой.
Если вовлечены в аневризматиче-ский процесс подвздошные артерии, последние выделяют на границе ди-стального края их аневризматического расширения.
Следующий
этап, который нередко бывает продолжительным
и трудным, — последовательное и
методичное отделение аневризматического
мешка от окружающих органов. Выделение
аневризмы лучше начинать снизу от
бифуркации аорты вверх. Если отделение
аневризмы от нижней полой вены удается
с трудом (при выраженных сращениях),
то нецелесообразно ее отделять. В
таких случаях после иссечения мешка
оставляют полоску стенки аневризмы,
спаянной с нижней полой веной. Нижняя
брыжеечная артерия у большинства больных
отходит от аневризматического мешка
и часто облитерирована. В последнем
случае ее пересекают и перевязывают.
Если артерия пульсирует, целесообразнее
ее сохранить, иссечь часть стенки
аневризмы в области ее устья с целью
последующей имплантации артерии в
протез. Однако при развитых коллатеральных
сосудах к верхней брыжеечной артерии
(дуга Риолана) и сохранении проходимости
левой внутренней подвздошной артерии
нижняя брыжеечная артерия может быть
лигирована после пересечения. Одним из
показателей

д e ж
Рис. 66. Схема типичной резекции аневризмы и протезирования брюшной аорты:
а — выделение аневризмы (по Dubost) и резекция; 6 — наложение проксимального анастомоза; в —• промывание протеза кровью (preclotting); г, д — наложен дистальный анастомоз одной ветви протеза и последовательность этапов при «включении» кровотока в конечностях; е — наложение анастомоза второй ветви протеза; ж — схема реконструкции аорты
удовлетворительного коллатерального кровоснабжения дистальных отделов толстого кишечника является хороший ретроградный кровоток из нижней брыжеечной артерии.
Левый мочеточник обычно распластан на передне-боковой поверхности аневризмы, и его осторожно отделяют. При аневризмах больших размеров мочеточник может быть сдавлен, изменен, плотно сращен с анев-ризматическим мешком. Если отделение мочеточника представляет большие трудности, целесообразно иссечь (после наложения зажимов на аорту) часть стенки аневризмы, сращенную
с мочеточником, с тем чтобы предохранить его от повреждения.
Одним из самых трудных этапов операции является выделение задней стенки аневризмы и отделение ее от нижней полой вены. Выделяя ее снизу вверх, последовательно перевязывают и пересекают среднюю крестцовую артерию, поясничные артерии и вены. При плотных сращениях заднюю стенку отделяют, используя следующий прием (Dubost с соавт., 1970, рис. 66). Накладывают зажим на относительно здоровый участок аорты между почечными артериями и верхним полюсом аневризмы. Пере- жимают и пересекают общие подвздошные артерии (или аорту над бифуркацией). Дистальный конец аневризмы приподнимают и ротируют кверху, последовательно отделяя ее от задней брюшной стенки и нижней полой вены, перевязывая и пересекая среднюю крестцовую и поясничные артерии. Этот прием облегчает также отделение аневризмы от нижней полой вены. Достоинством метода является меньшая опасность эмболии периферических артерий тромбами из аневризмы при ее выделении, недостатком — удлинение времени пережатия аорты.
В типичных случаях аневризмати-ческий мешок резецируют, дефект аорты замещают гофрированным сосудистым протезом. Почти у половины больных представляется возможным сохранить бифуркацию аорты и использовать для пластики простой трубчатый протез. При аневризмах аорто-подвздошного сегмента, а также при выраженном кальцинозе, стенозе или окклюзии подвздошных артерий используют бифуркационный протез с дистальным анастомозом к подвздошным или общей бедренной артериям.
Первым накладывают проксимальный анастомоз, как правило, конец в конец. Вначале мы обычно накладываем обвивной шов изнутри на заднюю полуокружность анастомоза, а затем снаружи на переднюю его полуокружность. В отдельных случаях заднюю стенку сшиваем двухрядным швом.
Наложение проксимального анастомоза может оказаться технически трудным в случае распространения аневризмы до устья правой почечной артерии. Правую почечную артерию временно пережимают, а зажим на аорту накладывают в таком случае между почечными артериями (рис. 67).
После выполнения проксимального анастомоза накладывают зажим на дистальный конец протеза и кратковременно ослабляют зажим на аорте с целью проверки герметичности шва, вымывания атероматозных и тромбо-
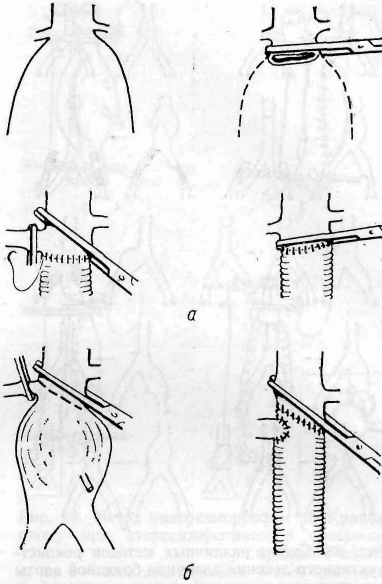
Рис. 67. К технике резекции инфраренальной аневризмы при вовлечении в процесс участка аорты, прилежащего непосредственно к почечным артериям (а) или правой почечной
артерии (б)
тических масс из аорты и заполнения пор трансплантата фибрином («ргес-lotting»).
Образовавшиеся в просвете протеза сгустки крови удаляются в последующем механически и путем вымывания с помощью отсоса.
Далее выполняют дистальный анастомоз. Анастомоз с аортой при сохранении ее бифуркации или с общими подвздошными артериями обычно накладывают по типу конец в конец. Однако при наличии кальци-ноза, значительного сужения или окклюзии подвздошных артерий дистальный анастомоз накладывают по типу конец в бок с менее пораженным участком подвздошных или общей бедренной артерий, а проксимальные концы пересеченных общих подвздошных артерий ушивают (рис. 68).
Рис. 68. Схемы различных методов реконструктивного лечения аневризм брюшной аорты и подвздошных артерий:
1—5 — резекция аневризмы и протезирование; 6—8 — резекция и протезирование аневризмы подвздошных артерий; 9 — резекция мешковидной аневризмы брюшной аорты с наружной пластикой (укреплением стенки) аорты; 10 — схема аневризморрафии и укрепления стенки фасцией по Краковскому
При этом целесообразно хотя бы один анастомоз — слева — выполнить так, чтобы внутренняя подвздошная артерия была включена в кровоток. У отдельных больных внутреннюю подвздошную артерию можно анастомозиро-вать с протезом. Последовательность анастомозирования правой или левой бранши протеза не имеет существенного значения, однако вначале целесообразнее наложить анастомоз с той стороны, где артерии менее поражены облитерирующим процессом. При его завершении включают в магистральный кровоток сосуды одной конечности, а затем анастомозируют вторую ветвь протеза. При наложении анастомозов следует обращать внимание на фиксацию интимы по всей линии шва.

Рис. 69. Схема резекции аневризмы и протезирования брюшной аорты с укутыванием трансплантата стенками аневризматического мешка (объяснение в тексте)
У больных с высоким операционным риском, особенно у пациентов пожилого и старческого возраста, с тяжелыми сопутствующими заболеваниями, при больших трудностях отделения аневризмы от нижней полой вены и задней брюшной стенки рекомендуется применять нетипичную методику резекции аневризмы с протезированием аорты и укутыванием протеза стенками аневризматического мешка (рис. 69). Некоторые авторы используют эту методику у большинства больных (А. А. Мартынов, 1972; М. Д. Князев и соавт., 1973). Техника операции отличается от типичной тем, что после наложения зажимов на аорту и подвздошные артерии аневризматический мешок вскрывают . продольно на всем протяжении, удаляют из его полости тромботи-ческие и атероматозные массы вместе с измененной интимой. Кровотечение из поясничных артерий останавливают путем прошивания и перевязывания их изнутри аневриз-матического мешка. Аорту и подвздошные артерии пересекают выше и ниже аневризмы, после чего дефект аорты замещают протезом, как описано выше. Оставленные in situ стенки аневризматического мешка используют для укутывания анастомозов и протеза. Эта техника операции является методом выбора при разрыве аневризмы. Она отличается следующими преимуществами: 1) сокращается время пережатия аорты и продолжительность всей операции; 2) уменьшается опасность повреждения нижней полой вены, мочеточника, подвздошных вен при выделении аневризмы; 3) не повреждается пара-аортальное нервное сплетение, играющее важную роль в регуляции функции кишечника; 4) укутывание протеза уменьшает способность образования пролежней окружающих органов, особенно двенадцатиперстной кишки, и опасность кровотечения из анастомоза. В целом риск операции меньше, а ближайший послеоперационный период протекает более благоприятно. Некоторые авторы (А. В. Покровский, 1977) фактически отказались от резекции аневризмы с полным ее удалением, производят резекцию аневризмы без выделения ее стенок, причем накладывают анастомоз с протезом без пересечения задней стенки аорты. Кроме этого, стремятся сохранить бифуркацию аорты и ограничиться наложением двух анастомозов. У отдельных больных с ограниченными по протяженности аневризмами резекцию ее производят без использования сосудистых протезов, за счет мобилизации аорты и подвздошных артерий с анастомозом конец в конец.
Устранение дефекта возможно при этом в связи с нередким удлинением и девиацией аорты и подвздошных артерий.
Стенку аневризматического мешка также используют для пластики стенки аорты — так называемый щадящий

Рис. 70. Метод аневризморрафии по Краковскому при атеросклеротической аневризме
брюшной аорты:
а, б, в — последовательность этапов операции;
г, д — схема укрепления стенки аорты свободным
лоскутом широкой фасции бедра
метод хирургического лечения атеро-склеротических аневризм брюшной аорты с помощью аневризморрафии, предложенный Н. И. Краковским (1971). Техника операции состоит в следующем (рис. 70). Выделяют и пережимают аорту проксимальнее, а подвздошные артерии дистальнее аневризматического мешка. Вскрывают мешок полулунным разрезом, обращенным вправо, с сохранением устья нижней брыжеечной артерии. Удаляют тромботические и атероматозные массы, а также атеросклеротически измененную внутреннюю оболочку. Оболочки аневризмы ушивают дубли-катурным швом и восстанавливают нормальный просвет брюшной аорты с наружной фиксацией оперированного сегмента аорты свободным лоскутом широкой фасции бедра с целью укрепления стенки аорты.
Н. И. Краковский, В. Я- Золото-ревский (1971, 1972) отмечают сле-
131 дующие преимущества этой операции: сравнительно малая травматичность, короткое время пережатия аорты, малая кровопотеря, отказ от бифуркационного протеза, сохранение функции поясничных и нижней брыжеечной артерий, что предупреждает ишемическое повреждение спинного мозга и толстого кишечника, связанных с перевязкой этих сосудов. Авторы экспериментально обосновали надежность укрепления брюшной аорты фасцией бедра после аневризмор-рафии (Н. И. Краковский и соавт., 1973).
Во время операции по поводу аневризмы брюшной аорты, как обычно при реконструктивных операциях на артериальных сосудах, мы применяем гепарин с целью предупреждения тром-ботических осложнений, связанных с временным выключением магистрального кровотока. Мы вводим 5000 ЕД гепарина в вену или в дистальное артериальное русло за 5 мин до наложения зажима на аорту. Необходимо, однако, учитывать, что применение гепарина значительно (почти в 2 раза) увеличивает кровопотерю. Если предполагается непродолжительное пережатие аорты, при условии хорошего состояния дистального сосудистого русла, гепарин можно не применять. При выраженном облитерирующем поражении подвздошных и бедренных артерий применение гепарина мы считаем обязательным. Для уменьшения кровопотери через поры протеза важно предварительно заполнить их фибрином, заполнив протез кровью после наложения проксимального анастомоза («preclotting»). Отдельным больным мы вводили протамин (из расчета 2 мг протамина на 1 мг введенного гепарина) внутривенно за несколько минут до включения протеза в магистральный кровоток.
Кровопотеря во время операции по поводу аневризмы брюшной аорты обычно большая и связана с большим объемом оперативного вмешательства, пересечением множества мелких сосудов, одномоментной потерей крови
через поры протеза и анастомозы после снятия зажимов. Отмечена зависимость послеоперационной летальности от величины кровопотери (А. А. Мартынов, 1972). В этой связи важными являются все меры профилактики кровопотери, а также своевременное и полное ее возмещение. До включения протеза в магистральный кровоток кровопотерю необходимо возместить полностью в условиях ги-перволемической гемодилюции, а также подготовить кровь и наладить струйное ее введение в момент снятия зажимов с аорты.
Снятие зажимов с аорты и подвздошных артерий с включением магистрального кровотока является важным этапом операции и может быть причиной острой гипотонии. Для развития ее имеют значение следующие факторы: острая кровопотеря через поры протеза и анастомозы, особенно при неполном возмещении кровопотери до снятия зажимов; реактивная гиперемия с депонированием крови в сосудах ишемизированной зоны (в конечностях); метаболический ацидоз в результате гипоксии тканей нижних конечностей во время операции; быстрое переливание больших количеств длительно хранимой цитратной крови с низким рН перед снятием зажимов с аорты (Burton и соавт., 1964).
Вначале снимают дистальный зажим с целью ретроградного заполнения протеза и вытеснения из него воздуха, затем —проксимальный зажим. В первую очередь лучше снять зажим только с внутренней подвздошной артерии, а кровоток через наружную подвздошную артерию включить после снятия проксимального зажима с аорты (предупреждение тромбоэмболии периферических артерий сгустками крови из аорты и протеза). Рекомендуется также использовать следующий прием (East-cott, 1969): аорту выше проксимального анастомоза сдавливают между большим и указательным пальцами и освобождают ее просвет на каждой 10-й пульсовой волне, затем на 9-й, 8-й и т. д. до полного включения магистрального кровотока в течение 5—10 мин. Напряжение аорты, контролируемое пальпаторно, может служить в определенной степени показателем уровня артериального давления. Протез и анастомозы перекрывают салфетками для лучшего гемостаза. Повторное наложение зажимов на аорту в связи с сильным кровотечением из анастомозов опасно с точки зрения возможности возникновения тромбо-эмболических осложнений, поэтому допустимо только в исключительных случаях. Обычно же достаточно эффективными являются компрессия салфетками области анастомозов продолжительное время и укутывание их гемостатическими материалами, например, гемостатической марлей.
После остановки кровотечения из протеза и анастомозов производят тщательный гемостаз, проверяют визуально и пальпаторно проходимость протеза и сосудов дистальнее анастомозов. Важно, чтобы не было перегиба и перекручивания протеза. Тщательную ревизию дистальной части толстой кишки осуществляют при перевязке нижней брыжеечной артерии, чтобы убедиться в адекватности ее кровоснабжения.
Операционное поле промывают раствором антибиотиков. Протез по возможности тщательно перекрывают окружающими тканями, задним листком париетальной брюшины, оставшимися оболочками аневризмати-ческого мешка. Особенно важно прикрыть аллотрансплантат в месте пред-лежания двенадцатиперстной кишки (предупреждение пролежней, инфицирования, вторичного кровотечения). С этой целью используют также большой сальник. Лапаротомную рану послойно закрывают с оставлением дренажей в брюшной полости или забрюшинном пространстве.
Квалифицированное анестезиологическое обеспечение операции по поводу аневризмы аорты имеет очень большое значение. Уже во время
операции проводят мероприятия с целью предупреждения почечной недостаточности, обусловленной нарушением гемодинамики в связи с пережатием аорты и последующим восстановлением магистрального кровотока: контроль диуреза через катетер, введенный в мочевой пузырь; поддержание артериального давления на достаточном уровне, своевременное восполнение кровопотери и устранение гиповолемии; введение растворов соды и электролитов с целью нейтрализации кислых продуктов метаболизма и коррекции электролитного баланса; введение низкомолекулярных декст-ранов, эуфиллина, маннитола (0,5—1 г на 1 кг массы больного) для увеличения диуреза. Коррекцию гипокалие-мии, обусловленной повышенным диурезом, осуществляют внутривенным введением 2—3 г и более калия в сутки (В. И. Старшинов и соавт., 1972). Большое значение для профилактики почечной недостаточности имеет поддержание артериального давления на достаточном уровне, своевременное замещение кровопотери и устранение гиповолемии. Только при таком условии введение препаратов, стимулирующих диурез, может быть эффективно.
Послеоперационное лечение такое же, как и при других больших сосудистых операциях. Оно должно быть направлено в первую очередь на предупреждение паралитической кишечной непроходимости, почечной недостаточности, шока и инфекции.
Супраренальные аневризмы. Аневризмы этой локализации представляют собой значительно более серьезную проблему по сравнению с аневризмами нижнего отдела брюшной аорты, так как в процесс вовлекаются крупные сосуды, снабжающие кровью органы брюшной полости. Диагностика надпочечных аневризм более трудная; в клинической картине могут преобладать симптомы патологии желудка, почек, поджелудочной железы, печени, селезенки. Точная диагностика основывается на данных аортографии. Резекция аневризм брюшной аорты надпочечной локализации —одна из наиболее сложных в техническом отношении и продолжительных операций в сосудистой хирургии. Это обусловлено необходимостью выделения нисходящей, грудной аорты и брюшного отдела аорты и предупреждения ишемического повреждения почек и органов брюшной полости при иссечении аневризмы, замещении аорты протезом и реимплантации 4 артерий: чревной, верхней брыжеечной и обеих почечных.
Доступ к супраренальному отделу аорты осуществляют путем торако-френолапаротомии или торакофрено-люмботомии.
В настоящее время обычно применяют технику операции, разработанную De Bakey и соавторами (I960),, с использованием аорто-аор-тального шунтирования через сосудистый протез, с последующей поэтапной имплантацией висцеральных артерий, резекцией аневризмы и превращением временного шунта в постоянный аллотрансплантат аорты (см. рис. 34).
Предложены также другие методы защиты органов брюшной полости от ишемического повреждения — гипотермия, селективная перфузия висцеральных артерий, предсердно-бед-ренное шунтирование с поэтапной имплантацией висцеральных артерий в краниальном направлении. Первые два способа не оправдали себя, а последний используют в единичных случаях.
Наибольшим опытом лечения аневризм торако-абдоминального отдела аорты располагает клиника De Bakey. Летальность больных, включая также пациентов с расслаивающей аневризмой (12%), составляет 26% (De Bakey и соавт., 1965). По данным А. В. Покровского (1977), коррекция почечного кровообращения потребовалась у 14 больных, кровотока по висцеральным артериям — у 11 больных, оперированных по поводу аневризмы брюшной аорты.
