
- •Кристаллография и минералогия
- •Для студентов высших учебных заведений
- •Предисловие
- •Содержание
- •Введение
- •Основы кристаллографии
- •Глава 1. Аморфные и кристаллические вещества
- •Историческая справка о развитии геолого-минералогических наук. Закон Стенона
- •1.3 Аморфные и кристаллические вещества
- •1.4 Основные свойства кристаллов
- •Глава 2. Зарождение и рост кристаллов
- •2.1 Пути образования кристаллов
- •2.2 Выращивание кристаллов из растворов
- •Факторы, влияющие на облик кристаллов
- •Практическое значение кристаллизации растворов в технологии силикатов
- •2.5 Кристаллизация из расплавов и стекол
- •2.6. Промышленные методы выращивания кристаллов
- •Глава 3. Симметрия кристаллов и их классификация
- •3.1 Элементы симметрии
- •Р исунок 3.1 - Центр симметрии
- •3.2 Взаимодействие между элементами симметрии в кристалле
- •3.3 Классификация кристаллов
- •Глава 4. Простые формы и их комбинации в кристаллах различных сингоний
- •4.1 Распределение простых форм по сингониям и категориям
- •Расшифровка комбинированных форм
- •Глава 5. Установка кристаллов. Определение индексов граней
- •5.1 Понятие о кристаллографических символах
- •Установка кристаллов
- •5.3 Закон Гаюи
- •5.4 Практические рекомендации по определению кристаллографических символов
- •Глава 6. Стереографические проекции кристаллов
- •6.1 Принципы стереографического проектирования
- •6.2 Проектирование элементов симметрии кристаллов
- •Глава 7. Изучение пространственной решетки
- •7.1 Решетки Браве
- •7.2 Определение формульной единицы
- •7.3 Координационные числа и координационные многогранники
- •Глава 8. Плотнейшие упаковки
- •8.1 Понятие о кристаллохимическом радиусе
- •8.2 Виды плотнейших упаковок в структурах
- •8.3 Доля заполненных пустот
- •Глава 9. Типы физико-химических связей в кристаллах
- •9.1 Типы кристаллических структур
- •9.2 Металлический тип связи
- •9.3 Ионная или гетерополярная связь
- •9.4 Ковалентная (гомеополярная) или атомная связь
- •9.6 Водородная связь
- •9.7 Явление поляризации в кристаллических телах
- •Глава 10. Полиморфизм, изоморфизм
- •10.1 Определение полиморфизма, его типы
- •10.2 Примеры полиморфных переходов
- •10.3. Полиморфные превращения в системе SiO2
- •10.4 Понятие об изоморфизме
- •10.5 Виды изоморфизма
- •Глава 11. Главнейшие типы кристаллических структур
- •11.1 Способы моделирования кристаллов. Метод координационных полиэдров
- •11.2 Понятие о структурном типе
- •11.3 Примеры основных структурных типов
- •Тема 12. Кремнекислородные структуры
- •12.1 Особенности строения силикатов
- •12.2 Состав силикатов в виде структурных формул
- •12.3 Классификация силикатов по типу кремнекислородных группировок (радикалов, мотивов)
- •12.4 Особенности структур кварца, тридимита, кристобалита
- •Глава 13. Дефекты кристаллической решетки
- •13.1 Классификация дефектов кристаллической решетки
- •13.2 Нульмерные (точечные) дефекты
- •13.3 Линейные дефекты
- •13.4 Свойства дислокации
- •13.5 Влияние дислокации на скорость роста кристаллов
- •Минералогия
- •Глава 14. Минералогия. Свойства минералов
- •14.1 Наука «минералогия» и объекты ее исследования. Написание формул минералов
- •14.2 Морфология минералов
- •14.3 Явление двойникования и эпитаксии в реальных кристаллах
- •14.4 Физико-химические свойства минералов
- •Тема 15. Геологические процессы образования минералов
- •15.1. Классификация минералов и горных пород по генезису
- •15.2.Эндогенные процессы образования минералов и пород
- •15.3 Экзогенные процессы минералообразования
- •15.4 Метаморфические процессы минералообразования
- •Глава 16. Классификация минералов. Особенности различных классов минералов
- •16.1 Классификация минералов по с.Д. Четверикову
- •16.2 Класс самородных элементов
- •16.3 Сульфиды. Сульфаты
- •16.4 Галоидные соединения. Бораты. Фосфаты
- •16.5 Карбонаты. Нитраты
- •16.6 Оксиды и гидроксиды
- •Глава 17. Силикаты
- •Основные сведения о силикатах
- •17.2 Островные силикаты
- •17.3 Цепочечные и ленточные силикаты
- •17.4 Слоистые силикаты
- •17.5 Каркасные силикаты
- •Литература
Факторы, влияющие на облик кристаллов
|
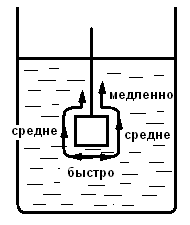
Рисунок 2.4 – Выращивание кристалла |
В связи с выделением тепла при кристаллизации в процессе роста кристалла на затравке, вблизи растущего кристалла повышается температура и таким образом понижается концентрация растворенного вещества, т.е. его концентрация в дворике кристаллизации. Изменение плотности приводит к появлению концентрационных потоков, которые существенно влияют на форму кристаллов. Кристалл сбоку и сверху омывается менее насыщенными струйками концентрационных потоков (рис. 2.4). Поэтому снизу кристалл растет наиболее быстро, сбоку менее интенсивно, а сверху – наиболее медленно. Следовательно, вместо правильных многогранников образуются уплощенные или вытянутые в определенных направлениях. Ослабить действие концентрационных потоков можно путем перемешивания раствора или вращения кристалла.
Другие факторы, влияющие на рост кристаллов:
наличие примесей;
степень пересыщения раствора – чем она больше, тем больше скорость роста кристалла и тем менее совершенный кристалл;
воздействие различных электромагнитных полей;
температура;
наличие соседних кристаллов и т.д.
В ненасыщенных растворах рост кристаллов прекращается, а при дальнейшем понижении концентрации - происходит их растворение, причем в первую очередь растворяются вершины и ребра, кристалл приобретает округлую форму. Если его поместить в раствор его же соли – он воссоздает форму, заложенную в него природой (этот процесс называется регенерацией). На регенерации основаны многие промышленные методы выращивания кристаллов.
Практическое значение кристаллизации растворов в технологии силикатов
Практическое значение кристаллизации растворов в силикатной технологии заключается в следующем:
особенно важно для правильного понимания процесса твердения вяжущих веществ и управления им;
для изготовления особо ответственных керамических материалов (сегнетоэлектрическая, магнитная керамика и др.), оптических стекол; например, вместо традиционного смешивания тонкомолотых компонентов исходной шихты получают смесь растворенных соединений соответствующих компонентов и воздействием на эту смесь специально подобранных реагентов-осадителей получают тонкодиспергированную, хорошо гомогенизированную шихту;
выращивание тугоплавких веществ из растворов гидротермальным синтезом и т.д.
2.5 Кристаллизация из расплавов и стекол
Зародышеобразование – процесс возникновения областей с более дальним порядком расположения атомов, чем это характерно в целом для расплава или стекла.
Различают следующие виды зародышеобразования:
г |
г |
За счет флуктуаций плотности (перераспределения частиц) в отдельных точках расплава происходит сближение атомов и образование группировок с кристаллоподобной структурой (зародыши) |
За счет присутствия в расплаве частиц другой фазы (затравки) |
Процесс кристаллизации зависит от следующих факторов:
Скорость зарождения центров кристаллизации характеризуется числом зародышей, образующихся в единице объема за единицу времени при постоянной температуре.
Линейной скорости роста кристаллов – скорости, с которой перемещается граница между расплавом и закристаллизовавшимся веществом в направлении, перпендикулярном границе.
Практическое значение кристаллизации расплавов и стекол:
это основной процесс в технологии каменного литья, плавленых огнеупоров, цементов;
на нем основана технология получения монокристаллов тугоплавких веществ: корунд (сапфир, рубин), диоксида циркония (фианит);
управляемая (направленная) кристаллизация реализуется в технологии ситаллов (стеклокристаллических материалов).
Производство последних включает – приготовление стекла, которому придают форму и подвергают регулируемой термообработке.
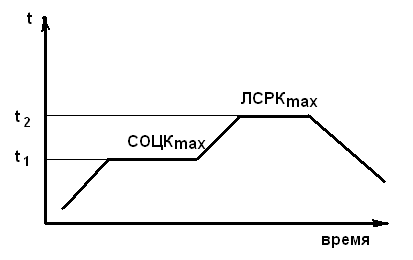
Рисунок 2.5 – Графическое изображение режима термообработки
Режим термообработки включает несколько этапов (рис. 2.5):
1 – повышение температуры до t1 – выдержка; при данной температуре максимальная скорость образования зародышей кристаллизации;
2 - повышение температуры до t2 – выдержка; при данной температуре максимальная линейная скорость роста кристаллов.
В результате - в готовом изделии до 85% кристаллической фазы, остальное – стеклофаза. Таким образом, можно достичь особых свойств, например, высокой термостойкости за счет низкого ТКЛР (температурного коэффициента линейного расширения) выделяемых кристаллов.

 омогенное
омогенное етерогенное
етерогенное