- •Кристаллография и минералогия
- •Для студентов высших учебных заведений
- •Предисловие
- •Содержание
- •Введение
- •Основы кристаллографии
- •Глава 1. Аморфные и кристаллические вещества
- •Историческая справка о развитии геолого-минералогических наук. Закон Стенона
- •1.3 Аморфные и кристаллические вещества
- •1.4 Основные свойства кристаллов
- •Глава 2. Зарождение и рост кристаллов
- •2.1 Пути образования кристаллов
- •2.2 Выращивание кристаллов из растворов
- •Факторы, влияющие на облик кристаллов
- •Практическое значение кристаллизации растворов в технологии силикатов
- •2.5 Кристаллизация из расплавов и стекол
- •2.6. Промышленные методы выращивания кристаллов
- •Глава 3. Симметрия кристаллов и их классификация
- •3.1 Элементы симметрии
- •Р исунок 3.1 - Центр симметрии
- •3.2 Взаимодействие между элементами симметрии в кристалле
- •3.3 Классификация кристаллов
- •Глава 4. Простые формы и их комбинации в кристаллах различных сингоний
- •4.1 Распределение простых форм по сингониям и категориям
- •Расшифровка комбинированных форм
- •Глава 5. Установка кристаллов. Определение индексов граней
- •5.1 Понятие о кристаллографических символах
- •Установка кристаллов
- •5.3 Закон Гаюи
- •5.4 Практические рекомендации по определению кристаллографических символов
- •Глава 6. Стереографические проекции кристаллов
- •6.1 Принципы стереографического проектирования
- •6.2 Проектирование элементов симметрии кристаллов
- •Глава 7. Изучение пространственной решетки
- •7.1 Решетки Браве
- •7.2 Определение формульной единицы
- •7.3 Координационные числа и координационные многогранники
- •Глава 8. Плотнейшие упаковки
- •8.1 Понятие о кристаллохимическом радиусе
- •8.2 Виды плотнейших упаковок в структурах
- •8.3 Доля заполненных пустот
- •Глава 9. Типы физико-химических связей в кристаллах
- •9.1 Типы кристаллических структур
- •9.2 Металлический тип связи
- •9.3 Ионная или гетерополярная связь
- •9.4 Ковалентная (гомеополярная) или атомная связь
- •9.6 Водородная связь
- •9.7 Явление поляризации в кристаллических телах
- •Глава 10. Полиморфизм, изоморфизм
- •10.1 Определение полиморфизма, его типы
- •10.2 Примеры полиморфных переходов
- •10.3. Полиморфные превращения в системе SiO2
- •10.4 Понятие об изоморфизме
- •10.5 Виды изоморфизма
- •Глава 11. Главнейшие типы кристаллических структур
- •11.1 Способы моделирования кристаллов. Метод координационных полиэдров
- •11.2 Понятие о структурном типе
- •11.3 Примеры основных структурных типов
- •Тема 12. Кремнекислородные структуры
- •12.1 Особенности строения силикатов
- •12.2 Состав силикатов в виде структурных формул
- •12.3 Классификация силикатов по типу кремнекислородных группировок (радикалов, мотивов)
- •12.4 Особенности структур кварца, тридимита, кристобалита
- •Глава 13. Дефекты кристаллической решетки
- •13.1 Классификация дефектов кристаллической решетки
- •13.2 Нульмерные (точечные) дефекты
- •13.3 Линейные дефекты
- •13.4 Свойства дислокации
- •13.5 Влияние дислокации на скорость роста кристаллов
- •Минералогия
- •Глава 14. Минералогия. Свойства минералов
- •14.1 Наука «минералогия» и объекты ее исследования. Написание формул минералов
- •14.2 Морфология минералов
- •14.3 Явление двойникования и эпитаксии в реальных кристаллах
- •14.4 Физико-химические свойства минералов
- •Тема 15. Геологические процессы образования минералов
- •15.1. Классификация минералов и горных пород по генезису
- •15.2.Эндогенные процессы образования минералов и пород
- •15.3 Экзогенные процессы минералообразования
- •15.4 Метаморфические процессы минералообразования
- •Глава 16. Классификация минералов. Особенности различных классов минералов
- •16.1 Классификация минералов по с.Д. Четверикову
- •16.2 Класс самородных элементов
- •16.3 Сульфиды. Сульфаты
- •16.4 Галоидные соединения. Бораты. Фосфаты
- •16.5 Карбонаты. Нитраты
- •16.6 Оксиды и гидроксиды
- •Глава 17. Силикаты
- •Основные сведения о силикатах
- •17.2 Островные силикаты
- •17.3 Цепочечные и ленточные силикаты
- •17.4 Слоистые силикаты
- •17.5 Каркасные силикаты
- •Литература
12.2 Состав силикатов в виде структурных формул
Чаще всего состав силикатов выражается в оксидном виде. Такой способ позволяет сразу оценить количественное содержание компонентов в составе силиката, но не выражает структурных особенностей таких веществ.
Поэтому состав силикатов выражается в виде структурных формул, отражающих их внутреннее строение. Структурные формулы пишутся следующим образом:
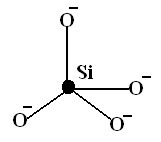
Кремнекислородный мотив, т.е. весь комплекс из тетраэдров [SiO4]4- и все катионы и анионы, непосредственно в него входящие (замещающие в нем кремний или кислород), записываются в квадратных скобках.
Слева от квадратных скобок пишутся катионы, не входящие в кремнекислородный мотив.
Справа от квадратных скобок пишутся анионы, не входящие в кремнекислородный мотив.
Примеры.
Каолинит (минерал глин)
В оксидном виде Al2O3·2SiO2·2H2O
В
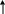
 структурном Al2[Si2O5](oh)4
структурном Al2[Si2O5](oh)4
Катионы, не входящие в мотив Кремнекислородный мотив Анионы, не входящие в мотив
Мусковит (минерал слюд)
В оксидном виде К2О·3Al2O3·6SiO2·2H2O
В структурном К2Al4[Al2Si6O20](oh)4 = КAl2[AlSi3O10](oh)2
В мусковите присутствует смешанный кремнекислородный мотив [AlSi3O10]5-, в котором один катион Si4+ изоморфно замещен на Al3+, остальные катионы алюминия, а также калий и группы (ОН)- находятся вне кремнекислородного мотива.
12.3 Классификация силикатов по типу кремнекислородных группировок (радикалов, мотивов)
По типу кремнекислородного мотива все силикаты делятся на 2 большие группы:
|
1. Силикаты с кремнекислородными мотивами конечных размеров |
2. Силикаты с кремнекислородными мотивами бесконечных размеров |
||
|---|---|---|---|---|
|
- ортосиликаты |
- цепочечные и ленточные |
||
|
- диортосиликаты |
- слоистые |
||
|
- смешанного типа |
- каркасные |
||
|
- кольцевые |
|
||
|
|
|||
|
|
|||
|
Рисунок 12.2 – Кремнекислородный радикал ортосиликата |
1. Ортосиликаты имеют мотив [SiO4]4- :
Форстерит* 2MgO·SiO2 - Mg2[SiO4]
Фаялит* 2FeO·SiO2 - Fe2[SiO4]
Монтичеллит CaO·MgO·SiO2 - CaMg[SiO4]
Циркон ZrO2·SiO2 - Zr[SiO4]
Гранат Al2O3 3CaO·3SiO2 - Al2Ca3[SiO4]3
Оливин (Mg, Fe)2[SiO4]
Двухкальциевый силикат (белит)** 2CaO·SiO2 - Ca2[SiO4]
_______________
*форстерит и фаялит – два крайних члена изоморфного ряда оливина
**белит – один из основных минералов портландцементного клинкера
|
Рисунок 12.3 – Кремнекислородный радикал диортосиликата |
Окерманит 2CaO·MgO·2SiO2 - Ca2Mg[Si2O7]
Силикаты смешанного типа – т.е. с группами [SiO4]4- и [Si2O7]6-:
Везувиан Са10(Mg, Fe)2 Al4[SiO4]5[Si2O7](ОН)4
В структуры силикатов наряду с анионом [SiO4]4-могут входить дополнительные анионы О2-, (ОН)-, F- и т.д.:
Топаз Al2[SiO4](F,OH)2
Дистен (кианит) Al2O3 SiO2 - Al2[SiO4]О
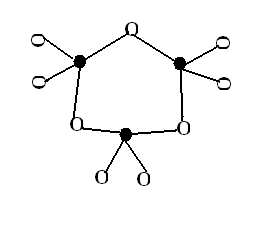
Кольцевые силикаты – структуры, когда несколько тетраэдров соединяются в кольцо (рис.12.4), или более сложные сдвоенные шестичленные кольца [Si12O30]12-
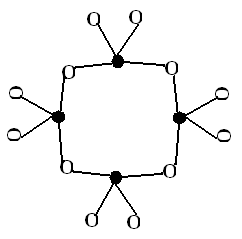
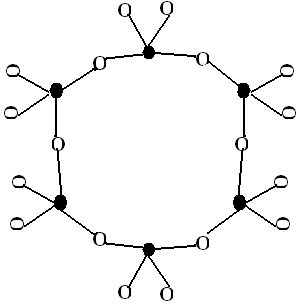
а) б) в)
Рисунок 12.4 – Пример кольцевых радикалов а) [Si3O9]6-, б) [Si4O12]8-, в) [Si6O18]12-
Берилл 3BeO·Al2O3·6SiO2 - Be3Al2[Si6O18] (формула изумруда)
Бенитоит BaO·TiO2·3SiO2 - BaTi[Si3O9]
Кордиерит 2MgO·2Al2O3·5SiO2 - Mg2Al3[AlSi5O18], в природном минерале (Mg,Fe)[AlSi5O18].
2. Цепочечные и ленточные силикаты с бесконечными в одном измерении цепочками или лентами тетраэдров [SiO4]4-соединяются двумя вершинами, при этом у каждого тетраэдра (если это упорядоченный силикат) остаются две свободные валентности, через которые катионы металлов соединяют цепочки в решетку. Ленточные силикаты получаются путем отражения цепочки в плоскости симметрии.
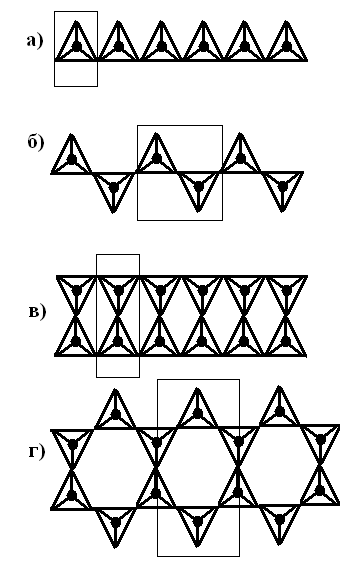
В зависимости от формы цепочек и лент могут быть выделены следующие мотивы:
|
Рисунок 12.5 – Кремнекислородные мотивы ленточных и цепочных силикатов: а) [SiO3]2-, б) [Si2O6]4-, в)[Si2O5]2-, г)[Si4O11]6 |
энстатит MgO·SiO2 - Mg[SiO3]
диопсид CaO·MgO·2SiO2 - CaMg[SiO3]2
волластонит CaO·SiO2 - Ca[SiO3]
авгит Ca(Mg,Fe)[Si2O6]
Cиллиманит Al2O3SiO2 – Al[AlSiO5] (ленточный силикат, пироксеноид).
Амфиболы [Si4O11]6- :
роговая обманка
Са2Na(Mg,Fe)4(Al,Fe)[Al Si3O11]2(ОН)2
Слоистые силикаты – структуры с бесконечными двухмерными слоями из тетраэдров [SiO4]4-, связанными тремя своими вершинами с соседними тетраэдрами (рис. 12.6). С помощью одной свободной валентности, оставшейся у каждого тетраэдра, через катионы металлов слои соединяются между собой.
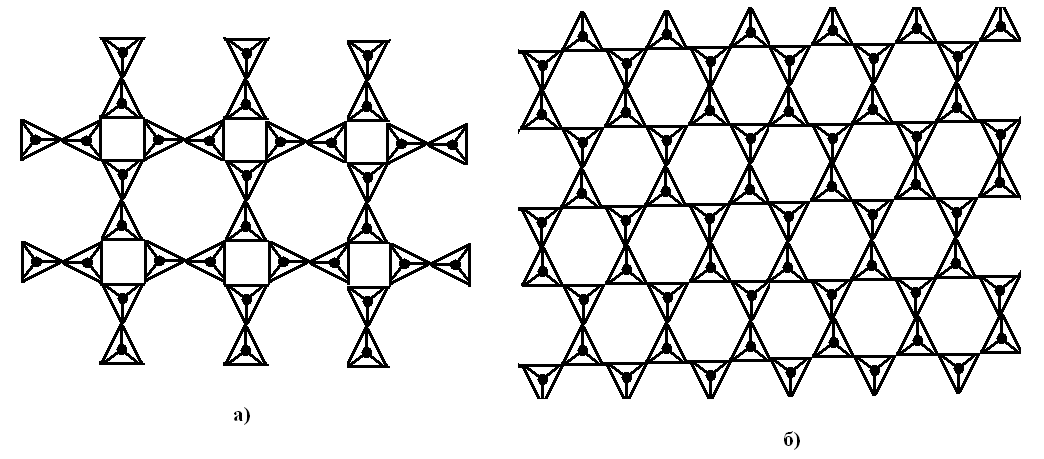
Рисунок 12.6 – Примеры слоистых силикатов: а) [Si2O5]2- ([Si4O10]4- ), б) [Si2O5]2-
Если мотив силиката неоднозначно выявляет его тип (слоистый [Si2O5]2- , ленточный [Si2O5]2-) нужно обратить внимание на форму кристаллов такого силиката: если форма кристалла плоская (чешуйки, пластиночки), то это слоистый силикат; если – удлиненная (иголочки), то это цепочечный или ленточный силикат.
Примеры слоистых минералов.
Каолинит Al2O3×2SiO2×2H2O - Al2[Si2O5](OH)4 , имеет пакетное строение. Каждый пакет состоит из двух слоев – из тетраэдрического слоя [SiO4]4- и октаэдрического слоя [Al(O,OH)6]9-. Между пакетами относительно сильная водородная связь, так как один пакет заканчивается атомами кислорода, а другой пакет начинается группами ОН-.
[SiO4]4- [Al(O,OH)6]9- [SiO4]4- [Al(O,OH)6]9-


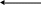 2
пакет водородная
связь
1 пакет
2
пакет водородная
связь
1 пакет
Поэтому каолинит обладает относительно низкой набухаемостью и невысокой пластичностью.
Каолинит – это название минерала. Он входит в состав многих глин, в том числе в сырьевой материал, который практически полностью состоит из каолинита, который называется каолином.
Монтмориллонит (Al2O34SiO2H2OnH2O - Al2[Si4O10](OH)2nH2O) имеет пакетное строение и каждый пакет состоит из 3 слоев:
[SiO4]4- [Al(O,OH)6]9- [SiO4]4-
Тетраэдрический слой |
Октаэдрический слой |
Тетраэдрический слой |
Ван-дер-Ваальсовская связь |
пакет пакет
Ввиду слабой Ван-дер-Ваальсовской связи между пакетами набирается большое количество воды, которая называется межпакетной (nH2O), что обусловливает высокую набухаемость и высокую пластичность минерала.
Монтмориллонит входит в состав бентонитовых глин, которые обладают высокой пластичностью и применяются для изготовления изделий сложной формы.
Примеры других минералов, имеющих слоистое строение.
Тальк MgO4SiO2H2O – Mg3[Si2O5]2(oh)2
Пирофиллит Al2O34SiO2H2O - Al2[Si4O10](OH)2
Каркасные силикаты – структуры с трехмерными непрерывными радикалами из кремнекислородных тетраэдров (рис.12.7).

Рисунок 12.7. - Кремнекислородные радикалы в трех измерениях
Все четыре аниона кислорода у каждого тетраэдра являются общими с анионами кислорода четырех соседних тетраэдров. При этом свободных валентностей не остается, то есть такой каркас является валентно насыщенным. Состав радикала [SiO2]0.
К таким структурам относятся все полиморфные модификации кремнезема SiO2.
Все каркасные структуры не подчиняются правилу плотнейшей упаковки и являются ажурными, рыхлыми, с крупными пустотами. Если в таком валентно насыщенном каркасе часть катионов кремния замещена на катионы Al3+, то такой каркас заряжается отрицательно. Для ликвидации заряженности каркаса в него внедряются катионы щелочных и щелочноземельных металлов. Таким образом получаются каркасные алюмосиликаты:
- полевые шпаты (альбит, анортит, ортоклаз, цельзиан)
- нефелин
- цеолиты (натролит).
Схемы образования алюмосиликатов:
[SiO2]0=4[SiO2]0=[Si4O8]0-1/4Si4++1/4Al3+ [AlSi3O8]-
K[AlSi3O8] ортоклаз
Na[AlSi3O8] альбит
[SiO2]0=4[SiO2]0=[Si4O8]0-1/2Si4++1/2Al3+ [Al2Si2O8]2-
Ca[Al2Si2O8] анортит
Ba[Al2Si2O8] цельзиан
2[SiO2]0=[Si2O4]0-1/2Si4++1/2Al3+ [AlSiO4]-
Na[AlSiO4] нефелин
5[SiO2]0=[Si5O10]0-2/5Si4++2/5Al3+ [Al2Si3O10]2-
Na2[Al2Si3O10] натролит
Цеолиты представляют собой каркасные алюмосиликаты, в структуре которых содержатся сквозные каналы, которые выходят на поверхность минерала. В этих каналах присутствует вода. Если из него осторожным нагреванием удалить воду, то такое вещество способно адсорбировать любые вещества (поэтому цеолиты используют как очистители воды, жиров, масел).