- •Кристаллография и минералогия
- •Для студентов высших учебных заведений
- •Предисловие
- •Содержание
- •Введение
- •Основы кристаллографии
- •Глава 1. Аморфные и кристаллические вещества
- •Историческая справка о развитии геолого-минералогических наук. Закон Стенона
- •1.3 Аморфные и кристаллические вещества
- •1.4 Основные свойства кристаллов
- •Глава 2. Зарождение и рост кристаллов
- •2.1 Пути образования кристаллов
- •2.2 Выращивание кристаллов из растворов
- •Факторы, влияющие на облик кристаллов
- •Практическое значение кристаллизации растворов в технологии силикатов
- •2.5 Кристаллизация из расплавов и стекол
- •2.6. Промышленные методы выращивания кристаллов
- •Глава 3. Симметрия кристаллов и их классификация
- •3.1 Элементы симметрии
- •Р исунок 3.1 - Центр симметрии
- •3.2 Взаимодействие между элементами симметрии в кристалле
- •3.3 Классификация кристаллов
- •Глава 4. Простые формы и их комбинации в кристаллах различных сингоний
- •4.1 Распределение простых форм по сингониям и категориям
- •Расшифровка комбинированных форм
- •Глава 5. Установка кристаллов. Определение индексов граней
- •5.1 Понятие о кристаллографических символах
- •Установка кристаллов
- •5.3 Закон Гаюи
- •5.4 Практические рекомендации по определению кристаллографических символов
- •Глава 6. Стереографические проекции кристаллов
- •6.1 Принципы стереографического проектирования
- •6.2 Проектирование элементов симметрии кристаллов
- •Глава 7. Изучение пространственной решетки
- •7.1 Решетки Браве
- •7.2 Определение формульной единицы
- •7.3 Координационные числа и координационные многогранники
- •Глава 8. Плотнейшие упаковки
- •8.1 Понятие о кристаллохимическом радиусе
- •8.2 Виды плотнейших упаковок в структурах
- •8.3 Доля заполненных пустот
- •Глава 9. Типы физико-химических связей в кристаллах
- •9.1 Типы кристаллических структур
- •9.2 Металлический тип связи
- •9.3 Ионная или гетерополярная связь
- •9.4 Ковалентная (гомеополярная) или атомная связь
- •9.6 Водородная связь
- •9.7 Явление поляризации в кристаллических телах
- •Глава 10. Полиморфизм, изоморфизм
- •10.1 Определение полиморфизма, его типы
- •10.2 Примеры полиморфных переходов
- •10.3. Полиморфные превращения в системе SiO2
- •10.4 Понятие об изоморфизме
- •10.5 Виды изоморфизма
- •Глава 11. Главнейшие типы кристаллических структур
- •11.1 Способы моделирования кристаллов. Метод координационных полиэдров
- •11.2 Понятие о структурном типе
- •11.3 Примеры основных структурных типов
- •Тема 12. Кремнекислородные структуры
- •12.1 Особенности строения силикатов
- •12.2 Состав силикатов в виде структурных формул
- •12.3 Классификация силикатов по типу кремнекислородных группировок (радикалов, мотивов)
- •12.4 Особенности структур кварца, тридимита, кристобалита
- •Глава 13. Дефекты кристаллической решетки
- •13.1 Классификация дефектов кристаллической решетки
- •13.2 Нульмерные (точечные) дефекты
- •13.3 Линейные дефекты
- •13.4 Свойства дислокации
- •13.5 Влияние дислокации на скорость роста кристаллов
- •Минералогия
- •Глава 14. Минералогия. Свойства минералов
- •14.1 Наука «минералогия» и объекты ее исследования. Написание формул минералов
- •14.2 Морфология минералов
- •14.3 Явление двойникования и эпитаксии в реальных кристаллах
- •14.4 Физико-химические свойства минералов
- •Тема 15. Геологические процессы образования минералов
- •15.1. Классификация минералов и горных пород по генезису
- •15.2.Эндогенные процессы образования минералов и пород
- •15.3 Экзогенные процессы минералообразования
- •15.4 Метаморфические процессы минералообразования
- •Глава 16. Классификация минералов. Особенности различных классов минералов
- •16.1 Классификация минералов по с.Д. Четверикову
- •16.2 Класс самородных элементов
- •16.3 Сульфиды. Сульфаты
- •16.4 Галоидные соединения. Бораты. Фосфаты
- •16.5 Карбонаты. Нитраты
- •16.6 Оксиды и гидроксиды
- •Глава 17. Силикаты
- •Основные сведения о силикатах
- •17.2 Островные силикаты
- •17.3 Цепочечные и ленточные силикаты
- •17.4 Слоистые силикаты
- •17.5 Каркасные силикаты
- •Литература
Глава 2. Зарождение и рост кристаллов
2.1 Пути образования кристаллов
Кристаллы возникают при переходе вещества из одного физического состояния в другое:
г |
ж |
т |
||
т |
т |
т |
||
Образование кристаллов в результате сублимации. В природе – образование кристаллов серы, борной кислоты в кратерах вулканов при охлаждении газов |
Образование кристаллов из расплава. В природе – кристаллизация магмы |
Образование кристаллов из раствора. В природе – выпадение солей из озер (с. Солотвино) |
Аморфное стекло в процессе эксплуатации раскристалли-зовывается |
Перекристаллизация под влиянием давления, температуры и др. факторов. Пример – преобразование «известняк→мрамор» |
Кристаллическое вещество может образовываться путем фазового перехода из любого малоупорядоченного состояния (паров, растворов, расплавов, аморфного) путем построения правильной кристаллической решетки или ее перестройки (перекристаллизации). Переход в кристаллическое состояние - качественный скачок, который происходит при определенной температуре.
Процесс кристаллизации всегда происходит в 2 этапа:
1 – возникновение субмикроскопического зародыша кристаллической фазы
2 – дальнейший рост этого зародыша.
Условия для возникновения зародыша – пересыщение раствора или переохлаждение расплава.
2.2 Выращивание кристаллов из растворов
В зависимости от количества растворенного вещества различают следующие виды растворов: ненасыщенный, насыщенный, пересыщенный.
Условие выделения кристаллов из растворов – наличие пересыщения.
П = С - Со,
Где П – пересыщение,
Со – растворимость данного вещества при определенной температуре,
С – концентрация содержащегося в растворе вещества.
Пересыщенный раствор – неустойчив, содержит избыток растворенного вещества, который с течением времени выделяется в виде кристаллического осадка. В зависимости от степени пересыщения, выделение твердой фазы из раствора может произойти при введении соответствующих затравок, за счет испарения или охлаждения раствора.
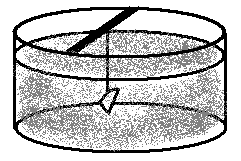
|
Рисунок 2.1 – Выращивание кристалла |
Рост кристаллов происходит за счет новых слоев вещества, откладывающихся так, что грани как бы передвигаются параллельно самим себе от центра кристаллизации (рис. 2.2).
Скорость роста грани – величина нормали, на которую переместилась данная грань за единицу времени.
|
AB, BC, CD – грани кристалла pg, mn, hk – скорости роста граней кристалла |
Рисунок 2.2 – Схема роста граней кристалла
Анизотропия свойств кристаллов проявляется в разных скоростях роста. Например, грани с наибольшей ретикулярной плотностью (т.е. плотностью расположения частиц на плоской сетке решетки) растут с наименьшей скоростью. Поэтому грань ВС со временем исчезает, т.к. скорость ее роста меньше скорости роста граней AB и CD.
В соответствии с теорией роста, образование нового слоя начинается только после завершения формирования последующего. Так создается идеальный кристалл – выпуклый многогранник с плоскими гранями.
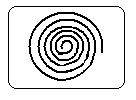
|
Рисунок 2.3 – Спирали на кристаллах |
Однако грани реальных кристаллов нередко отличаются наличием бугорков, впадин, штриховок – это так называемая скульптура грани. Более того, впервые на кристаллах корунда, а затем и на гематите, кварце, сфалерите были обнаружены на поверхности кристалла тончайшие спирали (рис. 2.3). Оказалось, что именно по этим винтовым лестницам, которые являются проявлением линейных дефектов кристаллических решеток (называемыми дислокациями), и растут кристаллы.
По расчетам, для роста кристаллов из раствора требуется пересыщение в 30-50%; на самом же деле, благодаря дислокациям, кристаллы растут при минимальных пересыщениях.

 азообразное
азообразное идкое
идкое вердое
вердое вердое
вердое
 вердое
вердое
 вердое
вердое