
- •Кафедра химической технологии переработки
- •Органическая химия
- •Москва, 2007
- •Введение
- •1. Основные теоретические положения органической химии
- •1.1. Классификация органических соединений
- •Органические соединения
- •Важнейшие классы органических соединений.
- •Названия наиболее часто встречающихся радикалов:
- •1.2. Номенклатура
- •1.3. Электронное строение σ- и π- связей Три типа гибридизации атомов углерода
- •1.5 Типы органических реакций
- •1.6. Механизмы химических реакций
- •Рост стабильности радикалов
- •Стабильность третичного иона карбония выше, т.К. Частичный положительный заряд на атоме углерода нейтрализуется индукционным эффектом наибольшего числа радикалов.
- •2. Алканы
- •Химические свойства
- •Алкены Общая характеристика
- •Химические свойства
- •Реакции присоединения (а)
- •4. Диеновые углеводороды (алкадиены или диолефины)
- •Химические свойства дивинила и его гомологов Реакции присоединения
- •Диеновые синтезы (синтезы Дильса-Альдера)
- •Реакции полимеризации
- •5. Алкины (непредельные углеводороды ряда ацетилена )
- •Реакции присоединения
- •Реакции окисления
- •Реакции замещения
- •6. Алициклические соединения
- •6.1 Химические свойства
- •6.2. «Теория напряжения» Байера
- •6.3. Пространственное расположение атомов углерода в циклопарафинах.
- •Оптическая изомерия
- •7. Ароматический ряд. Арены
- •7.1. Строение бензола
- •7. 2. Критерии ароматичности. Определение принадлежности вещества к ароматическим соединениям
- •7.3. Химические свойства бензола
- •Реакции электрофильного замещения se
- •Механизм реакции электрофильного замещения
- •Влияние заместителей I-п рода на реакционную способность кольца и ориентацию при реакциях электрофильного замещения (sе)
- •Заместители I рода орто- и пара-ориентанты
- •Заместители п рода -мета ориентанты
- •8. Галогенопроизводные углеводородов
- •Галогенопроизводные предельных углеводородов (галогеналкилы)
- •Химические свойства
- •Галогенопроизводные непредельных углеводородов
- •Ароматические галогенопроизводные
- •Влияние заместителей в кольце на реакционную способность галогена
- •9. Кислородсодержащие соединения
- •9.1. Спирты Спирты алифатического ряда.
- •Реакции гидроксильного водорода.
- •Реакции гидроксила
- •Окисление
- •Одноатомные непредельные спирты
- •Химические свойства
- •Взаимодействие со щелочами
- •Реакции электрофильного замещения se
- •Влияние заместителей на кислотные свойства фенолов
- •Ароматические спирты
- •9.2 Альдегиды и кетоны
- •Альдегиды и кетоны алифатического ряда Общая характеристика
- •Влияние акцепторных групп
- •Окисление альдегидов и кетонов
- •Реакции конденсации (уплотнения)
- •Механизм реакции
- •Непредельные альдегиды и кетоны
- •Основные химические реакции
- •Ароматические альдегиды и кетоны
- •9.3 Карбоновые кислоты Карбоновые кислоты алифатического ряда Общая характеристика
- •Основные химические реакции
- •Непредельные карбоновые кислоты.
- •Свойства кислот
- •Двухосновные или дикарбоновые кислоты (предельные и непредельные).
- •Ароматические карбоновые кислоты
- •Кислотные свойства
- •Реакция этерификации
- •10. Нитросоединения Нитросоединения алифатического ряда r - nо2
- •Нитросоединения с нитрогруппой в боковой цепи
- •11. Аминосоединеиия
- •Ароматические амины Общая характеристика
- •Влиянение заместителей на основные свойства аминов Акцепторный заместитель уменьшает основность
- •Реакции электрофильного замещения (sе)
- •12. Диазосоединения
- •Реакция диазотирования
- •Реакции солей диазония без выделения азота
- •Реакция сочетания с фенолом и ароматическими аминами
- •Влияние заместителей на реакцию азосочетания
- •13. Азосоединения
- •14. Вопросы для подготовки к зачету
- •Тема 1. Электрофильное и радикальное присоединение и замещение у алкенов. Элиминирование.
- •Тема 2. Нуклеофильные и радикальные (галогенирование, нитрование) реакции у насыщенного атома углерода
- •Тема 3. Окислительно-восстановительный процесс и дегидрирование
- •Тема 4. Электрофильное замещение в ароматических соединениях. Правила ориентации
- •Тема. 5. Нуклеофильное замещение у ароматических соединений. Кислотно-основные свойства органических соединений
- •Тема 6. Полимеризация, конденсация, поликонденсация. Диазосоединения и синтезы на их основе
- •15. Список рекомендуемой литературы Основной
- •Дополнительный
Тема 2. Нуклеофильные и радикальные (галогенирование, нитрование) реакции у насыщенного атома углерода
1. Как
влияют электронные эффекты (индукционный
и мезомерный) на прочность связи
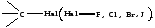
2. Сравните реакционную способность галогена в хлористом натрии, С2Н5Вг, СН2 = СНС1; СН2 = СН—СН2С1 и С6Н5Вг. Объясните на этих примерах причины изменения реакционной способности галогенов.
3. Механизм нуклеофильного замещения у первичных, вторичных и третичных галогенопроизводных предельных углеводородов.
4. Понятие о химической устойчивости радикалов (первичных, вторичных и третичных). Приведите примеры.
5. Какое из соединений, реагируя с аммиаком, имеет механизм реакции замещения Sn 1:

6. Какое из соединений, реагируя с КОН, имеет механизм замещения SN 2:

7. Укажите, какое из соединений: 2-хлорбутан; 3-бромпентан;
2-бром -2-метилпропан или хлористый аллил в реакции щелочного гидролиза имеет механизм нуклеофильного замещения Sn 1?
8. Из первичного пропилового спирта получите 1-бромпропан и
2-бромпропан.
9. Укажите место разрыва связей при реакции этерификации (за счет какого гидроксила — кислоты или спирта — происходит образование воды?). Как проводилось исследование с помощью меченых атомов?
10. Напишите реакции альдольного и кротонового уплотнения: а) пропаналя; б) масляного альдегида; в) диметилуксусного альдегида. Вступает ли в реакцию со щелочью триметилуксусный альдегид? Объясните течение этих реакций (механизм).
11. Что называют органической кислотой и органическим основанием?
12. Какая реакция называется «защитой» аминогруппы? Ее применение в органическом синтезе.
13. Из анилина получите метиланилин и диметиланилин. Расположите аминосоединения в порядке возрастания основных свойств.
14. Напишите реакции: а) анилина с ангидридом бензойной кислоты; б) метиланилина с хлористым ацетилом. Как называются реакции этого типа? К какому классу соединений относятся образующиеся вещества? Назовите их.
15. Осуществите следующие превращения:

Тема 3. Окислительно-восстановительный процесс и дегидрирование
1. Как относятся к действию окислителей альдегиды и кетоны? Приведите соответствующие реакции на примере:
а) уксусный альдегид и метилэтилкетон;
б) пропаналь и диэтилкетон.
2. Сопоставьте со спиртами реакционную способность кислот.
3. Рассмотрите получение уксусной кислоты из этанола как предельный случай окисления С –Н связи.
4. Напишите реакцию окисления толуола раствором КМпО4.
5. Отношение бензола к окислителям.
6. Напишите уравнения реакций окисления этилбензола раствором КМпо4 и Н2 SO4.
7. Какие продукты окисления толуола можно получить в зависимости от условий реакции?
8. Напишите уравнение реакции получения анилина из нитробензола. Для чего добавляют NaOH в реакционную смесь перед перегонкой?
Тема 4. Электрофильное замещение в ароматических соединениях. Правила ориентации
1. Механизм реакции электрофильного замещения в ароматических соединениях (p- и s-комплексы). Разберите на примере нитрования ароматических углеводородов (бензола, толуола).
2. В каких условиях нитрование: а) толуола; б) пропилбензола идет в ароматическое кольцо и в боковую цепь? Напишите уравнения реакций.
3. Объясните влияние функциональной группы хлора в реакции нитрования хлорбензола.
4. Напишите уравнение нитрования бензойной кислоты и объясните влияние функциональной группы на процесс нитрования.
5. Напишите уравнения реакций получения о-, п- и м-нитробензойных кислот из бензола, учитывая правила ориентации.
6. Напишите реакции нитрования хлорбензола и бензойной кислоты. Объясните, какое из этих соединений будет легче вступать в реакцию нитрования и почему.
7. Напишите реакции нитрования бензолсульфокислоты и фенола. Объясните, какое из этих соединений будет легче вступать в реакцию и почему.
8. Напишите реакции нитрования фенола. Объясните влияние функциональной группы — ОН на легкость протекания реакции нитрования (в сравнении с бензолом).
9. Напишите реакции нитрования фенола до пикриновой кислоты. Почему пикриновая кислота является одной из самых сильных кислот?
10. Напишите реакцию фенола с бромом. Объясните различное поведение фенола и нитробензола в этой реакции.
11. Как, пользуясь правилом ориентации в ароматическом ряду, получить из бензола: а) орто-нитрохлорбензол; б) мета-нитрохлорбензол?
12. Как относятся бензол и анилин к действию избытка брома? Чем объясняется легкость галогенирования анилина?
13. Напишите уравнения реакций последовательного превращения бензола в: а) орто-хлоранилин; б) мета-хлоранилин.
14. На примере взаимодействия фенола с HN03 объясните влияние группы — ОН на способность атомов водорода в бензольном кольце к реакциям электрофильного замещения.
