
- •В ведение
- •Глава 1 гели для электрофореза полиакриламидныи гель (пааг) Исходные материалы
- •Процесс полимеризации пааг
- •Выбор концентраций мономеров
- •Агароза
- •Ацетатцеллюлозная пленка, импрегнированная пааг
- •Глава 2 техника приготовления гелей и аппаратура
- •Вертикально расположенные трубки
- •Вертикально расположенные пластины
- •Горизонтально расположенные пластины
- •Глава 3 электрофорез белков
- •Замечания общего характера Миграция белков в геле
- •Напряженность электрического поля (н)
- •Выбор буфера рабочего геля
- •Выделение тепла при электрофорезе
- •Загрузка геля. Ширина белковых зон
- •Введение мочевины и -меркаптоэтанола. Некоторые артефакты
- •Лидирующие красители
- •Разделение белков по размерам и заряду
- •Выбор рабочего буфера
- •Использование мочевины
- •Загрузка геля и подготовка препарата
- •Некоторые примеры
- •Фракционирование гистонов и других щелочных белков.
- •Разделение белков по размеру с использованием ддс-Na Существо метода
- •Выбор пористости геля
- •Присутствие мочевины и неионных детергентов
- •Выбор рабочего буфера геля
- •Подготовка белкового препарата
- •Проведение электрофореза
- •Окрашивание и элюция белков
- •Ступенчатый электрофорез (disc-electrophoresis)
- •Градиент пористости пааг
- •Двумерный электрофорез в пааг
- •Электрофорез с использованием тритона х-100 и цетавлона Тритон х-100
- •Цетавлон
- •Окрашивание белков в пааг
- •Кислые красители
- •Другие красители и методы окрашивания
- •Флюоресцентные красители
- •Локализация ферментов после электрофореза
- •Локализация белковых полос осаждением ддс-Na
- •Элюция белков из геля
- •Определение радиоактивности белков после электрофореза в пааг
- •Счет радиоактивности в элюатах белка
- •Растворение пааг
- •Импрегнирование сцинтиллятора в гель
- •Авторадиография
- •Флюорография
- •Препаративныи электрофорез белков
- •Оглавление
- •Глава 1
- •Глава 2
- •Глава 3
- •Глава 4
- •Глава 1 . Основные понятия теории седиментации ............ 175
- •Глава 2 Ультрацентрифуга ..................... 177
- •Глава 3 Роторы и пробирки .................... 182
- •Глава 4 Раздельное осаждение частиц (дифференциальное центрифугирование) 199
- •Глава 5
Окрашивание белков в пааг
Обнаружение и локализацию белковых зон после их разде- ления электрофорезом в ПААГ в большинстве случаев осуще- ствляют путем их прокраски в геле. Зоны проявляются как ок- рашенные полоски или пятна различной интенсивности, в зависимости от содержания в них белка. Для окраски гель вы- мачивают в растворе красителя, который диффундирует внутрь него и прочно связывается с белками. Процесс диффузии, как правило, занимает несколько часов. Во избежание размывания полос за это время белки иногда предварительно фиксируют осаждением. Для этого гель сначала вымачивают в 10%- или 50%-ной трихлоруксусной кислоте (ТХУ). Чаще фиксацию сов- мещают с окрашиванием, используя раствор красителя в .смеси уксусной кислоты и метанола или в ТХУ.
Одновременно с белками окрашенным оказывается и сам гель. Это происходит как за счет простого замещения буфера ге- ля на раствор красителя, так и в результате некоторой сорбции его на геле. Однако связывание красителя с гелем значительно менее прочно, чем с белками, поэтому от «фона» удается без особого труда избавиться «отмывкой» геля, например вымачи- ванием его в относительно большом объеме растворителя с не-
88
сколькими сменами. Если отмывка идет только за счет диффу- зии красителя из геля, она занимает несколько часов, обычно ее ведут в течение ночи. Во избежание растворения осажденных белков краситель отмывают тоже уксусной кислотой, часто .в смеси с метанолом, который улучшает растворимость красите- ля. Отмывка ускоряется при повышенной температуре (37— 50°) и перемешивании растворителя, однако при этом есть опас- ность ослабления окраски полос.
Все типы обычно используемых красителей для белков несут на себе электрический заряд того или иного знака, поэтому от-
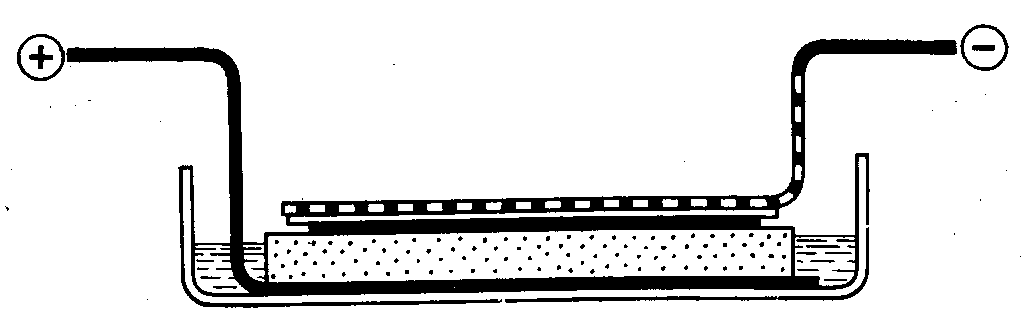
Рис. 28. Устройство для электрофоретической отмывки гелей [Shortess, 1974]
мывку геля можно еще ускорить, если в растворителе суспенди- ровать немного ионообменной смолы, связывающей краситель и тем самым сдвигающей равновесие диффузии. Часто исполь- зуют для этой цели смолу смешанного типа AG 501х8.
Наконец, процесс отмывки можно сократить до десятков ми- нут, если воспользоваться электрофорезом. Электрическое поле накладывают на гель в поперечном направлении — перпенди- кулярно оси трубки или поверхности пластины. Не связанные с белками молекулы красителя благодаря своему заряду быстро выходят из геля. Разумеется, для этой цели нужно иметь специ- альный, хотя и очень простой, прибор для поперечного электро- фореза. Такие приборы («дестейнеры») имеются в продаже, но их легко изготовить и в лаборатории.
Простое устройство для этой цели описано и схематически изображено на рис. 28 [Shortess, 1974]. На пластинку из нержа- веющей стали с отогнутым концом кладут кусок поролона, смо- ченного 10%-ным раствором уксусной кислоты. Его помещают в ванночку и заливают таким же раствором до уровня чуть ниже верхней поверхности поролона. Ряд трубок или пластину геля кладут на поролон, накрывают фильтровальной бумагой, смочен- ной уксусной кислотой, и прижимают перфорированной алюми- ниевой пластинкой или сеткой, также с отогнутым концом. К отогнутым концам обеих пластинок присоединяют провода от источника тока; стальная пластинка служит анодом. Перфора- ции в катодной пластинке нужны для выхода пузырей газа. Че- рез пластину геля размером 12х7х0,3 см нужно пропускать ток силой 0,6 А. Отмывка занимает 15—20 мин. Находящиеся в
89
осадке белки и прочно связанный с ними краситель при непро- должительном поперечном электрофорезе остаются на своих ме- стах в геле.
До сих пор речь шла о неспецифической окраске белков. Если в ходе электрофореза ферменты не утрачивают своей биологи- ческой активности, то их локализацию в геле можно осуществить с помощью специфической ферментативной реакции или цепи реакций, дающих окрашенные продукты. В этом случае гель вы- мачивают в растворе соответствующих субстратов. Разумеется, фиксировать белки осаждением в этом случае нельзя и прихо- дится мириться с некоторым размыванием белковых полос. Впрочем, низкомолекулярные субстраты зачастую диффунди- руют в гель быстрее, чем довольно крупные молекулы красите- лей, и продолжительность вымачивания бывает можно сократить.
Иногда возникает необходимость вести наблюдение за миг- рацией белковых зон в ходе электрофореза. Для этого исходную смесь белков можно окрасить красителем «Remazol» [Griffith, 1972], который ковалентно связывается с белком и мигрирует вместе с ним. Реакцию между белком и красителем проводят в присутствии ДДС-Na, в щелочной среде. Например, к 2 мг бел- ка, растворенного в 0,2 мл 0,15 М NaCI с 0,2 М NazHPt^ и 10% ДДС-Na, добавляют краситель до концентрации 0,16% и прогре- вают при 56° в течение 20 мин. Для очистки от свободного кра- сителя белок переосаждают ацетоном.
Чувствительность окрашивания белков многократно увеличи- вается при использовании перечисленных ниже флюоресцентных красителей. Многие из них связываются с белками или пептида- ми, в основном по концевым аминогруппам. Их также можно использовать для наблюдения за ходом электрофореза после предварительной обработки исходного препарата.
Рассмотрим теперь подробнее наиболее распространенные марки красителей и особенности их применения.
