- •Кафедра физики физика
- •1. Информация о дисциплине
- •1.1. Предисловие
- •Содержание дисциплины «Физика» и виды учебной работы
- •1.2.1. Содержание дисциплины «Физика» по гос
- •1.2.2. Объем дисциплины и виды учебной работы по курсу физики
- •Раздел 1. Физические основы механики (19 час.)
- •1.1. Элементы кинематики материальной точки и вращательного движения твердого тела
- •1.3. Элементы динамики вращательного движения твердого тела
- •1.4. Элементы механики жидкости и газа
- •Раздел 2. Молекулярная (статистическая) физика и термодинамика (15,5 час)
- •2.1. Кинетические явления и теория идеальных газов
- •3.6. Электромагнитная индукция
- •3.7. Уравнения Максвелла
- •Раздел 4. Физика колебаний и волн (15,5 час.)
- •4.3. Волновые процессы
- •Раздел 5. Волновая и квантовая оптика (15,5 час)
- •5.1. Волновые свойства света.
- •5.2. Квантовая теория излучения
- •Раздел 6. Квантовая физика (15,5 час.)
- •2.2.2. Тематический план для заочной формы обучения
- •2.2.3. Тематический план для заочно-ускоренной формы обучения
- •2.3. Структурно-логическая схема дисциплины
- •2.4. Временной график изучения курса физики
- •2.5. Практический блок
- •2.5.1. Практические занятия
- •2.5.1.1. Практические занятия для очно-заочной формы обучения
- •2.5.2. Лабораторные работы
- •2.5.2.1. Лабораторные работы для очно-заочной, заочной и заочной ускоренной форм обучения
- •Информационные ресурсы дисциплины
- •Библиографический список
- •3.2. Опорный конпект по дисциплине “физика”
- •Раздел 1. Физические основы механики (19 час.)
- •. Элементы кинематики материальной точки и вращательного движения твёрдого тела
- •1.1.1. Скорость.
- •Ускорение
- •1.1.3. Кинематика вращательного движения
- •1.2. Динамика материальной точки и системы материальных точек
- •1.2.1.Законы Ньютона
- •1.2.2. Силы в природе и технике
- •1.2.3. Закон сохранения импульса
- •1.2.4. Работа силы. Мощность
- •Мощность
- •1.2.5. Механическая энергия
- •1.2.6. Закон сохранения механической энергии
- •1.3. Элементы динамики вращательного движения твердого тела
- •1.3.1. Момент силы
- •1.3.2. Момент импульса
- •1.3.3. Основное уравнение динамики вращательного движения
- •1.3.4. Момент инерции
- •1.3.5. Закон сохранения момента импульса
- •1.3.6. Работа и кинетическая энергия при вращательном движении
- •1.4. Элементы механики жидкости и газа
- •1.5. Элементы релятивистской физики
- •Раздел 2. Молекулярная (статистическая) физика и термодинамика (15,5 час)
- •2.1. Кинетические явления и теория идеальных газов
- •2.1.1. Уравнение состояния идеального газа. Изопроцессы.
- •2.1.2. Основное уравнение молекулярно-кинетической теории
- •2.2. Основы классической статистической физики
- •2.3. Явления переноса неравновесных состояниях
- •2.4. Основы термодинамики
- •2.4.1. Внутренняя энергия
- •2.4.2. Работа
- •2.4.3. Теплота. Теплоёмкость газов
- •2.4.4. Первое начало термодинамики
- •Адиабатный процесс
- •2.4.5. Второе начало термодинамики
- •2.4.6. Тепловые машины
- •2.5. Реальные газы и жидкости
- •Раздел 3. Электричество и магнетизм (19 час.)
- •3.1. Электрическое поле в вакууме
- •3.1.1. Напряжённость электростатического поля.
- •3.1.2. Потенциал электростатического поля
- •3.1.3. Теорема Гаусса и её применение для расчёта электростатических полей
- •3.2. Электрическое поле в диэлектриках
- •3.3. Проводники в электростатическом поле
- •Энергия электростатического поля
- •3.4. Стационарные токи
- •3.4.1. Электрический ток и его характеристики
- •3.4.2. Закон Ома для однородного участка цепи
- •3.4.3. Электродвижущая сила источника тока. Закон Ома для неоднородного участка цепи
- •3.4.4. Работа и мощность тока. Закон Джоуля-Ленца
- •3. 5. Магнитное поле в вакууме и в веществе
- •3.5.1. Вектор магнитной индукции.
- •3.5.2. Магнитное поле постоянного тока
- •3.5.3. Частицы и токи в магнитном поле. Частицы в магнитном поле. Сила Лоренца
- •Поток вектора магнитной индукции
- •3.6. Электромагнитная индукция
- •3.6.1. Явление и основной закон электромагнитной индукции
- •3.6.2. Энергия магнитного поля
- •3.7. Уравнения Максвелла
- •Раздел 4. Физика колебаний и волн (15,5 час)
- •4.1. Механические колебания
- •4.1.1. Гармонические колебания
- •4.1.2. Сложение колебаний
- •Сложение колебаний одного направления
- •Сложение взаимно перпендикулярных колебаний
- •4.2. Электромагнитные колебания и переменный ток
- •4.2.1. Свободные электромагнитные колебания
- •4.3. Волновые процессы
- •4.3.1. Упругие волны
- •4.3.2. Электромагнитные волны
- •Раздел 5. Волновая и квантовая оптика
- •5.1. Волновые свойства света
- •5.1.1. Понятие об интерференции. Когерентность волн
- •5.1.2. Условия интерференционных максимумов и минимумов
- •5.1.3. Интерференция при отражении от тонких пластинок
- •5.1.4. Дифракция света
- •Дифракционная решётка
- •Дифракция от пространственной решётки
- •5.2.Квантовая теория излучения
- •5.2.1. Характеристики теплового излучения
- •5.2.2. Законы Стефана-Больцмана и Вина
- •5.2.3. Квантовая гипотеза Планка. Формула Планка
- •Раздел 6. Квантовая физика. (15,5 час)
- •6.1. Элементы квантовой механики
- •6.2. Элементы физики атома
- •6.2.2. Теория водородоподобных атомов
- •6.3.1. Состав и характеристики атомного ядра
- •6.3.2. Ядерные реакции
- •Глоссарий
- •Массовое число– это число нуклонов (протонов и нейтронов) в атомном ядре. Массовое число равно округленной до целого числа относительной атомной массе элемента.
- •Эквипотенциальная поверхность - поверхность, во всех точках которой потенциал электрического поля имеет одинаковое значение
- •4. Блок контроля освоения дисциплины
- •Методические указания к выполнению контрольных работ
- •4.2. Контрольная работа № 1
- •4.2.1. Примеры решения задач
- •4.2.2. Задание на контрольную работу № 1
- •4.3. Контрольная работа № 2
- •4.3.1. Примеры решения задач
- •Используя формулы (2) и (1), получаем
- •4.3.2. Задание на контрольную работу № 2
- •4.4. Некоторые сведения, необходимые для решения задач
- •1. Некоторые физические постоянные (округленные значения)
- •2. Некоторые астрономические величины
- •3. Некоторые физические постоянные (округленные значения)
- •4. Множители и приставки для образования десятичных кратных и
- •5. Греческий алфавит
- •4.5. Текущий контроль (тестовые задания)
- •4.5.1. Тренировочный тест №1 (к разделам 1 и 2)
- •4.5.2. Тренировочный тест №2 (к разделу 3)
- •4.5.3. Тренировочный тест № 3 (к разделам 4, 5, 6)
- •4.5.4. Правильные ответы на тренировочные тесты
- •4.6. Вопросы для подготовки к зачёту Физические основы механики
- •Молекулярная (статистическая) физика и термодинамика
- •Электричество и магнетизм
- •Физика колебаний и волн
- •Волновая и квантовая оптика
- •Квантовая физика
- •191186, Санкт-Петербург, ул. Миллионная, 5
2.4.5. Второе начало термодинамики
Первое начало термодинамики позволяет определить, возможен ли тот или иной процесс с энергетической точки зрения, но ничего не говорит о направлении самопроизвольно протекающих процессов. Например, с точки зрения первого начала возможен самопроизвольный переход теплоты от холодного тела к горячему, хотя в природе такие процессы не наблюдаются. Направление процессов определяет второе начало термодинамики. При этом используется ещё одна функция состояния системы – энтропия. Энтропия характеризует степень необратимости процесса. Количественно изменение энтропии равно приведённой теплоте:
![]() .
(2.26)
.
(2.26)
здесь Т – температура, при которой происходит теплообмен. Для конечного процесса приведенная теплота равна сумме приведённых теплот, тогда
![]() .
(2.27)
.
(2.27)
Физический смысл энтропии устанавливается на молекулярно-кинетическом уровне методами статистической физики. Австрийским физиком Л. Больцманом было доказано, что энтропия связана со статистическим весом или термодинамической вероятностью данного макросостояния (W):
![]() .
(2.28)
.
(2.28)
Состояние, которое осуществляется многими способами, называется беспорядочным (хаотическим).
Таким образом, энтропия может рассматриваться как мера беспорядка в термодинамической системе.
Чем сильнее система упорядочена, тем меньше энтропия. Например, твердому телу, в котором атомы закреплены в узлах кристаллической решетки соответствует практически одно микросостояние.
Сообщение системе тепла приводит к усилению теплового движения молекул, к увеличению степени беспорядка в системе и возрастанию энтропии.
Термодинамическая система, предоставленная самой себе, переходит в наиболее вероятное состояние, которое является равновесным
Обобщение огромного количества опытных данных выражается в виде фундаментального закона природы второго начала термодинамики:
В изолированной системе все процессы протекают так, что энтропия не убывает.
![]() .
(2.29)
.
(2.29)
Энтропия изолированной
системы не изменяется (![]() ),
если процесс обратимый или адиабатный
и возрастает (
),
если процесс обратимый или адиабатный
и возрастает (![]() ),
если процесс необратимый.
),
если процесс необратимый.
Существует несколько других эквивалентных формулировок второго начала термодинамики, они отражают частные случаи, различные стороны проблемы и исторический ход развития знаний в этой области.
Формулировка Клаузиуса: невозможен процесс, единственным результатом которого является передача энергии в форме теплоты от холодного тела к горячему.
Формулировка Томсона (Кельвина): невозможно преобразовать в работу всю теплоту, взятую от тела с однородной температурой, не производя никаких других изменений в состоянии системы.
2.4.6. Тепловые машины
Одним из приложений термодинамики, важным для практики, является теория тепловых машин.
Под тепловой машиной понимают устройство, совершающее работу за счет части внутренней энергии.
В основе непрерывно действующей машины лежит круговой (циклический) термодинамический процесс.
Круговым процессом
(циклом) называется процесс, в результате
которого система после ряда изменений
возвращается в исходное состояние.
Изменение внутренней энергии за цикл
равно нулю (![]() ).
).
Основной
характеристикой цикла является
коэффициент полезного действия
![]() :
:
![]() ,
(2.30)
,
(2.30)
![]() – работа, совершаемая
за цикл, Q1
– количество теплоты, полученной
системой за цикл.
– работа, совершаемая
за цикл, Q1
– количество теплоты, полученной
системой за цикл.
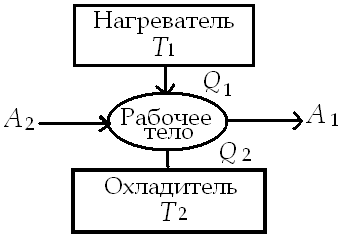
Периодически действующий двигатель, совершающий работу за счет получаемого извне тепла, называется тепловой машиной. Схематически тепловая машина показана на рис. 2.2.
Рис. 2.2 |
Рабочее тело (газ, пар и др.) получает от нагревателя с температурой Т1 количество теплоты Q1. При расширении рабочего тела связанный с ним механизм совершает работу А1; часть теплоты Q2 отдается охладителю – телу с более низкой температурой Т2. Для возвращения рабочего тела в исходное состояние внешними силами совершается работа А2. |
Применяя первое начало термодинамики к прямой и обратной частям цикла получим для коэффициента полезного действия тепловой машины
![]() .
(2.31)
.
(2.31)
Согласно второму
началу термодинамики изменение энтропии
всей системы для обратимого
процесса
,
то есть
![]() или
или
![]() и
и
![]() .
(2.32)
.
(2.32)
Тепловая машина, работающая на цикле из обратимых процессов, называется идеальной. КПД идеальной тепловой машины определяется по формуле (2.32). Примером идеальной тепловой машины является машина, работающая по циклу Карно, состоящему из двух изотерм и двух адиабат.