
- •Техника безопасности
- •1. Электропроводность растворов электролитов
- •Электропроводность растворов электролитов
- •Удельная электропроводность
- •Кондуктометрическое титрование
- •Определение растворимости труднорастворимой соли.
- •Работа 1.1. Определение концентрационной зависимости удельной и молярной электропроводности сильного электролита
- •Порядок выполнения работы:
- •Работа 1.2. Определение константы диссоциации слабого электролита методом электропроводности
- •Порядок выполнения работы:
- •Работа 1.3. Кондуктометрическое титрование
- •Порядок выполнения работы:
- •Работа 1.4. Кондуктометрическое определение термодинамических параметров растворения труднорастворимого соединения
- •Порядок выполнения работы:
- •Перед выполнением работы:
- •К защите работы:
- •2. Электродвижущие силы Возникновение потенциалов на границах фаз.
- •Электродный потенциал
- •Водородный электрод
- •Измерение электродных потенциалов
- •Электрохимический (гальванический) элемент
- •Концентрационный гальванический элемент
- •Измерение эдс гальванического элемента компенсационным методом
- •Температурная зависимость эдс.
- •Электроды сравнения
- •Хлорсеребряный электрод
- •Окислительно-восстановительные электроды и их потенциалы
- •Мембранные равновесия. Стеклянный электрод
- •Кислотно-основные буферные системы
- •Механизм буферного действия
- •Буферная емкость
- •Порядок выполнения работы:
- •Порядок выполнения работы:
- •Порядок выполнения работы:
- •Окислительно-восстановительных потенциалов
- •Порядок выполнения работы:
- •Буферной ёмкости буферных систем
- •Порядок выполнения работы:
- •Порядок выполнения работы:
- •Контрольные вопросы Перед выполнением работы:
- •К защите работы:
- •3. Адсорбция
- •Метод полных концентраций
- •Термодинамика адсорбции по Гиббсу
- •Уравнение адсорбции Гиббса
- •Адсорбция из жидких растворов на поверхности твердых адсорбентов
- •Теплоты адсорбции
- •Работа 3.1. Изучение адсорбции паров воды на твердом адсорбенте
- •Порядок выполнения работы:
- •Перед выполнением работы:
- •К защите работы:
- •Работа 3.2. Изучение адсорбции уксусной кислоты из водного раствора на активированном угле
- •Интерферометрический метод анализа концентрации растворов.
- •Технология проведения адсорбции и методика определения равновесных концентраций растворов и расчета адсорбции по результатам эксперимента:
- •Перед выполнением работы:
- •К защите работы:
- •Работа 3.3. Изучение адсорбции поверхностно-активных веществ (пав) на границе воздух-раствор
- •Измерение поверхностного натяжения жидкостей методом Ребиндера.
- •Расчет адсорбции на границе раздела водный раствор – воздух.
- •Порядок выполнения работы:
- •Проверка выполнимости правила Дюкло – Траубе
- •Перед выполнением работы:
- •К защите работы:
- •4. Газовая хроматография
- •Общие сведения о газовом хроматографе
- •Детекторы
- •Детектор по теплопроводности (дтп)
- •Пламенно-ионизационный детектор (пид)
- •Качественный и количественный анализ в газовой хроматографии.
- •Определение мольных теплот растворения газов и паров в жидкостях газохроматографическим методом
- •Порядок работы на хроматографе лхм-80
- •Работа 4.1. Качественный и количественный анализ смеси углеводородов с помощью газовой хроматографии на колонке с апьезоном, нанесенным на хроматон.
- •Определение качественного состава смеси углеводородов по совпадению времен удерживания компонентов контрольной смеси с временами удерживания углеводородов c6 - с9 .
- •Расчет поправочных коэффициентов для углеводородов c6 - с9 и определение количественного состава контрольной смеси углеводородов в мольных процентах.
- •Перед выполнением работы:
- •К защите работы:
- •Работа 4.2. Определение мольных теплот растворения нормальных углеводородов c6- c9 в апьезоне хроматографическим методом
- •Перед выполнением работы:
- •К защите работы:
- •Работа 4.3. Определение индексов ковача веществ и их температурных коэффициентов на апьезоне
- •Перед выполнением работы:
- •К защите работы:
- •Химическая кинетика
- •Кинетические уравнения реакций различных порядков Реакции нулевого порядка
- •Реакции первого порядка
- •Реакции второго порядка
- •Реакции n-го порядка
- •Способы определения порядков реакции.
- •Зависимость скорости реакции от температуры
- •Сложные реакции
- •Работа 5.1. Кинетика омыления этилацетата в присутствии ионов гидроксила.
- •Порядок выполнения работы:
- •Определение æ0.
- •Определение константы скорости реакции при разных температурах.
- •Определение энергии активации и предэкспоненциального множителя.
- •Перед выполнением работы:
- •К защите работы:
- •Работа 5.2. Изучение кинетики гомогенно-каталитического разложения н2о2 .
- •Порядок подготовки установки к работе и работа на ней.
- •Порядок проведения кинетических опытов:
- •Варианты задания и методика расчетов.
- •Изучение зависимости скорости реакции разложения перекиси водорода от концентрации катализатора.
- •Влияние начальной концентрации н2о2 на период полупревращения. Определение порядка реакции.
- •III. Определение константы равновесия и константы скорости реакции разложения перекиси водорода.
- •Перед выполнением работы:
- •К защите работы:
- •Работа 5.3. Изучение кинетики инверсии сахарозы.
- •Методика измерения угла вращения на поляриметре (сахариметре)
- •Методика измерения угла вращения на автоматическом поляриметре
- •Порядок выполнения работы:
- •Перед выполнением работы:
- •К защите работы:
- •Работа 5.4. Изучение кинетики реакции окисления иодид-ионов ионами трёхвалентного железа фотометрическим методом
- •Порядок выполнения работы:
- •Перед выполнением работы:
- •К защите работы:
III. Определение константы равновесия и константы скорости реакции разложения перекиси водорода.
Для расчета константы равновесия и константы скорости реакции используют уравнение (5.34).

Уравнение (5.34) можно преобразовать в линейную форму, взяв обратное значение скорости:
![]() 5.39
5.39
Из графика в координатах
![]() по тангенсу угла наклона прямой при
известной исходной концентрации
катализатора
находят произведение k2K1,
а по отрезку, отсекаемому на оси ординат,
значение k2.
по тангенсу угла наклона прямой при
известной исходной концентрации
катализатора
находят произведение k2K1,
а по отрезку, отсекаемому на оси ординат,
значение k2.
Порядок проведения опыта:
Провести кинетический опыт, как описано в п.п.А.1-8 (концентрации перекиси водорода и катализатора указываются преподавателем). Получить зависимость количества выделившегося кислорода от времени. Результаты записать в таблицу 5.2.1.
Построить кинетическую кривую в координатах
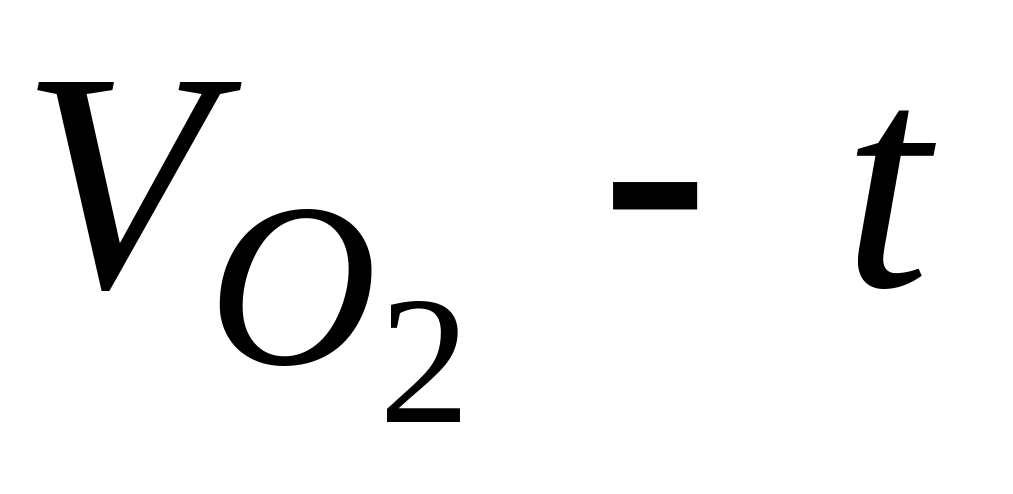 .
Из кривой для 6-7 значений t
графическим дифференцированием
определить величину
.
Из кривой для 6-7 значений t
графическим дифференцированием
определить величину
 .
.По формуле (5.36) вычислить скорость реакции
 .
.По формуле (5.35) рассчитать максимальный объем кислорода
 ,
который может выделиться при полном
разложении
заданной
концентрации.
,
который может выделиться при полном
разложении
заданной
концентрации.Учитывая, что концентрация перекиси водорода в момент времени t пропорциональна величине
 рассчитать концентрацию
по формуле (5.40)
рассчитать концентрацию
по формуле (5.40)
![]() 5.40
5.40
Результаты вычислений записать в таблицу 5.2.4. Построить зависимость
 от
от
 .
Тангенс угла наклона прямой позволяет
найти произведение
.
Тангенс угла наклона прямой позволяет
найти произведение
 ,
а отрезок, отсекаемый на оси ординат,
значение
,
а отрезок, отсекаемый на оси ординат,
значение
 ,
см. уравнение (5.39). Из найденных
произведений, зная концентрацию
катализатора, найти величины
и
.
,
см. уравнение (5.39). Из найденных
произведений, зная концентрацию
катализатора, найти величины
и
.
Таблица 5.2.4
![]() ……………….
……………….
![]() ……………….
……………….
![]() …………….
…………….
![]() ……………..
……………..
![]() ……………………
……………………![]() ……………….
……………….
t,мин. |
|
|
|
|
|
|
|
|
|
|
|
![]() …………….
…………….
![]() ……………
……………
КОНТРОЛЬНЫЕ ВОПРОСЫ К РАБОТЕ 5.2
Перед выполнением работы:
Расскажите последовательность подготовки системы к работе и порядок проведения опыта.
Какие концентрации рабочих растворов и растворов катализатора следует приготовить для работы?
Как проверить установку на герметичность?
Как рассчитать максимально возможный объём кислорода, который может выделиться в результате разложения ?
Запишите реакции, протекающие в системе при разложении перекиси водорода раствором бихромата калия.
Как определить текущую концентрацию ?
Как рассчитать методом графического дифференцирования?
Как определить константу скорости и константу равновесия реакции разложения перекиси из экспериментальных данных?
К защите работы:
Дайте определение скорости реакции, порядка реакции. Поясните физический смысл константы скорости реакции.
Запишите кинетические уравнения необратимых реакций нулевого и второго порядка.
Запишите механизм разложения перекиси водорода в присутствии ионов .
Каковы условия проведения реакции разложения в присутствии бихромата калия по а) нулевому, б) второму порядку?
Перечислите известные вам виды катализа. В чем состоит особенность каталитических процессов?
Отразится ли на константе скорости реакции замена одного катализатора другим?
Как катализатор влияет на энергию активации данной реакции? Как графически моно определить энергию активации?
Объясните последовательность выполненных Вами расчетов.
