
- •Практикум по общей химии
- •ЧАсть I
- •1. Порядок работы в химической лаборатории
- •Правила безопасности при работе студентов в химической лаборатории
- •Правила пользования газовой горелкой
- •Правила пользования реактивами, посудой, правила нагревания
- •Оказание первой помощи в лаборатории при несчастных случаях
- •2. Основные законы химии
- •3.Основные классы химических соединений
- •Практические работы
- •4. Строение атома и радиоактивность
- •Правила заполнения электронами атомных орбиталей (ао)
- •Практические работы
- •5. Периодический закон и система д.И. Менделеева. Свойства элементов
- •Практические работы Свойства s-элементов
- •Свойства р-элементов
- •Свойства р-элементов четвертой группы
- •Свойства р-элементов пятой группы
- •Свойства р-элементов шестой группы
- •Свойства р-элементов седьмой группы
- •Свойства d-металлов.
- •Свойства d-металлов шестой группы
- •Свойства d-элементы восьмой группы.
- •Свойства d-элементов второй группы.
- •6. Химия координационных соединений
- •Координационная связь. Свойства комплексных соединений
- •Практические работы
- •7. Химическая связь и строение молекул
- •Схемы образования мо
- •Заполнение мо лкао электронами
- •Схемы гибридизации
- •Практические работы
- •1. Изучение строения молекул с помощью комплекта шарико-стержневых моделей атомов и химических связей.
- •2. Химические (кислотно-основные, окислительно-восстановительные) свойства атомов и молекул элемента.
- •8. Основы химической термодинамики
- •Практические работы Тепловой эффект (энтальпия) реакции нейтрализации.
- •9. Кинетика и равновесие химических реакций
- •Практические работы
- •10. Растворы электролитов
- •10.1 Свойства растворов электролитов
- •П Рис. 5. Установка для определения электропроводности растворов: 1 - амперметр; 2 - стакан с электролитом; 3 - графитовые электроды; 4 - пробка; 5 - реостат. Рактические работы
- •10.2 Электролитическая диссоциация и рН раствора
- •Практические работы
- •10.3 Гидролиз солей
- •Практические работы
- •11. Окислительно-восстановительные реакции
- •11.1 Окислительно-восстановительные реакции и потенциалы
- •Практические работы
- •3. Влияние характера среды на протекание окислительно-восстановительной реакции:
- •11.2 Химическая стойкость металлов в водных растворах
- •Практические работы
- •12. Электрохимические процессы
- •12.1 Исследование работы химического источника тока
- •Практические работы
- •12.2 Электролиз и нанесение гальванических покрытий
- •Практические работы
- •12.3 Коррозия металлов и защита от коррозии
- •Практические работы
- •2. Электрохимическая коррозия и защита в растворах электролитов
- •Правила оформления лабораторных работ
- •Литература
- •Приложение
- •Давление водяного пара (h; мм.Рт.Ст.)
- •Стандартные энтальпии образования н0298, энтропии s0298 и энергии Гиббса g0298 некоторых веществ при 298 к (250 с)
- •Константы диссоциации кислот и оснований
- •Множители и приставки для образования десятичных кратных
- •Правила «выживания» в химической лаборатории
- •Издательство «Экоцентр»
Схемы образования мо
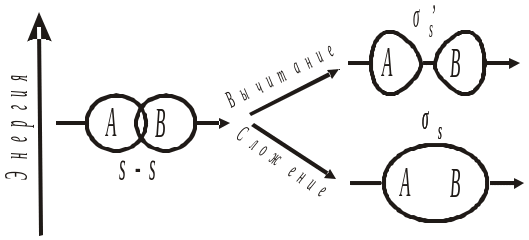
Схема образования МО
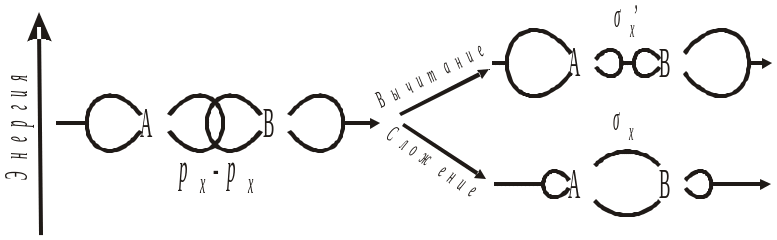
Схема образования МО из р-атомных орбиталей
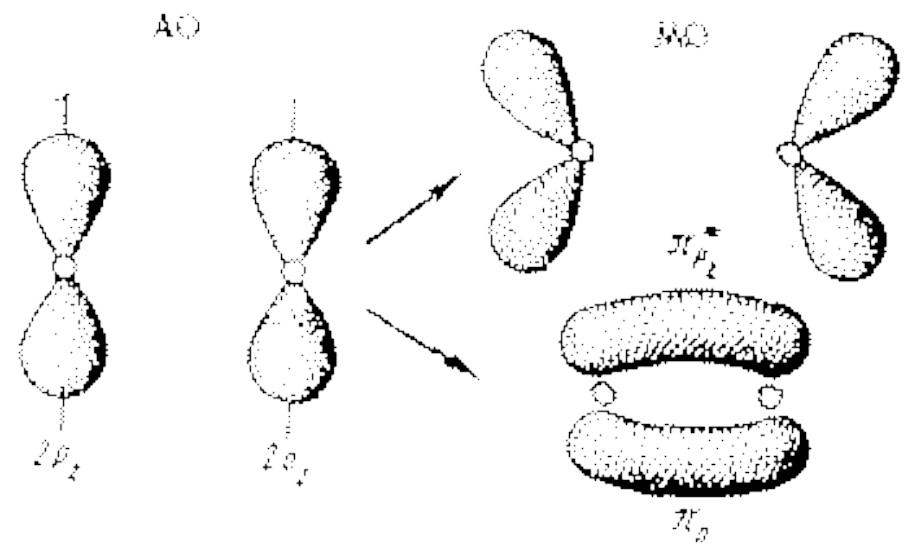
Схема образования связывающей и разрыхляющей π–МО из рz–АО

Энергетическая диаграмма АО и МО молекулы Н2
Заполнение мо лкао электронами
|
H2+ |
|
H2 |
|
(He2) |
|
He2+ |
|
Li2 |
|
Be2 |
1s* |
|
|
|
|
|
|
|
2s* |
|
|
|
1s |
|
|
|
|
|
|
|
2s |
|
|
|
|
|
B2 |
|
|
|
C2 |
|
|
|
N2 |
|
|
|
N2+ |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
2s* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2s |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
O2+ |
|
|
|
O2 |
|
|
|
F2 |
|
|
|
(Ne2) |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2s* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2s |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Метод МО хорошо объясняет оптические и магнитные свойства молекул, метод ВС удобен для объяснения строения (геометрия) молекул, при этом он базируется на явлении и методе гибридизации, заключающемся в том, что при образовании химической связи, атомные орбитали смешиваются, выравниваются (по энергии), приобретают одинаковую (симметричную) геометрию. При этом число гибридных орбиталей соответствует числу атомных, из которых они образовались, например:
sp – гибридизация одной s- и одной р-АО.
sp2 – гибридизация одной s- и двух р-АО.
sp3 – гибридизация одной s- и трех р-АО.
