
- •Тема 1.1. Основні закони хімії
- •Закон збереження маси речовини
- •Контрольні запитання:
- •Тема 1.2. Оксиди
- •Визначення. Класифікація оксидів.
- •Контрольні запитання:
- •Тема 1.3. Основи
- •Визначення. Класифікація основ.
- •Контрольні запитання:
- •Тема 1.4. Кислоти
- •Визначення. Класифікація кислот.
- •Контрольні запитання:
- •Тема 1.5. Солі
- •Визначення. Класифікація солей.
- •Контрольні запитання:
- •Тема 1.6. Хімічний зв'язок
- •Поняття про хімічний зв'язок. Типи хімічного зв’язку.
- •Контрольні запитання:
- •Тема 1.7. Електролітична дисоціація. Реакції йонного обміну
- •Контрольні запитання:
- •Тема 1.8. Окисно-відновні реакції
- •Контрольні запитання:
- •Тема 2.1. Загальна характеристика металів
- •Контрольні запитання:
- •Тема 2.2. Корозія металів
- •Корозія металів. Види корозії.
- •Контрольні запитання:
- •Тема 2.3. Лужні метали
- •Контрольні запитання:
- •Тема 2.4. Кальцій
- •Кальцій.**
- •Контрольні запитання:
- •Тема 2.5. Сполуки Кальцію
- •Контрольні запитання:
- •Тема 2.6. Алюміній
- •Контрольні запитання:
- •Тема 2.7. Залізо
- •Контрольні запитання:
- •Тема 2.8. Сульфур. Сірка.
- •Контрольні запитання:
- •Тема 2.9. Сполуки Сульфуру
- •Контрольні запитання:
- •Тема 2.10. Сульфатна кислота та її солі
- •Контрольні запитання:
- •Тема 2.11. Нітроген. Азот.
- •Контрольні запитання:
- •Тема 2.12. Аміак. Солі амонію.
- •Контрольні запитання:
- •Тема 2.13. Сполуки Нітрогену
- •Контрольні запитання:
- •Тема 2. 14.Фосфор
- •Фосфор.
- •Контрольні запитання:
- •Тема 2.15. Сполуки Фосфору
- •Контрольні запитання:
- •Тема 2.16. Карбон. Вуглець.
- •Контрольні запитання:
- •Тема 2.16. Сполуки Карбону
- •Контрольні запитання:
- •Тема 2.18. Силіцій.
- •Контрольні запитання:
- •Тема 2.19. Сполуки Силіцію.
- •Контрольні запитання:
- •Тема 3.1. Теорія будови органічних речовин о.М. Бутлерова
- •Контрольні запитання:
- •Тема 3.2. Алкани
- •Контрольні запитання:
- •Тема 3.3. Алкени
- •Контрольні запитання:
- •Тема 3.4. Алкіни
- •Контрольні запитання:
- •Тема 3.5. Алкадієни (дієнові вуглеводні)
- •Контрольні запитання:
- •Тема 3.6. Ароматичні вуглеводні (арени)
- •Контрольні запитання:
- •Тема 3.7. Природні джерела вуглеводнів
- •Контрольні запитання:
- •Тема 4.1. Одноатомні спирти
- •Контрольні запитання:
- •Тема 4.2. Багатоатомні спирти
- •Контрольні запитання:
- •Тема 4.3. Феноли
- •Контрольні запитання:
- •Тема 4.4. Альдегіди
- •Контрольні запитання:
- •Тема 4.5. Карбонові кислоти
- •Контрольні запитання:
- •Тема 4.6. Естери
- •2. Номенклатура:
- •Контрольні запитання:
- •Тема 4.7. Жири. Мило
- •Контрольні запитання:
- •Тема 5.1. Вуглеводи. Глюкоза
- •Контрольні запитання:
- •Тема 5.2. Сахароза
- •Контрольні запитання:
- •Тема 5.3. Крохмаль і целюлоза
- •Контрольні запитання:
- •Тема 5.4. Аміни
- •Контрольні запитання:
- •Тема 5.5. Амінокислоти
- •Контрольні запитання:
- •Тема 5.6. Білки
- •Контрольні запитання:
Тема 5.6. Білки
План
-
Визначення.
-
Поширення в природі.
-
Склад і будова молекул.*
-
Хімічні властивості.**
-
Застосування.
-
Білки – високомолекулярні сполуки, утворені амінокислотними залишками, які з’єднані між собою пептидним зв’язком –С–N–
|| |
О Н
2. Білки є найважливішою складовою частиною живих організмів, вони входять до скажу шкіри, рогових покривів, м’язової і нервової тканин.
3. Кожен білок має набір амінокислот, сполучених у певній, властивій тільки йому послідовності. Кількість сполучених у різній послідовності амінокислотних залишків сягає 1018.
Структури білка:
-
Первинна – послідовність амінокислот
-
Вторинна – утворення спіралі з поліпептидного ланцюга за допомогою водневих зв’язків між –С=О і –NН
| |
-
Третинна – складання ділянок спіралі у клубки (глобули) за допомогою зв’язків між групами –NH2, –ОН, –СООН, –S–S–, які не брали участі в утворенні пептидних зв’язків
-
Четвертинна – розміщення в просторі декількох клубків поліпептидних спіралей
С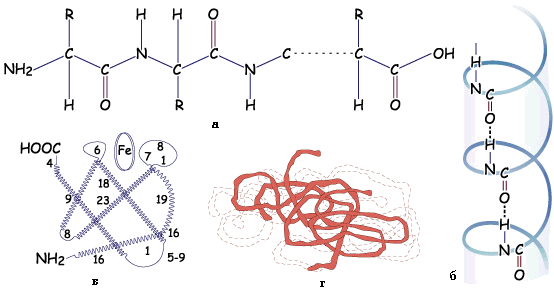 труктура
білка:
труктура
білка:
а, б, в - первинна, вторинна, третинна структури міоглобіну
(цифри - число амінокислотних залишків у молекулі);
г - четвертинна структура гемоглобіну
4. Хімічні властивості:
1) Гідроліз: під дією кислот, лугів, ферментів відбувається розщеплення полімерної білкової молекули на амінокислоти. Молекули води приєднуються за місцем пептидних зв'язків, останні руйнуються, замість пептидних груп утворюються аміно- й карбоксильні групи.
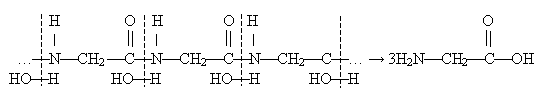
2) Денатурація – руйнування вторинної, третинної, четвертинної структур при нагріванні, опромінюванні, дії сильних кислот і лугів, дії солей важких металів.
3) Кольорові реакції на білки:
а) біуретова: білок + луг + CuSO4 → фіолетове забарвлення
б) ксантопротеїнова:
tºС NH3∙H2O
білок + HNO3(конц) → жовтий колір ———→ оранжевий колір
5. Застосування: 1) обумовлюють існування живих організмів;
2) для добування амінокислот
Контрольні запитання:
-
Які органічні речовини називаються білками?
-
Як називається хімічна реакція за допомогою якої з амінокислот утворюється поліпептид?
-
Опишіть структури білків.
-
Що розуміють під поняттям «денатурація білка»?
-
Якісні реакції на білки.
-
Які об’єми азоту та вуглекислого газу утворяться при горінні 120 г метиламіну?
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 151-152.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІІ, Гл. 18, § 160, с. 167-169.
-
Стахеєв О.Ю. Хімія. Узагальнюючі схеми і таблиці. – Тернопіль.: «Богдан», 1998. – с. 45 .
-
Березан О.В. Органічна хімія. – К.: Абрис, 2000. – Р. ІХ, §§ 14-15, с. 203-204.
