- •Тема 1.1. Основні закони хімії
- •Закон збереження маси речовини
- •Контрольні запитання:
- •Тема 1.2. Оксиди
- •Визначення. Класифікація оксидів.
- •Контрольні запитання:
- •Тема 1.3. Основи
- •Визначення. Класифікація основ.
- •Контрольні запитання:
- •Тема 1.4. Кислоти
- •Визначення. Класифікація кислот.
- •Контрольні запитання:
- •Тема 1.5. Солі
- •Визначення. Класифікація солей.
- •Контрольні запитання:
- •Тема 1.6. Хімічний зв'язок
- •Поняття про хімічний зв'язок. Типи хімічного зв’язку.
- •Контрольні запитання:
- •Тема 1.7. Електролітична дисоціація. Реакції йонного обміну
- •Контрольні запитання:
- •Тема 1.8. Окисно-відновні реакції
- •Контрольні запитання:
- •Тема 2.1. Загальна характеристика металів
- •Контрольні запитання:
- •Тема 2.2. Корозія металів
- •Корозія металів. Види корозії.
- •Контрольні запитання:
- •Тема 2.3. Лужні метали
- •Контрольні запитання:
- •Тема 2.4. Кальцій
- •Кальцій.**
- •Контрольні запитання:
- •Тема 2.5. Сполуки Кальцію
- •Контрольні запитання:
- •Тема 2.6. Алюміній
- •Контрольні запитання:
- •Тема 2.7. Залізо
- •Контрольні запитання:
- •Тема 2.8. Сульфур. Сірка.
- •Контрольні запитання:
- •Тема 2.9. Сполуки Сульфуру
- •Контрольні запитання:
- •Тема 2.10. Сульфатна кислота та її солі
- •Контрольні запитання:
- •Тема 2.11. Нітроген. Азот.
- •Контрольні запитання:
- •Тема 2.12. Аміак. Солі амонію.
- •Контрольні запитання:
- •Тема 2.13. Сполуки Нітрогену
- •Контрольні запитання:
- •Тема 2. 14.Фосфор
- •Фосфор.
- •Контрольні запитання:
- •Тема 2.15. Сполуки Фосфору
- •Контрольні запитання:
- •Тема 2.16. Карбон. Вуглець.
- •Контрольні запитання:
- •Тема 2.16. Сполуки Карбону
- •Контрольні запитання:
- •Тема 2.18. Силіцій.
- •Контрольні запитання:
- •Тема 2.19. Сполуки Силіцію.
- •Контрольні запитання:
- •Тема 3.1. Теорія будови органічних речовин о.М. Бутлерова
- •Контрольні запитання:
- •Тема 3.2. Алкани
- •Контрольні запитання:
- •Тема 3.3. Алкени
- •Контрольні запитання:
- •Тема 3.4. Алкіни
- •Контрольні запитання:
- •Тема 3.5. Алкадієни (дієнові вуглеводні)
- •Контрольні запитання:
- •Тема 3.6. Ароматичні вуглеводні (арени)
- •Контрольні запитання:
- •Тема 3.7. Природні джерела вуглеводнів
- •Контрольні запитання:
- •Тема 4.1. Одноатомні спирти
- •Контрольні запитання:
- •Тема 4.2. Багатоатомні спирти
- •Контрольні запитання:
- •Тема 4.3. Феноли
- •Контрольні запитання:
- •Тема 4.4. Альдегіди
- •Контрольні запитання:
- •Тема 4.5. Карбонові кислоти
- •Контрольні запитання:
- •Тема 4.6. Естери
- •2. Номенклатура:
- •Контрольні запитання:
- •Тема 4.7. Жири. Мило
- •Контрольні запитання:
- •Тема 5.1. Вуглеводи. Глюкоза
- •Контрольні запитання:
- •Тема 5.2. Сахароза
- •Контрольні запитання:
- •Тема 5.3. Крохмаль і целюлоза
- •Контрольні запитання:
- •Тема 5.4. Аміни
- •Контрольні запитання:
- •Тема 5.5. Амінокислоти
- •Контрольні запитання:
- •Тема 5.6. Білки
- •Контрольні запитання:
Контрольні запитання:
-
Які органічні речовини відносяться до ароматичних вуглеводнів?
-
Які типи хімічних реакцій притаманні ароматичним вуглеводням?
-
Які властивості бензену вказують на його подібність: а) з насиченими вуглеводнями; б) ненасиченими вуглеводнями?
-
Який об’єм повітря (н.у.) знадобиться, щоб спалити 1 л бензену, густина якого 0,88 г/см3?
-
Під час гідрування 7,8 г бензену до циклогексану при нагріванні за наявності каталізатора поглинулось 3,36 л водню. Визначити масову частку виходу циклогексану.
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 78-81.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІІ, Гл. 16, §§ 138-139, с. 142-144.
-
Стахеєв О.Ю. Хімія. Узагальнюючі схеми і таблиці. – Тернопіль.: «Богдан», 1998. – с. 38.
-
Березан О.В. Органічна хімія. – К.: Абрис, 2000. – Р. ІІІ, §§ 1-4, с. 60-66.
Тема 3.7. Природні джерела вуглеводнів
План
-
Кам’яне вугілля.*
-
Природний газ.*
-
Супутний нафтовий газ.*
-
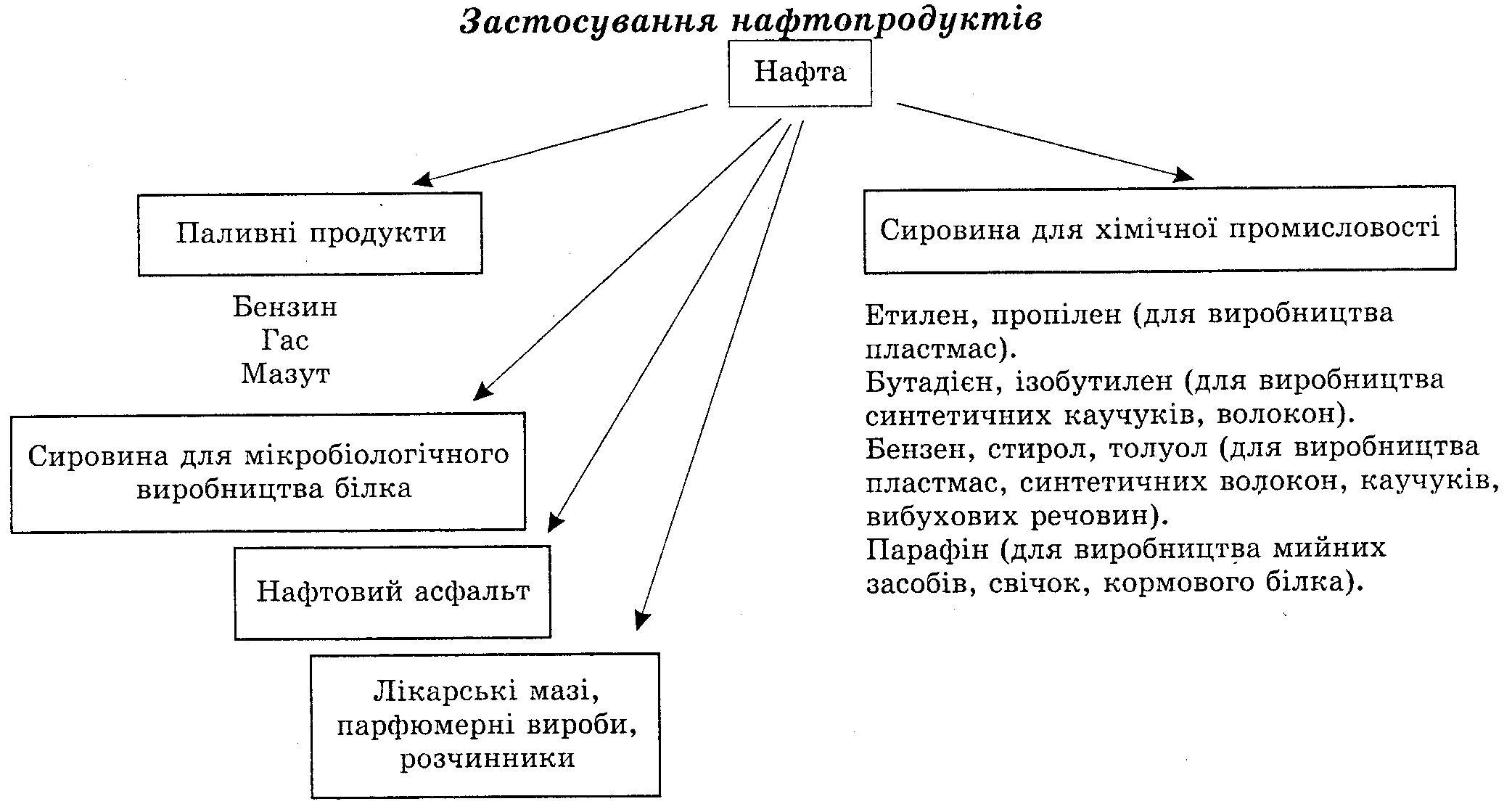
Нафта.*
1. До складу кам’яного вугілля входять вільний вуглець (до 10%), органічні речовини, що містять С, Н, О, S, N, мінеральні речовини.
М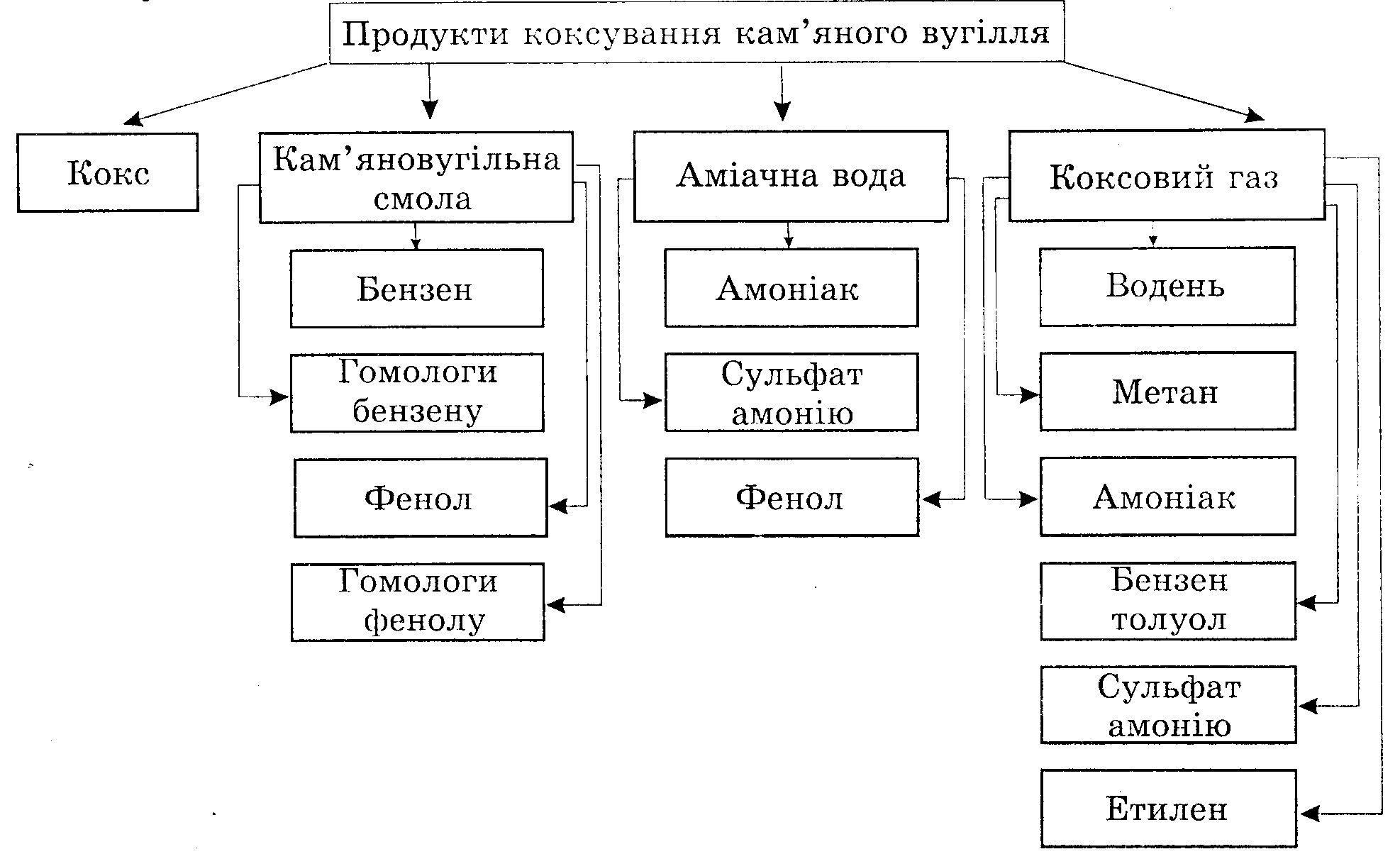 етод
переробки – суха перегонка (1000ºС) без
доступу кисню (коксування). У результаті
утворюється кокс, леткі продукти
(кам’яновугільна смола, аміачна вода
та коксовий газ)
етод
переробки – суха перегонка (1000ºС) без
доступу кисню (коксування). У результаті
утворюється кокс, леткі продукти
(кам’яновугільна смола, аміачна вода
та коксовий газ)
2. В природному газі містяться вуглеводні з низькою молекулярною масою. Основною складовою частиною є метан (80-90%), решта – етан, пропан, бутан, пентан і невелика кількість домішок – сірководень, азот, благородні гази, вуглекислий газ, водяна пара.
Є цінним паливом і хімічною сировиною (добування сажі, водню, ацетилену, синтез-газу)
3. Існують поклади природного газу, що залягають разом із нафтою – супутний нафтовий газ. Це суміш легких вуглеводнів з вмістом метану до 40%, решта – гомологи метану.
Використовується як паливо і хімічна сировина.
4. За фізичними властивостями нафта – це густа оліїста рідина зі специфічним запахом, темно-бурого чи чорного кольору, легша за воду і нерозчинна в ній.
Нафта не є індивідуальною речовиною, це суміш близько 1000 різних речовин, серед яких переважають рідкі насичені вуглеводні, в ній також містяться домішки сульфуро-, нітрогено-, оксигеновмісних органічних сполук, водний розчин неорганічних солей.
Для вилучення продуктів, які містяться в нафті, її піддають переробці. Як суміш речовин нафта не має певної температури кипіння, а переходить у газуватий стан у широкому інтервалі температур. Нафту можна розділити на складові частини (фракції) із значно вужчими інтервалами температур кипіння за допомогою методу фракційної перегонки. Нафтові фракції – теж не індивідуальні речовини, хоча й містять близькі за складом і властивостями сполуки.
Продукти первинної переробки нафти
Фракції
|
Фракція |
Склад молекул |
Інтервал температур кипіння |
Застосування |
|
Бензин |
С4-С12 |
40-120 |
Моторне, авіаційне і автомобільне паливо; розчинник масел |
|
Лігроїн |
С8-С14 |
120-240 |
Пальне для тракторів, розчинник у лакофарбовій промисловості |
|
Гас |
С12-С18 |
180-300 |
Пальне для реактивних і тракторних двигунів |
|
Газойль (дизельне паливо) |
С18-С25 |
270-350 |
Пальне для дизелів, котельне паливо |
|
Мазут |
Від С20 і вище. Залишок перегонки |
Від 300 і вище |
Мастила, парафін, вазелін, котельне рідке паливо, гудрон |
Цей метод переробки заснований на різних фізичних властивостях речовин, що входять до складу нафти (різних температурах кипіння).
Є способи переробки нафти, під час яких відбуваються хімічні реакції, наприклад крекінг. В результаті крекінгу нерозгалужені сполуки перетворюються у більш розгалужені молекули. Відбувається також розщеплення важкокиплячих фракцій у сполуки з меншою молекулярною масою, які придатні як автомобільне паливо.
Застосовують термічний і каталітичний крекінг. Термічний проводять при високій температурі (450 - 600ºС) і підвищеному тискові. Каталітичний крекінг проводять за наявності каталізаторів (переважно алюмосилікатів) при 450 ºС і атмосферному тиску.