
- •Тема 1.1. Основні закони хімії
- •Закон збереження маси речовини
- •Контрольні запитання:
- •Тема 1.2. Оксиди
- •Визначення. Класифікація оксидів.
- •Контрольні запитання:
- •Тема 1.3. Основи
- •Визначення. Класифікація основ.
- •Контрольні запитання:
- •Тема 1.4. Кислоти
- •Визначення. Класифікація кислот.
- •Контрольні запитання:
- •Тема 1.5. Солі
- •Визначення. Класифікація солей.
- •Контрольні запитання:
- •Тема 1.6. Хімічний зв'язок
- •Поняття про хімічний зв'язок. Типи хімічного зв’язку.
- •Контрольні запитання:
- •Тема 1.7. Електролітична дисоціація. Реакції йонного обміну
- •Контрольні запитання:
- •Тема 1.8. Окисно-відновні реакції
- •Контрольні запитання:
- •Тема 2.1. Загальна характеристика металів
- •Контрольні запитання:
- •Тема 2.2. Корозія металів
- •Корозія металів. Види корозії.
- •Контрольні запитання:
- •Тема 2.3. Лужні метали
- •Контрольні запитання:
- •Тема 2.4. Кальцій
- •Кальцій.**
- •Контрольні запитання:
- •Тема 2.5. Сполуки Кальцію
- •Контрольні запитання:
- •Тема 2.6. Алюміній
- •Контрольні запитання:
- •Тема 2.7. Залізо
- •Контрольні запитання:
- •Тема 2.8. Сульфур. Сірка.
- •Контрольні запитання:
- •Тема 2.9. Сполуки Сульфуру
- •Контрольні запитання:
- •Тема 2.10. Сульфатна кислота та її солі
- •Контрольні запитання:
- •Тема 2.11. Нітроген. Азот.
- •Контрольні запитання:
- •Тема 2.12. Аміак. Солі амонію.
- •Контрольні запитання:
- •Тема 2.13. Сполуки Нітрогену
- •Контрольні запитання:
- •Тема 2. 14.Фосфор
- •Фосфор.
- •Контрольні запитання:
- •Тема 2.15. Сполуки Фосфору
- •Контрольні запитання:
- •Тема 2.16. Карбон. Вуглець.
- •Контрольні запитання:
- •Тема 2.16. Сполуки Карбону
- •Контрольні запитання:
- •Тема 2.18. Силіцій.
- •Контрольні запитання:
- •Тема 2.19. Сполуки Силіцію.
- •Контрольні запитання:
- •Тема 3.1. Теорія будови органічних речовин о.М. Бутлерова
- •Контрольні запитання:
- •Тема 3.2. Алкани
- •Контрольні запитання:
- •Тема 3.3. Алкени
- •Контрольні запитання:
- •Тема 3.4. Алкіни
- •Контрольні запитання:
- •Тема 3.5. Алкадієни (дієнові вуглеводні)
- •Контрольні запитання:
- •Тема 3.6. Ароматичні вуглеводні (арени)
- •Контрольні запитання:
- •Тема 3.7. Природні джерела вуглеводнів
- •Контрольні запитання:
- •Тема 4.1. Одноатомні спирти
- •Контрольні запитання:
- •Тема 4.2. Багатоатомні спирти
- •Контрольні запитання:
- •Тема 4.3. Феноли
- •Контрольні запитання:
- •Тема 4.4. Альдегіди
- •Контрольні запитання:
- •Тема 4.5. Карбонові кислоти
- •Контрольні запитання:
- •Тема 4.6. Естери
- •2. Номенклатура:
- •Контрольні запитання:
- •Тема 4.7. Жири. Мило
- •Контрольні запитання:
- •Тема 5.1. Вуглеводи. Глюкоза
- •Контрольні запитання:
- •Тема 5.2. Сахароза
- •Контрольні запитання:
- •Тема 5.3. Крохмаль і целюлоза
- •Контрольні запитання:
- •Тема 5.4. Аміни
- •Контрольні запитання:
- •Тема 5.5. Амінокислоти
- •Контрольні запитання:
- •Тема 5.6. Білки
- •Контрольні запитання:
Контрольні запитання:
-
Які вуглеводи називають полісахаридами? Наведіть приклади.
-
Чим відрізняється целюлоза від крохмалю за складом і будовою?
-
Які хімічні властвисоті характерні крохмалю і целюлозі?
-
Якісна реакція на крохмаль.
-
Скільки етилового спирту можна одержати з однієї тони пшениці, масова частка крохмалю в якій становить 70%, якщо масова частка втрат при виробництві – 15%?
-
З 400 г фільтрувального паперу під час гідролізу в присутності концентрованої хлоридної кислоти одержали 170 г глюкози. Яка масова частка виходу глюкози?
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 141-142.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІІ, Гл. 17, § 155, с. 161-163.
-
Березан О.В. Органічна хімія. – К.: Абрис, 2000. – Р. VІІІ, § 5, с. 175-176.
Тема 5.4. Аміни
План
-
Визначення та загальна формула класу.
-
Номенклатура.*
-
Ізомерія.*
-
Хімічні властивості.**
-
Добування.*
-
Анілін – ароматичний амін.*
-
Застосування аніліну.
1. Аміни – це похідні вуглеводнів, що містять функціональну групу – NH2. Аміни можна розглядати також як похідні аміаку, в якому атоми Гідрогену повністю або частково заміщені на вуглеводневі радикали.
Загальна формула амінів: R–NH2.
Залежно від числа вуглеводневих радикалів, зв’язаних з атомом Нітрогену – первинні, вторинні, третинні.
первинний вторинний третинний
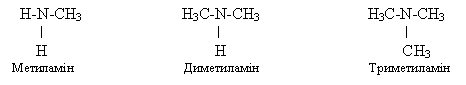
2. 1) Назви первинних амінів будують з назв вуглеводнів, додаючи до них префікс аміно- або закінчення –амін. Нумерація проводять з боку аміногрупи.
2) Назви вторинних і третинних амінів найчастіше утворюють за принципами раціональної номенклатури, перераховуючи радикали в сполуці.
3. Ізомерія: а) карбонового скелету;
б) положення аміногрупи;
в) міжвидова (первинні, вторинні, третинні аміни)
4. Аміни мають основні властивості завдяки неподіленій електронній парі атома Нітрогену.
1) Горіння: 2СН3 –NH2 + 4O2 → 2CO2 + N2 + 4H2O
2) Подібно до аміаку реагують з водою, кислотами:
СН3 –NH2 + H2O → [СН3 –NH3]OH
СН3 –NH2 + HCl → [СН3 –NH3]Cl
3) вступають у реакцію заміщення: СН3 –NH2 + Cl2 → СН2Cl –NH2 + НCl
5. Добування:
Al2O3, tº
1) з спиртів: CH3OH + NH3 ——→ СН3 –NH2 + H2O
2) з галогенпохідних: R–Cl + NH3 + NaOH → R–NH2 + NaCl + H2O
-
Найбільше практичне значення має ароматичний амін – анілін (феніламін).
С6H5NH2
Ф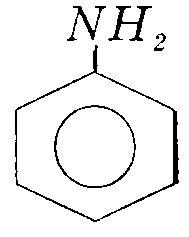 ізичні
властивості:
ізичні
властивості:
Анілін – безбарвна масляниста рідина з неприємним запахом, майже нерозчинна у воді, tпл=184ºС. Дуже токсична.
Хімічні властивості:
1) За хімічними властивостями анілін дещо відмінний від насичених амінів. Він не змінює забарвлення індикаторів, реагує лише з сильними кислотами:
С6Н5 –NH2 + HCl → С6Н5 NH3Cl
хлорид феніламонію
2) вступає в реакції заміщення (подібно до фенолу):
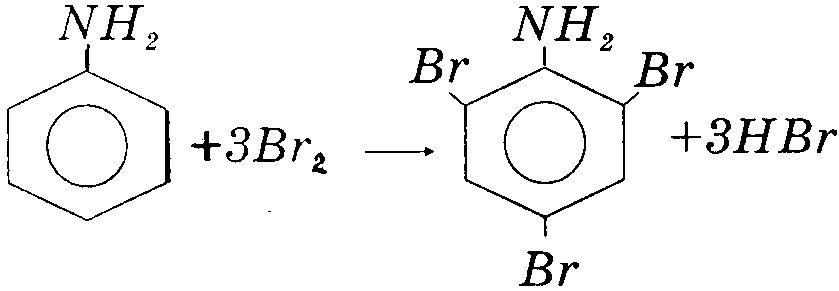
2,4,6-триброманілін (білий осад)
Добування: реакція Зініна – відновлення нітробензену воднем за температури 250—350оС та наявності каталізатора: С6Н5 –NО2 + 3H2 → С6Н5 NH2 + 2Н2О
-
Застосування аніліну: 1) для синтезу барвників;
2) для синтезу лікарських речовин (сульфаніламідних);
3) для синтезу вибухових речовин і ВМС
(анілінформальдегідних смол)
