
- •Тема 1.1. Основні закони хімії
- •Закон збереження маси речовини
- •Контрольні запитання:
- •Тема 1.2. Оксиди
- •Визначення. Класифікація оксидів.
- •Контрольні запитання:
- •Тема 1.3. Основи
- •Визначення. Класифікація основ.
- •Контрольні запитання:
- •Тема 1.4. Кислоти
- •Визначення. Класифікація кислот.
- •Контрольні запитання:
- •Тема 1.5. Солі
- •Визначення. Класифікація солей.
- •Контрольні запитання:
- •Тема 1.6. Хімічний зв'язок
- •Поняття про хімічний зв'язок. Типи хімічного зв’язку.
- •Контрольні запитання:
- •Тема 1.7. Електролітична дисоціація. Реакції йонного обміну
- •Контрольні запитання:
- •Тема 1.8. Окисно-відновні реакції
- •Контрольні запитання:
- •Тема 2.1. Загальна характеристика металів
- •Контрольні запитання:
- •Тема 2.2. Корозія металів
- •Корозія металів. Види корозії.
- •Контрольні запитання:
- •Тема 2.3. Лужні метали
- •Контрольні запитання:
- •Тема 2.4. Кальцій
- •Кальцій.**
- •Контрольні запитання:
- •Тема 2.5. Сполуки Кальцію
- •Контрольні запитання:
- •Тема 2.6. Алюміній
- •Контрольні запитання:
- •Тема 2.7. Залізо
- •Контрольні запитання:
- •Тема 2.8. Сульфур. Сірка.
- •Контрольні запитання:
- •Тема 2.9. Сполуки Сульфуру
- •Контрольні запитання:
- •Тема 2.10. Сульфатна кислота та її солі
- •Контрольні запитання:
- •Тема 2.11. Нітроген. Азот.
- •Контрольні запитання:
- •Тема 2.12. Аміак. Солі амонію.
- •Контрольні запитання:
- •Тема 2.13. Сполуки Нітрогену
- •Контрольні запитання:
- •Тема 2. 14.Фосфор
- •Фосфор.
- •Контрольні запитання:
- •Тема 2.15. Сполуки Фосфору
- •Контрольні запитання:
- •Тема 2.16. Карбон. Вуглець.
- •Контрольні запитання:
- •Тема 2.16. Сполуки Карбону
- •Контрольні запитання:
- •Тема 2.18. Силіцій.
- •Контрольні запитання:
- •Тема 2.19. Сполуки Силіцію.
- •Контрольні запитання:
- •Тема 3.1. Теорія будови органічних речовин о.М. Бутлерова
- •Контрольні запитання:
- •Тема 3.2. Алкани
- •Контрольні запитання:
- •Тема 3.3. Алкени
- •Контрольні запитання:
- •Тема 3.4. Алкіни
- •Контрольні запитання:
- •Тема 3.5. Алкадієни (дієнові вуглеводні)
- •Контрольні запитання:
- •Тема 3.6. Ароматичні вуглеводні (арени)
- •Контрольні запитання:
- •Тема 3.7. Природні джерела вуглеводнів
- •Контрольні запитання:
- •Тема 4.1. Одноатомні спирти
- •Контрольні запитання:
- •Тема 4.2. Багатоатомні спирти
- •Контрольні запитання:
- •Тема 4.3. Феноли
- •Контрольні запитання:
- •Тема 4.4. Альдегіди
- •Контрольні запитання:
- •Тема 4.5. Карбонові кислоти
- •Контрольні запитання:
- •Тема 4.6. Естери
- •2. Номенклатура:
- •Контрольні запитання:
- •Тема 4.7. Жири. Мило
- •Контрольні запитання:
- •Тема 5.1. Вуглеводи. Глюкоза
- •Контрольні запитання:
- •Тема 5.2. Сахароза
- •Контрольні запитання:
- •Тема 5.3. Крохмаль і целюлоза
- •Контрольні запитання:
- •Тема 5.4. Аміни
- •Контрольні запитання:
- •Тема 5.5. Амінокислоти
- •Контрольні запитання:
- •Тема 5.6. Білки
- •Контрольні запитання:
Контрольні запитання:
-
Які речовини називають солями?
-
Як класифікують солі?
-
Які хімічні властивості характерні для середніх солей?
-
Способи одержання солей.
-
Скласти рівняння реакцій за схемою Н2S→SO2→SO3→H2SO4→К2SO4
-
Визначте масу натрій хлориду, який утворився при взаємодії 11,2л хлору з 23г натрію.
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 8 – 9 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 54-55.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. І, Гл. 6, § 52, с. 62-64.
Тема 1.6. Хімічний зв'язок
План
-
Поняття про хімічний зв'язок. Типи хімічного зв’язку.
-
Ковалентний зв'язок. **
-
Йонний зв'язок.**
-
Металічний зв'язок.*
1. Хімічний зв'язок – взаємодія атомів, яка приводить до утворення хімічно стійкої двох- або багатоатомної системи (молекули або кристалу).
Природа хімічного зв’язку має електростатичний характер.
Типи хімічного зв’язку

2. Ковалентний зв’язок – це зв’язок, що утворюється за рахунок спільних електронних пар.
Природа ковалентного зв’язку визначається силою електростатичного притягання двох сусідніх ядер до пари електронів, розташованої між ними.
-
Ковалентний хімічний зв’язок утворюється 2 електронами з протилежно напрямленими спінами, причому ця електронна пара належить двом атомам.
-
Ковалентний зв’язок тим міцніший, чим більшою мірою перекриваються взаємодіючі електронні хмари.
Перекривання можливе тільки при певній взаємній орієнтації електронних хмар; при цьому область перекривання розміщується в певному напрямі відносно взаємодіючих атомів. Тобто ковалентний зв'язок має певну напрямленість:
σ – зв’язок (перекривання атомних хмар відбувається поблизу прямої, що сполучає ядра взаємодіючих атомів)
π – зв’язок (перекривання атомних хмар відбувається з обох боків від прямої, що сполучає ядра взаємодіючих атомів).
Найчастіше ковалентний зв'язок утворюється за обмінним механізмом. Сутність обмінного механізму полягає в тому, що кожний атом надає по 1 електрону для спільної електронної пари.
Приклад: 1) Н2
H∙ + ∙H → H : H або H – H
2) HCl
H∙ + ∙Cl: → H :Cl: або H – Cl
Ковалентний зв'язок за полярністю (симетричністю розташування електронної пари відносно атомів) поділяється на ковалентний полярний та ковалентний неполярний.
Ковалентний неполярний зв’язок – зв’язок, утворений атомами з однаковою електронегативністю.
Приклад: Н2, О2, N2
Ковалентний полярний зв’язок – зв’язок, утворений атомами, електронегативності яких мало відрізняються.
Приклад: HCl, H2O
Крім цього зв'язок може утворюватися і за донорно-акцепторним механізмом: один атом (акцептор) дає вільну орбіталь, а другий (донор) віддає неподілену пару електронів.
Приклад: NH4+
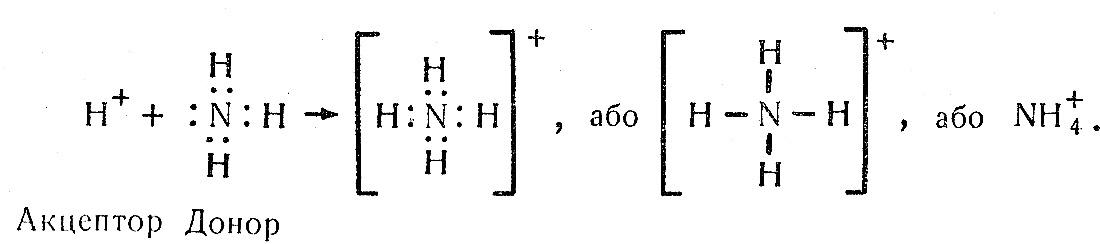
3. Йонний зв’язок – хімічний зв’язок між йонами.
Природа йонного зв’язку полягає в електростатичному притяганні протилежнозаряджених йонів.
Приклад: NaF
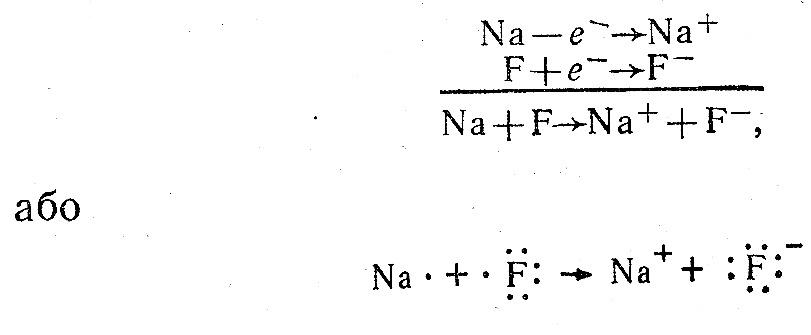
Відмінність йонного зв’язку від ковалентного:
-
не має напрямленості
-
не має насичуваності
Властивості речовин залежать від типи зв’язку:
-
речовини з ковалентним неполярним зв’язком краще розчиняються в неполярних розчинниках
-
речовини з ковалентним полярним зв’язком гарно проводять електричний струм; добре розчиняються в полярних розчинниках.
-
речовини з йонним зв’язком мають високі температури кипіння і плавлення; високу електропровідність у розчинах і розплавах.
4. Металічний зв'язок утворюється внаслідок електростатичного притягання між йонами металу та вільними електронами.
Приклад: Атом натрію на останньому енергетичному рівні містить чотири орбіта лі й один валентний електрон, який атом віддає дуже легко. Всі чотири орбіта лі й один електрон останнього рівня атоми натрію у кристалі металу надають для утворення хімічного зв’язку. Виходить, що в кристалі натрію електронів більше значно менше, ніж орбіта лей. Це дозволяє електронам у металі вільно переміщуватись, переходячи з однієї орбіта лі на іншу. Такі рухливі електрони називаються усуспільненими або електронним газом. Тому метал можна подати як структуру, що складається з атомів металу, розміщених у вузлах кристалічної гратки, які утримуються за рахунок усуспільнених електронів.
Отже, металічний зв'язок зумовлений утворенням електронами усіх атомів речовини єдиної рухливої електронної хмари.
Металічний зв’язок є нелокалізованим, тобто таким, що не має певної напрямленості: у ньому беруть участь усі атоми кристалу металу.
